肺癌驱动基因研究
- 格式:pptx
- 大小:169.81 KB
- 文档页数:19

非小细胞肺癌常见的驱动基因突变类型非小细胞肺癌(Non-Small Cell Lung Cancer,NSCLC)是目前肺癌的主要类型,约占所有肺癌的85%。
驱动基因突变是NSCLC发生和发展的重要原因之一。
本文将介绍非小细胞肺癌中常见的几种驱动基因突变类型。
1. EGFR突变表皮生长因子受体(Epidermal Growth Factor Receptor,EGFR)是一种经常发生突变的驱动基因。
EGFR突变包括点突变和插入/缺失突变,常见的突变位点有Exon 19和Exon 21。
EGFR突变可以导致受体激活异常,进而促进细胞增殖和进化,是NSCLC中最为常见的驱动基因突变。
EGFR突变与亚型NSCLC的发生有关,对EGFR酪氨酸激酶抑制剂(EGFR-TKI)有较好的治疗反应。
2. ALK融合基因ALK基因重排是NSCLC中另一种常见的驱动基因突变。
ALK基因重排导致ALK蛋白与其他蛋白(如EML4)融合,形成具有激酶活性的融合蛋白。
这种融合蛋白能够激活多个信号通路,促进肿瘤细胞的增殖和生存。
ALK融合基因在NSCLC中的检出率约为5%,主要见于非吸烟者和年轻患者。
对于ALK阳性的NSCLC患者,ALK 抑制剂是一种有效的治疗选择。
3. ROS1融合基因ROS1基因融合是NSCLC中另一种重要的驱动基因突变。
ROS1融合基因的患者通常是非吸烟者和年轻人。
ROS1融合基因可以激活多个信号通路,促进肿瘤细胞的增殖和生存。
ROS1融合基因在NSCLC中的检出率约为1-2%。
针对ROS1阳性的NSCLC患者,ROS1抑制剂是一种有效的治疗选择。
4. BRAF突变BRAF基因突变是NSCLC中较为罕见但具有重要意义的驱动基因突变。
BRAF突变通常见于不吸烟的患者,尤其是女性。
BRAF突变可以导致信号通路的异常激活,进而促进肿瘤细胞的增殖和生存。
BRAF突变在NSCLC中的检出率约为1-4%。
对于BRAF阳性的NSCLC患者,BRAF抑制剂是一种有效的治疗选择。

肿瘤驱动基因的特征和功能研究肿瘤驱动基因是引发癌症的一类基因,它们可以在细胞内发挥重要的功能,促进癌症的发展和生长。
随着分子生物学的研究,我们已经了解了许多肿瘤驱动基因的特征和功能。
本文将探究肿瘤驱动基因的定义、特征及其功能,以期更好地理解肿瘤病理生理学。
1. 肿瘤驱动基因的定义肿瘤驱动基因,即促进细胞癌变和肿瘤形成的基因,这些基因有不同的作用,但它们的共同点是能够通过突变、拷贝数增加等方式对细胞的生长和分裂产生重要影响。
肿瘤驱动基因的存在是一个重要的发现,它引起了关于癌症起源和发展的许多理论。
2. 肿瘤驱动基因的特征肿瘤驱动基因的特征主要体现在以下几个方面:(1)拷贝数变异:肿瘤驱动基因的拷贝数改变可以是整倍体增加也可以是基因座突变。
这种变异可能唤起肿瘤形成。
(2)突变:某些突变会导致肿瘤抑制基因失去了正常功能,同时肿瘤驱动基因的突变往往会导致基因失去控制。
(3)化学修饰:一些化学修饰如DNA甲基化、羟甲基化等也可能影响肿瘤驱动基因的功能。
3. 肿瘤驱动基因的功能肿瘤驱动基因可以对细胞的正常生理功能产生影响,并促进癌症的发展。
其主要功能体现在三个方面:(1)参与细胞生长和分裂的调节:肿瘤驱动基因可以促进或抑制细胞的生长和分裂,这是它们的基本功能。
突变或拷贝数增加等变异可能导致基因失去对生长和分裂的正常调节作用,从而引起癌细胞的不受限制生长。
(2)细胞信号通路的激活:细胞通路是细胞间通信网络的重要组成部分,肿瘤驱动基因可以通过激活信号通路的某些分子来参与信号传递。
这些分子可能是细胞内的激活酶、受体或转录因子等,在突变时导致某些分子一直处于激活状态。
(3)参与细胞程序化死亡调节:细胞程序性死亡(apoptosis)是细胞生命周期的一个重要环节,避免细胞癌变的发生。
但在某些情况下,肿瘤驱动基因可以抑制细胞凋亡的发生,从而促进持续的生长。
这种抑制可能与直接抑制凋亡信号通路的分子有关,或者与促进细胞生长和分裂的信号通路紊乱有关。

肺癌分子诊断标志物与个体化治疗一、肺癌分子诊断标志物的研究进展肺癌是世界范围内最常见的恶性肿瘤之一,其发病率和死亡率一直居高不下。
根据统计数据显示,全球每年有数百万人被诊断出患有肺癌,并有数以百万计的人因此去世。
由于早期肺癌通常没有明显症状,许多患者往往在晚期才发现罹患该病,导致治愈率大幅下降。
因此,寻找有效的早期诊断标志物对于改善肺癌诊断和治疗具有重要意义。
1. 碱基质金属蛋白酶(MMPs)家族碱基质金属蛋白酶(Matrix Metalloproteinases, MMPs)是一类能够降解胶原纤维和其他基质组分的酶类蛋白,在多种生理和病理过程中起到重要作用。
近年来,越来越多的研究表明MMPs家族参与了肺癌的发生和发展,并且已经成为一项新颖而可靠的肺癌诊断标志物。
MMPs家族成员主要包括MMP-1、MMP-2、MMP-9等,并且它们的表达水平在肿瘤组织中明显升高。
因此,检测患者血液和组织中MMPs家族成员的表达水平,有助于早期发现肺癌。
2. 微小RNA(microRNAs)微小RNA(microRNAs, miRNAs)是一类长度约为22个核苷酸的非编码小分子RNA,已被广泛认可为一种关键的基因调控分子。
近年来,越来越多的研究表明miRNAs与肺癌发生和进展密切相关,并且具有潜在的临床应用价值。
例如,某些特定miRNAs(如miR-21、miR-125b等)在肺癌组织中高表达,并被认为是患者预后不良的标志物;而其他miRNAs(如let-7、miR-34家族等)则被发现具有抑制肿瘤生长和转移的作用。
因此,通过监测这些miRNAs在体液和组织中的表达水平,可以实现肺癌早期诊断、分型和预后评估。
二、个体化治疗在肺癌中的应用随着对肺癌分子机制的深入研究,个体化治疗不断受到重视,并为患者提供了更精准、有效的治疗策略。
根据个体基因组分析结果,医生可以针对特定变异基因或蛋白靶点进行有针对性的药物治疗。
1. 靶向治疗靶向治疗是利用具有特异性作用于特定分子靶点的药物来抑制肿瘤生长和扩散。

论文题目:肺癌的遗传易感性研究和家族遗传分析1. 引言肺癌是全球最常见的恶性肿瘤之一,其发病率和死亡率在所有癌症中均居前列。
虽然吸烟是肺癌的主要风险因素,但遗传因素在肺癌的发生中也扮演着重要角色。
近年来,随着基因组学和分子生物学研究的进展,人们对肺癌的遗传易感性和家族遗传机制有了更深入的了解。
本文将系统探讨肺癌的遗传易感性研究、家族遗传分析以及相关的分子机制。
2. 肺癌的遗传易感性2.1 遗传易感基因的发现●EGFR基因:EGFR突变在非小细胞肺癌(NSCLC)中常见,特别是亚洲人群。
EGFR突变患者对酪氨酸激酶抑制剂(TKI)治疗反应良好。
●KRAS基因:KRAS突变在吸烟相关的NSCLC中较为常见,预示着较差的预后和对TKI治疗的耐药性。
●ALK基因重排:ALK基因重排在NSCLC患者中约占5%,ALK抑制剂对这类患者有显著疗效。
●TP53基因:TP53突变在多种癌症中普遍存在,突变形式多样,预示着肿瘤的侵袭性和预后差。
2.2 全基因组关联研究(GWAS)全基因组关联研究通过分析大规模人群的基因型与表型数据,识别出多个与肺癌易感性相关的基因位点:●5p15.33位点:包含TERT和CLPTM1L基因,与多种癌症的易感性相关。
●6p21位点:HLA基因簇所在区域,提示免疫反应在肺癌发生中的作用。
●15q25位点:包含CHRNA5-CHRNA3-CHRNB4基因簇,与尼古丁依赖和肺癌风险相关。
3. 家族遗传分析3.1 家族性肺癌的特点●家族聚集性:家族中多名成员患有肺癌,且发病年龄较早。
●非吸烟相关:一些家族性肺癌病例发生在非吸烟者或轻度吸烟者中,提示遗传因素的作用。
3.2 家族性肺癌的遗传模式●常染色体显性遗传:某些家族性肺癌表现为常染色体显性遗传模式,即携带致病基因的个体有50%的概率将基因传递给子女。
●多基因遗传:家族性肺癌可能涉及多个基因的共同作用,这些基因的累积效应增加了患病风险。
3.3 遗传咨询和风险评估●家族史采集:详细记录家族中每位成员的疾病史,识别高风险个体。

非小细胞肺癌驱动基因谱《非小细胞肺癌驱动基因谱》非小细胞肺癌(Non-small cell lung cancer,NSCLC)是一种常见的肺癌类型,占据了肺癌患者的大部分比例。
尽管在治疗方法和技术上有了显著进步,但NSCLC仍然是一个具有挑战性的疾病。
为了更好地理解NSCLC的发病机制和开发更有效的治疗策略,科学家们开始关注NSCLC的驱动基因谱。
驱动基因谱是指与肿瘤发展、进展和预后相关的一组突变基因。
在NSCLC中,研究人员已经鉴定出许多驱动基因,这些基因的突变直接参与了肿瘤形成和发展的过程。
下面,我们将介绍一些目前已知的NSCLC驱动基因。
第一个被发现的驱动基因是EGFR基因突变。
EGFR基因突变在NSCLC患者中非常常见,特别是在亚洲人群中。
EGFR突变导致了受体激活通路的过度激活,进而促进了细胞生长和增殖。
由于EGFR突变的存在,EGFR酪氨酸激酶抑制剂成为了NSCLC治疗的重要药物。
另一个重要的驱动基因是ALK基因突变。
ALK基因突变在NSCLC患者中也比较常见。
ALK融合蛋白的过度表达与肿瘤细胞增殖和生存的异常相关。
针对ALK突变的靶向治疗剂已经在临床试验中显示出显著的疗效。
此外,研究人员还发现了ROS1、RET、KRAS、HER2等一系列驱动基因。
这些基因的突变与肺癌的发生和发展密切相关。
研究人员通过对这些驱动基因的研究,为NSCLC的治疗带来了新的机会。
了解NSCLC的驱动基因谱对于治疗选择至关重要。
通过对患者进行基因检测,可以确定突变的存在与否,从而为个体化治疗提供指导。
有了对驱动基因的更好理解,科学家们正在努力开发更多的靶向药物,以提高NSCLC患者的生存率和生活质量。
总之,《非小细胞肺癌驱动基因谱》的研究揭示了NSCLC发病机制中重要的驱动基因,为肺癌的治疗策略提供了新的思路。
未来,随着对这些驱动基因的进一步研究,我们有望开发出更多的靶向药物,提供更加个体化的NSCLC治疗方案。

肺癌做基因检测注意什么肺癌是一种常见的恶性肿瘤,基因检测在肺癌的早期诊断、个体化治疗和预后评估等方面具有重要的应用价值。
进行肺癌基因检测时,需要注意以下几个方面。
首先,选择合适的检测方法。
目前,常用的肺癌基因检测方法包括传统的基因突变检测、基因重排检测和基因表达检测,以及新兴的全基因组测序技术等。
根据具体的临床需求和病情特点,选择合适的检测方法可以提高检测的准确性和敏感性。
其次,选择合适的检测样本。
肺癌基因检测常用的样本包括肿瘤组织样本和体液样本,如血液、尿液和痰液等。
对于手术切除的肿瘤组织,可以直接提取DNA 进行基因检测;对于无法获得组织样本的患者,可以采集体液样本进行检测。
选择合适的样本对于提高检测的可靠性和准确性至关重要。
再次,筛选适用的检测基因。
肺癌基因检测主要包括驱动基因、免疫相关基因和预后相关基因等。
驱动基因是肺癌发生和发展的关键基因,如EGFR、ALK、ROS1基因等;免疫相关基因与免疫治疗的疗效密切相关,如PD-L1、TMB等;预后相关基因能够预测患者的生存期和复发风险,如KRAS、TP53基因等。
根据患者的具体情况和医疗需求,选择合适的检测基因可以为个体化治疗和预后评估提供有力的依据。
此外,合理解读基因检测结果也是基因检测中的重要环节。
基因检测结果通常包括阳性和阴性,阳性意味着存在基因异常,阴性则表示基因正常。
但需要注意的是,阳性结果并不一定意味着患者就一定会发生肺癌,而阴性结果也不能排除患者发生肺癌的风险。
因此,应结合临床病史、检查结果和其他辅助检测手段综合判断。
最后,个体化治疗是肺癌的重要治疗策略之一。
通过基因检测可以明确患者的基因型,从而指导选择合适的个体化治疗方案。
例如,EGFR基因突变阳性的患者可选用靶向治疗药物,ALK基因重排阳性的患者可以应用相关的靶向药物。
个体化治疗能够提高治疗效果,延长患者的生存期,因此在进行肺癌基因检测时要注意与临床治疗的紧密结合。
综上所述,肺癌基因检测在临床应用中具有重要的价值,正确选择检测方法、样本和基因,合理解读检测结果,并结合个体化治疗,能够为肺癌的早期诊断和个体化治疗提供有力支持。

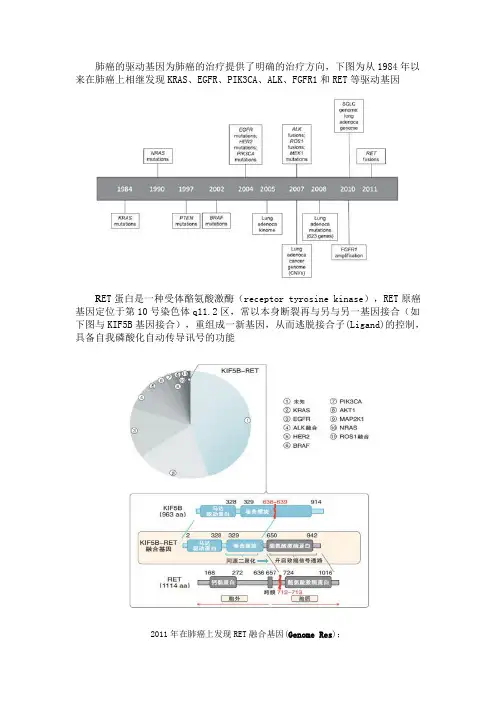
肺癌的驱动基因为肺癌的治疗提供了明确的治疗方向,下图为从1984年以来在肺癌上相继发现KRAS、EGFR、PIK3CA、ALK、FGFR1和RET等驱动基因R ET蛋白是一种受体酪氨酸激酶(receptor tyrosine kinase),RET原癌基因定位于第10号染色体q11.2区,常以本身断裂再与另与另一基因接合(如下图与KIF5B基因接合),重组成一新基因,从而逃脱接合子(Ligand)的控制,具备自我磷酸化自动传导讯号的功能2011年在肺癌上发现RET融合基因(Genome Res);2012年初,Dana-Farber等癌症中心,在24位NSCLC上发现1例RET融合基因,扩大到561位肺腺癌上后,又发现11位RET融合基因(2%),(Nature medicine);2012年初,日本学者在319为肺腺癌上发现9位发生RET融合基因(2.8%),并且发现含该驱动基因的肺癌细胞可被vandetanib抑制,(Nature medicine);2012年初,日本学者在1529例肺癌患者上发现44例ALK融合基因,14例RET融合基因,13例ROS1融合基因,共71例(均为肺腺癌),(Nature medicine);2012年11月,中国学者在936位发现13位RET融合基因,11位为肺腺癌,2位为腺鳞癌(JCO)。
2012年7月,斯隆凯瑟琳癌症中心,启动II期临床试验:Cabozantinib in Patients With KIF5B/RET Positive Advanced NSCLC。
Cabozantinib可同时 MET, VEGFR, and RET。
一些医学平台目前已开展临床认可的ALK、ROS1等融合基因商业化检测(FISH方法);一些EGFR突变阴性的晚期NSCLC患者,在化疗耐药或耐受不了化疗时,可根据ALK或ROS1融合基因的结果选择Crizotinib药物治疗;相信不久的未来,将有更多的驱动基因被发现后相应的药物也会随即得到FDA的批准,如RET融合基因和Cabozantinib。


经验交流63青年型肺癌的临床和基因表型特征研究现状潮力格尔1,彻力格尔2# (1.内蒙古民族大学附属医院,内蒙古自治区通辽市 028007 ;2.科尔沁右翼中旗蒙医医院,内蒙古自治区兴安盟 029400)摘要:我国肺癌人均发病年龄约为72岁,若年龄在18~40岁,临床称为青年肺癌,其占患肺癌者总数的5%左右[1]。
与一般的肺癌相较而言,青年肺癌的起病十分隐匿,临床体征不显著,通常情况下较难发现,当被察觉时病情已处于疾病末期,且大部分患者病变部位附近的淋巴转移活跃度高,且会出现向远处转移现象[2]。
然而,大部分青年肺癌患者为单器官发生病灶转移,少数为多个器官发生病灶转移。
现阶段,经过大量临床医疗研究发现,青年肺癌的基因表型特征有着一定的特异性,其癌变的驱动基因突变丰度相对很高,并与其临床具体表征、治疗预后存在紧密联系[3]。
近几年,青年肺癌一直是整体医学领域关注重点,本文就青年肺癌及其基因性状的特点作一综述,以期为后期青年肺癌的临床治疗、研究提供参考。
关键词:青年;肺癌;干预;基因表型特征肺癌为异质性疾病,其在世界范围内有着较高患病率与死亡率,对国民的生命健康构成较大威胁。
肺癌的产生、病程进展、病灶部位的转移等各项因素非常复杂,通常与肿瘤细胞自身、肿瘤微环境因素具有相关性[4]。
大部分肺癌的癌变细胞为肺上皮细胞,其由人体上皮细胞损伤引起的癌变细胞无限增殖,严重时将快速转移至胸腔、肺门淋巴和远端器官,如脑、肝、肾脏等。
2021年数据统计,全世界约有1950万肺癌新患病例与980万肺癌死亡病例;到2022年,全球将会比去年增加222万新肺癌病例与170万肺癌死亡病例。
其中,我国肺癌新病例占据约35%,死亡病例约占37.8%。
此外,在所有肺癌患者中,男性远多于女性,各自占比为2.20:1[5]。
基于上述,临床对青年肺癌病症行进一步研究,探索其本身和微环境对癌变分子的发病机制认知,帮助肺癌患者提高生存质量和时间,为肺癌诊断和治疗提供重要的理论依据。

非小细胞肺癌EGFR基因靶向治疗研究进展一、本文概述非小细胞肺癌(NSCLC)是全球范围内发病率和死亡率均较高的恶性肿瘤之一。
表皮生长因子受体(EGFR)是非小细胞肺癌中常见的异常表达基因之一,因此,针对EGFR的靶向治疗已成为非小细胞肺癌治疗的重要手段。
本文旨在全面综述非小细胞肺癌EGFR基因靶向治疗的研究进展,包括EGFR基因突变与表达的研究、EGFR抑制剂的研发与临床应用、EGFR靶向治疗的耐药机制以及联合治疗策略等方面的最新成果和进展。
通过本文的阐述,期望能够为非小细胞肺癌EGFR基因靶向治疗的深入研究与实践提供有益的参考和启示。
二、EGFR基因及其与NSCLC的关系EGFR,即表皮生长因子受体,是一种关键的跨膜蛋白酪氨酸激酶受体,主要参与细胞生长、增殖、分化和凋亡等过程。
在人体中,EGFR 基因位于第七号染色体上,其编码的EGFR蛋白广泛存在于上皮组织,尤其在肺、脑和乳腺等组织中表达最为丰富。
近年来,大量的研究表明,EGFR与NSCLC的发生和发展密切相关。
NSCLC细胞常常存在EGFR基因的突变或过度表达,这些变化导致EGFR蛋白的持续激活,从而引发细胞的无序增殖和肿瘤的形成。
EGFR突变最常见的是酪氨酸激酶域的突变,这些突变能够增加EGFR 的活性,使细胞对EGFR配体的反应增强,导致细胞增殖失控。
EGFR作为NSCLC的重要治疗靶点,其靶向药物的开发和应用已经成为NSCLC治疗领域的研究热点。
目前,针对EGFR的靶向药物主要包括酪氨酸激酶抑制剂(TKIs)和单克隆抗体两大类。
这些药物通过抑制EGFR的活性或阻断其与配体的结合,从而抑制肿瘤细胞的增殖和转移,提高NSCLC患者的生存质量和生存期。
然而,尽管EGFR靶向治疗在NSCLC治疗中取得了显著的成效,但仍存在一些问题。
如部分患者对EGFR靶向药物不敏感,部分患者在初始敏感后会出现耐药性等。
这些问题的存在提示我们,对EGFR 及其与NSCLC关系的深入研究,以及新的靶向药物的研发,仍然是NSCLC治疗领域的重要任务。
本科毕业论文(设计)文献综述一、国内外现状肺癌是当今世界上最常见的恶性肿瘤之一,仅次于乳腺癌和前列腺癌,是癌症死亡的主要原因。
男性的发病率(13%)通常高于女性(12%)。
肺癌的发病率在中国男性癌症患者中最高;女性癌症患者中肺癌的比例位居第二,且呈逐年增加的趋势,男女死亡率均最高[1]。
肺癌可分为两类:小细胞肺癌(SCLC)和非小细胞肺癌。
其中,非小细胞肺癌(NSCLC)约占所有肺癌患者的85%,小细胞肺癌约占肺癌总发病率的15%。
近年来,研究发现,一些基因的突变可以驱动肺癌的发生和发展,即肺癌的驱动基因。
随着基因分析和分子诊断技术的不断发展和新一代测序技术的应用,分析肺癌的遗传特征谱和发现更多新型肺癌驱动基因将更加方便,并可在临床上更新和简化肺癌基因的检测方法,为肺癌的靶向治疗提供了更多潜在的药物靶点[2]。
二、研究方向(一)非小细胞肺癌驱动基因研究非小细胞肺癌又可分为肺腺癌( lung adenocarcinoma,AC) 、肺鳞状细胞癌( lung squamous cell carcinoma,SCC) 和大细胞癌 ( large cell lung cancer,LCLC)等[3]。
1.肺腺癌的驱动基因。
Zhou X,Cai L,Liu J(2018)指出,肺腺癌中约60%的驱动基因已被识别。
其中,EGFR、ALK和KRAS是肺腺癌中更常见的研究和特征性驱动基因。
最近的研究表明,肺腺癌患者的EGFR突变率为50.7%。
最常见的突变是外显子21中的L858R替换突变和外显子19中的缺失突变。
EGFR突变和19Del突变是肺腺癌患者的独立预后因素[4]。
Rao S等人分析了120个不同亚型的肺癌组织样本,并在每种肺癌组织类型中检测到强烈的肿瘤RANK表达;腺癌的发病率和表达强度最高。
72%的肺腺癌RANK阳性,发现RANK阳性与KRAS 突变相关[5]。
Ooki A等人的研究证明,PAX6作为一种致癌物,通过PAX6-GLI-SOX2信号轴诱导肺腺癌的癌干细胞特征,并支持PAX6启动子甲基化作为早期肺癌检测的生物标志物的临床应用[6]。
肺癌egfr突变细胞系
肺癌是全球癌症死亡率最高的疾病,每年导致大量患者失去生命。
在肺癌中,EGFR(表皮生长因子受体)突变是一种常见的驱动基因突变,它在肺癌的发生、发展及治疗中起着重要作用。
EGFR突变主要发生在肺癌患者的腺癌组织中,突变会导致EGFR酶活性增加,从而促进肺癌细胞的生长和扩散。
通过检测EGFR突变,可以更好地判断患者的病情和预后,为个体化治疗提供依据。
在EGFR突变肺癌的研究中,细胞系发挥着重要作用。
细胞系是指在体外培养条件下,具有连续无性繁殖能力的细胞群。
通过培养和鉴定EGFR突变肺癌细胞系,研究者可以更深入地研究EGFR突变的分子机制,为药物研发和临床治疗提供理论依据。
我国在EGFR突变肺癌研究方面取得了世界领先的成果。
近年来,我国科研人员发现了一些新的EGFR突变位点,并对EGFR靶向药物进行了深入研究。
例如,我国自主研发的EGFR靶向药物奥西替尼(Osimertinib)已经获得批准上市,为EGFR突变肺癌患者带来了新的治疗选择。
EGFR突变肺癌的诊断和治疗是临床工作中的重点和难点。
目前,临床诊断主要依赖病理检测和基因检测,治疗方面主要包括化疗、放疗和靶向治疗。
随着研究的深入,未来有望开发出更多针对EGFR突变肺癌的靶向药物和治疗方法,提高患者的生活质量和生存率。
总之,EGFR突变肺癌作为一种常见的肺癌亚型,已经成为医学界关注的焦点。
通过对EGFR突变的研究,我们可以更好地了解肺癌的发生发展机制,
为诊断和治疗提供有力支持。
研究揭示基因突变与肺癌的关系近年来,肺癌已成为全球范围内最常见的恶性肿瘤之一,其高发和死亡率给人类健康带来了巨大的威胁。
多年的研究表明,基因突变在肺癌的发生和发展过程中起着重要的作用。
本文将就基因突变与肺癌的关系展开探讨,进一步了解其机制,为肺癌的早期诊断和治疗提供理论依据。
肺癌作为一种恶性肿瘤,其起源和发展涉及多个复杂的生物学过程,包括基因突变。
基因突变是指地球上所有生物体产生新的遗传变异或表型的基本原因之一。
在肺癌中,基因突变可以分为两大类:驱动基因突变和通过影响基因表达的突变。
这些突变可能导致细胞的增殖、分化以及凋亡方面的异常,进而导致癌细胞的出现和肿瘤的发展。
研究发现,肺癌发生的基因突变呈现出多样化的模式。
其中,最常见的突变是肿瘤抑制基因的突变。
肿瘤抑制基因一直被认为是肿瘤的“守门人”,通过抑制细胞生长和转化来维持正常组织的稳定。
然而,当这些肿瘤抑制基因发生突变时,细胞的抑制功能受到削弱,从而增加了肺癌的风险。
另一类常见的基因突变是激活型突变。
这种突变通常发生在肿瘤驱动基因中,驱动基因是指在肿瘤细胞中具有变异而导致细胞增殖的基因。
这些突变可以使驱动基因永久地打开并持续表达,从而导致细胞无节制的增殖和分化。
EGFR基因的突变是肺癌中常见的激活型突变,这种突变可以导致肿瘤细胞对某些靶向治疗药物敏感,进而提供了治疗肺癌的新思路。
除了这些常见的基因突变外,研究还发现一些罕见但具有重要意义的突变。
比如,TP53基因突变在肺癌中是最为常见的基因突变之一,其突变频率与肺癌的发生和预后密切相关。
此外,还有一些其他基因突变如KRAS、ALK、ROS1等也被发现与肺癌的发生和发展紧密相关。
随着研究的不断深入,越来越多的基因突变与肺癌的关系得到了揭示。
这些研究不仅帮助我们了解基因突变在肺癌发生和发展中的作用,还为肺癌的早期诊断和治疗提供了新的思路。
例如,基于肺癌突变基因的检测技术已经广泛应用于肺癌的早期筛查,从而提高了早期发现肺癌的机会。
非小细胞肺癌驱动基因突变的CT影像特征研究进展王景亮1,2,禚孝丽1,3,李叶琴4,5,徐威1,5,王翠艳4,付国斌1,6*1.山东第一医科大学附属山东省立医院肿瘤中心,山东济南250021;2.山东中医药大学第二临床学院,山东济南250002;3.山东第一医科大学(山东省医学科学院)临床医学院,山东济南250117;4.山东大学附属省立医院放射科,山东济南250021;5.山东大学临床医学院,山东济南250021;6.山东第一医科大学第三附属医院,山东济南250031;*通信作者付国斌【基金项目】国家自然科学基金(81802284);泰山学者青年专家计划(tsqn202103179);山东省科技发展计划(2014GSF118157);山东省优秀中青年科学家奖励基金(BS2013YY058);山东省医学会临床科研资金(YXH2022ZX02176)【摘要】肺癌是全球癌症相关死亡的主要原因,非小细胞肺癌约占肺癌的85%,晚期非小细胞肺癌传统化疗效果不佳,针对特定驱动基因突变的分子靶向药物在临床治疗上取得巨大突破,改写了肺癌临床治疗实践。
肺癌CT影像特征与驱动基因突变的关联分析一直是肿瘤影像研究领域的热点,尤其是近年影像组学研究方法的进步给研究者提供了新的手段和视角。
本文对不同驱动基因突变(人表皮生长因子受体1、渐变性淋巴瘤激酶、人表皮生长因子受体2等)和野生型非小细胞肺癌人群的CT影像特征(肿瘤位置、直径、形态、肿瘤密度、胸膜播散、淋巴结转移等)和影像组学特征(CT衰减能量、肿瘤主方向、归一化灰阶不均匀特征、最大二维直径列等)进行总结分析,并对CT影像特征在不同驱动基因突变中的鉴别作用进行分析。
【关键词】癌,非小细胞肺;驱动基因;CT影像特征;影像组学;综述【中图分类号】R734.2;R445.3 【DOI】10.3969/j.issn.1005-5185.2023.08.021Advances in CT Imaging Characteristics of Driving Gene Mutations in Non-Small Cell Lung CancerWANG Jingliang1,2, ZHUO Xiaoli1,3, LI Yeqin4,5, XU Wei1,5, WANG Cuiyan4, FU Guobin1,6*1. Cancer Center, Provincial Hospital Affiliated to Shandong First Medical University, Jinan 250021, China; 6. The Third Affiliated Hospital of Shandong First Medical University, Jinan 250031, China; *Address Correspondence to: FU Guobin; E-mail:【Abstract】Lung cancer is the leading cause of cancer-related death worldwide, of which non-small cell lung cancer accounts for about 85% of all lung cancer. The effect of traditional chemotherapy for advanced non-small cell lung cancer is not good, and the molecular targeting drugs that drive specific gene mutations have made a great breakthrough in clinical treatment, which rewrote the clinical treatment practice of lung cancer. The correlation analysis between CT image features and driving gene mutations of lung cancer has always been a hot spot in the field of tumor imaging research, especially the progress of imaging research methods in recent years has provided researchers with new means and perspectives. In this study, CT image features and image omics features such as tumor location, diameter, shape, tumor density, pleural spread, lymph node metastasis, etc. of different driver gene mutations, such as human epidermal growth factor receptor 1, progressive lymphoma kinase, human epidermal growth factor receptor 2, and wild non-small cell lung cancer populations, as well as omics features such as CT attenuation energy and tumor host, were analyzed the orientation, normalized gray scale inhomogeneity and maximum two-dimensional diameter column were summarized and analyzed, and the role of CT image features in differentiating different driver gene mutations was analyzed.【Key words】Carcinoma, non-small-cell lung; Driving gene; CT imaging characteristics; Radiomics; ReviewChinese Journal of Medical Imaging, 2023, 31 (8): 897-902肺癌是全球癌症相关死亡的主要原因,也是我国发病率和死亡率最高的癌症类型[1-2]。