高中化学竞赛培训专题作业
- 格式:pdf
- 大小:527.16 KB
- 文档页数:14

高中化学竞赛专题练习1、BF3是平面三角形的几何构型,但NF3却是三角的几何构型,试用杂化轨道理论加以说明。
2、试用价层电子互斥理论判断下列分子或离子的中心原子轨道的杂化类型及空间构型。
HgCl2 BCl3 SnCl2 NH3 H2O PCl5 TeCl4 ClF3ICl-2SF6 IF5 FCl4 CO2 COCl2 SO2 NOClSO2Cl2 POCl3 SO-23 ClO-2IO2F-23、已知NO2,CO2,SO2分子其键角分别为132°,180°,120°,判断它们的中心原子轨道的杂化类型?4、写出NO+,NO,NO-分子或离子的分子轨道式,指出它们的键级,其中哪一个有磁性?5、写出XeO3在酸性介质中被I-离子还原得到Xe的反应方程式。
6、写出下列分子或离子的共轭酸。
SO-24, S-2, H2PO-4, NH3, HNO3,H2O7、写出下列分子或离子的共轭碱。
HAc, H2O, NH3, HPO-24, HS-8、MnO -24离子的歧化反应能否自发进行?写出反应式及电池符号。
已知电对的标准电极电势为:θϕ--244/MnO MnO =+0.56,θϕ224/MnO MnO -=+2.26V9、写出在碱性介质中Cl 2氧化Bi(OH)3的反应方程式,10、CCl 4不易发生水解,而SiCl 4较易发生水解,其原因是什么?11、在实验室中如何制备乙硼烷,乙硼烷的结构如何?12、说明InCl 2为什么式反磁性物质?TlI 3为什么不能稳定存在?13、焊接铁皮时,为什么常先用浓ZnCl 2溶液处理铁皮表面?14、热分解CuCl 2·2H 2O 时得不到无水CuCl 2;15、将1.008克铜—铝合金样品溶解后,加入过量碘离子,然后用0.1052mol ·dm -3Na 2S 2O 3溶液滴定生成得碘,共消耗29.84cm -3Na 2S 2O 3溶液,试求合金中铜得质量分数。
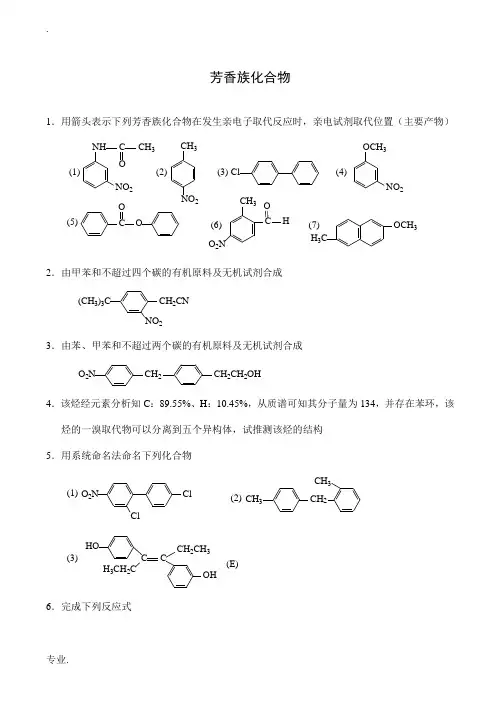
芳香族化合物1.用箭头表示下列芳香族化合物在发生亲电子取代反应时,亲电试剂取代位置(主要产物)NO 2CH 3ClCOOOCH 3NO 2H 3COCH 3(1)(2)(3)(4)(5)(6)(7)NH NO 2C CH 3O CH 3CO 2NOH2.由甲苯和不超过四个碳的有机原料及无机试剂合成CH 2CN NO 2(CH 3)3C3.由苯、甲苯和不超过两个碳的有机原料及无机试剂合成O 2NCH 2CH 2CH 2OH4.该烃经元素分析知C :89.55%、H :10.45%,从质谱可知其分子量为134,并存在苯环,该烃的一溴取代物可以分离到五个异构体,试推测该烃的结构 5.用系统命名法命名下列化合物O 2NClClCH 3CH 2CH 3(1)(2)(3)OHCH 3CH 2CCCH 2CH 3HO (E)6.完成下列反应式NO 2(1)Br 2?(2)?CH 3HNO 324(3)?CHO2(4)CH 3O CH 3OCH 2CHCH 2COClAlCl 3?(5)CH 2CH 2CHCH 2C OHCH 3CH 3H 2SO 4?(6)CH 2H 2SO 4?CH 2C OHCH 3CH 3CH 2CH 2(7)CH 2CHCH 2CHCHCH3H 2SO 4?(8)OCH 3?稀D 2SO 42(9)OCH 2CH 2CHClCH3AlCl 3???(10)OCH 3CClO +AlCl 348%HBr??(11)+AlCl 3CH 2CH 2OH 2O(12)CH3KCNH 3O ?7.用芳环取代反应,写出由苯及不超过三个C 原子的有机原料合成正丙基苯的三种不同方法。
8.写出由苯及适当的试剂合成的两种方法9.以甲苯为原料合成 (1) 对溴苯甲酸;(2) 间溴苯甲酸;(3) 邻溴苯甲酸。
10.以苯或甲苯为原料,合成下列化合物(1)H 2N C CH 3O(2)CH 3CH 2COOH(3)CH 2CH 2C CH (4)COOHBrBr(5)CH 2(6)CH 2CH CH 2BrCH 311.以苯及不超过2个C 原子的有机原料合成CH 2CH 2CH 2(1)(2)CH 2CH 2DDCH 2CH 3(3)12.请推测符合下列条件芳香族化合物的结构式 (1) 分子式为C 8H 10仅能生成一种一硝化产物 (2) 分子式为C 6H 3Br 3能生成三种一硝化产物 (3) 分子式为C 10H 14不能被强氧剂氧化成芳香族羧酸(4) 分子式为C10H14有六个可能的一溴取代物(光照下发生),其中有两个一溴取代物可拆分为一对对映体,该化合物经氧化后生成一个酸性物质C8H6O4;后者只有一种硝化产物C8H5NO6。
高中化学竞赛辅导练习及答案第一章基础化学第一节原子化学与元素周期律一.在极性分子中,正电荷重心同负电荷重心间的距离称偶极长,通常用d表示。
极性分子的极性强弱同偶极长和正(或负)电荷重心的电量(q)有关,一般用偶极矩(μ)来衡量。
分子的偶极矩定义为偶极长和偶极上一端电荷电量的乘积,即μ=d·q。
试回答以下问题:(1)HCl、CS2、H2S、SO2 4种分子中μ=0的是;(2)对硝基氯苯、邻硝基氯苯、间硝基氯苯,3种分子的偶极矩由大到小的排列顺序是:;(3)实验测得:μPF3=1.03德拜、μBCl3=0德拜。
由此可知,PF3分子是构型,BC13分子是构型。
(4)治癌药Pt(NH3)2Cl2具有平面四边形结构,Pt处在四边形中心,NH3和Cl分别处在四边形的4个角上。
已知该化合物有两种异构体,棕黄色者μ>0,淡黄色者μ=0。
试画出两种异构体的构型图,并比较在水中的溶解度。
构型图:淡黄色,棕黄色;在水中溶解度较大的是。
二.电离能是指由蒸气状态的孤立原子失去电子形成阳离子需要的能量。
从中性原子中移去第一个电子所需要的能量为第一电离能(I1),移去第二个电子所需要的能量为第二电离能(I2),依次类推。
现有5种元素,A、B、C、D、E,其I1~I3分别如下表,根据表中数据判断其中的金属元素有,稀有气体元素有,最活泼的金属是,显二价的金属是。
三.若在现代原子结构理论中,假定每个原子轨道只能容纳一个电子,则原子序数为42的元素的核外电子排布式将是怎样的?按这种假设而设计出的元素周期表,该元素将属于第几周期、第几族?该元素的中性原子在化学反应中得失电子情况又将怎样?四.超重元素“稳定岛”的假设预言自然界中可能存在着原子序数为114号的稳定同位素描208X。
请根据原子结构理论和元素周期律,预测:1.208X原子的核外电子排布式;2.它在周期表哪一周期?哪一族?是金属还是非金属?3.写出它的最高价态氧化物、氢氧化物(或含氧酸)的化学式并估计后者的酸碱性质。

智浪教育-普惠英才文库高中化学竞赛辅导练习参考答案与解析第一章元素与化合物第一节卤素一.1.IO3-十5I-+6CH3COOH===3I2+6CH3COO-+3H2O2.KI在潮湿空气里,在阳光的作用下会被空气氧化而产生紫黑色固体(或紫色蒸气),而KIO3不被空气氧化。
4I-+O2+2H2O===2I2+4OH-二.l.(1)主要反应:I2+2KClO3==2KIO3+C12↑(2)可能的副反应:C12+H2O(冷)==HClO+HClC12+H2O==2HCl+1/2O2 3C12+3H2O(热)==HClO3+5HClI2+5Cl2+6H2O==2HIO3+10HCl一步:I2+5H2O2−−催化剂2HIO3+4H2O−→二步:2HIO3+K2CO3==2KIO3+CO2↑+H2O2.使氧化生成的I2再还原为碘化物I2+2S2O32-==S4O62-+2I-三.3I2+6OH-===IO3-+5I-+3H2OS2O32-+4I2+10OH-===2SO42-十8I-+5H2OS2O32-+2H+===SO2↑十S↓+H2O4I-+O2+4H+===2I2+2H2O四.加入过量KI生成I3-离子以减少I2挥发1.在强酸性溶液中S2O32-遇酸分解,且I-易被空气氧化:(反应略);在碱性溶液中:S2O32-+4I2+10OH-===SO42-+8I-+5H2O3I2+6OH-===IO3-+5I-+3H2O上述到反应的发生,使定量反应难以准确.2.前者,I2与S2O32-的反应速度大于I2与OH-的反应速度;后者,S2O32-与I2的反应速度大于S2O32-与H+的反应速度。
五.I2(反应略)七.A CaF2 B H2SO4 C HF D NaF E NaHF2九.紫2I-+CI2===I2+2CI-棕紫2Br-+Cl2===Br2+2Cl-棕红色I2+5Cl2+6H2O===2IO3-+5Cl-+12H+十.A AgNO3 B AgCl C [Ag(NH3)2]Cl D AgBrE Na3[Ag(S2O3)2]F AglG Na[Ag(CN)2]H Ag2S (反应略)十三.1.该固体一定含钠和碘,使煤气灯火焰显黄色表明钠的存在;不溶于NH3,而溶于强络合剂CN-或S2O32-的黄色银盐一定是碘化银。

高中化学竞赛样题及答案一、选择题1. 下列关于元素周期表的描述,错误的是:A. 元素周期表是按照原子序数递增的顺序排列的B. 同一周期内,原子核外电子层数相同C. 同一族元素,最外层电子数相同D. 过渡元素包括副族和第Ⅷ族元素答案:B二、填空题2. 酸碱中和反应的实质是______与______的反应。
答案:H⁺;OH⁻三、判断题3. 燃烧是一种氧化还原反应。
答案:对四、简答题4. 请简述酸碱中和反应的原理。
答案:酸碱中和反应是指酸和碱在一定条件下反应生成盐和水的化学反应。
酸碱中和反应的实质是氢离子(H⁺)和氢氧根离子(OH⁻)的反应。
在反应过程中,酸释放出H⁺离子,碱释放出OH⁻离子,二者结合生成水,同时形成盐。
五、计算题5. 某溶液中含有KOH和NaOH,其浓度分别为0.2 mol/L和0.3 mol/L。
求该溶液的pH值。
答案:首先,我们需要计算出溶液中氢氧根离子(OH⁻)的浓度:c(OH⁻) = c(KOH) + c(NaOH) = 0.2 mol/L + 0.3 mol/L = 0.5mol/L然后,根据水的离子积(Kw = 10⁻¹⁴)计算出氢离子(H⁺)的浓度:c(H⁺) = Kw / c(OH⁻) = 10⁻¹⁴ / 0.5 mol/L = 2 × 10⁻¹⁴ mol/L最后,根据pH的定义计算出溶液的pH值:pH = -lg(c(H⁺)) = -lg(2 × 10⁻¹⁴) ≈ 13.7六、实验题6. 设计一个实验方案,用于检验某溶液中是否含有Cl⁻离子。
答案:实验步骤:1. 取一定量的待测溶液放入试管中。
2. 向溶液中加入过量的硝酸钡溶液,过滤掉沉淀。
3. 向滤液中加入硝酸银溶液。
4. 观察是否生成白色沉淀。
实验现象及结论:若生成白色沉淀,说明原溶液中含有Cl⁻离子;若没有生成白色沉淀,说明原溶液中不含Cl⁻离子。
实验原理:氯离子(Cl⁻)与银离子(Ag⁺)反应生成不溶于稀硝酸的白色沉淀——氯化银(AgCl)。

高一化学竞赛辅导练习(一)班级 姓名( )1.设N A 为阿伏加德罗常数,下列说法正确的是: A .标准状况下,5.6L 四氯化碳含有的分子数为0.25N A B .标准状况下,14g 氮气含有的核外电子数为5N AC .标准状况下,22.4L 任意比的氢气和氯气的混合气体中含有的分子总数均为N AD .标准状况下,铝跟氢氧化钠溶液反应生成1mol 氢气时,转移的电子数为N A( )2.在a LAl 2(SO 4)3和(NH 4)2SO 4的混合溶液中加入b molBaCl 2,恰好使溶液中的SO 42—离子完全沉淀;如加入足量强碱并加热可得到c molNH 3气体,则原溶液中的Al 3+离子浓度(mol ·L —1)为A .a cb 22- B .ac b 22- C .a c b 32- D .acb 62- ( )3.某氯化镁溶液的密度为1.18g ·cm —3,其中镁离子的质量分数为5.1%。
300mL 该溶液中Cl —离子的物质的量约等于A .0.37molB .0.63molC .0.74molD .1.5mol( )4.在标准状况下,ag 气体A 及bg 气体B 的分子数相同。
则及此有关的下列说法中不正确的是A .气体A 及气体B 的摩尔质量之比为a ∶b B .同温同压下,气体A 及气体B 的密度之比为b ∶aC .质量相同的气体A 及气体B 的分子数之比为b ∶aD .相同状况下,同体积的气体A 及气体B 的质量之比为a ∶b( )5.将a%的酒精和(100—a)%的乙醇溶液等体积混合,所得的溶液的质量分数 A .大于50% B .小及50% C .小及或等於50% D .大及或等於50% ( )6.下列离子方程式及所述事实相符且正确的是 A .漂白粉溶液在空气中失效:ClO —+ CO 2 + H 2O = HClO + HCO 3—B .用浓盐酸及反应制取少量氯气:MnO 2 + 2H ++ 2Cl —=== Mn 2++ Cl 2↑+ 2H 2OC .向NaAlO 2溶液中通入过量CO 2制Al(OH)3:AlO 2—+CO 2 +2H 2O = Al(OH)3↓+ HCO 3-D .在强碱溶液中次氯酸钠及Fe(OH)3反应生成Na 2FeO 4: 3ClO —+2Fe(OH)3= 2FeO 42—+3Cl —+H 2O+4H +( )7.有一无色溶液,可能含有K +、Al 3+、Mg 2+、NH 4+、Cl -、SO 42-、HCO 3-、MnO 4-中的几种。

高中化学竞赛辅导练习(按章节分块有详细解答)第一章元素与化合物第一节卤素一.为实现2000年消除碘缺乏病的目标,国家卫生部规定食盐必须加碘,其中碘以碘酸钾或碘化钾的形式存在。
1.有人烹调时,把两种不同厂家生产的加碘食盐混合,当滴食醋时,产生紫色蒸气,反应的离子方程式为2.这两种加碘食盐可以在潮湿的空气中曝露而加以鉴别,其原理是,反应的离子方程式为二.1.食盐加碘剂—碘酸钾的制备可以采用二条工艺路线:第一条:利用碘与氯酸钾反应来制备。
试回答:(1)该制备法的主要反应为:(2)可能的副反应有:第二条:碘与过氧化氢在催化剂作用下反应生成碘酸,再与碳酸钾作用生成碘酸钾,请写出以上二步的反应方程式:一步:二步:2.在传统的加碘盐中,使用的加碘剂主要是碘化钾。
为减少碘元素的损失,需加入一定量的硫代硫酸钠,为什么?三.分析化学上常用硫代硫酸钠与单质碘反应来进行元素分析。
硫代硫酸根(S2O3-2)离子与I2之间的反应进行得迅速、完全,但必须在中性或弱酸性溶液中进行。
因为在碱性溶液中,I2会发生反应,其离子方程式为:而且I2与S2O32-发生副发应,其离子方程式为。
若在强酸性溶液中,Na2S2O3会发生分解,其离子方程式为,同时I-离子容易与空气中的氧气发生反应,其反应的离子方程式为。
在用碘量法进行测定时,为防止碘的挥发,在实验中首先应该采取的措施是。
四.I2和Na2S2O3之间发生既快又完全的反应:I2+2Na2S2O32NaI+Na2S4O61.若相互倾倒时上述反应需要在接近中性(pH值为5~9)的条件下进行,为什么?2.当把I2溶液滴入Na2S2O3溶液中时,即使在碱性溶液中(pH=11)也能发生完全的反应;若把Na2S2O3溶液滴入I2溶液中,那么在酸性溶液中亦能发生完全反应,试简要解释上述两个实验事实。
五.物质Z是有金属光泽的微晶状粉末.将2.8g Z的称样分成两等份。
在加热下将其中一份溶于过量的浓硝酸中,蒸发溶液至恒量的HNO3逸出。

高中化学竞赛辅导练习1. (02上海)在25℃,101kPa条件下,将15 L O2通入10 L CO和H2的混合气中,使其完全燃烧,干燥后,恢复至原来的温度和压强。
(1)若剩余气体的体积是15L,则原CO和H2的混合气中V(CO)= L, V(H2)= L。
(2)若剩余气体的体积为a L,则原CO和H2的混合气中V(CO)︰V(H2)=。
(3)若剩余气体的体积为aL,则a的取值范围是2. (02天津)沼气是一种能源,它的主要成分是CH4。
0.5molCH4完全燃烧生成CO2和H2O时,放出445kJ热量,则下列化学方程式中正确的是A. 2CH4(g) + 4O2(g) ==== 2CO2(g) + 4H2O(l) ΔH= + 890kJ/mol B. CH4(g) + 2O2(g) ==== CO2(g) + 2H2O(l) ΔH = + 890kJ/mol C. CH4(g) + 2O2(g) ==== CO2(g) + 2H2O(l) ΔH = —890kJ/mol D.(1/2)CH4(g) + O2(g)====(1/2)CO2(g) + H2O(l) ΔH= —890kJ/mol3. (99上海保送生)化学需氧量(COD)是水体质量的控制项目之一,它是量度水中还原性污染物的重要指标。
COD是把用强氧化剂(我国采用K2Cr2O7)处理一定量水样时所消耗的氧化剂的量,并换算成以O2作为氧化剂时,1L水样所消耗O2的质量(mg/L)。
现有某废水样品20.00mL,加入10.00mL 0.0400mol/L K2Cr2O7溶液,并加入适量酸和催化剂,加热反应2小时。
在指示剂存在下用0.100mol/L Fe(NH4)2(SO4)2溶液滴定多余的K2Cr2O7,共用去Fe(NH4)2(SO4)2溶液12.00mL。
(1)已知K2Cr2O7在酸性溶液中作氧化剂时,还原成Cr3+离子,Fe2+离子氧化成Fe3+离子。

高中化学竞赛辅导练习第一节必备原理知识一.原子核外电子的排布现代原子结构理论认为,电子在原子核外高速运动,而且没有一定的轨道,所以,电子在核外运动时就像一团带负电荷的云雾笼罩着带正电荷的原子核,因此,通常把核外电子的运动比喻为电子云。
原子结构理论进一步指出,核外电子是在不同层上运动,这些层叫做电子层;电子层又分为若干亚层;亚层还有不同的轨道;而在每个轨道中运动的电子还有两种不同的自旋。
电子层、亚层、轨道、自旋四个方面决定了一个核外电子的运动状态。
不同元素的原子核外有不同数目的电子,这些电子是怎样在原子核外不同的电子层、亚层和轨道中排布的?原子结构理论指出,电子在原子核外的排布遵循三条规律,即泡利不相容原理、能量最低原理和洪特规则三条规律可以写出不同元素的电子排布式。
以上是对核外电子运动和排布的概括叙述。
这一部分内容还应着重了解以下几点:1.关于电子云的含义电子云是一个形象的比喻,是用宏观的现象去想象微观世界的情景,电扇通常只有三个叶片,但高速转起来,看到的却是一团云雾,像是叶片化成了云雾;电子在核外运动速度极高,而且没有一定的轨迹,因而可以在想象中“看”到电子的运动“化”成了云雾,一团带负电荷的云雾。
因此电子云不是实质性的云雾,不能理解为由无数电子组成的云雾。
应该指出,氢原子核外只有一个电子,也仍可以用电子云来描述。
电子云常用由许多小黑点组成的图形表示。
小黑点密集的地方表示在该处的单位体积内,电子出现机会较多(或称为几率密度较大)。
电子云图中单独一个小黑点没有任何意义。
2.关于电子层、亚层、轨道的意义①电子层——表示两方面意义:一方面表示电子到原子核的平均距离不同,另一方面表示电子能量不同。
K、L、M、N、O、P电子到原子核的平均距离依次增大,电子的能量依次增高。
②亚层——也表示两方面意义:一方面表示电子云形状不同,电子云是以原子核为中心的球形,p电子云是以原子核为中心的无柄哑铃形,d和f电子云形状更复杂一些;另一方面,表示能量不同,、p、d、f电子能量依次增高。

高一化学竞赛培优辅导练习(2)三、氧化还原反应1.氮化铝(AlN)具有耐高温、抗冲击、导热性好等优良性质,被广泛应用于电子工业、陶瓷工业等领域。
在一定条件下,氮化铝可通过如下反应合成:Al2O3 + N2 + 3 C 2 AlN + 3 CO下列叙述正确的是A、在氮化铝的合成反应中,N2是还原剂,Al2O3是氧化剂B、氮化铝晶体属于分子晶体C、上述反应中每生成2 mol AlN,N2得到3 mol电子D、氮化铝中氮元素的化合价为—32.重铬酸铵(NH4)2Cr2O7是一种受热易分解的盐,下列对重铬酸铵受热分解的产物的判断符合实际的是A.CrO3+NH3+H2O B.Cr2O3+NH3+H2O C.CrO3+N2+H2O D.Cr2O3+N2+H2O. 3.NaH是—种离子化合物,它跟水反应的化学方程式为:NaH+H2O→NaOH+H2↑,它也能跟液氨、乙醇等发生类似的反应,并都产生氢气。
下列有关NaH的叙述错误的是A.跟水反应时,水作氧化剂B. NaH中H-半径比Li+半径小C.跟液氨反应时,有NaNH2生成D.跟乙醇反应时,NaH被氧化4.对于反应H—+ NH3 = H2 + NH2—的正确说法是A.属于置换反应B.被氧化的仅是HC.H2既是氧化产物又是还原产物D.每生成1molH2,必转移电子2mol5.下列叙述正确的是A.在氧化还原反应中,肯定有一种元素被氧化,另一种元素被还原B.有单质参加或生成的反应一定属于氧化还原反应C.失电子难的原子,获得电子的能力一定强D.元素由化合态变成游离态时,它可能被氧化,也可能被还原6.将铜片溶于稀硝酸中,发生下列反应:3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O在上述反应中,参加反应的氧化剂和还原剂的个数比为A.3:8 B.8:3 C.2:3 D.3:27.已知化学反应3Cl2+8NH3 =6NH4Cl+N2,则氧化剂与还原剂物质的量之比是A.1:8 B.8:1 C.3:2 D.2:18.2003年10月15日,我国成功发射“神舟五号”载人飞船,飞船以铝粉与高氯酸铵的混合物为固体燃料,点燃时铝粉氧化放热引发高氯酸铵反应:2NH4ClO4=N2↑+4H2O↑+Cl2+2O2↑;△H<0。

化学高中竞赛试题及答案一、选择题(每题3分,共30分)1. 下列元素中,属于金属元素的是:A. 碳B. 氧C. 铁D. 硫答案:C2. 根据元素周期表,下列元素中原子半径最大的是:A. 锂(Li)B. 钠(Na)C. 钾(K)D. 铯(Cs)答案:D3. 化学反应中,能量变化的表现形式不包括:A. 热能B. 光能C. 电能D. 机械能答案:D4. 以下化合物中,属于共价化合物的是:A. NaClB. CaOC. H2OD. MgO5. 根据酸碱理论,下列物质中属于酸的是:A. NaOHB. HClC. NH3D. KOH答案:B6. 根据化学平衡原理,下列说法正确的是:A. 反应物的浓度增加,平衡向正反应方向移动B. 反应物的浓度减少,平衡向逆反应方向移动C. 温度升高,平衡向吸热方向移动D. 催化剂可以改变平衡位置答案:A7. 以下反应中,属于氧化还原反应的是:A. 2H2O → 2H2 + O2B. 2Na + 2H2O → 2NaOH + H2C. 2H2 + O2 → 2H2OD. 2HCl + Na2CO3 → 2NaCl + CO2 + H2O答案:B8. 根据电子排布规律,下列元素中电子排布最外层电子数最多的是:A. 氢(H)B. 氦(He)C. 氖(Ne)D. 氩(Ar)答案:D9. 根据化学键理论,下列物质中属于离子键的是:B. NaClC. H2OD. SO2答案:B10. 以下物质中,属于非电解质的是:A. 硫酸B. 蔗糖C. 氯化钠D. 醋酸答案:B二、填空题(每题4分,共20分)1. 常温下,水的离子积常数Kw是______。
答案:1.0×10^-142. 元素周期表中,第VIIA族元素的原子最外层电子数为______。
答案:73. 根据化学计量学,1摩尔任何物质都含有约______个基本单位。
答案:6.02×10^234. 根据酸碱中和反应,当酸和碱完全中和时,溶液的pH值为______。
高中化学培优工程(竞赛、“强基计划”考试)综合模拟题(三套)特级教师胡征善高中化学培优工程(竞赛、“强基计划”考试)模拟题(一)特级教师胡征善1.写化学方程式(10分)(1)2009年复旦大学的周鸣飞教授课题组与德国柏林自由大学的Riedel教授合作,通过金属铱原子和氧气分子反应的方法首次在低温稀有气体基质中制备了四氧化铱中性分子(Ir:5d76s2),后又采用脉冲激光溅射-超声分子束载带技术在气相条件下制备了四氧化铱离子。
(2)(SCSN3)2溶于NaOH溶液中(3)在乙醚中,四氢铝锂与四氯化硅反应生成一种气体和两种盐(4)天然气的无机成因说十分诱人。
据称,地幔主要成分之一的橄榄石与水和二氧化碳反应,可生成甲烷。
橄榄石是原硅酸镁和原硅酸亚铁,反应后变为蛇纹石[3MgO·2SiO2·2H2O]和磁铁矿。
(5)甲基丙基苯膦(有一对对映体)与HCl反应生成鏻盐2.(10分)化合物A是白色固体,不溶于水,加热剧烈分解,产生一固体B和气体C。
固体B不溶于水或HCl(aq),但溶于热的稀HNO3,得一溶液D及气体E。
E无色在空气中变红。
溶液D用HCl(aq)处理时得一白色沉淀F。
气体C与普通试剂不起反应,但与热的金属镁作用则生成白色固体G。
G与水作用得另一种白色固体H及气体J。
J使湿润的红色石蕊试纸变蓝,固体H可溶于稀H2SO4得溶液I。
化合物A用H2S溶液处理得黑色沉淀K、无色溶液L和气体C。
过滤后,固体K溶于浓HNO3得气体E、黄色固体M和溶液D。
滤液L用NaOH溶液处理得气体J。
(1)写出G、I、M所代表物质的化学式。
(2)写出A用H2S溶液处理的化学方程式,并分析电子转移情况。
(3)已知(F/B)=0.2223 V,(D/B)=0.7996V。
求F在水中的K sp(F)。
3.(11分)电解法回收废气中NO制备NH4NO3,其工作原理如下图所示。
(1)电极a、b属于阴极的是______,电极反应为__________________________。