有机化学第六章2炔烃
- 格式:pps
- 大小:1.32 MB
- 文档页数:41
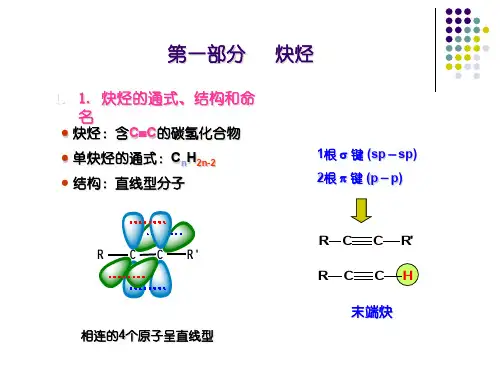



第6章 炔烃和二烯烃问题参考答案1.炔烃没有顺反异构体。
因为三键碳是sp 杂化,为直线形构型,故无顺反异构现象。
2.HC CCH 2CH 2CH 2CH 3H 3CC CCH 2CH 2CH 3H 3CH 2CC CCH 2CH 2CH 3HCCCHCH 2CH 3HCCCH 2CHCH 3HCCCCH 3H 3CC CCHCH 3CH 3CH 3CH 3CH 3CH 31-己炔2-己炔3-己炔3-甲基-1-戊炔4-甲基-1-戊炔3,3-二甲基-1-丁炔4-甲基-2-戊炔3.化)4. 表面上看来,碳碳三键更具不饱和性,那末怎样来理解这些事实呢? 解释烯烃比炔烃更容易亲电加成的原因,有以下三点:(1).由于三键和双键的碳原子的杂化状态不同三键碳原子的杂化状态为sp ,较双键(sp 2)的s 成份为多,由于s 成份的增加,使sp 杂化轨道比sp 2杂化轨道的直径短,因而造成碳碳三键较双键为短。
所以在炔烃中形成π键的两个p 轨道的重叠程度较烯烃为大,使炔烃中的π键更强些。
而且由于不同杂化状态的电负 性为sp >sp 2>sp 3,炔烃分子中的sp 碳原子和外层电子(π电子)结合得更加紧密,使其不易给出电子,因而使快烃不易发生亲电加成反应。
(2).由于电子的屏蔽效应不同炔烃和烯烃分子中,都存在着σ电子和π电子,可以近似地看成π电子是在σ电子的外围。
σ电子受原子核的吸引而π电子除受原子核的吸引外还受内层电子的排斥作用,因而就减弱了受核的束缚力,即为电子的屏蔽效应。
乙烯分子中有五个σ键,即有五对σ电子,而乙炔分子中只有三个σ键即只有三对σ电子,因而乙烯分子中的电子的屏蔽效应大于乙炔分子,所以乙烯分子中的π电子受原子核的吸引力小,易给出电子,也就容易发生亲电加成反心,而乙炔则较难。
(3).炔烃比烯烃的加成较难的原因,还可以从形成的中间体碳正离子的稳定性不同来说明:R CH CH 2+E+R +H C H 2C E RCCH+E +RC +C HE由于烷基正离了要比烯基正离子稳定些,所以烯烃的亲电加成较易。

炔烃反应通式-概述说明以及解释1.引言1.1 概述炔烃是一类化合物,其分子中含有至少一个炔基(C≡C)的有机物。
炔烃反应是指炔烃分子发生各种转化反应的过程,是有机化学中重要的研究领域之一。
炔烃反应具有广泛的应用价值,可以用于合成各种有机化合物,包括药物、天然产物、材料等。
炔烃反应通式可以描述不同类型的炔烃反应,帮助我们理解和研究这些反应的机理和规律。
炔烃反应的基本概念包括反应物、产物、反应条件等。
根据反应物的不同,炔烃反应可以分为与亲电试剂的加成反应、与亲核试剂的取代反应、与自由基试剂的加成反应等不同类型。
不同类型的炔烃反应具有不同的特点和应用范围。
炔烃反应的机理是研究炔烃分子转化过程的关键。
了解炔烃反应的机理可以帮助我们设计和优化反应条件,提高反应的选择性和效率。
炔烃反应的机理涉及多种反应步骤,包括亲电加成、亲核取代、脱氢、自由基反应等。
总之,炔烃反应是有机化学中非常重要的研究领域,其在有机合成和药物化学等方面具有广泛的应用价值。
通过研究炔烃反应的基本概念和机理,我们可以更好地理解和应用这些反应,推动有机化学的发展和应用。
在本文中,我们将详细介绍炔烃反应的分类和机理,并对其重要性和未来发展进行总结和展望。
1.2文章结构文章结构部分的内容可以根据以下内容进行编写:文章结构部分是论文的一个重要组成部分,它将为读者提供一个清晰的指南,帮助他们理解整篇文章的组织和流程。
本文将按照以下结构组织并介绍炔烃反应的基本概念、分类和机理。
首先,在第一节中,我们将对炔烃反应的基本概念进行介绍。
我们将解释炔烃的定义以及其在化学领域中的重要性。
此外,我们还将探讨炔烃反应的一些基本特点,例如其较高的反应活性和选择性。
接下来,在第二节中,我们将详细介绍炔烃反应的分类。
我们将根据反应类型和反应物的不同特征将炔烃反应分为若干类别,并对每一类别进行详细的解释。
这些分类将帮助读者更好地理解炔烃反应的整体框架,并为后续的机理解析提供基础。





课程名称:有机化学第六章 炔烃和二烯烃§6.1 炔 烃 一、炔烃的命名1 炔烃的系统命名法和烯烃相似,只是将“烯”字改为“炔”字。
2 烯炔(同时含有三键和双键的分子)的命名: (1)选择含有三键和双键的最长碳链为主链。
(2)主链的编号遵循链中双、三键位次最低系列原则。
(3)通常使双键具有最小的位次。
二、炔烃的结构与异构 1炔烃的结构最简单的炔烃是乙炔,我们以乙炔来讨论三键的结构。
现代物理方法证明,乙炔分子是一个线型分子,分之中四个原子排在一条直线上杂化轨道理论认为三键碳原子既满足8电子结构结构年 月 日 x0404-08≡C C H 0.106nm0.12nm180°课程名称:有机化学和碳的四价,又形成直线型分子,故三键碳原子成键时采用了SP 杂化方式 . 1 sp 杂化轨道杂化后形成两个sp 杂化轨道(含1/2 S 和1/2 P 成分),剩下两个未杂化的P 轨道。
两个sp 杂化轨道成180分布,两个未杂化的P 轨道互相垂直,且都垂直于sp 杂化轨道轴所在的直线。
2 三键的形成σ年 月 日2s2p2s2pspp激发杂化180°spspz 两个的空间分布sp 三键碳原子的轨道分布图课程名称:有机化学三、炔烃的物理性质(自学) 炔烃的沸点比对应的烯烃高10-20°C ,比重比对应的烯烃稍大,在水里的溶解度也比烷和烯烃大些。
四、炔烃的化学性质 1炔烃的酸性1.叁键碳sp 杂化,电负性大(3.29),σ电子靠近C 原子,易异裂出H +和C ≡C -,∴炔烃具有酸性。
乙炔的酸性比乙烷乙烯强,比水弱。
2.炔烃的鉴定三键碳上的氢原子具有微弱酸性(pK a =25),可被金属取代,生成炔化物。
生成炔银、炔铜的反应很灵敏,现象明显,可用来鉴定乙炔和端基炔烃。
年 月 日H-C C-H ≡2AgNO 3 + 2NH 4OH≡Cu-C C-Cu ≡2NH 4NO 3 + 2H 2O2NH 4Cl + 2H 2OR-C C-H ≡R-C C-Ag ≡R-C C-Cu ≡Ag(NH )+乙炔银(白色)乙炔亚铜(棕红色)炔铜(棕红课程名称:有机化学例:鉴别己烷、己烯、己炔己烷己烯己炔Br 2/CCl 4不褪色褪色褪色323生成沉淀无沉淀干燥的炔银或炔铜受热或震动时易发生爆炸生成金属和碳。
乙炔 炔烃知识重点1.乙炔的分子结构、化学性质、实验室制法; 2.炔烃的组成、结构、通式、通性。
炔烃是一类含有碳碳三键的脂肪烃。
其通式为CnH2n-2,属于不饱和烃。
一、乙炔分子的结构和组成分子式 电子式 结构式 结构简式 C 2H 2 H -C ≡C -H CH ≡CH 或 HC ≡CH 空间结构:直线型,键角1800 乙炔是无色、无味的气体,微溶于水几类重要烃的代表物比较二、乙炔的实验室制法CaC 2+2H 2O C 2H 2↑+Ca(OH)2 实验中采用块状CaC2和饱和食盐水,为何? 为了减缓电石与水的反映速度,实验室长滴加 饱和食盐水而不是直接滴加水。
三、化学性质 (1)氧化反映a.燃烧 2CH≡CH+5O 2−−→−点燃4CO 2+2H 2O 火焰敞亮,并伴有浓烟。
b.易被酸性KMnO 4溶液氧化,乙炔能使酸性KMnO4溶液褪色。
(2)加成反映乙炔与乙烯类似,也可以与溴水中的溴发生加成反映而使溴水褪色,且加成也是分步进行的;乙炔除和溴可发生加成反映外,在必然条件下还可以与氢气、氯化氢等发生加成反映。
乙炔与氢气加成时第一步加成产物为乙烯,第二步产物为乙烷, 乙炔是一种重要的大体有机原料,可以用来制备氯乙烯HC≡CH+HCl H 2C==CHCl四、炔烃1.炔烃的概念分子里含有碳碳三键的一类链烃 2.炔烃的通式 C n H 2n -2烯烃在组成上比等碳原子数的饱和烷烃少两个氢,通式变成C n H 2n ,炔烃的碳碳叁键,使得分子内氢原子数比等碳原子数的烯烃又少了两个,故其通式应为C n H 2n -2 3.炔烃的物理性质①一系列无支链、叁键位于第一个碳原子和第二个碳原子之间的炔烃,随着分子里碳原子数的增加,也就是相对分子质量的增加,熔沸点逐渐升高,相对密度逐渐增大; ②炔烃中n ≤4时,常温常压下为气态,其他的炔烃为液态或固态; ③炔烃的相对密度小于水的密度; ④炔烃不溶于水,但易溶于有机溶剂。
炔烃知识点总结文库一、炔烃的基本概念炔烃是一类含有碳碳三键的有机化合物,通式为CnH2n-2。
由于炔烃中含有碳碳三键,其分子结构比较特殊,因此具有一些特殊的性质和用途。
炔烃可以通过碱土金属(如钾、钠)与卤代烴反应制得,也可以通过卤代烴与碱溶液反应得到。
炔烃的分子式为CnH2n-2,其中n为炔烃的碳数。
二、炔烃的命名炔烃的命名是按照碳碳三键的位置及数量进行命名的。
一般情况下,炔烃的命名是根据碳碳三键的位置和数量进行的。
以乙炔为例,其分子式为C2H2,是由两个碳原子和两个氢原子组成的。
乙炔的分子结构中含有一个碳碳三键,因此其又称为二碳炔烃。
在命名时,通常采用代号25的形式来命名,即碳碳三键所在的位置及数量,如C2H2就是二碳炔烃。
三、炔烃的性质1. 物理性质(1)炔烃的密度较小,常温下呈气态或液态。
(2)炔烃的沸点和熔点较低,易挥发。
2. 化学性质(1)炔烃易发生加成反应,可以和溴水、卤代烴等发生加成反应。
(2)炔烃易发生氢化反应,可以和氢气发生氢化反应,生成烷烃。
3. 炔烃的应用(1)炔烃是有机合成的重要原料,可以作为烯烃的合成中间体,还可制备醇、羧酸等。
(2)炔烃可用于制备聚合物,如聚乙炔(Polyacetylene)。
四、炔烃的用途1. 炔烃在有机合成中的应用炔烃是有机合成中的重要原料,可以作为合成其他有机化合物的中间体。
例如,炔烃可以通过氢化反应制备烯烃,还可以作为聚合物的原料,如聚乙炔。
2. 炔烃在化工行业的应用炔烃在化工行业中有广泛的应用,主要是作为有机合成的原料,可以用于生产聚乙炔等聚合物,还可以用于生产乙炔醇、丙炔等。
3. 炔烃在医药行业的应用炔烃在医药行业中有一定的应用,可以作为一些药物的原料,如苯甲醛的合成中就需要使用炔烃。
五、结语炔烃是一类含有碳碳三键的有机化合物,具有较高的反应活性,可以作为有机合成的重要原料。
炔烃在化工、医药等行业都有广泛的应用,是一类重要的有机化合物。
认识和了解炔烃对于学习有机化学和应用有机化合物具有重要的意义,相信通过本文的介绍,读者对炔烃有了更深入的了解。