制备壳聚糖纳米粒的影响因素考察
- 格式:doc
- 大小:28.50 KB
- 文档页数:4

壳聚糖纳米颗粒的制备及应用壳聚糖是一种天然产物,由负离子化的氨基葡萄糖和乙酰胺葡萄糖组成,具有生物相容性、生物可降解性、低毒性等优良特性,在生物医学应用领域有广泛的应用。
然而,壳聚糖本身具有高分子量和极度亲水性的特点,限制了其在水相环境中的应用。
这些不足之处可以通过将壳聚糖转化为纳米颗粒来弥补。
壳聚糖纳米颗粒的制备壳聚糖纳米颗粒的制备方法主要包括电吸积、化学沉淀、反应溶液混合等方法。
其中,化学沉淀法属于传统方法,依靠溶液中钙离子的存在,将壳聚糖逐渐转化为淀粉状沉淀,再利用离心等方法将细小的沉淀分离出来,干燥后得到纳米级壳聚糖颗粒。
反应溶液混合法是近年来常用的制备方法之一,其基本原理是将两种溶液混合,触及到一定的环境或反应条件时会发生化学反应,生成纳米级壳聚糖纳米颗粒。
这种方法的优点在于操作简单、价格低廉。
壳聚糖纳米颗粒的应用壳聚糖纳米颗粒在生物医学领域有广泛的应用,其中包括生物医学成像、药物输送、组织工程等。
壳聚糖纳米颗粒可以作为生物医学成像方面的载体。
由于其表面极易修饰,可以通过化学方法添加不同的功能单元,例如荧光标记,以达到自身发光的目的,或者添加金属等,用于磁共振核磁共振成像等等。
壳聚糖纳米颗粒还可以作为药物输送系统。
其纳米粒子在药物体内的分布优化,能够让药物更多地达到靶组织,减少药物的剂量和在体内的停留时间,同时还能够提高药物的生物利用度。
这种方法已经被证实在肿瘤治疗方面有良好的前景。
最后,壳聚糖纳米颗粒还可以应用于组织工程。
由于其天然且生物相容性好,能够以纳米颗粒形式制备,壳聚糖纳米颗粒可以作为组织修复材料的神经修复、骨修复等重要组成部分。
这种方法已经在实验室环境中得到了良好的应用和发展,具有广阔的前景。
总之,在生物医学应用领域,壳聚糖纳米颗粒具有广泛的应用价值。
随着科学发展的进一步,相信壳聚糖纳米颗粒在治疗和诊断方面的应用前景会越来越广泛。


槲皮素/壳聚糖纳米粒的制备、表征及其体外抗氧化活性研究刘康;秦梦;杨婷婷;石玮玮;唐铭泽;唐金宝;张维芬【摘要】Objective To prepare quercetin ( QUE) loaded chitosan nanoparticles ( CS-NPs), evaluate its physicochemical properties and antioxidation activity in vitro.Methods Quercetin chitosan nanoparticles were prepared by ionic crosslinking method and self-assembly method.The preparation method was optimized using entrapment efficiency (EE), drug loading (DL) and size as indexes.The best formulation and preparation conditions were optimized by orthogonal test based on single-factor test, evaluation indicator as particle size and EE.The physicochemical properties of the obtained QUE-CS-NPs were characterized by the following methods: the transmission electron microscope (TEM), dynamic light scattering (DLS) analysis for morphology, size distribution and Zeta potential.In vitro release behavior in 0.5% SDS solution was evaluated by dialysis tube method.In vitro antioxidant activity assays were performed by evaluating the abilities of the microspheres for hydroxide radicals and superoxide anions .Results TEM results revealed QUE-CS-NPs with round and uniform.Particle-size analysis showed that the diameters and Zeta potential of the QUE-CS-NPs were (282.9 ±20) nm and (30.5 ±2) mV, with uniform distribution (polydispersity below 0.185).DL and EE of QUE-CS-NPs were (8.81 ±0.65) %and (80.02 ±1.04) %, respectively.QUE-CS-NPs showed extended administration times with 66.2% cumulative release within 72 h.QUE-CS-NPs showed pronounced antioxidant activity and aconcentration dependent, even more substantial than that of pureQUE.Conclusion QUE-CS-NPs show a good size, sustain release effect and pronounce antioxidant activity.%目的:制备载槲皮素(quercetin,QUE)的壳聚糖纳米粒(chitosan nanoparticles,CS-NPs)并考察其理化特性及体外抗氧化活性。
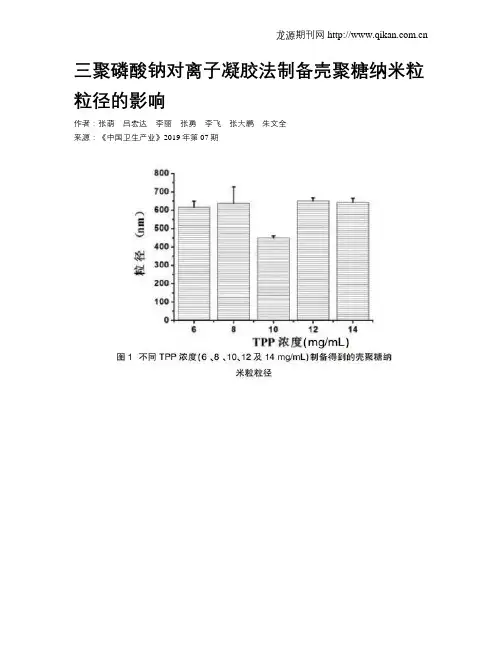
三聚磷酸钠对离子凝胶法制备壳聚糖纳米粒粒径的影响作者:张萌吕宏达李丽张勇李飞张大鹏朱文全来源:《中国卫生产业》2019年第07期[摘要] 目的研究三聚磷酸钠对壳聚糖纳米粒粒径的影响。
方法采用离子凝胶法制备壳聚糖纳米粒,考察三聚磷酸钠的浓度、滴加速度以及液滴大小等因素对壳聚糖纳米粒粒径的影响。
结果三聚磷酸钠在浓度(6~14 mg/mL)范围内对于壳聚糖纳米粒的粒径影响较小。
三聚磷酸钠滴加速度越快(1.0 s/滴以上),壳聚糖纳米粒的平均粒径越大。
当针头直径在0.50~0.60 mm范围内壳聚糖纳米粒的平均粒径随着针头直径的增加逐渐增大。
结论离子凝胶法制备壳聚糖纳米粒粒径主要受到三聚磷酸钠滴加速度以及三聚磷酸钠液滴大小的影响,受三聚磷酸钠浓度影响较小。
[关键词] 壳聚糖;三聚磷酸钠;纳米粒;粒径[中图分类号] R19 [文献标识码] A [文章编号] 1672-5654(2019)03(a)-0058-02壳聚糖(Chitosan,CS)是甲壳素最重要的衍生物,也是一种天然的碱性多糖,具有很好的生物相容性、生物活性以及生物降解性。
可生物降解的壳聚糖纳米粒也被广泛研究,壳聚糖纳米粒是集缓释、靶向以及控制药物释放等多功能于一体的天然纳米药物传递系统[1-3]。
壳聚糖纳米粒的制备方法包括凝聚/沉淀法、离子凝胶法以及乳滴聚结法等方法,其中离子凝胶法通过相反电荷相互作用发生物理交联反应,常采用多聚阴离子三聚磷酸钠(tripolyphosphate,TPP)与壳聚糖的氨基发生分子内或分子间的交联反应,从而形成球状凝胶的过程[4-5]。
TPP 是影响壳聚糖纳米粒粒径的重要因素,然而在国内外研究中,TPP对于壳聚糖纳米粒粒径影响的系统研究较少,因此该文对TPP的浓度、滴加速度以及液滴大小等因素对壳聚糖纳米粒粒径的影响进行了系统考察。
1; 材料与试剂1.1; 材料壳聚糖(江苏古贝生物科技有限责任公司);三聚磷酸钠(天津博迪化工股份有限公司);氢氧化钠、冰醋酸(天津市光复科技发展有限公司)。



第24卷第10期2007年10月沈 阳 药 科 大 学 学 报Journal of Shenyang Pharmaceutical University Vol 124 No 110 Oct 12007p 1593 收稿日期:2007201229作者简介:王宇(19812),女(汉族),天津人,硕士研究生,E 2m ail dlwy -81@ ;陈大为(19592),男(汉族),辽宁海城人,教授,主要从事药物新剂型设计与评价研究,T el .024*********,E 2m ail cdw2002yd @ 。
文章编号:100622858(2007)1020607204离子凝胶法制备水杨酸壳聚糖纳米粒王 宇,陈大为,乔明曦,王 薇,胡海洋,赵秀丽(沈阳药科大学药学院,辽宁沈阳110016)摘要:目的以壳聚糖为载体材料制备水杨酸壳聚糖纳米粒,并对其制备工艺及体系pH 值对药物包封率的影响进行考察,初步探讨壳聚糖纳米粒的载药机制。
方法以水杨酸为模型药物,采用离子凝胶法制备壳聚糖纳米粒,以包封率及粒径为指标,考察处方因素对纳米粒制备的影响。
结果壳聚糖浓度、体系的pH 值、药物质量浓度是影响制备工艺的主要因素;体系的pH 值可显著提高壳聚糖纳米粒的包封率。
结论药物与壳聚糖之间的离子相互作用较弱,并不是纳米粒载药的主要机制。
关键词:水杨酸;壳聚糖;离子凝胶法;纳米粒;包封率中图分类号:R 944 文献标志码:A 壳聚糖(chitosan )是甲壳素的脱乙酰衍生物,是一类由22氨基222脱氧葡萄糖通过β21,4糖苷键连接而成的带正电荷直链多糖。
壳聚糖来源广泛,廉价易得,且具有很好的生物相容性和生物可降解性,因此,壳聚糖作为药物载体材料的研究受到了极大的关注,壳聚糖纳米粒被认为是一类极具应用前景的药物载体。
壳聚糖载药纳米粒的主要制备方法包括共价交联、沉淀析出、大分子复合、自组装构筑和离子凝胶法等[1]。
与其他方法相比,离子凝胶法能在温和条件下迅速生成粒径几十至数百纳米的壳聚糖纳米粒,不需使用有机溶剂和醛类交联固化剂,反应过程简便迅速,所以很有实用价值[2-3]。


离子凝胶法制备壳聚糖纳米粒的研究进展【关键词】离子凝胶法;壳聚糖纳米粒近年来随着科学技术的发展,制药技术和药物剂型也有了很大的发展,出现了很多新剂型和新技术。
其中载药纳米微粒作为药物、基因传递和控释的载体。
是近年来出现的药物控释和缓释的新剂型。
引起了国内外的极大关注和兴趣。
纳米粒是由高分子物质组成,粒径在10-100nm范围,药物可以溶解、包裹于其中或吸附在表面上。
20世纪70年代,narty等人首先将纳米囊与纳米球作为药物载体,30多年来在药剂学领域得到广泛的推广。
壳聚糖作为一种天然的生物大分子,是自然界中唯一的碱性多糖,它具有生物可降解性、生物相容性、低毒性、良好的粘附性和成膜能力,且价格低廉。
因而被广泛应用于生物医学、制药工业和医疗卫生中。
壳聚糖纳米粒的制备方法有很多种,包括:共价交联法、离子凝胶法、大分子复合法、去溶剂化法、自组装法等。
其中离子凝胶法是制备壳聚糖纳米微球的一种简单、迅速的方法,该方法反应条件温和,无需使用有机溶剂,能得到坚固、稳定性好、粒径均匀的壳聚糖纳米微球[1]。
本文就离子凝胶法制备壳聚糖纳米粒的原理、质量评价以及体外释放性等做简单介绍。
1 离子凝胶法制备壳聚糖纳米粒的原理离子凝胶法是利用无毒副作用的三聚磷酸钠(tpp)对壳聚糖进行离子诱导凝胶化而制备纳米粒。
由于tpp中含有多个po-na十基团,而溶解于醋酸的壳聚糖分子链中又含有nh3+结构,类似于壳聚糖-tpp聚离子复合膜的成膜原理,二者发生反应:chitosan-nh3++tpp-po-→ chitosan-nh+—op-pp[2]。
壳聚糖载药纳米粒的形成主要是靠正负电荷之间的吸引作用,壳聚糖的伯氨基带有阳离子,它与带有阴离子的三聚磷酸钠在适宜的条件下交联并把药物包裹在其中形成载药纳米粒。
2 离子凝胶法制备壳聚糖纳米粒的工艺研究及其质量评价离子凝胶化法制备纳米粒有两种方法,即一步法和二步吸附法。
一步法是在纳米粒制备过程中直接加入药物,载体形成的同时将药物包裹进去,形成纳米粒;二步吸附法是先制得空白纳米粒,再将药物溶液与纳米粒混合吸附制得含药纳米粒。

硫酸庆大霉素-壳聚糖纳米粒的制备及性能评价李亮亮;王黎明;徐燕【摘要】BACKGROUND: Gentamicin beads as a local drug delivery system was earlier used for tie treatment of chronic osteomyelitis ofthe local drug delivery system, but due to its degradation and absorption in the body, it cannot be the second out, thus itsapplication is limited. Therefore, domestic and foreign scholars have been working to study absorbable materials loaded withantibiotics device.OBJECTIVE: To formulate the gentamicin sulfate-loaded chitosan nanospheres (GS-CS nanospheres) and to evaluate itsperformance and to study its releasing behavior and the anti-staph a u re us efficacy in vitro.METHODS: The GS-CS nanospheres were prepared by ion cross-linking technique using chitosan as drug carrier andgentamicin sulfate as model drug and sodium trip olyphosp hate as cross linker reagent. The drug loading and encapsulationefficiency were estimated. The releas ing behavior of the GS-CS nanospheres was studied and the diameter of inhibition zone ofthe GS-CS nanospheres was measured.RESULTS AND CONCLUSION: The nanospheres were s ph eric a I with the diameter ranging from 40 nmto 70 nm, theencapsulation efficiency and drug loading were estimated to be 31.3% and 15.4%, respectively, toirtn releasing behavior coufclco nti n ue a b o ut 14 days; th e a nt I-sta p h a u re us eff ica cy in vitro co u I d c o nti n u e a b o ut 25 days .the gr e atest a nti-staph a ureusefficacy reached at 5 days and then decreased gradually.%背景:庆大霉素珠链是较早用于治疗慢性骨髓炎的局部释药系统,但是由于其不能在体内降解吸收,须二次取出,因而限制了其的应用.因此国内外学者一直致力于可吸收材料负载抗生素装置的研究.目的:制备负载庆大霉素的壳聚糖纳米粒,评价其性能,观察其体外释药行为及体外抗金黄色葡萄球菌的作用.方法:以壳聚糖为药用载体,硫酸庆大霉素为模型药物,三聚磷酸钠为离子交联剂,采用离子交联法制备庆大霉素-壳聚糖纳米粒,在MH平板上进行抑菌实验,观察及评价其抑制金黄色葡萄球菌的作用.结果与结论:制备的纳米粒形态为类圆形,粒径为40~70 nm,包封率及载药量分别为31.3%和15.4%,体外释药可持续14 d左右,对金黄色葡萄球菌的体外抑菌效果可持续25 d,在第5天纳米粒的抑菌作用达到最大,随着时间的推移,抑菌圈逐渐缩小.【期刊名称】《中国组织工程研究》【年(卷),期】2011(015)042【总页数】4页(P7847-7850)【关键词】硫酸庆大霉素;壳聚糖;纳米粒;体外释放;骨髓炎【作者】李亮亮;王黎明;徐燕【作者单位】南京医科大学附属南京第一医院骨科,江苏省南京市,210001;南京医科大学附属南京第一医院骨科,江苏省南京市,210001;南京医科大学附属南京第一医院骨科,江苏省南京市,210001【正文语种】中文【中图分类】R3180 引言庆大霉素珠链是较早用于治疗慢性骨髓炎的局部释药系统[1-2],但是由于其不能在体内降解吸收,须二次取出,因而限制了其的应用。

离子凝胶法制备壳聚糖纳米粒的研究进展【关键词】离子凝胶法;壳聚糖纳米粒近年来随着科学技术的发展,制药技术和药物剂型也有了很大的发展,出现了很多新剂型和新技术。
其中载药纳米微粒作为药物、基因传递和控释的载体。
是近年来出现的药物控释和缓释的新剂型。
引起了国内外的极大关注和兴趣。
纳米粒是由高分子物质组成,粒径在10-100nm范围,药物可以溶解、包裹于其中或吸附在表面上。
20世纪70年代,Narty等人首先将纳米囊与纳米球作为药物载体,30多年来在药剂学领域得到广泛的推广。
壳聚糖作为一种天然的生物大分子,是自然界中唯一的碱性多糖,它具有生物可降解性、生物相容性、低毒性、良好的粘附性和成膜能力,且价格低廉。
因而被广泛应用于生物医学、制药工业和医疗卫生中。
壳聚糖纳米粒的制备方法有很多种,包括:共价交联法、离子凝胶法、大分子复合法、去溶剂化法、自组装法等。
其中离子凝胶法是制备壳聚糖纳米微球的一种简单、迅速的方法,该方法反应条件温和,无需使用有机溶剂,能得到坚固、稳定性好、粒径均匀的壳聚糖纳米微球[1]。
本文就离子凝胶法制备壳聚糖纳米粒的原理、质量评价以及体外释放性等做简单介绍。
1 离子凝胶法制备壳聚糖纳米粒的原理离子凝胶法是利用无毒副作用的三聚磷酸钠(TPP)对壳聚糖进行离子诱导凝胶化而制备纳米粒。
由于TPP中含有多个PO-Na十基团,而溶解于醋酸的壳聚糖分子链中又含有NH3+结构,类似于壳聚糖-TPP聚离子复合膜的成膜原理,二者发生反应:Chitosan-NH3++TPP-PO-→ Chitosan-NH+—OP-PP[2]。
壳聚糖载药纳米粒的形成主要是靠正负电荷之间的吸引作用,壳聚糖的伯氨基带有阳离子,它与带有阴离子的三聚磷酸钠在适宜的条件下交联并把药物包裹在其中形成载药纳米粒。
2 离子凝胶法制备壳聚糖纳米粒的工艺研究及其质量评价离子凝胶化法制备纳米粒有两种方法,即一步法和二步吸附法。
一步法是在纳米粒制备过程中直接加入药物,载体形成的同时将药物包裹进去,形成纳米粒;二步吸附法是先制得空白纳米粒,再将药物溶液与纳米粒混合吸附制得含药纳米粒。
离子凝胶法制备壳聚糖纳米粒的影响因素研究喻红英1 ,向娟2,林晓春1 ,李庆德1,郑锦坤\1.粤北人民医院,广东韶关512000;2.吉首大学,湖南吉首416000)摘要:目的探讨离子凝胶法制备壳聚糖纳米粒(CS-NPs)的影响因素。
方法用碱降解法制备高脱乙酰度的壳聚糖(CS), 并以之为材料,采用离子凝胶法制备CS-NPs,以微粒的平均粒径、分散度和Z eta电位为指标,考察C S及三聚磷酸钠(T P P)的 质量浓度、C S/T PP质量比、C S溶液p H值和C S溶液温度对制备CS-NPs的影响。
并用透射电子显微镜观察纳米粒的形态。
结果CS-NPs的平均粒径随CS、T P P质量浓度及C S/T PP质量比的增大而增大,C S/T PP质量比的增加、C S溶液p H值的降低可引起CS-NPs的Z eta电位增高,C S溶液p H值和温度对CS-NPs的分散度影响较大;制备的壳聚糖纳米粒形态较为规则,类 似球形。
结论C S及T P P的质量浓度、质量比、C S溶液p H值是制备壳聚糖纳米粒并影响其特征的主要因素。
关键词:壳聚糖;纳米粒;离子凝股法;影响因素中图分类号:R943 文献标志码:A 文章编号:1674-229X (2021)02-0124-04Doi : 10.12048/j. issn. 1674-229X.2021.02.009Study on Influencing Factors for Preparation of Chitosan Nanoparticles by Ionic Gelation TechniqueYU Hongying1 ,XIANG Juan2,LIN Xiaochun1 ,LI Qingde1 ,ZHENG Jinkun^l.Yue Bei People's Hospital,Shaoguan, Guangdong 512000, China;2. Jishou University, JLshou, Hunan416000, China )ABSTRACT:OBJECTIVE To explore the factors for the preparation of chitosan nanoparticles ( CS-NPs) by ionic gelation technique. METHODS Highly deacetylated chitosan ( CS) were prepared by alkaline degradation, land were used as materials to prepare CS-NPs by ionic gelation technique. Variations in CS mass concentration, sodium tripolyphosphate( TPP) mass concentration, CS to TPP mass ratio,pH value and temperature of CS solution were examined systematically for their effects on the perparatiopn of CS-NPs by using nanoparticle size, dispersion and zeta potential as indexes. Besides, the morphology of nanoparticle was observed by transmission electron microscope. RESULTS The nanoparticle average size was increased by increasing of CS mass concentration, TPP mass concentration and CS/TPP mass ratio. When CS to TPP mass ratio increased and pH value of CS solution decreased, zeta potential increased. The pH value and temperature of CS solution had great influence on the dispersion of CS-NPs. Chitosan nanoparticles had a regular shape quite like a sphere. CONCLUSION CS mass concentration,TPP mass concentration, CS/TPP mass ratio and pH value of CS are the main factors influencing the preparation and characteristics of CS-NPs.KEY WORDS:chitosan;nanoparticles;ionic gelation;influencing factors壳聚糖(chit〇san,CS)是甲壳素经过脱乙酰基后 得到的一种可生物降解的多糖类物质,具有生物相 容性好、细胞毒性小、价廉易得等优点,近年来已成 为医药领域的研究热点[〜。
壳聚糖纳米粒及其制备方法壳聚糖纳米粒是一种具有广泛应用前景的纳米材料,其制备方法也备受关注。
本文将介绍壳聚糖纳米粒的特性、应用以及常用的制备方法。
1. 壳聚糖纳米粒的特性壳聚糖纳米粒是由壳聚糖分子聚集形成的纳米尺度的颗粒。
壳聚糖是一种天然多糖,具有生物相容性好、生物降解性高、低毒性等特点,因此在医药、食品、化妆品等领域有广泛应用。
壳聚糖纳米粒具有较大的比表面积和高度的表面活性,可以用作药物载体、基因传递体和生物传感器等。
2. 壳聚糖纳米粒的应用壳聚糖纳米粒在医药领域中广泛应用于药物传递系统。
其纳米粒子的尺寸和表面性质可以通过调节制备方法进行调控,从而实现对药物的控制释放和靶向输送,提高药物的疗效和减少副作用。
此外,壳聚糖纳米粒也被用作生物传感器的敏感材料,可以用于检测生物分子和环境污染物等。
3. 壳聚糖纳米粒的制备方法常用的壳聚糖纳米粒制备方法包括离子凝胶法、乳化法、溶剂蒸发法等。
离子凝胶法是将壳聚糖与交联剂反应,形成凝胶颗粒,再经过处理得到纳米粒。
乳化法是将壳聚糖溶解于有机溶剂中,与乳化剂进行乳化,再通过溶剂挥发得到纳米粒。
溶剂蒸发法是将壳聚糖溶解于有机溶剂中,与溶剂不相溶的非溶剂混合均匀,通过溶剂蒸发得到纳米粒。
4. 制备方法的优缺点比较离子凝胶法制备的壳聚糖纳米粒尺寸一般较大,但有较好的稳定性和可控性,适用于药物传递系统的制备。
乳化法制备的壳聚糖纳米粒尺寸较小,但稳定性较差,适用于生物传感器的制备。
溶剂蒸发法制备的壳聚糖纳米粒具有较好的稳定性和尺寸可控性,适用于药物传递和生物传感器等领域。
壳聚糖纳米粒具有广泛的应用前景,其制备方法多样,可根据具体需求选择合适的方法进行制备。
未来随着纳米材料研究的深入,壳聚糖纳米粒的应用领域还将不断拓展,为人类的生活和健康带来更多的益处。
壳聚糖纳米粒的制备、表征及生物学效应研究的开题报告一、研究背景和意义:壳聚糖(Chitosan)是一种天然产物,具有良好的生物相容性和生物降解性,因此被广泛应用于生物医学领域。
随着纳米技术的发展,壳聚糖纳米粒成为一种重要的纳米载体,具有广阔的应用前景。
壳聚糖纳米粒具有很高的比表面积、良好的生物相容性、可调控的形貌和表面性质等特点,能够在药物输送、基因传递、组织工程等领域中发挥重要作用。
目前,壳聚糖纳米粒制备技术已经得到发展,但还存在一些挑战,如粒径分布较大、稳定性差、药物的包封率和释放性能有待优化等问题。
因此,本研究旨在通过改进壳聚糖纳米粒的制备方法,探究其对细胞的生物学效应,以提高其在药物输送和组织工程方面的应用价值。
二、研究内容和方法:(1)制备壳聚糖纳米粒:采用离子凝胶法制备壳聚糖纳米粒,并对其粒径、分散性、Zeta电位等进行表征。
通过优化制备条件,提高壳聚糖纳米粒的质量和稳定性。
(2)药物输送性能研究:将壳聚糖纳米粒与药物包封,并探究其在体外释放的性能。
通过荧光显微镜、细胞毒性实验等方法,评估壳聚糖纳米粒在体内输送药物的效果和安全性。
(3)细胞生物学效应研究:使用不同细胞系(如肝癌细胞、肺癌细胞、肝细胞等)探究壳聚糖纳米粒的细胞毒性、吞噬作用和细胞代谢效应。
测试壳聚糖纳米粒对细胞增殖、凋亡、减轻毒副作用等方面的作用。
三、预期成果:通过本研究,预计获得以下成果:(1)成功制备具有优异性能的壳聚糖纳米粒,并对其进行粒径、分散性、Zeta电位等方面的表征。
(2)优化壳聚糖纳米粒载药体系,并探究其体外释放性能和体内安全性。
(3)研究壳聚糖纳米粒在不同细胞系中的生物学效应,提供关于壳聚糖纳米粒生物学特性的新认识。
四、研究意义:(1)本研究将为壳聚糖纳米粒的制备和应用提供一定的理论基础和实验依据。
(2)优化制备方法并提高壳聚糖纳米粒质量和稳定性,有助于提高其在医学领域的应用价值。
(3)通过探究壳聚糖纳米粒的生物学效应,有助于了解其与细胞及健康人体的相互作用,为壳聚糖纳米粒的临床应用提供参考。
制备壳聚糖纳米粒的影响因素考察
【摘要】本文主要以粒径为壳聚糖纳米粒的评价指标,通过对乳化交联法和离子凝聚法(Sodium Polyphosphate做交联剂)制备壳聚糖纳米粒的影响因素考察,确定摩尔分子量是影响制备壳聚糖纳米粒的关键因素.对于乳化交联法,分别考察了机械搅拌法和高压均质法这两种乳化的方法的各种影响因素。
对于离子凝聚法,考察的影响因素包括加入顺序、不同规格壳聚糖、药物曲尼司特、多聚磷酸钠的浓度和用量等。
结果证明乳化交联法只能制备出微米级的粒子,而离子交联法只能制备出粒子浓度特别低的纳米粒溶液。
【关键词】壳聚糖,纳米粒,曲尼司特,离子交联法
1仪器与材料
1.1实验仪器
高压均质机Emulsiflex—CSAvestin
微米粒度仪Zetasizer Malvern instrument Ltd.
BS110S型电子天平北京赛多利斯天平公司
KQ-250超声仪中国江苏昆山超声仪
纳米粒子测定仪Zetasizer 3000HSaMalvern
1.2实验试剂及药品
戊二醛溶液(25%)国药集团化学试剂有限公司
多聚磷酸钠(Polyphosphate Sodium,TPP)国药集团化学试剂有限公司
多种规格壳聚糖Zhejiang Aoxing Biotechnology
曲尼司特原料药中国药科大学制药厂
2实验方法和结果
本实验制备壳聚糖纳米粒主要采用了两种方法,一是乳化交联法[1],另一个是离子凝聚法[2]。
乳化交联法中影响壳聚糖纳米粒的主要因素有:乳化方法,搅拌方法,交联时间,交联剂的用量,壳聚糖的用量等。
离子凝聚法制备壳聚糖纳米粒得主要影响因素有:壳聚糖的分子量,壳聚糖的浓度和用量,药物的浓度和用量,交联剂的浓度和用量等。
2.1乳化交联法中搅拌方式对制备壳聚糖纳米粒的影响[3]将100ml 浓度为2.5%(W/V)的壳聚糖(分子量330万),加入20ml2.78mg/ml的曲尼司特药物溶液(溶剂为乙醇:丙酮=1:1),再加入20ml液体石蜡,加入数滴吐温80,用高压均质机300Bar乳匀后,得到120ml的乳剂。
取4份22毫升的乳液分别用20毫升水稀释,加入15.7毫升的戊二醛溶液,分别用200、600、1400转/分的机械搅拌和磁力搅拌2小时。
用微米粒度仪测定粒径结果见表1。
Tab.1 The effect of different stirring methods on nanoparticle size
由表中可以看出,随着机械搅拌速度的增加粒径变大。
而相同条件下采用磁力搅拌处理得到的微球的粒径分布范围变窄,大小相差不大。
所以此后胶联时主要采用磁力搅拌进行处理。
2.2交联剂用量、交联时间、温度和初乳的浓度对制备壳聚糖纳米粒的影响
2.2.1高压均质法制备初乳[4]将125ml 浓度为2.5%(W/V)的壳聚糖(黏均分子量330万),加入20ml2.78mg/ml的曲尼司特的药物溶液(溶剂为乙醇:丙酮=1:1),再加入20ml液体石蜡,加入数滴吐温80,用高压均质机600Bar乳匀后,得到115ml的初乳。
2.2.2交联法制备微(纳)米球每次取12ml上述初乳,按照下表进行处理。
即将初乳稀释,加水至C倍原体积,在温度D水浴条件下,磁力搅拌下滴加体积为B的交联剂戊二醛溶液(25%),继续搅拌A小时,之后用石油醚萃取三次,得到壳聚糖微球的混悬液,用马尔文微米粒度仪测定大小分布。
结果见表2。
A 是交联时间,分为1、2、3小时三个水平;B是交联剂用量,是对初乳中所含2.5%壳聚糖溶液的体积的倍数,分为0.5、1.0、1.5倍三个水平;C是初乳稀释的倍数,分为4、6、8倍三个水平;D是水浴温度,分为30、40、50℃三个水平。
Tab.2Investigation of different influential factors in preparing nanoparticles by orthogonal test (L934)
从结果看出,第七和九个实验得到粒径分布范围比较集中,虽然制备的粒子没有达到纳米级别,但此后在进行对初乳进行交联处理时仍主要采用这两个方式。
2.3乳化交联法中压力对制备壳聚糖纳米粒的影响采用2因素2水平的星点复合设计考察高压均质时压力和壳聚糖用量两个因素对制备初乳的影响,压力(A),两水平300和800bar,壳聚糖体积(B)两水平40和120ml,考察对制备壳聚糖纳米粒的影响。
固定液体石蜡的量20ml,取制备的初乳16ml,用表2中的第七种方法实验,结果见表
3.
Tab.3Investigation the influences of pressure and chitosan amount in preparing
nanoparticles by center design
用设计软件Design Expert6.0.10分析,最后得到结果如下:以水平代码表示的方程Response=+1.77+0.29* A-0.64* B,从结果可以看出,制备的粒子主要是微米级别,而且变化都是在同一数量级内发生,所以压力对用高压均质法制备壳聚糖纳米粒粒径影响不大。
2.4离子凝聚法中壳聚糖分子量、浓度和交联剂的用量对制备空白壳聚糖纳米粒的影响
离子凝聚法制备空白壳聚糖纳米粒的基本方法:配制浓度为 1.0mg/ml和2.0mg/ml的壳聚糖溶液25ml,室温磁力搅拌下分别用恒流泵加入2.0、4.0、6.0ml 的1.0 mg/ml多聚磷酸钠溶液(Sodium Polyphosphate,TPP),加入速度为1ml/min,搅拌30分钟后停止搅拌,静置20min,用双层纱布和G-1漏斗过滤后,用纳米粒度仪测定。
记录每一种壳聚糖粒子的最小粒径,结果见表4和图3。
从结果看出,纳米粒分散指数较大,粒径在261nm以上。
Tab.4 The influences of chitosan(CS) molecular weight and sodium polyphosphate(TPP) amounts in preparingnanoparticles
Fig.3Particle size of blank nanoparticles prepared with different molecular weight chitosan:(A)MW=594,000, (B)MW=875,000,(C)MW=906,000(D)MW=330,000,(E)MW=400,000
2.5离子凝聚法载药壳聚糖纳米粒的制备将分子量分别为59.4万、87.5万、90.6万、330万和400万的壳聚糖溶解成0.5、1.0、2.0mg/ml的溶液,室温磁力搅拌下,加入药物溶液或药物与TTP的混合液,加入后即见到肉眼可见蓝色悬浮物,搅拌一定时间后,用0.8um滤膜过滤,滤液中几乎得不到纳米粒。
药物浓度为1.0mg/ml,溶解药物主要使用三种溶剂:一是pH大于10.0的强碱性NaOH 水溶液;二是乙醇和丙酮等份的混合溶剂;三是添加增溶剂聚乙二醇400的中性水溶液。
这表明这些高分子量的壳聚糖均不能制成载曲尼司特的壳聚糖纳米粒。
3讨论
通过对乳化交联法制备壳聚糖纳米粒的各种影响因素的考察,发现高压均质法优于机械搅拌法,对制备得初乳的处理方式都是一样,说明两者之间的差异主要是制备的初乳的乳滴大小不同,这一点也已通过实验证明。
高压均值法制备乳剂时,油相采用的是液体石蜡,造成清洗高压均质机时消耗大量的丙酮和和乙醇,试验成本高而且不环保。
离子凝聚法制备工艺简单,成本低,通过各种影响因素考察发现,壳聚糖分子量是影响粒子粒径的主要因素。
制备时发现,无论何种高分子量的壳聚糖溶液,只要加入即使是浓度很低的药物溶液都会产生大的悬浮物,随着壳聚糖分子量的增大,最后过滤除掉的大的悬浮物越多,虽然从图3看来,制备的粒子达到了纳
米级别,但是多分散指数太大,而且产率太低,原料和辅料浪费严重。
因此下一步工作,从壳聚糖的分子量方面着手,对壳聚糖进行降解,制备低分子量的壳聚糖。
参考文献
[1] 赵琳琳,韩刚,宋树美等. 姜黄素壳聚糖微球的制备及体外药物释放研究[J].中药材2007,30(2):230-232.
[2] 陈浮,黄园. 尿素酶三甲基壳聚糖亚微球的制备及其相关性质的初步研究[J].华西药学杂志2007,22(1): 012-014.
[3] 张艳华,魏玉辉,刘志红等. 苦参碱壳聚糖微球的制备及体外释药[J].中国医院药学杂志2006,26 (3):307-310.
[4] 古永红,王连艳,谭天伟等. 尺寸均一的壳聚糖微球的制备及其作为胰岛素控释载体的研究[J].生物工程学报2006,22(1):150-155
通讯作者:李飞豹
注:本文中所涉及到的图表、注解、公式等内容请以PDF格式阅读原文。