第一章 基本概念
- 格式:ppt
- 大小:433.50 KB
- 文档页数:31

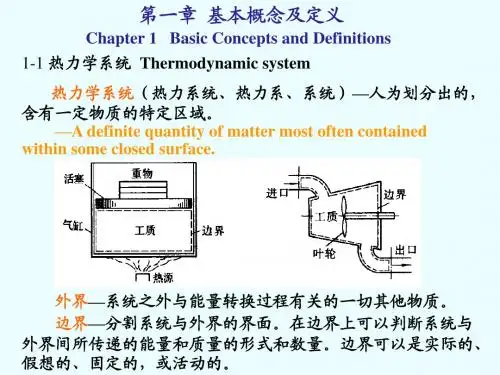



第一章基本概念与定义1。
闭口系与外界无物质交换,系统内质量保持恒定,那么系统内质量保持恒定的热力系一定是闭口系统吗? 答:不一定.稳定流动开口系统内质量也可以保持恒定.2.有人认为,开口系统中系统与外界有物质交换,而物质又与能量不可分割,所以开口系统不可能是绝热系。
对不对,为什么?答:这种说法是不对的。
工质在越过边界时,其热力学能也越过了边界。
但热力学能不是热量,只要系统和外界没有热量地交换就是绝热系。
3.平衡状态与稳定状态有何区别和联系,平衡状态与均匀状态有何区别和联系?答:只有在没有外界影响的条件下,工质的状态不随时间变化,这种状态称之为平衡状态。
稳定状态只要其工质的状态不随时间变化,就称之为稳定状态,不考虑是否在外界的影响下,这是他们的本质区别.平衡状态并非稳定状态之必要条件.物系内部各处的性质均匀一致的状态为均匀状态。
平衡状态不一定为均匀状态,均匀并非系统处于平衡状态之必要条件。
4。
倘使容器中气体的压力没有改变,试问安装在该容器上的压力表的读数会改变吗?绝对压力计算公式b e p p p =+()e p p >,b e p p p =-()e p p <中,当地大气压是否必定是环境大气压?答:压力表的读数可能会改变,根据压力仪表所处的环境压力的改变而改变.当地大气压不一定是环境大气压。
环境大气压是指压力仪表所处的环境的压力。
5.温度计测温的基本原理是什么?答:选作温度计的感应元件的物体应具备某种物理性质随物体的冷热程度不同有显著的变化。
有两个系统分别和第三个系统处于热平衡,则两个系统彼此必然处于热平衡。
6.经验温标的缺点是什么?为什么?答:任何一种经验温标不能作为度量温度的标准.由于经验温标依赖于测温物质的性质,当选用不同测温物质的温度计、采用不同的物理量作为温度的标志来测量温度时,除选定为基准点的温度,其他温度的测定值可能有微小的差异。
7。
促使系统状态变化的原因是什么?举例说明答:系统内部各部分之间的传热和位移或系统与外界之间的热量的交换与功的交换都是促使系统状态变。

基本概念第一章数和数的运算一概念(一)整数1整数的意义:自然数和0都是整数。
2自然数:我们在数物体的时候,用来表示物体个数的1,2,3……叫做自然数。
一个物体也没有,用0表示。
0也是自然数。
3计数单位一(个)、十、百、千、万、十万、百万、千万、亿……都是计数单位。
每相邻两个计数单位之间的进率都是10。
这样的计数法叫做十进制计数法。
4数位:计数单位按照一定的顺序排列起来,它们所占的位置叫做数位。
5数的整除整数a除以整数b(b≠0),除得的商是整数而没有余数,我们就说a 能被b整除,或者说b能整除a。
如果数a能被数b(b≠0)整除,a就叫做b的倍数,b就叫做a的约数(或a的因数)。
倍数和约数是相互依存的。
因为35能被7整除,所以35是7的倍数,7是35的约数。
一个数的约数的个数是有限的,其中最小的约数是1,最大的约数是它本身。
例如:10的约数有1、2、5、10,其中最小的约数是1,最大的约数是10。
一个数的倍数的个数是无限的,其中最小的倍数是它本身。
3的倍数有:3、6、9、12……其中最小的倍数是3,没有最大的倍数。
个位上是0、2、4、6、8的数,都能被2整除,例如:202、480、304,都能被2整除。
个位上是0或5的数,都能被5整除,例如:5、30、405都能被5整除。
一个数的各位上的数的和能被3整除,这个数就能被3整除,例如:12、108、204都能被3整除。
一个数各位数上的和能被9整除,这个数就能被9整除。
能被3整除的数不一定能被9整除,但是能被9整除的数一定能被3整除。
一个数的末两位数能被4(或25)整除,这个数就能被4(或25)整除。
例如:16、404、1256都能被4整除,50、325、500、1675都能被25整除。
一个数的末三位数能被8(或125)整除,这个数就能被8(或125)整除。
例如:1168、4600、5000、12344都能被8整除,1125、13375、5000都能被125整除。



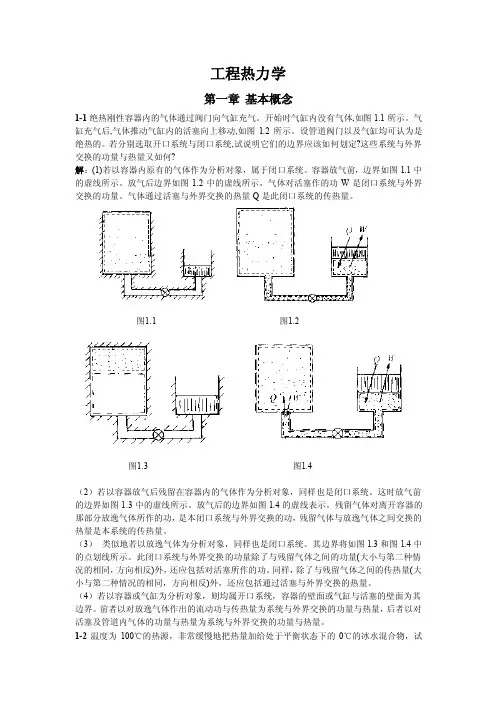
工程热力学第一章基本概念1-1绝热刚性容器内的气体通过阀门向气缸充气。
开始时气缸内没有气体,如图1.1所示。
气缸充气后,气体推动气缸内的活塞向上移动,如图1.2所示。
设管道阀门以及气缸均可认为是绝热的。
若分别选取开口系统与闭口系统,试说明它们的边界应该如何划定?这些系统与外界交换的功量与热量又如何?解:(1)若以容器内原有的气体作为分析对象,属于闭口系统。
容器放气前,边界如图1.1中的虚线所示。
放气后边界如图1.2中的虚线所示。
气体对活塞作的功W是闭口系统与外界交换的功量。
气体通过活塞与外界交换的热量Q是此闭口系统的传热量。
图1.1 图1.2图1.3 图1.4(2)若以容器放气后残留在容器内的气体作为分析对象,同样也是闭口系统。
这时放气前的边界如图1.3中的虚线所示。
放气后的边界如图1.4的虚线表示。
残留气体对离开容器的那部分放逸气体所作的功,是本闭口系统与外界交换的功,残留气体与放逸气体之间交换的热量是本系统的传热量。
(3)类似地若以放逸气体为分析对象,同样也是闭口系统。
其边界将如图1.3和图1.4中的点划线所示。
此闭口系统与外界交换的功量除了与残留气体之间的功量(大小与第二种情况的相同,方向相反)外,还应包括对活塞所作的功。
同样,除了与残留气体之间的传热量(大小与第二种情况的相同,方向相反)外,还应包括通过活塞与外界交换的热量。
(4)若以容器或气缸为分析对象,则均属开口系统,容器的壁面或气缸与活塞的壁面为其边界。
前者以对放逸气体作出的流动功与传热量为系统与外界交换的功量与热量,后者以对活塞及管道内气体的功量与热量为系统与外界交换的功量与热量。
1-2温度为100℃的热源,非常缓慢地把热量加给处于平衡状态下的0℃的冰水混合物,试问:1、冰水混合物经历的是准静态过程吗?2、加热过程是否可逆?解:此热力过程为准静态过程,因为此热力过程的弛豫时间很短,热源非常缓慢地把热量加给冰水混合物,则冰水混合物重建热力平衡的时间远远小于传热过程对冰水混合物平衡状态的破坏,所以可以近似地把此热力过程看作是准静态过程。

工程热力学与传热学第一章基本概念典型问题分析典型问题一.基本概念分析1闭口系统具有恒定的质量,但具有恒定质量的系统不一定就是闭口系统。
2孤立系统一定是闭口的,反之则不然。
3孤立系统一定是绝热系统,但绝热系统不一定都是孤立的。
4孤立系统的热力学状态不能发生变化。
5平衡状态的系统不一定是均匀的,均匀系统则一定处于平衡状态。
6摄氏温度的零点相当于热力学温度的273.15K。
7只有绝对压力才能表示工质所处的状态,才是状态参数。
8只有平衡状态,才能用状态参数坐标图上的一点来表示。
9非平衡状态,因为没有确定的状态参数,无法在状态参数坐标图中表示。
10不平衡过程,一定是不可逆过程;11不可逆过程就是指工质不能恢复原来状态的过程;12一个可逆过程必须同时也是一个准平衡过程,但准平衡过程不一定是可逆的。
13实际过程都是不可逆过程。
14功可以全部转变为热,但热不能全部转变为热15质量相同的物体A和B,若T A >T B,则物体A具有的热量比物体B多。
二.计算题分析1测得容器内气体的表压力为0.25MPa,当地大气压为755mmHg,求容器内气体的绝对压力p,并分别用(1)MPa(兆帕);(2)bar(巴);(3)atm(物理大气压);(4)at(工程大气压)表示。
2某种气体工质从状态1(p1,V1)可逆地膨胀到状态2。
膨胀过程中:(1)工质的压力服从p=a-bV,其中a,b为常数;(2)工质的pV保持恒定为p1V1。
试分别求两过程中气体的膨胀功。
3利用体积为2m3的储气罐中的压缩空气给气球充气,开始时气球内完全没有气体,呈扁平状,可忽略其内部容积。
设气球弹力可忽略不计,充气过程中气体温度维持不变,大气压力为0.9 ╳105Pa。
为使气球充到2m3,问气罐内气体最低初压力及气体所作的功是多少?已知空气满足状态方程式pV=mR g T。
分析解答一. 基本概念分析解答1 √;2 √;3 √;4 ╳;5 √;6 √;7 √;8 √;9 √;10 √;11 ╳;12 √;13 √;14 ╳;15 ╳;二. 计算题分析解答1 解:依据: Pa Pa Pa p Pa mmHg p p p b e 66107305.04322.1337551025.04332.1331,⨯=⨯+⨯==+=单位换算:at Pa Pa atm PaPa bar Pa Pa MPa PaPa 7575.35.06698107305.0)4(7460.3325101107305.0)3(057.310107305.0)2(7305.010107305.01665666=⨯=⨯=⨯=⨯)( 2 解:过程为可逆过程: 1211212121212221122121ln )2()(2)()(1V V V p V dV pV pdV W V V b V V a dV bV a pdV W ===---=-==⎰⎰⎰⎰--)( 分析:在上述两过程中,系统的初,终态相同,但中间途径不同,因而气体的膨胀功也不同。
第一章知识点一、知识结构:本章知识主要分为集合、简单不等式的解法(集合化简)、简易逻辑三部分:二、知识回顾: (一)集合1. 基本概念:集合、元素;有限集、无限集;空集、全集;符号的使用.2. 集合的表示法:列举法、描述法、图形表示法.3. 集合元素的特征:确定性、互异性、无序性.4. 集合运算:交、并、补.{|,}{|}{,}A B x x A x B A B x x A x B A x U x A ⇔∈∈⇔∈∈⇔∈∉U 交:且并:或补:且C 5. 主要性质和运算律 (1) 包含关系:,,,,,;,;,.U A A A A U A U A B B C A C A B A A B B A B A A B B ⊆Φ⊆⊆⊆⊆⊆⇒⊆⊆⊆⊇⊇C(2) 等价关系:U A B A B A A B B A B U ⊆⇔=⇔=⇔=C (3) 集合的运算律:交换律:.;A B B A A B B A ==结合律:)()();()(C B A C B A C B A C B A == 分配律:.)()()();()()(C A B A C B A C A B A C B A == 0-1律:,,,A A A UA A UA U Φ=ΦΦ===等幂律:.,A A A A A A ==求补律:A ∩ U A =φ A ∪ U A =U U U =φ U φ=U U U ( U A )=A 反演律: U (A ∩B)= ( U A )∪( U B ) U (A ∪B)= ( U A )∩( U B )6. 有限集的元素个数定义:有限集A 的元素的个数叫做集合A 的基数,记为card( A)规定 card(φ) =0.基本公式:(1)()()()()(2)()()()()()()()()card A B card A card B card A B card A B C card A card B card C card A B card B C card CA card ABC =+-=++---+(3) card ( U A )= card(U)- card(A)(二)含绝对值不等式、一元二次不等式的解法及延伸 1.整式不等式的解法 根轴法(零点分段法)①将不等式化为a 0(x-x 1)(x-x 2)…(x-x m )>0(<0)形式,并将各因式x 的系数化“+”;(为了统一方便) ②求根,并在数轴上表示出来;③由右上方穿线,经过数轴上表示各根的点(为什么?);④若不等式(x 的系数化“+”后)是“>0”,则找“线”在x 轴上方的区间;若不等式是“<0”,则找“线”在x 轴下方的区间.+-+-x 1x 2x 3x m-3x m-2xm-1x mx(自右向左正负相间)则不等式)0)(0(0022110><>++++--a a x a x a x a n n n n 的解可以根据各区间的符号确定.特例① 一元一次不等式ax>b 解的讨论;②一元二次不等式ax 2+box>0(a>0)解的讨论. 0>∆ 0=∆ 0<∆二次函数c bx ax y ++=2 (0>a )的图象一元二次方程有两相异实根)(,2121x x x x <有两相等实根abx x 221-==无实根2.分式不等式的解法 (1)标准化:移项通分化为)()(x g x f >0(或)()(x g x f <0);)()(x g x f ≥0(或)()(x g x f ≤0)的形式, (2)转化为整式不等式(组)⎩⎨⎧≠≥⇔≥>⇔>0)(0)()(0)()(;0)()(0)()(x g x g x f x g x f x g x f x g x f 3.含绝对值不等式的解法(1)公式法:c b ax <+,与)0(>>+c c b ax 型的不等式的解法.(2)定义法:用“零点分区间法”分类讨论.(3)几何法:根据绝对值的几何意义用数形结合思想方法解题. 4.一元二次方程根的分布一元二次方程ax 2+bx+c=0(a ≠0) (1)根的“零分布”:根据判别式和韦达定理分析列式解之. (2)根的“非零分布”:作二次函数图象,用数形结合思想分析列式解之. (三)简易逻辑1、命题的定义:可以判断真假的语句叫做命题。
工程热力学概念第一章基本概念1.热力系:就是具体指定的研究对象。
(用界面将所要研究的对象将周围环境分开,这种人为分割的研究对象,称为热力系统。
)2.边界:分割系统与外界的分界面称为边界。
3.外界:与热力系有相互作用的周围物体称为外界。
4.根据热力系内部情况不同,热力系可分为:单元系:由单一化学成分组成。
多元系:由多种化学成分组成。
单相系:由单一的相组成。
复相系:由多种相组成。
均匀系:各部分性质均匀一致。
非均匀系:各部分性质不均匀。
5.根据热力系和外界相互作用情况不同,热力系可分为:闭口系:和外界无物质交换。
开口系:和外界有物质交换。
绝热系:和外界无热量交换。
孤立系:和外界无任何相互作用。
6.状态:是热力系在指定瞬间所呈现的全部宏观性质的总称。
7.状态参数:从各个不同方面描写宏观状态的物理量称为工质的状态参数。
8.基本状态参数:在工程热力学中常用的状态参数有6个,即压力、比体积、温度、热力学能、焓和熵。
其中压力、比体积、温度可以直接测量,也比较直观,称为基本状态参数。
9.真空度:当气体的绝对压强低于大气压力时,真空计所指示的是绝对压力低于大气压的部分,称为真空度。
10.热力学能:组成热力系的大量微观粒子本身所具有的能量(不包括热力系宏观运动的能量和外场作用的能量)。
11.比热力学能:单位质量物质的热力学能称为比热力学能。
12.平衡状态:是指热力系在没有外界作用的情况下宏观性质不随时间变化的状态。
13.简单热力系:和外界只有热能和机械能交换的热力系统称为简单热力系。
14.过程:是指热力系从一个状态向另一个状态变化时所经历的全部状态的总和。
15.内平衡过程:热力系从一个平衡(均匀)状态连续经历一系列(无数个)平衡的中间状态过渡到另一个平衡状态,这样的过程称为内平衡过程。
内平衡过程也称作准静态过程。
16.循环过程:热力系从某一状态开始,经过一系列中间状态后,有回复到原来状态。
17.做功量:热力系通过界面和外界进行的机械能的交换量称为做功量,简称功。