质量守恒定律专题复习
- 格式:ppt
- 大小:288.50 KB
- 文档页数:16




质量守恒定律复习题含答案一、选择题1.重铬酸钾(K2Cr2O7)可用于测定酒驾中的酒精(C2H5OH)含量,下列说法正确的是()A.K2Cr2O7中铬元素的化合价为+7B.K2Cr2O7属于氧化物C.C2H5OH中氢元素的质量分数最小D.C2H5OH中C、H、O的原子个数比为2:5:1解析:C【解析】【详解】A.钾元素显+1价,氧元素显﹣2价,设铬元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:(+1)×2+2x+(﹣2)×7=0,则x=+6价;故选项说法错误。
B.K2Cr2O7是由钾、铬、氧三种元素组成的化合物,不属于氧化物,故选项说法错误。
C.乙醇中碳、氢、氧元素的质量比为:(12×2):(1×6):16=12:3:8,可见其中氢元素的质量分数最小,故正确;D.1个分子由2个碳原子、6个氢原子和1个氧原子构成,则C2H5OH中C、H、O的原子个数比为2:6:1,故选项说法错误。
故选:C。
2.如图是微信热传的“苯宝宝表情包”,苯(化学式C6H6)、六氯苯(化学式C6Cl6)都是重要的化工原料,下列有关说法正确的是()A.苯分子由碳、氢两种元素组成B.苯中氢元素的质量分数小于10%C.六氯苯中碳氯两种元素的质量比为1:1D.六氯苯有6个碳原子和6个氯原子构成解析:B【解析】【分析】【详解】A、苯是由苯分子构成的,苯是由碳元素与氢元素组成的,说法错误;故不符合题意;B、苯中氢元素的质量分数为16100%7.7%<10%16+126⨯⨯≈⨯⨯,说法正确;故符合题意;C、由六氯苯的化学式C6Cl6。
可知,其中碳元素和氯元素的质量比为:(12×6):(35.5×6)=12:35.5,说法错误;故不符合题意;D、一个六氯苯分子由6个碳原子和6个氯原子构成,说法错误;故不符合题意;故选B【点睛】本题难度不大,考查同学们结合新信息、灵活运用化学式的含义与有关计算进行分析问题、解决问题的能力。




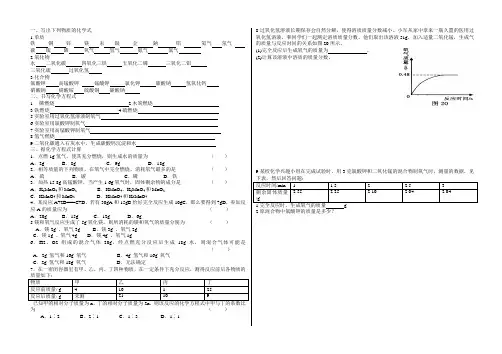
一、写出下列物质的化学式 1.单质 铁 铜 锌 镁 汞 银 金 鈉 铝 氦气 氖气 碳 硫 磷 氧气 氢气 氮气 氯气 2.氧化物 水 二氧化碳 四氧化三铁 五氧化二磷 三氧化二铝三氧化硫 过氧化氢 3.化合物 氯酸钾 高锰酸钾 锰酸钾 氯化钾 碳酸钠 氢氧化钙硝酸钠 硝酸铵 硫酸铜 碳酸钠 二、书写化学方程式 1. 磷燃烧 2.木炭燃烧 3.铁燃烧 4.硫燃烧 5.实验室用过氧化氢溶液制氧气 6.实验室用氯酸钾制氧气 7.实验室用高锰酸钾制氧气 8.氢气燃烧 9.二氧化碳通入石灰水中,生成碳酸钙沉淀和水 三、据化学方程式计算 1.点燃1g 氢气,使其充分燃烧,则生成水的质量为 ( ) A .2g B .8g C .9g D .18g 2.相等质量的下列物质,在氧气中完全燃烧,消耗氧气最多的是 ( ) A .硫 B .碳 C .磷 D .铁 3.加热15.8g 高锰酸钾,当产生1.6g 氧气时,固体剩余物的成分是 ( ) A .K 2MnO 4和MnO 2 B .KMnO 4、K 2MnO 4和MnO 2 C .KMnO 4和MnO 2 D .KMnO 4和K 2MnO 4 4.某反应A+2B===C+D ,若有30gA 和15gB 恰好完全反应生成10gC ,那么要得到7gD ,参加反应A 的质量应为 ( ) A .20g B .15g C .12g D .6g5.镁和氧气反应生成了5g 氧化镁,则所消耗的镁和氧气的质量分别为 ( )A .镁2g 、氧气3gB .镁3g 、氧气2gC .镁1g 、氧气4gD .镁4g 、氧气1g6.H2、O2组成的混合气体20g ,经点燃充分反应后生成18g 水,则混合气体可能是( )A .2g 氢气和16g 氧气B .4g 氢气和16g 氧气C .2g 氢气和18g 氧气D .无法确定7.在一密闭容器里有甲、乙、丙、丁四种物质,在一定条件下充分反应,测得反应前后各物质的质量如下:物质 甲 乙 丙 丁反应前质量/ g4 10 1 25 反应后质量/ g 未测21 10 9 已知甲的相对分子质量为n ,丁的相对分子质量为2n ,则该反应的化学方程式中甲与丁的系数比为 ( )A .1∶2B .2∶1C .1∶3D .1∶18.过氧化氢溶液长期保存会自然分解,使得溶质质量分数减小。


化学学科精讲精练——质量守恒定律及相关计算专题知识点一、质量守恒定律1.概念:参加反应的反应物质量总和等于反应生成的生成物质量总和2.适用范围:(1)只适用于化学变化(2)只适用于质量(3)只适用于参与反应的物质3.规律“五”不变:①反应物和生成物的总质量不变;②元素的种类不变;③元素的质量不变;④原子的种类不变;⑤原子的个数不变“二”一定变:①物质的种类一定变;②构成物质的粒子一定变“一”可能变:物质的状态和分子数可能变二、化学方程式1.书写步骤(1)写:正确写出反应物、生成物、反应条件,并用横线连接(2)配:在反应物和生成物前配正确的序数(3)改:改横线为等号(4)标:正确标出“↑”“↓”(5)查:检查所写方程式是否符合质量守恒定律2. “↑”“↓”的适用条件(1)“↑”:反应物中无气体参与,生成物中有气体(2)“↓”:在溶液中的反应,生成难溶于水的沉淀3.化学方程式的含义(1)宏观:反应物在反应条件下生成生成物(2)数量:几个反应物分子在反应条件下生成生成物分子(3)质量:几份反应物在反应条件下生成几份生成物三、化学方程式的计算——书写步骤1.设:设所求量为x注:①通常求什么设什么;②x 后不带单位2.写:写出正确的化学方程式3.列:上:系数×相对分子质量中:实际质量下:列比例式4.解:解出x 的值5.答:写出答案例题(2019•鼓楼二模)在高温下,铁与水蒸气能发生反应生成一种常见的铁的氧化物和一种气体。
某兴趣小组进行如下实验探究B 装置中剩余固体成分。
【查阅资料】①四氧化三铁能与盐酸反应生成氯化亚铁、氯化铁和水。
②氯化铁能与铁反应生成氯化亚铁。
③氧化亚铁和氧化铁不能被磁铁吸引,铁和四氧化三铁能被磁铁吸引。
【初步探究】装置中剩余固体全部是黑色的,并且都能被磁铁吸引。
【猜想与假设】猜想1:固体成分是四氧化三铁;猜想2:。
【探究与结论】小华取少量黑色固体于试管中,加入足量的稀盐酸,她认为若固体全部溶解,没有气泡冒出,则猜想1 正确;若固体全部溶解,有气泡冒出,则猜想2 正确。
中考化学专题复习:质量守恒定律及其应用命题点1质量守恒定律的理解1.下列现象能用质量守恒定律解释的是()A.蔗糖溶于水后总质量不变B.浓硫酸敞口放置质量增加C.饱和硝酸钾溶液升温,溶液质量不变D.硫酸铜溶液和氢氧化钠溶液混合,溶液质量减小2.下列关于3Fe+2O2Fe3O4的叙述中,正确的是()A.表示铁生锈的反应B.表示铁与氧气在点燃的条件下反应生成氧化铁C.如果把反应条件“点燃”去掉,这个反应不符合客观事实D.上述反应中10gFe和10gO2反应,能生成20gFe3O43.《科学》刊登了用CO2为原料。
不依赖光合作用人工合成淀粉的成果,其中第一步反应如图所示。
下列说法正确的是()A.该反应为置换反应B.反应前后分子数目不相等C.反应前后原子数目不相等D.反应前后ZnO﹣ZrO2的质量不相等4.在反应C+2ZnO2Zn+CO2↑中,下列有关说法正确的是()A.反应前后各元素的化合价均无变化B.反应前后锌元素的质量没有发生改变C.参加反应的碳与氧化锌的质量比为4:27D.反应后固体质量减轻,不遵循质量守恒定律命题点2质量守恒定律的验证5.化学兴趣小组用气密性良好的不同装置进行下列实验,验证质量守恒定律。
(1)实验一:称量装置和药品的总质量为m1保持装置密闭。
使红磷燃烧,待装置冷却后。
再次称量装置和药品的总质量为m2,m1与m2的大小关系是:m1m2;(2)实验二:将气球中的碳酸钠粉末倒入锥形瓶中,观察到的现象是;(3)为克服实验二中气球受浮力的影响。
在实验三中利用硬塑料纸改进实验装置,用电子天平称量装置和药品的总质量,接下来的实验操作,待反应结束后,再次称量装置和药品的总质量,电子天平示数不变;(4)化学反应遵守质量守恒定律,其微观原因是。
6.1777年,法国化学家拉瓦锡利用天平在密闭容器中进行了多种金属和非金属的煅烧实验,研究了实验中物质的质量关系,得出了质量守恒定律的具体内容。
质量守恒定律的发现,使得化学科学由定性研究走向定量研究。
知识点一物质的变化与性质1.物质的变化(1)物理变化:。
例如:。
(2)化学变化:。
例如:。
(3)判断依据:。
2.物质的性质(1)物理性质:。
例如:。
(2)化学性质:。
例如:。
(3)性质与用途的关系:。
【典例1】中华传统文化博大精深,下列词句中蕴含化学变化的是()A.木已成舟B.只要功夫深,铁杵磨成针C.百炼成钢D.日照香炉生紫烟【答案】C。
【解析】A、木已成舟的过程中没有新物质生成,只是形状的改变,属于物理变化,故A错。
B、铁杵磨成针的过程中,只是将其磨细,没有新物质生成,属于物理变化,故B错。
C、百炼成钢的过程包含着碳与氧气反应生成二氧化碳,有新物质生成,属于化学变化,故C正确。
D、日照香炉生紫烟属于光的散射,没有新物质生成,属于物理变化,故D错。
【典例2】下列做法中一定发生化学变化的是()A.用石油分馏制得汽油、柴油等B.用碱和树叶制作“叶脉书签”C.用钢丝球擦除灶具上的污渍D.用汽油清洗衣服上的油污【答案】B。
【解析】A、用石油分馏制得汽油、柴油等,是利用物质的沸点不同,进行混合物的分离,属于物理变化,故A错;B、用碱和树叶制作“叶脉书签”是利用碱与叶肉发生反应,属于化学变化,故B正确;C、用钢丝球擦除灶具上的污渍,是利用将其摩擦掉,没有新物质生成,属于物理变化,故C错;D、用汽油清洗衣服上的油污,是利用汽油能溶解油污,属于物理变化,故D错。
【典例3】我国古代文献记载中蕴含着丰富的化学知识。
下列记载中不涉及化学变化的是()A.《易经》——“泽中有火······上火下泽”B.《淮南万毕术》—— “曾青得铁则化为铜”C.《抱朴子》——“丹砂(HgS)烧之成水银,积变又还成丹砂”D.《天工开物》—— “侯潮一过,明月天睛,半日晒出盐霜”【答案】D。
【解析】A、泽中有火·····上火下泽,包含着物质燃烧,属于化学变化,故A错;B、曾青得铁则化为铜是铁和硫酸铜反应生成铜和硫酸亚铁,有新物质生成,属于化学变化,故B错;C、丹砂(HgS)烧之成水银,积变又还成丹砂,发生了两个化学变化,先生成汞,再合成丹砂,故C错;D、侯潮一过,明月天睛,半日晒出盐霜是由于水分蒸发,析出晶体,没有新物质生成,属于物理变化,故D 正确。
课题:质量守恒定律【学习目标】1、知道质量守恒定律的内容,能说明常见化学反应中的质量关系。
2、能从宏观和微观正确理解质量守恒定律,并能用它解释一些简单的现象。
一、本节知识网络知识归纳:要从宏观、微观角度理解质量守恒定律,要抓住:6个一定不变:①;②________③;④________⑤_________;⑥________2个一定改变:①_________;②___________1个可能改变:_________________________二、典例分析1、判断说法①1g氢气与10g氧气反应,其中有2g氧气未反应。
生成水的质量是11g②根据质量守恒定律,2L氢气和1L氧气反应能生成3L水。
③2g水加热后变成2g水蒸气,这个过程遵守质量守恒定律。
【变式训练】下列叙述完全符合质量守恒定律的是()A.水结成冰前后,质量保持不变B.50mL水和50 mL乙醇混合后总体积小于100 mLC.在100g过氧化氢溶液中,含有30g过氧化氢和70g水D.1.2g碳与3.2g氧气恰好完全反应可生成4.4g二氧化碳2、判断反应物或生成物的元素组成植物的光合作用如下:水+二氧化碳淀粉+氧气由此可推知,淀粉中一定会有的元素是___元素,可能含有_____元素,依据是_______________。
【相应练习】化学上常用燃烧法测定有机物的组成。
现取3.2g某有机物在足量的氧气中充分燃烧,除生成4.4g CO2和3.6g H2O外,没有其他物质生成。
则该有机物中()。
A、一定含有碳、氢两种元素,可能含有氧元素B、一定含有碳、氢、氧三种元素C、一定含有碳、氧,可能含有氢元素D、只含碳、氢,不含氧元素3、判断化学反应中某物质的化学式浓硝酸和锌反应的化学方程式为:Zn+4HNO3=Zn(NO3)2+2H2O+2X↑,则X为()A、H2B、NH3C、NOD、NO24、推断化学反应中化学式前的计量数(2013•兰州),地震.震后灾区人民的可用漂白粉消毒.漂白粉的制取原理为:2Cl2+xCa(OH)2=CaCl2+Ca(ClO)2+2H2O,此反应中x的数值为()A、1B、2C、3D、45、应用质量守恒定律对化学反应进行分析(2013.庆阳)将一定量的乙醇(C2H6O)和氧气置于一个封闭的容器中引燃,测得反应前后下列判断正确的是()A、表中a的值为2.6B、X一定是该反应的催化剂C、X可能含有氢元素D、若起始时氧气的质量是9.6g,则无X生成6、考查化学反应的实质(2013•浙江)(1)X、Y、Z 中属于化合物的是_______(选填字母).(2)反应生成Y和Z分子个数比是_________7、质量守恒定律是物质科学中的一条重要规律,具体表述为:参加化学反应的各物质的质量总和,等于反应后生成的各物质的质量总和.(1)某科学兴趣小组的同学设计了如下三个实验装置(天平略)来验证质量守恒律.其中,只有A装置能用来验证质量守恒定律,B、C装置则不能.否定B、C装置的理由是:__(2)小明将C装置进行改进,如图D所示.①此实验的现象是______________.②待完全反应后,将装置D置于天平上称量,所得数据较反应前的小.若整个操作过程无差错,则造成上述实验误差的原因是___________.8、利用质量守恒定律的有关计算(2013•潍坊)混合加热,A与发生化学反应,完全反应后生成8gC4gD,则参加反应A与质量比是()A.5:1B.4:1C.2:1D.1:1三、当堂达标题(一)选择题1、化学变化前后符合质量守恒定律的原因是( )A..分子种类不变 B .元素种类改变 C .原子的种类、数目、质量都不变 D .分子数目不变2、(2013•东营模拟)化学中有多种“守恒”,下面是部分“守恒”和对应的“解释”,其中搭配正确的是( ) ①Ⅰ化学反应前后元素的种类与不变②原子Ⅱ参加反应的各物质的总和等于生成的各物质的总和 ③元素Ⅲ化学反应前后原子的种类和数目不变④溶质Ⅳ溶液在稀释前后溶质的不变.A .①-ⅣB .②-ⅢC .③-ⅡD .④-Ⅰ3、镁在空气中燃烧,下列说法符合质量守恒定律的是(Mg-24,O-16)( )A .4g 镁和1g 氧气发生反应生成5g 氧化镁B .3g 镁和2g 氧气反应生成5g 氧化镁C .2.5g 镁与2.5氧气反应生成5g 氧化镁D .2g 镁和3g 氧气反应生成5g 氧化镁4、(2003•攀枝花)在X+2O 2 CO 2+2H 2O 的反应中,根据质量守恒定律可推知X 是( )A .CH 3OHB .C 2H 5OH C .CH 3COOHD .CH 4 5、下列现象能用质量守恒定律解释的是( ) A .水受热形成水蒸气B .煤燃烧后留下的煤灰比原煤质量少C .10 g 食盐溶于70 g 水中得到80 g 食盐水D .湿衣服晾干后,质量变小6、下列叙述完全符合质量守恒定律的是( ) A .水结成冰前后,质量保持不变B .50mL 水和50mL 乙醇混合后总体积小于100mLC .1.2g 碳与3.6g 氧气完全反应可生成4.8g 二氧化碳D .澄清的石灰水放在敞口的容器内,其质最不断增加7、(2013•葫芦岛)下列事实能用质量守恒定律解释的是( ) A .一定量的铜丝在空气中灼烧后,质量变大B .10gNaCl 溶解在90g 水中,形成100gNaCl 溶液C .化学反应中常伴随能量变化,有的放热,有的吸热D .100mL 酒精与100mL 水混合后,溶液体积小于200mL 8、根据质量守恒定律,化学反应前后不发生改变的是()A .分子个数B .物质种类C .分子种类D .元素种类9、(2011•沙湾区二模)下列实验能够直接用于验证质量守恒定律的是( )A .B .C .D .10、下列验证质量守恒定律的实验中,能得出正确结论的是()C.D.A.B.11、(2013•合肥二模)下列变化中,属于化学变化,并且能用质量守恒定律解释的是()A.5g水受热变成5g水蒸气B.5g食盐溶解在95g水中,成为100g食盐溶液C.100mL水加入100mL酒精,成为体积小于200mL的溶液D.木炭燃烧后质量减少12、已知反应X2+3Y2=2Z,根据质量守恒定律可推知,下列说法一定错误的是()A.若X2的相对分子质量为a,Y2的相对分子质量为b,则Z的相对分子质量为(a+3b)B.若ag X2与b g Y2恰好完全反应,则生成(a+b)g ZC.Z的化学式为XY3D.若a g x2完全反应生成b g Z,则同时消耗(b-a)g Y213、在化学反应A+2B=C+3D中,已知2gA与4.1gB完全反应,生成5.6gC.当有1.5gD生成时,参加反应的A的质量是()A.该反应为分解反应B.该反应中X与Q的质量比是1:4C.X中未测值为零D.若Q为氧气,则该反应为氧化反应(二)填空题1、根据质量守恒定律,某化学反应为:2XY+Y2═2Z,则Z的化学式为__________。