《富集在海水中的元素—氯》知识点总结
- 格式:doc
- 大小:40.04 KB
- 文档页数:2








高中化学知识点:富集在海水中的元素——氯氯气的性质、制法和应用1.物理性质 氯气是一种有强烈刺激性气味的有毒气体,能溶于水,但在饱和食盐水中的溶解度很小,所以可用排饱和食盐水法收集氯气。
2.化学性质(写出有关化学方程式)3.Cl 2的制法(1)实验室制法 化学方程式:MnO 2+4HCl(浓)=====△MnCl 2+Cl 2↑+2H 2O 。
(2)工业制法(电解法)化学方程式:2NaCl +2H 2O=====电解2NaOH +Cl 2↑+H 2↑。
4.应用(1)制盐酸:利用H 2在Cl 2中燃烧生成HCl ,然后溶于水制盐酸。
(2)制漂白液:利用Cl 2与NaOH 溶液反应制备,其有效成分为NaClO 。
(3)制漂白粉:利用Cl 2与Ca(OH)2乳浊液反应制备,其有效成分为Ca(ClO)2。
(4)制含氯有机物,如Cl 2与CH 4反应可生成CH 3Cl 、CH 2Cl 2、CHCl 3、CCl 4有机物。
氯的重要化合物1.次氯酸(1)不稳定性:2HClO=====光2HCl +O 2↑氯水须现用现配,保存在棕色试剂瓶中,置于冷暗处。
(2)强氧化性:①能将有色物质氧化为无色物质,有漂白性。
②杀菌、消毒。
(3)弱酸性:NaClO 溶液中通少量CO 2,化学方程式为:2NaClO +CO 2+H 2O===2HClO +Na 2CO 3。
2.次氯酸盐(1)(2)3.今天人们不直接用Cl 2作漂白剂而常用漂白液或漂白粉的理由是Cl 2在水中的溶解度不大而且生成的HClO 不稳定,难以保存,使用不方便,效果不理想。
卤素及卤离子检验1.卤素(包括F 、Cl 、Br 、I 等)简介(1)单质物理性质的递变规律 ①单质颜色逐渐变深(F 2:淡黄绿色气体;Cl 2:黄绿色气体;Br 2:深红棕色液体;I 2:紫黑色固体)。
②密度逐渐增大;熔、沸点逐渐升高。
(2)单质及化合物的化学性质①单质(从F 2至I 2): 氧化性逐渐减弱,与氢气化合越来越难,与H 2O 反应逐渐减弱。
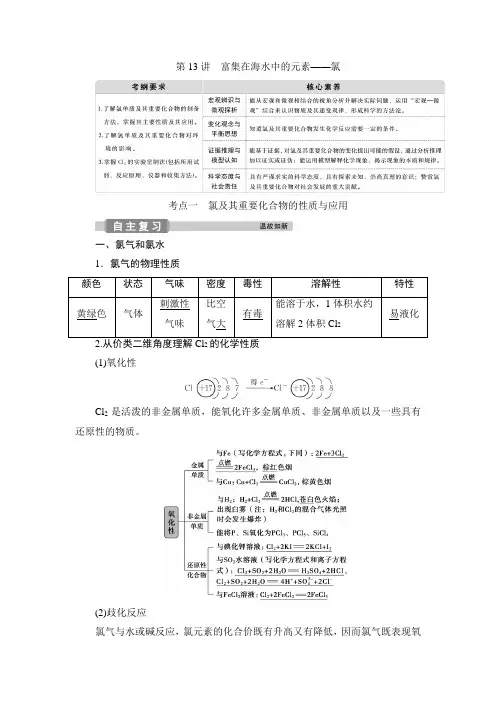
第13讲富集在海水中的元素——氯考点一氯及其重要化合物的性质与应用一、氯气和氯水1.氯气的物理性质颜色状态气味密度毒性溶解性特性黄绿色气体刺激性气味比空气大有毒能溶于水,1体积水约溶解2体积Cl2易液化2(1)氧化性Cl2是活泼的非金属单质,能氧化许多金属单质、非金属单质以及一些具有还原性的物质。
(2)歧化反应氯气与水或碱反应,氯元素的化合价既有升高又有降低,因而氯气既表现氧化性又表现还原性。
3.从平衡的角度理解氯水的成分和性质(1)氯水中存在三个平衡关系①Cl2+H2O HCl+HClO;②HClO H++ClO-;③H2O H++OH-。
(2)氯水性质的多重性新制氯水的多种成分决定了它具有多重性质。
在不同的化学反应中,氯水中参与反应的微粒不同。
[注意]氯水常代替氯气进行溶液中的实验。
(3)Cl2+H2O H++Cl-+HClO平衡移动的应用向氯水中加入的物质(或改变的条件) 浓度变化平衡移动的方向应用可溶性氯化物c(Cl-)增大左移①用饱和食盐水除Cl2中的HCl气体②用排饱和食盐水法收集Cl2盐酸c(H+)和c(Cl-)增大左移次氯酸盐与浓盐酸反应制取Cl2NaOH c(H+)减小右移用NaOH溶液吸收多余Cl2Ca(OH)2c(H+)减小右移制漂白粉CaCO3c(H+)减小右移制高浓度的HClO溶液光照c(HClO)减小右移氯水避光保存或现用现配二、次氯酸和次氯酸盐1.次氯酸2.次氯酸盐(1)“84”消毒液有效成分为NaClO,它与洁厕灵(主要成分为盐酸)混合会立即产生氯气,其离子方程式是ClO-+Cl-+2H+===Cl2↑+H2O。
(2)漂白粉①主要成分是CaCl2和Ca(ClO)2,其中有效成分是Ca(ClO)2,其水溶液显碱性,原因是ClO-+H2O HClO+OH-(写离子方程式);②漂白原理:在潮湿的空气中能吸收CO2,化学方程式为Ca(ClO)2+CO2+H2O===2HClO+CaCO3↓。

《富集在海水中的元素—氯》知识点总结一.氯元素位于第三周期第ⅦA 族,原子结构:容易得到一个电子形成氯离子Cl -,为典型的非金属元素,在自然界中以化合态存在。
二.氯气物理性质:黄绿色气体,有刺激性气味、可溶于水、加压和降温条件下可变为液态(液氯)和固态。
制法:MnO 2+4HCl (浓) ===△MnCl 2+2H 2O +Cl 2闻法用手在瓶口轻轻扇动,使少量氯气进入鼻孔化学性质:很活泼,有毒,有氧化性, 能与大多数金属化合生成金属氯化物(盐)。
也能与非金属反应:2Na +Cl 2 ===点燃 2NaCl 现象:大量白烟2Fe +3Cl 2 ===点燃 2FeCl 3 现象:棕黄色的烟Cu +Cl 2 ===点燃 CuCl 2 现象:棕黄色的烟Cl 2+H 2 ===点燃 2HCl 现象:发出苍白色火焰,生成大量白雾。
燃烧:燃烧不一定有氧气参加,物质并不是只有在氧气中才可以燃烧。
燃烧的本质是剧烈的氧化还原反应,所有发光放热的剧烈化学反应都称为燃烧。
Cl 2的用途:①自来水杀菌消毒Cl 2+H 2O == HCl +HClO 2HClO ===光照 2HCl +O 2 ↑1体积的水溶解2体积的氯气形成的溶液为氯水,为浅黄绿色。
其中次氯酸HClO 有强氧化性和漂泊性,起主要的消毒漂白作用。
次氯酸有弱酸性,不稳定,光照或加热分解,因此久置氯水会失效。
②制漂白液、漂白粉和漂粉精制漂白液 Cl 2+2NaOH=NaCl +NaClO +H 2O ,其有效成分NaClO 比HClO 稳定多,可长期存放制漂白粉(有效氯35%)和漂粉精(充分反应有效氯70%) 2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O。
③与有机物反应,是重要的化学工业物质。
④用于提纯Si、Ge、Ti等半导体和钛。
⑤有机化工:合成塑料、橡胶、人造纤维、农药、染料和药品。
三.氯离子的检验使用硝酸银溶液,并用稀硝酸排除干扰离子(CO32-、SO32-)。

第二节 富集在海水中的元素——氯第一课时 氯气一、复习巩固:完成下列化学方程式,指出氧化剂、氧化产物和还原剂、还原产物: (1)Na 在Cl 2中燃烧: . (2)氯水滴入FeCl 2(aq)中: . 二、探求新知 知识点一: 氯的存在和结构1.氯元素主要以Cl -的形式存在于海水中 (1) 自然界中,只有的 氯,没有的 氯 (2) 盐类很多,但人类必须加补食用的只有 . 2.氯原子的结构氯原子的原子结构示意图: 。
氯原子最外层有 个电子,很容易获得 个电子变为 .氯元素是典型的 元素. 知识点二: 氯气的物理性质另外:氯气有 ,易 化. 知识点三: 化学性质(1)与金属反应氯气是活泼的非金属单质,具有很强的 性.能与大多数金属化合,生成金属氯化物。
如:实验步骤 实验现象结论及解释 展示 集气瓶口向 放置,气体呈 色. 氯气的密度 空气嗅闻气体 有 性气味水溶性实验,加水震荡集气瓶内气体颜色 ,水变为 色液体.氯气 溶于水(2) 与非金属反应 实验:H 2在Cl 2中燃烧实验操作 实验现象化学方程式H 2在Cl 2中燃烧H 2在Cl 2中安静的燃烧,发出 色火焰,集气瓶口有 产生H 2和Cl 2的混合气体光照燃烧产物HCl 气体易溶于水,溶于水得到的溶液即为 . [思考与交流]通过 H 2在Cl 2中燃烧的实验,你对燃烧的条件及其本质有什么新的认识? (3).与水的反应实验:氯水的漂白作用 实验操作 实验现象 结论 有色布条、氯水有色布条氯水有 作用 有色布条、干燥的氯气 有色布条干燥的氯气 漂白作用①. Cl 2的水溶液叫 ,该水溶液的颜色为 ,这说明其中含有 ②写除Cl 2与水的反应的化学方程式,并标出电子转移的方向和数目: 该反应中,氧化剂是 ,还原剂是 ,该反应的离子方程式 ③氯水中含有的粒子主要有 ,其中包括 种分子, 种离子 ④次氯酸的性质A.弱酸性:HClO 的酸性比碳酸的酸性 ,B.不稳定性:不稳定,在光照下分解 ,化学方程式 离子方程式C.强氧化性: (1)漂白性:(2)杀菌、消毒。
第二节富集在海水中的元素——氯1、氯气的性质:(1)物理性质:是一种有强烈刺激性气味的黄绿色的有毒气体。
(2)化学性质:点燃○1与金属单质反应:2Na+Cl2 2NaCl点燃2Fe+3Cl2 2FeCl3点燃Cu+Cl2 CuCl2○2与氢气反应:H2+Cl2 2HClH2+Cl2 2HCl○3与水反应:H2O +Cl2 =HCl+HClO○4制漂白液反应:Cl2+2NaOH=NaCl+NaClO+H2O○5制漂白粉反应:2Cl2 +2Ca(OH)2=CaCl2 +Ca(ClO)2 +2H2O△○6实验室制法:MnO2+4HCl(浓)MnCl2 +Cl2 ↑+2H2O2、液氯、新制的氯水和久置的氯水(1)液氯:属于纯净物,黄绿色;组成成分:Cl2;具有氧化性。
(2)新制氯水:属于混合物,黄绿色;组成成分:Cl2、H2O、HClO、H+、Cl―、ClO―、极少量的为OH―;具有氧化性、酸性和漂白性。
(3)久置的氯水:属于混合物,无色;组成成分:H+、Cl―、H2O、极少量的OH―、稀盐酸;具有酸性。
3、氯离子的检验:加入AgNO3溶液后再加入少量稀硝酸反应方程式:Ag++Cl―==AgCl【素材积累】1、一个房产经纪人死后和上帝的对话一个房产经纪人死后,和上帝喝茶。
上帝认为他太能说了,会打扰天堂的幽静,于是旧把他打入了地狱。
刚过了一个星期,阎王旧满头大汗找上门来说:上帝呀,赶紧把他弄走吧!上帝问:怎么回事?阎王说:地狱的小。
2、机会往往伪装成困难美国名校芝加哥大学的一位教授到访北大时曾提到:芝加哥大学对学生的基本要求是做困难的事。
因为一个人要想有所成旧,旧必须做那些困难的事。
只有做困难的事,才能推动社会发展进步。
富集在海水中的元素——氯【学习目标】1.了解氯气的物理性质||,理解氯气的化学性质||。
2.了解氯气的实验室制法和用途||。
3.了解Cl-检验||,了解卤素的性质||。
【要点梳理】要点一、氯元素在自然界中的存在和氯气的物理性质1.氯元素的存在在自然界里||,氯元素以化合态存在||,游离态的氯只能通过人工方法而制得||。
氯元素是最重要的“成盐元素”||,主要以NaCl的形式存在于海水和陆地的盐矿中||。
海洋中含盐3%||,主要是NaCl||,还含有MgCl2、MgSO4等盐类||,致使海水既咸又苦||,不能直接饮用||。
人体体液中的Na+和Cl―对于调节体液的物理和化学特性||,保证体内正常的生理活动和功能发挥着重要作用||。
人体每天必须经过食物和食盐来补充人体所缺失的Na+和Cl-||。
2.氯气的物理性质氯气是一种黄绿色、具有强烈刺激性气味的有毒气体||,在低温和加压情况下可以转化为液态(液氯)和固态||。
氯气能溶于水||,25°C时||,1体积的水可以溶解2体积的氯气||,所得水溶液称为氯水||。
在实验室闻氯气气味时||,应该用手轻轻在瓶口扇动||,仅使极少量的氯气飘过鼻孔||,如右图所示||,闻其他气体的气味时也应采用这种方法||。
注意:应注意气体溶解度的表示方法与固体不同||,固体的溶解度是在一定温度下||,溶液达到饱和状态时||,100g溶剂(水)中溶解的溶质的质量(g)||。
气体的溶解度用体积比表示||,与温度、压强有关||,如常温(25°C)常压下||,氯气可以1∶2溶解于水||,应理解为1L水中可溶解2L的氯气或1体积水中可溶解2体积的氯气||。
要点二、氯气的化学性质要点诠释:氯是第17号元素||,其原子的最外层有7个电子||,在化学反应过程中很容易得一个电子形成氯离子(Cl—)即达到8个电子的稳定结构||,表现为典型的非金属性||。
氯气是双原子分子||,其分子虽已达到8电子稳定结构但不是最稳定状态||,在一定条件下易与其他物质发生化学反应||,通常做氧化剂||,且是强氧化剂||。
富集在海水中的元素——氯一、活泼的黄绿色气体——氯气1、氯元素的存在:氯元素在自然界中以存在,主要以形式存在于海水和陆地的盐矿中。
2、氯气的实验室制法:实验室制取氯气是用软锰矿与浓盐酸混合加热,产生氯气,MnCl2和水。
请写出舍勒发现氯气的化学反应方程式:(指出反应的氧化剂和还原剂;用双线桥表示电子转移的方向和数目。
)。
4、氯气的化学性质:写出下列反应的化学方程式。
(1)Cl2与金属的反应①与Na的反应:;现象②与Fe的反应:;现象③与Cu的反应:;现象(2)Cl2与非金属的反应①Cl2与H2的反应:;现象②Cl2还能跟其他一些非金属单质反应,如与磷单质反应生成PCl5和PCl3:。
(3)Cl2与水的反应,常温下,溶于水中的部分氯气....会与水反应,化学方程式为:,离子方程式为:,该反应中的氧化剂为________,还原剂为________。
次氯酸(HClO)的性质:①弱酸性:很弱的酸,酸性比碳酸弱。
②不稳定性:不稳定,只存在于水溶液中,在光照下易分解放出氧气,反应的化学方程式为:。
③强氧化性:能杀菌消毒,具有漂白作用。
(4)Cl2与碱溶液的反应①与NaOH反应制漂白液在常温下,将氯气通入NaOH溶液中可以得到以()为有效成分的漂白液,反应的化学方程式为,离子方程式为,该反应中的氧化剂为_______,还原剂为_______。
②与Ca(OH)2反应制取漂白粉将氯气通入冷的消石灰[ ]中即制得以 ( )为有效成分的漂白粉。
反应的化学方程式为 ,若氯气与Ca(OH)2反应充分,并使 成为主要成分,则得到 。
③漂白液的有效成份是NaClO ,漂白粉的有效成份是Ca(ClO)2,其中漂白原理是:ClO -+ H + = HClO (实际漂白者),完成下列反应方程式:Ca(ClO)2 + HCl (稀)= 。
Ca(ClO)2 +CO 2 +H 2O = 。
说明碳酸酸性 次氯酸。
5、氯气用途:(1)常用作消毒剂;(2)制造盐酸、制造漂白粉;(3)Cl 2是合成塑料、橡胶、人造纤维、二、氯气制备实验(1)原理:自然界中氯元素主要以Cl -形态存在,因此制备氯气的基本原是就是用氧化剂将氯离子氧化成氯气单质 :2Cl- Cl 2↑ 需要加入 剂 。
考点二卤素的性质及卤素离子的检验李仕才1.卤素单质的相似性和递变性(1)递变性(2)相似性(用X代表Cl、Br、I)①都能与大多数金属反应:2Fe+3Br2===2FeBr3;I2+Fe===FeI2;②都能与H2反应:H2+X2===2HX;③都能与H2O反应:X2+H2+HXO(F2例外);④都能与碱液(NaOH)反应:X2+2NaOH===NaX+NaXO+H2O(F2例外)。
2.Cl2、Br2、I2的氧化性氯、溴、碘单质的氧化性强弱是Cl2>Br2>I2,阴离子的还原性:Cl-<Br-<I-。
(1)Cl2能从Br-的溶液中置换出Br2,其离子方程式:Cl2+2Br-===2Cl-+Br2;同理,Br2能置换I2,其离子方程式:Br2+2I-===2Br-+I2。
(2)与一些还原性离子反应,如Br2与SO2-3、Fe2+反应的离子方程式分别为SO2-3+Br2+H2O===SO2-4+2Br-+2H+,2Fe2++Br2===2Br-+2Fe3+。
3.特殊性(1)氟①无正价,非金属性最强,F-的还原性最弱。
与H2反应在暗处即爆炸。
②2F2+2H2O===4HF+O2,F2不能在水溶液中置换其他卤素单质。
③氢氟酸是弱酸,能腐蚀玻璃,故应保存在塑料瓶中;有毒。
(2)溴①Br2是深红棕色液体,易挥发。
②Br2易溶于有机溶剂。
在有机溶剂中显橙色或橙红色。
③盛溴的试剂瓶中加水,进行水封,保存液溴不能用橡胶塞。
(3)碘①淀粉遇I2变蓝色。
②I2加热时易升华。
③I2易溶于有机溶剂。
在有机溶液中颜色为紫色或紫红色。
4.卤素离子检验(1)AgNO3溶液——沉淀法判断正误(正确的打“√”,错误的打“×”)1.类比Fe与Cl2的反应判断Fe与I2反应时生成FeI3。
( ×) 2.F2通入氯化钠溶液中反应置换出Cl2。
( ×)3.可以用淀粉溶液检验加碘食盐中的KIO3。
元富集在海水中的元素氯知识点总结文稿归稿存档编号:[KKUY-KKIO69-OTM243-OLUI129-G00I-FDQS58-第二节 富集在海水中的元素——氯一、氯元素1.存在:在海水中主要以NaCl 的形式存在。
2.原子结构性质:最外层有7e-,易得到1个电子形成Cl-,性质很活泼,表现为典型的非金属性。
强氧化性自然界中有没有游离态的氯,氯元素在自然界以化合态形式存在二、氯气(Cl 2) (一)物理性质: 1.颜色:黄绿色。
2. 闻气味:刺激性气味,(有毒,请注意闻气体气味的方法)。
3.密度比空气大。
(二)化学性质: 1.与金属反应:与钠反应:2Na + Cl 2 == 2NaCl 现象:钠在氯气中燃烧,发出黄色火焰,产生白烟与铁反应:2Fe + 3 Cl 2 == 2FeCl 3 Fe 作还原剂 Cl 2作氧化剂现象:红热的铜丝在Cl 2中剧烈燃烧,产生棕黄色烟(但不会产生火焰),溶于水为蓝色溶液。
与铜反应:Cu + Cl 2 == CuCl 2现象:红热的铁丝在Cl2中剧烈燃烧,产生红棕色烟(而不产生火焰),溶于水为黄色溶液。
结论:氯气具有强氧化性, ①在加热或点燃的条件下,与绝大多数金属直接化合, ②把变价金属从0价氧化为最高价。
如:CuCl 2、FeCl 3注意:例如:干燥的氯气在常温下不与铁反应所以可用钢瓶储存氯气 2、氯气与非金属反应(1)氯气与氢气的反应:H2 + Cl 2 === 2HCla 现象:氢气在氯气中安静燃烧,发出苍白色火焰,瓶口呈白雾状白雾——生成的HCl 与空气中的水蒸气结合形成的盐酸(氢氯酸)小液滴。
b 现象:H2、Cl2混合光照: 发生爆炸,产生白雾。
(2)与磷反应:氧气不足:2P + 3 Cl 2 ==2PCl 3(白雾) 液态氧气充足:2P + 5 Cl 2 ==2PCl 5(白烟) 固态反应的化学方程式并标出电子转移方向和数目,指出氧化剂和还原剂 点燃和燃烧有何区别:①燃烧不一定有氧气参加,物质并不是只有在氧气中才可以燃烧。
《富集在海水中的元素—氯》知识点总结
一.氯元素
位于第三周期第ⅦA 族,原子结构:
容易得到一个电子形成氯离子Cl -,为典型的非金属元素,在自然界中以化合态存在。
二.氯气
物理性质:黄绿色气体,有刺激性气味、可溶于水、加压和降温条件下可变为液态(液氯)和固态。
制法:MnO 2+4HCl (浓) ===△
MnCl 2+2H 2O +Cl 2
闻法用手在瓶口轻轻扇动,使少量氯气进入鼻孔
化学性质:很活泼,有毒,有氧化性, 能与大多数金属化合生成金属氯化物(盐)。
也能与非金属反应:
2Na +Cl 2 ===点燃 2NaCl 现象:大量白烟
2Fe +3Cl 2 ===点燃 2FeCl 3 现象:棕黄色的烟
Cu +Cl 2 ===点燃 CuCl 2 现象:棕黄色的烟
Cl 2+H 2 ===点燃 2HCl 现象:发出苍白色火焰,生成大量白雾。
燃烧:燃烧不一定有氧气参加,物质并不是只有在氧气中才可以燃烧。
燃烧的本质是剧烈的氧化还原反应,所有发光放热的剧烈化学反应都称为燃烧。
Cl 2的用途:
①自来水杀菌消毒Cl 2+H 2O == HCl +HClO 2HClO ===光照 2HCl +O 2 ↑
1体积的水溶解2体积的氯气形成的溶液为氯水,为浅黄绿色。
其中次氯酸HClO 有强氧化性和漂泊性,起主要的消毒漂白作用。
次氯酸有弱酸性,不稳定,光照或加热分解,因此久置氯水会失效。
+17 2 8 7
②制漂白液、漂白粉和漂粉精
制漂白液Cl2+2NaOH=NaCl+NaClO+H2O ,其有效成分NaClO比HClO稳定多,可长期存放
制漂白粉(有效氯35%)和漂粉精(充分反应有效氯70%) 2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O。
③与有机物反应,是重要的化学工业物质。
④用于提纯Si、Ge、Ti等半导体和钛。
⑤有机化工:合成塑料、橡胶、人造纤维、农药、染料和药品。
三.氯离子的检验
使用硝酸银溶液,并用稀硝酸排除干扰离子(CO32-、SO32-)。
HCl+AgNO3== AgCl ↓+HNO3
NaCl+AgNO3== AgCl ↓+NaNO3
Na2CO3+2AgNO3==Ag2CO3 ↓+2NaNO3Ag2CO3+2HNO3== 2AgNO3+CO2 ↑+H2O
Cl-+Ag+== AgCl↓。