铯的基本常识.
- 格式:doc
- 大小:233.00 KB
- 文档页数:2

铯在医学上的应用铯,一种神秘的元素,它的存在挑战了我们对物质世界的理解,铯究竟怎么读音呢?它又有哪些独特的性质和用途呢?让我们一起来探索这个神秘的世界吧!铯的读音铯的读音是[sè],发音时舌头要卷起,舌尖抵住上齿龈,发出清脆的声音,这是一个比较简单的音节,但在化学领域中,铯的重要性却不容忽视。
铯的基本性质1、物理性质铯是一种银白色的金属,具有良好的导电性和热导性,它的密度较大,为1.96克/立方厘米,铯的熔点较低,仅为98.2°C,因此在工业生产中常用液态铯进行制备,铯还具有很好的延展性,可以加工成各种形状的零件。
2、化学性质铯是一种碱金属元素,位于周期表的第5周期、第1主族,它在元素周期表中的序数为55,铯的最外层只有一个电子,因此具有较强的还原性,当铯与其他元素发生化学反应时,容易失去最外层的电子,形成阳离子,铯还可以与其他碱金属元素形成合金,如铯钙合金、铯镁合金等。
3、核性质铯的原子序数为55,原子量为197.02,铯原子的质子数为55,中子数为94,铯原子的核电荷数为55,因此也被称为“重氢”,铯原子的核外电子排布与钠原子相似,即有一个电子层和一个最外层电子,由于铯的最外层只有一个电子,因此它具有较强的还原性。
铯的主要用途1、半导体材料铯因其良好的半导体性能而广泛应用于电子工业,铯化合物可以作为半导体材料,用于制造晶体管、太阳能电池等电子器件,铯还可以与其他元素形成复合半导体材料,提高其光电性能。
2、催化剂铯在化学反应中具有催化作用,可以加速某些化学反应的速率,铯在有机合成中被用作催化剂,促进羟基化反应等,铯还可以用于制备催化剂载体,如碳布、陶瓷等。
3、医疗用途铯在医学领域也有广泛的应用,铯盐类药物可以用于治疗甲状腺功能亢进症、高血压等疾病,铯还可以用于放射性同位素治疗,如铯-137放射治疗乳腺癌、肺癌等恶性肿瘤。
4、工业应用铯在工业生产中也有重要的应用,液态铯可以用于制备铝酸盐玻璃、陶瓷等材料;固态铯可以用于制备高温合金、火花塞等零部件;气态铯可以用于制备制冷剂、喷雾剂等产品。
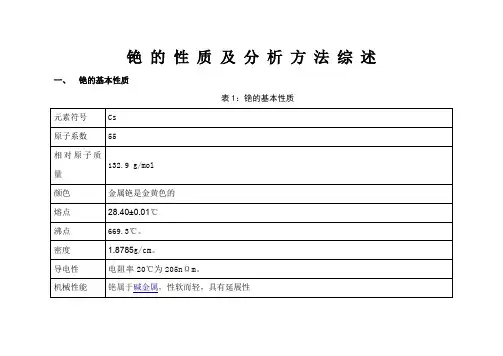
铯的性质及分析方法综述一、铯的基本性质
表1:铯的基本性质
二、铯的试样分解方法
表2:铯的试样分解方法比较
目前,常用的铯试样分解方法是和酸溶法。
碳酸钙-氯化铵烧结法
表3:铯的分离、富集方法比较
目前在在铯试样的分离富集中常用的是纸色谱法和离子交换法。
三、铯的测定方法及干扰
表5:铯的测定方法比较
目前在铯试样的分析方法中,常用的是等离子体质谱法和原子吸收光谱法。
五、应用
目前,开展了矿物中铯的检测,进行了酸溶分解方法比对和仪器比对试验:
1.固体样品中铯的测定:前期试验中采用盐酸、硝酸、氢氟酸、高氯酸两次溶矿结果偏低,采用氢氟酸、硫酸溶矿结果较好,流程短。
5300DV测定,85
2.1nm为仪器推荐波长,分析结果系统偏高;610.362nm部分国家标准物质结果偏低。
依据《锂矿石、铷矿石、铯矿石化学分析方法第3部分铯量测定GB/T17413.3-2010》,硫酸-硝酸分解,原子吸收测定,检测矿石中铯,外检合格。
2.液体样品中铯的测定:未有送检样品,建议样品酸化后,采用原子吸收测定。
如基体复杂,可开展加标回收等试验。
参考资料书籍:
1.岩石矿物分析第四版第三分册,P291-302。


元素铯限度铯(Cesium)是一种化学元素,属于碱金属元素。
它的化学符号是Cs,原子序数为55。
铯是一种银白色金属,具有低熔点和低沸点的特性。
虽然在地壳中的含量相对较低,但铯在科学和工业领域中有着重要的应用。
铯在原子钟中起着重要的角色。
原子钟是一种利用原子的振荡频率来测量时间的设备。
铯原子钟利用铯-133同位素的特性,通过测量铯原子的振荡频率来精确计算时间。
这种原子钟的精度非常高,可以达到每秒钟误差不超过1秒,因此在科学研究和导航系统中得到了广泛应用。
铯还用于研究基本粒子的物理实验。
在粒子加速器中,科学家们利用高能粒子的碰撞来研究基本粒子的性质和相互作用。
铯是一种常用的粒子束源,在实验中起到了重要的作用。
通过研究铯粒子的碰撞,科学家们可以更深入地了解基本粒子的行为和性质。
铯还可以用于光学器件和光学仪器中。
铯原子可以吸收和发射特定频率的光线,因此在激光器、光谱仪和光学传感器中得到了广泛应用。
铯原子的特性使得它在光学器件中具有重要的角色,可以用来制造高精度的光学元件,提高设备的测量精度。
铯还有一些医学应用。
铯-137同位素是一种放射性同位素,可以用于治疗癌症。
放射治疗可以通过杀死癌细胞来治疗癌症,而铯-137可以作为放射性源用于放射治疗。
当然,放射治疗需要专业人士的指导和控制,以确保安全和有效性。
总的来说,铯作为一种化学元素,在科学研究、工业应用和医学领域中有着广泛的应用。
它的特性使得它在原子钟、粒子物理实验、光学器件和放射治疗中发挥着重要的作用。
铯的应用不仅推动了科学技术的发展,也为人类带来了更多的福祉。

铯元素的奇特性质世界最轻的金属铯元素(Cs)是一种奇特的化学元素,它在化学性质上表现得非常活泼而且极其不稳定。
作为世界最轻的金属,铯拥有多种独特的性质和应用。
本文将介绍铯元素的奇特特性以及其在现代科学和技术领域中的应用。
一、铯元素的物理特性铯元素是一种碱金属,位于周期表第五族,原子序数为55,相对原子质量为132.9。
它的颜色是银白色,外观类似于钠和钾。
与其他碱金属相比,铯的密度和熔点最低,而沸点则相对较高。
铯元素在常温下是固体,但它的熔点仅为28.5°C,因此,在室温下,铯元素可以迅速融化成为液态。
铯元素具有极高的放射性,它的放射性同位素铯-137是一种广泛应用于医学和工业的放射性标记物质。
值得一提的是,铯元素在自然界中非常稀少,主要存在于钾矿石中。
因此,铯元素的分离和提纯是一项极具挑战性的工作。
二、铯元素的化学特性铯元素在化学反应中表现出极强的活性,它可以与绝大多数非金属元素和大部分金属元素发生反应。
铯与水反应会生成铯氢氧化物和氢气,而与氧气反应则会生成铯氧化物。
此外,铯还能与氯气、溴气和碘气等卤素发生反应,产生相应的铯卤化物。
由于铯元素的活泼性,它在常温下很难保存。
当铯暴露在空气中时,会迅速与氧气和水蒸气发生反应,产生铯氧化物和铯氢氧化物。
因此,在实际应用中,需要特殊的方法和设备来储存和处理铯元素。
三、铯元素的应用1. 时间测量由于铯元素拥有极高的精确度和稳定性,它被广泛应用于原子钟的制造中。
原子钟是目前世界上最精确的时间测量装置,其工作原理是通过测量铯元素原子的振动频率来实现时间的精确测量。
这种技术在卫星导航、通信网络和科学研究等领域具有重要的应用价值。
2. 医学影像放射性同位素铯-137广泛用于医学诊断和治疗中,尤其是在肿瘤治疗中。
铯-137的放射线可以杀死癌细胞,起到治疗肿瘤的效果。
此外,铯元素还用于制备各种放射性示踪物质,用于医学影像学研究和临床诊断。
3. 光电子学铯元素对光的敏感性很高,因此被广泛应用于光电子学领域。

铯化学符号(Cs)简介铯是一种碱金属元素,化学符号为Cs(来自拉丁文名字caesium)。
它是一种银白色的金属,在常温和常压下是固体,且很容易切割。
铯是一种高度反应性的金属,与大多数非金属和金属都能生成化合物。
它在自然界中很少存在,主要以矿石的形式存在,如铯石英石和铈石。
物理性质•原子序数:55•原子量:132.9•密度:1.873 g/cm³•熔点:28.44℃•沸点:671℃铯是所有稳定同位素中密度最大的金属。
它具有很低的电离能,因此在与其他元素反应时非常活泼。
铯在高温下会发出蓝色的火焰,并在空气中迅速氧化,生成氧化铯。
化学性质铯是一种高度活泼的金属,在室温下与氧、氮、硫、卤素等非金属直接反应,形成相应的化合物。
它的反应性比钠和钾还要强,但比锂要低。
铯和水反应,会生成氢气并产生烈火。
由于铯对湿气和空气敏感,因此需要在惰性气体环境中储存和处理。
铯离子是一种重要的催化剂,广泛应用于有机合成和工业化学反应中。
它还用作照相闪光灯的原料,以及原子钟的基本元素。
应用领域1.化学研究:铯离子的催化剂性质对于有机合成具有重要意义。
它可用于多种重要的反应,如氧化、烯烃同位素、酰基化和傅-克酰基化反应。
2.科学研究:铯的原子钟是一种高精度的时间测量装置,广泛应用于科学、导航和卫星通信等领域。
3.医学应用:由于铯在人体组织中的分布和运输与钠相关,因此铯在医学影像学中有一定的应用。
例如,铯的化合物可以用作医学扫描中的显影剂,用于增强显影效果。
4.金属工业:铯也用于制备有机金属化合物,这些化合物在金属工业中起着重要的作用。
5.光学应用:铯在某些光学设备中具有重要应用,如光学窗口、透镜和光调制器等。
安全注意事项由于铯是一种高度反应性的金属,需要在处理和储存时采取一定的安全措施。
以下是一些关于铯安全性的注意事项:•铯与水反应会产生剧烈的加热和火焰,因此在处理铯的过程中需要小心。
避免将铯暴露于水或湿气中。
•铯离子对机体具有一定的毒性,因此需要小心处理铯化合物。

化学元素铯铯(Cesium)是一种化学元素,属于碱金属元素。
它的化学符号为Cs,原子序数为55,原子量为132.9。
铯是一种银白色的金属,具有很高的化学反应性和电导率。
在自然界中,铯非常稀少,它主要存在于矿石中。
铯的发现可以追溯到1860年,由德国科学家Gustav Kirchhoff和Robert Bunsen首次发现并命名为"铯",源自拉丁文的"caesium",表示"天蓝色"。
铯的发现是通过光谱分析实验得出的,当时的科学家们发现了一条非常奇特的蓝色谱线,后来确认这条谱线与铯元素的存在有关。
铯是一种非常活泼的金属,它与水反应时会发生剧烈的化学反应,产生氢气并生成碱性溶液。
因此,铯在实验室和工业上的应用相对较少。
但是,铯的某些化合物在光电子学和电子器件中具有重要的应用价值。
例如,铯化合物可以用于制造光电倍增管和光电池等器件,这些器件在光谱分析和粒子探测等领域具有重要的应用。
铯的原子结构非常特殊,它的外层电子只有一个。
这使得铯具有很高的电导率和热导率。
铯的电导率是所有金属中最高的,因此在某些特殊的应用中,铯可以用作导电材料。
此外,铯还具有很高的反射率,因此可以用于制造镜子和反射镜等光学器件。
铯还具有较强的放射性,其中铯-137是一种常见的放射性同位素。
铯-137具有较长的半衰期,可以持续地发出放射线。
这使得铯-137在医学影像学和放射治疗中具有重要的应用。
铯-137还可以用作辐射源,用于无损检测和工业辐照等领域。
尽管铯在自然界中非常稀少,但它在地球上的分布是相对均匀的。
它可以在一些矿石中找到,例如石方石和石英等。
此外,铯还可以通过核反应或离子交换等方法从其他化合物中提取出来。
铯是一种重要的化学元素,具有很高的化学反应性和电导率。
尽管在实验室和工业上的应用有限,但铯的某些化合物在光电子学和放射治疗等领域具有重要的应用价值。
铯的发现和研究不仅拓宽了我们对元素的认识,也为科学技术的发展做出了贡献。

立志当早,存高远
稀有金属矿--铯
铯一、性质和用途
铯是银白色的轻金属。
其特性与铷相似。
熔点28.5℃,比重(固态,20
℃)1.9(液态,40℃)1.827。
铯的用途除与铷相同外,铯的氯化物亦可作高能固体燃料,铯可制造人工离子云、铯离子加速器,以及反作用系统材料与烟火制造材料。
用铯的化合物制成的红外辐射灯可发现夜间不易发现的讯号,铯还用于跟踪、阻截飞行敌机的瞄准弹,放射性铯用于辐射化学、医学、食品和药品的照射等,铯还是化工催化剂、特种玻璃原料。
二、主要矿物
目前已知铯的独立矿物有四种。
常见的有铯榴石Cs(Al Si2O6)nH2O,铯绝大多数分散在锂辉石、锂云母、铁锂云母中。
在钾长石、天河石、钾盐和光卤石等矿物中与钾、钠、锂呈类质同像。
三、一般工业要求
综合利用伴生铯矿参考性工业指标
矿床类型
边界品位机选氧化物(%)
工业品位
机选氧化物(%)
手选铯榴石(%)
花岗伟晶岩类矿床
0.3。

人体中铯元素-回复什么是铯元素?铯元素(Cs)是一种属于碱金属家族的化学元素,它在化学周期表中位于氨元素(Am)之后。
铯元素是一种非常活泼的金属,具有与其他碱金属相似的性质。
它的原子序数为55,原子量为132.90。
铯元素的历史铯元素于1860年被罗贝尔·威廉·伯克利(Robert Wilhelm Bunsen)和古斯塔夫·罗伯特·基尔霍夫(Gustav Robert Kirchhoff)发现。
当时,两位科学家在哈勒市的一座冶金厂进行实验时,注意到一种新元素通过发射一种深蓝色光线来确定其存在。
为了纪念该元素在拉丁文中的含义“蓝色”(caesius),他们将其命名为铯元素。
铯元素的性质和特点铯元素是一种柔软的金属,具有银白色的外观。
它是一种非常反应性强的金属,能够迅速与氧气、水和其他非金属元素发生化学反应。
铯元素的熔点相对较低,只有28.5摄氏度,因此在室温下可以变为液态。
铯元素的密度为1.93克每立方厘米,是所有常见金属中密度最高的之一。
铯元素的应用由于其高度反应性和独特的性质,铯元素在多个领域中都有广泛的应用。
以下是一些常见的应用领域:1. 核能领域:铯-137是一种放射性同位素,具有较长的半衰期。
它被广泛用于医学放射治疗和工业测量。
2. 光学设备:铯元素可以用于制造光学设备,例如光子器件和激光技术。
3. 电池:偏高纯度的铯元素可以用于制造高能量密度的电池,例如铯离子电池。
4. 催化剂:铯元素可以用作某些化学反应的催化剂,以提高反应速率和效率。
5. 铯钟:由于铯元素的震荡频率极其稳定,它被广泛应用于原子钟和GPS 系统中,以提供高精度的时间和位置测量。
铯元素对人体的影响铯元素在人体中存在于微量,主要通过自然食物、饮水和空气中吸入而摄入。
虽然人体对铯元素敏感,但在适量摄入的情况下,其对人体的影响非常有限。
铯元素在人体中的主要作用之一是参与电解质平衡调节。
它帮助维持正常细胞功能,特别是神经细胞的正常工作。

人体中铯元素铯(Cs)是一种化学元素,原子序数为55,属于第六周期、ⅠA族的金属元素。
铯元素在自然界中非常罕见,主要以铯矿石的形式存在,如蓝闪石(Pollucite)和翡翠角闪石(Rhodizite)。
在人体中,铯元素的存在及其影响一直备受科学家们的关注。
铯元素的来源和分布铯元素在地球上非常稀有,常见的铯矿物只占全球矿产储量的几乎零。
铯元素主要以镉铯矿和钽铯矿的形式存在,这些矿石主要分布在澳大利亚、加拿大、俄罗斯等地。
铯元素的生物地球化学循环复杂。
铯元素进入生物圈的途径主要有大气沉降、水域沉积物、土壤和农产品等。
由于铯元素在土壤中可与土壤颗粒结合或被植物根系吸收,它也会通过食物链进入人体。
铯元素在人体中的吸收和代谢铯元素在人体内的吸收和代谢与多种因素有关,如铯元素的化学形态、食物中的浓度和饮食习惯等。
铯元素可被人体经由呼吸系统、皮肤或消化道吸收。
铯元素进入人体后,会在体内通过血液循环和淋巴系统分布到各个组织和器官。
在组织和器官中,铯元素主要与细胞内液相互作用,并很容易进入细胞内。
尽管铯元素在人体内的代谢方式并不完全清楚,但它很快被生物吸收和分布。
铯元素的生物学效应铯元素对人体的生物学效应一直备受关注。
在低剂量暴露下,铯元素对人体的影响仍然有待进一步研究。
然而,在高剂量暴露下,铯元素表现出不同的毒性效应。
铯元素的毒性主要通过其放射性同位素Cs-137而导致,该同位素是铯元素的最稳定同位素。
Cs-137具有较长的半衰期,能够释放β射线和γ射线。
铯元素放射性同位素的辐射对人体组织和器官的损害可能导致许多不良的生理和健康效应,如白血病、放射性疾病等。
铯元素的应用尽管铯元素的毒性效应需要引起关注,但它也具有一些实际应用。
铯元素的化合物常被用于医学成像和放射治疗的核医学领域。
此外,铯元素还在电子器件、光电器件等方面发挥重要作用。
结论铯元素是一种在人体中存在的化学元素,它的存在及其影响一直受到科学家们的关注。

caesium介绍铯(Caesium)是一种银白色的碱金属元素,化学符号为Cs。
它是周期表中第55号元素,属于第一主族元素,原子序数为55。
铯在自然界中主要以矿产形式存在,如铯长石和铯榴石等。
铯的化学性质非常活泼,容易与水反应生成氢气和碱性溶液。
因此,在自然界中,铯通常以水合离子的形式存在。
铯的应用范围广泛,主要包括以下几个方面:1.核能:铯具有良好的核反应性能,可用作核反应堆的燃料。
铯-137和铯-135是两种常用的核燃料同位素,它们在核反应中释放出大量的能量。
2.光谱学:铯具有丰富的光谱线,可用于光谱分析和研究。
铯的焰色反应为深蓝色,因此在实验室中常用于检测其他元素的焰色反应。
3.化学催化剂:铯化合物具有较高的活性,可用作催化剂。
例如,铯催化剂可用于醇酸酯化反应、烷基化反应等。
4.生物学:铯离子在生物体内具有重要的生理功能。
例如,铯离子可影响细胞膜的通透性,影响神经传导和肌肉收缩。
5.电子产品:铯具有较高的电导率和热导率,可用于制作高性能电子元件。
然而,铯的同位素中有一些具有放射性,如铯-137和铯-135。
这些放射性同位素对人体和环境具有较大的危害性。
因此,在生产和使用铯的过程中,必须严格遵守安全规程。
铯-137主要用于核反应堆的燃料棒和放射性废料处理。
铯-135主要用于核能研究和核能发电。
然而,这两种同位素在事故泄漏时会对环境和人体健康造成严重影响。
因此,铯的生产、储存、运输和使用都必须严格遵循安全规定。
铯的其他同位素,如铯-123、铯-127等,虽然非放射性,但在生产过程中仍需注意安全。
由于铯的活泼性质,操作时应采取防护措施,避免与皮肤和眼睛直接接触。
总之,铯作为一种重要的碱金属元素,在科学技术和生产领域具有广泛的应用。
然而,在使用铯及其同位素时,我们必须关注其安全性和环境影响。
铯(Caesium)·Cs·55IA族,原子量132.9,体心立方晶体高二(1)陈正昊铯是一种非常柔软、延展性很强的的白色金属,其莫氏硬度(一种利用矿物的相对刻划硬度划分矿物硬度的标准)在所有的元素中最低,熔点为28.4℃,接近室温的条件下为液态。
汞是唯一的熔点低于铯的金属元素。
沸点仅有641℃,铯的化合物燃烧时具有蓝色或紫色。
铯可以和除锂之外的碱金属混合形成合金,并且摩尔比例为41%铯,47%钾以及12%钠的合金的熔点为-78℃,在所有已知的金属合金中熔点最低CsHg2为黑色并具有紫色金属光泽,而CsHg 具有金色,同样具有金属光泽。
铯具有高度的活性,非常容易自燃。
在空气中能够自发燃烧外,在很低温度下就能与水发生爆炸性反应,比碱金属中的其他元素更剧烈。
铯可以在温度低达-116℃的条件下与冰发生反应。
铯通常在矿物油等的干燥的饱和烃中储存和运输。
必须在惰性气体的保护下处理铯。
然而,铯-水的爆炸威力通常比同样量的钠-水的威力小,这是由于铯在接触到水的时候立即爆炸,聚集氢气的时间很少。
2Cs+2H2O→2CsOH+H2↑铯的化学性质与其他碱金属类似,但是更接近于其上面的铷的化学性质。
其通常的化合价为+1。
铯是电正性最强的化学元素。
注:电正性是指元素脱去电子成为阳离子的难易度Cs+的盐通常无色,除非阴离子有颜色。
许多具有潮解性,铯的乙酸盐、碳酸盐、卤化物、氧化物、硝酸盐和硫酸盐可溶于水。
复盐通常溶解度较小,硫酸铝铯溶解度较小的性质常用来从矿石中提纯铯。
氢氧化铯(CsOH)是一种具有强烈吸水性的强碱。
它能迅速腐蚀半导体材料(例如硅)表面。
过去化学家曾认为CsOH是“最强的碱”,因为Cs+与OH-的相互作用很微弱。
但是许多无法存在于水溶液中的化合物的碱性远比CsOH强,例如正丁基锂和氨基钠。
铯与金的化学计量1:1的混合物加热后可以反应形成黄色的金化铯。
这里的金阴离子表现为拟卤素。
该化合物能够与水发生剧烈反应,生成氢氧化铯、金属金以及氢气。
铯的特性和在原子钟中的应用铯(Cs)是一种余辉金属元素,具有一些独特的特性,使其在科学和技术领域有着广泛的应用。
本文将讨论铯的特性及其在原子钟中的应用。
一、铯的特性铯具有以下几个重要的特性:1. 原子结构:铯的原子序数为55,原子结构为1s²2s²2p⁶3s²3p⁶4s²3d¹⁰4p⁶5s²4d¹⁰5p⁶6s¹,其中最外层只有一个电子。
这使得铯可以很容易地丢失外层电子,形成正离子。
2. 金属性质:铯是一种银白色的金属,具有良好的导电性和热导性。
它的熔点相对较低,为28.4摄氏度,使得它可以在常温下被轻松液化。
3. 化学反应性:铯是一种高度活泼的金属,它可以与氧气、水和其他非金属元素反应。
与水反应时,会剧烈放出氢气并产生碱性氢氧化铯。
4. 原子钟精准度:铯拥有非常稳定的原子核结构,因此被广泛用于制造原子钟。
它的电子外层只有一个电子,这使得其原子核与电子之间的相互作用较小,不受外界条件影响较小。
二、原子钟中的铯应用原子钟是一种利用放射性元素的原子振荡频率来测量时间的仪器。
铯在原子钟中的应用主要集中在以下两个方面:1. 铯原子振荡:原子钟利用铯原子内部的电子进行振荡。
当铯原子经过精确的能级跃迁时,会放出一个特定的微波频率。
原子钟通过测量这个频率来计算时间的流逝。
2. 原子钟稳定性:铯原子具有非常稳定的振荡频率。
根据国际单位制,1秒被定义为铯原子的某个特定跃迁的9,192,631,770次振荡的持续时间。
这种稳定性使得原子钟具有非常高的时间测量精度。
三、其他应用领域铯的特性使其在其他领域也有应用:1. 医学:铯-137(Cs-137)是一种放射性铯同位素,广泛用于放射治疗和放射诊断。
2. 密封材料:由于铯的低熔点和良好的密封性能,它被用作制造密封材料,如真空管封材料。
3. 光学:铯在一些光学应用中起到重要作用,如光谱分析和光纤通信。
caesium介绍
【原创实用版】
目录
1.铯的基本信息
2.铯的发现历史
3.铯的化学性质
4.铯的应用领域
5.铯的环保及安全问题
正文
铯(Cs,Caesium)是一种碱金属元素,原子序数为 55,位于周期表的第六周期第 IA 族。
它的原子半径较大,电子亲和能和电离能较低,因此具有活泼的化学性质。
铯的英文名称“Caesium”来源于拉丁文“caesius”,意为“天蓝色”,这是因为铯的化合物在溶液中呈现天蓝色。
铯的发现历史可以追溯到 1860 年,德国化学家罗伯特·本生在分析矿泉水时发现了这种新元素。
他通过光谱分析发现,这种矿泉水中含有一
种未知的碱金属元素,并根据其光谱线的特征,将其命名为铯。
在化学性质方面,铯具有较强的还原性,容易与水反应生成氢气和氢
氧化铯。
由于它的活泼性,铯在自然界中主要以化合物的形式存在,很少有游离态的铯。
在工业上,铯的制备通常采用电解法制备,通过电解熔融的氯化铯得到金属铯。
铯在许多领域都有广泛的应用。
在原子钟制造中,铯是一种重要的元素,因为铯原子的辐射频率非常稳定,可以用来制作高精度的原子钟。
此外,铯还用于医学成像设备、光电子器件、磁流体密封等高科技领域。
然而,铯的使用也带来了一些环保和安全问题。
由于铯具有较强的放
射性,因此在使用过程中需要严格遵循安全规程。
此外,铯在环境中的迁
移和累积可能会对生态环境造成影响。
铯137小知识1、什幺是铯137?铯(Cs)是一种呈银色的软金属。
铯(Cs)是一种呈银色的软金属。
它的同位素中,天然存在的铯133是一种稳定同位素,而其他铯同位素则属于放射性。
它的同位素中,天然存在的铯133是一种稳定同位素,而其他铯同位素则属于放射性。
铯137是核弹、核武器试验和核反应堆内核裂变的副产品之一,它会释放伽玛射线。
铯137是核弹、核武器试验和核反应堆内核裂变的副产品之一,它会释放伽玛射线。
因为铯137的半衰期较长,达30年,如果透过进食或呼吸,摄入了铯137,或受到沉降在地面上的铯137所照射,都会对身体有较持久的影响。
因为铯137的半衰期较长,达30年,如果透过进食或呼吸,摄入了铯137,或受到沉降在地面上的铯137所照射,都会对身体有较持久的影响。
2、铯137如何应用在医院?铯137是一种常用的伽马辐射源。
铯137是一种常用的伽马辐射源。
辐射源是用于校对医治癌症的放射治疗设备,也可以用于校对用来监测放射治疗人员及病人所接受的辐射水平的辐射监测仪器。
辐射源是用于校对医治癌症的放射治疗设备,也可以用于校对用来监测放射治疗人员及病人所接受的辐射水平的辐射监测仪器。
这些医疗设备和仪器需要定期校对,以确保它们的准确性。
这些医疗设备和仪器需要定期校对,以确保它们的准确性。
3、铯137对人类健康有什幺影响?铯137对人体的影响取决于其辐射强度,暴露时间和受影响的人体细胞种类等。
铯137对人体的影响取决于其辐射强度,暴露时间和受影响的人体细胞种类等。
如果涉及的铯137是一个非常高辐射的放射源,可能会引起急性放射病症例如:恶心,疲倦,呕吐及毛发脱落等,如果受到约1希沃特辐射剂量的直接照射,甚至可以引致死亡。
如果涉及的铯137是一个非常高辐射的放射源,可能会引起急性放射病症例如:恶心,疲倦,呕吐及毛发脱落等,如果受到约1希沃特辐射剂量的直接照射,甚至可以引致死亡。
处理如此高辐射的放射源需要专业或受过适当训练的人员。
铯原子质子数
(原创实用版)
目录
1.铯原子的基本信息
2.铯原子的质子数
3.铯原子的应用
正文
铯原子是一种化学元素,它的原子序数是 55,属于碱金属元素。
铯原子的原子结构是由 55 个质子和不同数量的中子组成的。
质子是原子核中带正电荷的粒子,它们的数量决定了元素的原子序数。
铯原子的质子数是 55,这意味着它的原子核中含有 55 个质子。
由于质子带正电荷,它们之间的排斥力使原子核变得非常稳定。
同时,铯原子的电子层结构为 2, 8, 18, 18, 7,这意味着它的外层电子属于第七周期。
铯原子有许多应用,其中最重要的是在原子钟中的应用。
铯原子钟是一种精密的时间测量设备,它利用铯原子的特定谱线来测量时间。
由于铯原子的振动频率非常稳定,因此铯原子钟的精度非常高,被广泛用于科学研究和精密测量领域。
此外,铯原子还被用于医学成像技术中。
由于铯原子能够与人体组织相互作用,因此它们可以用于医学成像。
例如,铯原子可以用于正电子发射断层扫描(PET)和单光子发射计算机断层扫描(SPECT)等技术中。
总之,铯原子是一种碱金属元素,它的原子序数是 55,原子核中含有 55 个质子。
第1页共1页。
铯离子的半径1. 引言铯(Cs)是一种化学元素,位于周期表的第六组,属于碱金属。
铯离子是指铯原子失去一个电子后形成的带正电荷的离子。
本文将探讨铯离子的半径及其相关性质。
2. 铯离子的定义和特点铯离子(Cs+)是一个带正电荷的铯原子,它具有以下特点: - 带正电荷:铯原子失去了一个外层电子,从而形成带正电荷的离子。
- 大尺寸:由于失去了一个外层电子,铯离子比原来的铯原子更大。
3. 铯离子半径与周期表趋势周期表中,元素的原子半径通常随着周期数增加而增加。
然而,在同一周期内,随着从左到右移动,原子半径会减小。
这是由于核电荷增加导致外层电子受到更强吸引力的结果。
对于碱金属来说,它们在同一周期内具有相似的化学性质,并且具有类似趋势的原子半径变化。
铯位于第六周期,是周期表中最大的元素之一。
因此,铯离子的半径相对较大。
4. 铯离子半径的测量方法实验中,测量离子半径的常用方法是通过晶体结构分析。
晶体结构分析可以确定晶体中离子的位置和间距,从而得出离子半径。
另一种常用的方法是通过X射线衍射实验来测量晶体的空间结构。
通过测量X射线衍射图案中的衍射角度和强度,可以得到晶格常数和离子半径。
5. 铯离子半径的实际值根据实验数据和理论计算,铯离子的半径约为1.81 Å(埃)。
需要注意的是,铯离子在不同化合物中可能具有不同的半径。
这是由于与其他原子形成化学键时,电荷分布可能会发生变化,从而影响到离子半径。
6. 铯离子半径的应用铯离子具有较大的半径和正电荷,并且在许多领域具有广泛应用: - 原子钟:铯原子钟利用铯离子的特性来测量时间,其中铯离子的振荡频率用作钟摆的基准。
- 光学器件:铯离子在光学器件中用作激光器的工作介质,其大尺寸和稳定性使其成为理想的选择。
- 医学应用:铯离子在医学放射治疗中常用于治疗癌症,其较大的半径有助于增强辐射效果。
7. 结论铯离子是带正电荷的铯原子失去一个外层电子后形成的离子。
由于失去了一个电子,铯离子比原来的铯原子更大。
铯的基本常识
铯是低熔点金属,纯净的金属铯呈金黄色,密度1.878,熔点28.4℃,沸点669.3℃。
在碱金属中,铯的熔点和沸点最低,蒸气压最高,正电性最强,电离势和电子逸出功最小。
在室温下,金属铯在空气中猛烈燃烧,在纯氧中则会发生爆炸,生成超氧化铯。
铯与水剧烈作用,甚至与-116℃的冰也能剧烈反应,生成氢氧化铯和氢气。
因此,铯必须在严密隔绝空气的情况下保存在液体石蜡中。
铯与有限量氧气作用,可生成氧化铯,还能与卤素发生反应。
铯和其他碱金属可形成低熔点合金,如含钠12%、钾47%、铯41%的合金,熔点为-78℃;含铷13%、铯87%的合金,熔点为-39℃;含钠5.5%、铯94.5%的合金,熔点为-29℃。
铯在地壳中含量比较少, 主要分散在锂辉石、锂云母、铁锂云母中,在钾长石、天河石、钾盐和光卤石等矿物中与钾、钠、锂呈类质同像存在。
主要的铯矿物是铯榴石(2Cs2O•2Al2O3•9SiO2•H2O),含Cs2O 34.6%。
还有硼铯铷矿,含Cs2O 3.5%;铯绿柱石,含Cs2O1.72~3.6%,但较稀少。
铯化合物的提取:从铯榴石中提取铯化合物的方法有盐酸法,还有氯化焙烧法、盐熔法和硫酸法。
盐酸法是将经过拣选或浮选的铯榴石的精矿(含Cs2O 20~30%)磨细后,以浓盐酸搅拌浸出,精矿中的铯转化成氯化铯,以水稀释,并加入三氯化锑盐酸溶液,析出氯化锑铯复盐(3CsCl•2SbCl3)。
由于锑铯复盐在盐酸溶液中的溶解度比铷、钾复盐小,铷、钾大部分留在母液中而与铯分离。
锑铯复盐加入10倍重量的水,煮沸,水解生成白色的碱式氯化锑沉淀,反应式为:3CsCl•2SbCl3+2H2O→3CsCl+2SbOCl↓+4HCl,氯化铯重新进入溶液。
溶液中通入H2S气体,除去残余的锑及其他重金属。
将精制液煮沸,蒸发浓缩,冷却结晶,经干燥得到氯化铯。
氯化焙烧法是将铯榴石同碳酸钙和氯化钙混合,在800~900℃焙烧后以水浸出。
盐熔法是将铯榴石与氯化纳和碳酸钠混合,于800~850℃熔融,再以水浸出。
两种方法的浸出液经过净化均可以用4-仲丁基-2(α-甲苄基)苯酚(简称BAMBP)-脂肪烃煤油萃取,以盐酸或二氧化碳加水反萃,得氯化铯或碳酸铯产品。
金属铯的制取:常用金属热还原法以钙还原氯化铯。
此法在小于10-3托真空下,温度700~900℃进行还原反应,产生的铯蒸气,经冷凝后成液态收集。
熔盐电解法制取金属铯是以液态铅作阴极,石墨作阳极,于700℃电解氯化铯,由阴极得到含铯8.5%的铅铯合金。
合金于600~700℃真空蒸馏,除去铅等杂质,制得纯铯。
铯的主要工业用途是制造光电池、光电倍增管和电视摄象管以及用作真空管的吸气剂。
由钠和铊激活的碘化铯可制作工业和医疗用的X射线图象放大板或荧光屏。
用铯形成的人工铯离子云,可以进行电磁波的传播和反射。
铯在多种有机、无机合成中用作助催化剂或催化剂。
铯盐还用于生产激光用的玻璃、低熔点玻璃和纤维透镜玻璃。
铯还可用于制作铯原子钟。
在铯离子热电转换器、铯离子发动机、磁流体发电系统以及超临界蒸气发电系统等新能源研究中均用到铯。
多种铯盐用于微量分析和用作药物。
金属铯的活性很强,在空气中燃烧会喷溅,产生浓密的碱性烟雾,伤害眼睛、呼吸系统和皮肤。
因此在生产、贮存及运输时必须严格防止金属铯同空气或水接触。
金属铯转移时,
一般在熔融状态(65℃)进行。
常用的方法有针筒抽吸,虹吸,惰性气体中倾注、压送,或真空抽吸等。