核外电子的排布(1)
- 格式:ppt
- 大小:741.50 KB
- 文档页数:3

【21】以第1、2、3周期的元素为例,了解原子核外电子排布规律。
1.核外电子排布的一般规律。
(1)各电子层最多容纳的电子数目为2n2。
(2)最外层不超过8个电子(K层例外)。
(3)次外层电子数目不超过18个,倒数第三层电子数目不超过32个。
核外电子排布规律的依据:(1)核外电子运动的特点①电子的质量很小,运动空间很小,但电子的运动速度很快,接近于光速。
②在高速的运动时,不能找到运动轨迹,不能准确地测量和计算出电子的确切位置。
(2)核外电子总是尽先排布在能量最低电子层里,然后由里到外,依次排布在能量逐步升高的电子层里。
总之,是核外电子运动的客观事实。
2.元素的性质与元素的原子核外电子排布的关系。
(1)稀有气体的不活泼性。
稀有气体元素的原子最外层有8个电子(氦是2个)处于稳定结构,因此化学性质稳定,一般不跟其它物质发生化学反应。
(2)非金属性与金属性(一般规律)最外层电子数得失电子趋势元素的性质金属元素4易得非金属性3.第1、2、3周期的元素(短周期元素)微粒结构特点(1)稀有气体原子的电子层结构与同周期的非金属元素形成的阴离子的电子层结构相同,与下一周期的金属元素形成的阳离子的电子层结构相同(所谓电子层结构相同是指:电子层数相同;电子总数相同;各层电子数相同)。
①与He核外电子排布相同的离子有:H-、Li、Be2②与Ne电子层结构相同的离子有:F-、O2-、N3-、Na、Mg2、A3③与Ar原子电子层结构相同的离子有:C-、S2-、和Y n-的核外电子排布相同,则下列关系式中正确的是()A a=b+m+nB a=b-m+nC a=b+m-nD a=b-m-n【解析】由元素X、Y的核电荷数分别是a和b,离子X m和Y n-的核外电子排布相同,可得:a-m=b+n,即a=b+m+n。
【答案】A【点评】离子X m和Y n-可表示为:a X m和b Y n-。
a X m意为a X原子失去m个电子形成的阳离子,所以a X m的电子数为a-m;b Y n-意为b Y原子得到n个电子形成的阴离子,所以b Y n-的电子数为b+n。

核外电子排布规律:(1)电子尽量先排能量低的电子层,再排能量高的。
(2)每个电子层最多能容纳22n个电子(3)最外层不能超过8个(4)次外层不能超过18个,类推倒数第三层不能超过32个电子。
怎样确定原子的电子层排布唐荣德一、电子层容量原理在原子核外电子排布中,每个电子层最多容纳的电子数为2n2,这个规律在一些无机化学教材中叫做最大容量原理。
我认为,该原理并不能全面反映原子核外电子排布的真实情况,其一,它只适合于离核近的内电子层,且不是最大,而是等于2n2;其二,离核远的外电子层,实际排布的电子数则远远小于2n2,根本不能用此原理来描述。
离核近的内电子层与离核远的外电子层,各有其电子容量的规律,原子的电子层排布,就是这两种规律结合而成的。
为此,我总结出内电子层和外电子层的各自的容量规律,并将两者结合起来,称为“电子层容量原理”,其内容如下:设ω为原子的电子层数,n为从原子核往外数的电子层数,m为由原子最外层往里数的电子层数。
当n<22ω+时,为内电子层,每个电子层容纳的电子数=2n2。
当n≥22ω+时,为外电子层,每个电子层最多容纳的电子数=2(m+1)2。
核外只有k层时,最多容纳2个电子。
由上述两个关系组成的电子层排布如下:从以上图示可知,原子的电子排布是两头少,中间多。
应用电子层容量原理,可使外电子层不用2n2,避免出现太大偏差。
应用外电子层的公式,可以取代中学教材中的如下规律:(1)最外层电子数不超过8个(最外层为K层,则不超过2个)。
(2)次外层电子数不超过18个。
(3)外数第三层电子数不超过32个。
……因为这些规律可直接从外电子层的公式推出。
稀有气体原子的电子层排布则是很规整的相等关系,其内电子层电子数为2n2,外电子层电子数为2(m+1)2,因此,稀有气体元素原子的电子层结构是一种稳定结构。
主族元素的原子,最外层未达到2(m +1)2个电子(即8个电子),一般副族元素的原子,最外层和次外层的电子数均小于2(m +1)2。


核外电子的排布规律一、能量最低原理所谓能量最低原理是,原子核外的电子,总是尽先占有能量最低的原子轨道,只有当能量较低的原子轨道被占满后,电子才依次进入能量较高的轨道,以使原子处于能量最低的稳定状态.原子轨道能量的高低为:1.当n相同,l不同时,轨道的能量次序为s<p<d<f.例如,E3S<E3P<E3d。
2.当n不同,l相同时,n愈大,各相应的轨道能量愈高。
例如,E2S<E3S<E4S.3.当n和l都不相同时,轨道能量有交错现象.即(n-1)d轨道能量大于ns轨道的能量,(n-1)f轨道的能量大于np轨道的能量.在同一周期中,各元素随着原子序数递增核外电子的填充次序为ns,(n-2)f,(n-1)d,np。
核外电子填充次序如图1所示。
图1 电子填充的次序图2 多电子原子电子所处的能级示意图最外层最多能容纳8电子,次外层最多能容纳18电子。
每个电子层最多容纳的电子数为2n2个(n为电子层数的数值)如:各个电子层中电子的最大容纳量电子层(n) K(1)L(2)M(3) N(4)电子亚层s s p s p d s p d f 亚层中的轨道数 1 1 3 1 3 5 1 3 5 7 亚层中的电子数 2 2 6 2 6 10 2 6 10 14 每个电子层中电子2 8 18 32的最大容纳量(2n2)从表可以看出,每个电子层可能有的最多轨道数为n2,而每个轨道又只能容纳2个电子,因此,各电子层可能容纳的电子总数就是2n2。
二、鲍利(Pauli)不相容原理鲍利不相容原理的内容是:在同一原子中没有四个量子数完全相同的电子,或者说在同一原子中没有运动状态完全相同的电子。
例如,氦原子的1s轨道中有两个电子,描述其中一个原子中没有运动状态的一组量子数(n,l,m,ms)为1,0,0,+1/2,另一个电子的一组量子数必然是1,0,0,-1/2,即两个电子的其他状态相同但自旋方向相反。
根据鲍利不相容原理可以得出这样的结论,在每一个原子轨道中,最多只能容纳自旋方向相反的两个电子。

结构理论(一)核外电子的运动状态和排布规律围绕在原子核外作高速运动的电子,有它特殊的运动状态。
早在本世纪初,科学实验已证明了电子是一种质量为9.11×10-28g的微小粒子,证明了电子的运动具有粒子性。
但是,以后科学实验又证明了电子的运动和光、X射线一样具有波动性。
这就是说,电子的运动具有波粒二象性。
电子运动的这种波粒二象性,使它难以用经典物理学的一些基本定律来描述。
现代研究核外电子运动状态的理论叫做原子波动力学。
它是在上世纪20年代末由奥地利物理学家薛定谔等人发展起来的。
它的基本方面是一些复杂的数学波动方程,叫做薛定谔方程。
核外电子的运动正是通过计算薛定谔方程的解来加以描述的。
这里,我们只能按照原子波动力学的基本观点,初步形象地去认识核外电子的运动状态,从而再寻找出原子核外电子的排布有着怎样的规律。
一、电子云在描绘核外电子运动时,只能指出它在原子核外空间各处出现机会的多少。
电子在核外空间一定范围内出现,好像是带负电荷的云雾笼罩在原子核的周围。
可以形象地称它为“电子云”。
核外电子出现机会愈多的区域,电子云的密度愈大。
下图描绘了氢原子处于基态时的电子云。
氢原子核外只有1个电子,图中的“雾状”,说明氢原子核外电子在一个球形的空间里作高速运动。
图中表示,黑点密集处是电子出现机会多的地方,黑点稀疏处是电子出现机会少的地方。
二、描述核外电子运动状态的四个方面对于原子核外的每一个电子的运动状态,都可以从以下四个方面来描述。
1.电子层原子核外的电子可以看作是分层排布的。
处于不同层次中的电子,离核的远近也不同。
离核愈近的电子层能量愈低,离核愈远的电子层能量愈高。
通常用n=1、2、3…等数值来表示电子层离核的远近。
n=1,即表示离核最近的电子层,其中的电子能量最小。
n=2,即表示为第二电子层。
有时也用K、L、M、N、O等分别表示1、2、3、4、5等电子层。
我们怎么知道含有多个电子的原子里核外电子的能量并不相同呢?根据对元素电离能数据的分析,可以初步得到这个结论。


精心整理原子核外电子排布规律①能量最低原理:电子层划分为K<L<M<O<P<Q,对应电子层能量增大;原子核外电子排布按照能量较低者低优先排布原则.②每个电子层最多只能容纳2n2个电子。
③最外层最多只能容纳8个电子(K层为最外层时不能超过2个)次外层最多只能容纳18个电子(K层为次外层时不能超过2个倒数第三层最多只能容纳32个电子注意:多条规律必须同时兼顾。
简单例子的结构特点:(1)离子的电子排布:主族元素阳离子跟上一周期稀有气体的电子层排布相同,如钠离子、镁离子、铝离子和氖的核外电子排布是相同的。
阴离子更同一周期稀有气体的电子排布相同:负氧离子,氟离子和氖的核外电子排布是相同的。
(2)等电子粒子(注意主要元素在周期表中的相对位置)①10电子粒子:CH4、N-3、NH-2、NH3、NH+4、O-2、OH-、H2O、H3O+、F-、HF、Ne、Na+、Mg+2、Al+3等。
②18电子粒子:SiH4、P-3、PH3、S-2、HS-、H2S、Cl-、HCl、Ar、K+、Ca+2、PH+4等。
特殊情况:F2、H2O2、C2H6、CH3OH③核外电子总数及质子总数均相同的阳离子有:Na+、NH+4、H3O+等;阴离子有:F-、OH-、NH-2;HS-、Cl-等。
前18号元素原子结构的特殊性:(1)原子核中无中子的原子:11H(2)最外层有1个电子的元素:H、Li、Na;最外层有2个电子的元素:Be、Mg、He(3)最外层电子总数等于次外层电子数的元素:Be、Ar(4)最外层电子数等于次外层电子数2倍的元素:C;是次外层电子数3倍的元素:O;是次外层电子数4倍的元素:Ne(5)最外层电子数是内层电子数一半的元素:Li、P(6)电子层数与最外层电子数相等的元素:H、Be、Al(7)电子总数为最外层电子数2倍的元素:Be(8)次外层电子数是最外层电子数2倍的元素:Li、Si元素周期表的规律:(1)最外层电子数大于或等于3而又小于8的元素一定是主族元素,最外层电子数为1或2的元素可能是主族、副族或0族元素,最外层电子数为8的元素是稀有气体(He例外)(2)在元素周期表中,同周期的ⅡA、ⅢA族元素的原子序数差别有:①第2、3周期(短周期)元素原子序数都相差1;②第4、5周期相差11;③第6、7周期相差25(3)同主族、邻周期元素的原子序数差①位于过渡元素左侧的主族元素,即ⅠA、ⅡA族,同主族、邻周期元素原子序数之差为下一周期元素所在周期所含元素总数;相差的数分别为2,8,8,18,18,32②位于过渡元素左侧的主族元素,即ⅢA~ⅦA族,同主族、邻周期元素原子序数之差为下一周期元素所在周期所含元素种数。

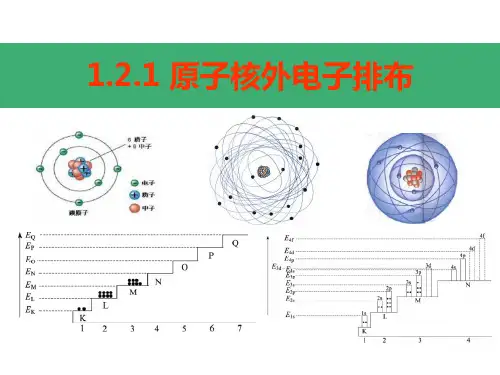

核外电子的排布规律之一首先,各电子层最多容纳的电子数目是2n2。
其次,最外层电子数目不超过8个(K层为最外层时不超过2个)。
第三,次外层电子数目不超过18个,倒数第三层电子数目不超过32个。
核外电子总是尽先排布在能量最低的电子层里,然后再由里往外依次排布在能量逐步升高的电子层里。
以上几点是互相联系的,不能孤立地理解。
核外电子的排布规律之二核外电子排布遵循泡利不相容原理、能量最低原理和洪特规则。
能量最低原理就是在不违背泡利不相容原理的前提下,核外电子总是尽先占有能量最低的轨道,只有当能量最低的轨道占满后,电子才依次进入能量较高的轨道。
也就是尽可能使体系能量最低。
洪特规则是在等价轨道(相同电子层、电子亚层上的各个轨道)上排布的电子将尽可能分占不同的轨道,且自旋方向相同。
后来量子力学证明,电子这样排布可使能量最低,所以洪特规则可以包括在能量最低原理中,作为能量最低原理的一个补充。
在同一个原子中,离核越近、n越小的电子层能量越低。
在同一电子层中,各亚层的能量按s、p、d、f的次序增高的。
因此,E1s<E2s<E3s……;E4s<E4p <E4d……。
在多电子的原子里的各个电子之间存在相互作用,研究某个外层电子的运动状态时,必须同时考虑到核及其它电子对它的作用。
由于其它电子的存在,往往减弱了原子核对外层电子的作用力,从而使多电子原子的电子能级产生交错现象核外电子的排布规律之三(1)泡利不相容原理泡利不相容原理是奥地利物理学家泡利提出来的。
他指出,在同一个原子中,不可能有运动状态完全相同的两个电子存在。
或者说,运动状态完全相同的电子在同一原子里是不能并存的、是互不相容的。
如果同一原子中的电子前三种运动状态完全一样,那么处于同一轨道上的电子其第四种运动状态——自旋方向必然不同。
由此,可以推论:同一原子中每一个轨道上只能容纳两个自旋方向相反的电子。
根据泡利不相容原理可推算出各个电子层可能容纳的电子数为2n2个。

原子结构核外电子排布原子是构成物质的基本粒子,由原子核和核外电子组成。
原子的核心包含质子和中子,而电子则以轨道的方式绕核心运动。
核外电子的排布对原子的化学性质和化合能力产生重要影响。
以下是关于原子结构核外电子排布的详细介绍。
在经典的玻尔理论中,电子的排布被描述为沿不同轨道(也称为能级)绕核心旋转。
每个能级最多能容纳一定数量的电子,根据波尔理论,每个能级上的电子数量可以用以下公式计算:2n²(n为能级的编号)根据这个公式,第一能级(最靠近原子核的能级)最多可以容纳2个电子,第二能级最多可以容纳8个电子,第三能级最多可以容纳18个电子,以此类推。
这个公式说明了为什么特定能级上的电子数量不同。
然而,随着量子力学的发展,人们意识到玻尔理论只能部分解释原子结构。
量子力学描述了电子运动的波动性质,并引入了概率密度的概念,用来描述电子在不同位置出现的可能性。
根据量子力学,电子不能准确地被定位在轨道上的一些点上,而是存在于一个电子云中。
电子云是描述电子出现概率分布的三维区域,具有不同概率密度的区域对应着不同的轨道形状。
根据不同的轨道形状,电子的能量也不同。
主要能级被标记为1,2,3...,并由字母s,p,d,f等来表示不同的子能级。
每个主要能级的子能级又分别由s,p,d,f等轨道来区分。
s轨道是最基本的,是球形对称的,最多能容纳2个电子。
每个能级的第一个子能级都是s轨道,即1s,2s,3s等。
p轨道是具有 dumbbell(哑铃形)形状的轨道,并且在空间中有不同的方向。
每个能级的第二个子能级都是p轨道,即2p,3p,4p等。
每个p轨道最多能容纳6个电子。
d轨道是复杂的轨道形状,涉及到更多的区域和方向。
每个能级的第三个子能级都是d轨道,即3d,4d,5d等。
每个d轨道最多能容纳10个电子。
f轨道是更复杂的轨道形状,涉及到更多的区域和方向。
每个能级的第四个子能级都是f轨道,即4f,5f等。
每个f轨道最多能容纳14个电子。
v核外电子层排布
核外电子的分层排布规律:
1、第一层不超过2个,第二层不超过8个;
2、最外层不超过8个。
每层最多容纳电子数为2n2个(n代表电子层数),即第一层不超过2个,第二层不超过8个,第三层不超过18个;
3、最外层电子数不超过8个(只有1个电子层时,最多可容纳2个电子)。
4、最低能量原理:电子尽可能地先占有能量低的轨道,然后进入能量高的轨道,使整个原子的能量处于最低状态。
5、泡利原理:每个原子轨道里最多只能容纳2个电子,且自旋状态相反。
6、洪特规则:当电子排布在同一能级的不同轨道时,基态原子中的电子总是优先单独占据一个轨道,且自旋状态相同。