大学化学自招,“强基计划”针对训练-2008年复旦大学自主招生化学真题
- 格式:docx
- 大小:393.56 KB
- 文档页数:3
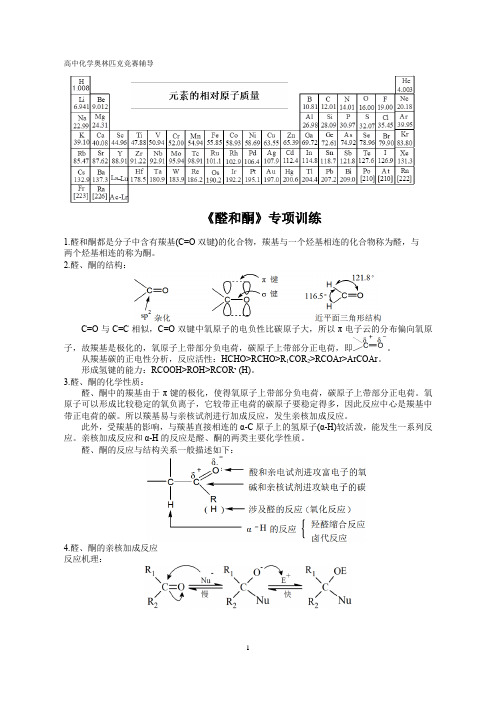
高中化学奥林匹克竞赛辅导《醛和酮》专项训练1.醛和酮都是分子中含有羰基(C=O双键)的化合物,羰基与一个烃基相连的化合物称为醛,与两个烃基相连的称为酮。
2.醛、酮的结构:C=O与C=C相似,C=O双键中氧原子的电负性比碳原子大,所以π电子云的分布偏向氧原子,故羰基是极化的,氧原子上带部分负电荷,碳原子上带部分正电荷,即。
从羰基碳的正电性分析,反应活性:HCHO>RCHO>R1COR2>RCOAr>ArCOAr。
形成氢键的能力:RCOOH>ROH>RCOR、(H)。
3.醛、酮的化学性质:醛、酮中的羰基由于π键的极化,使得氧原子上带部分负电荷,碳原子上带部分正电荷。
氧原子可以形成比较稳定的氧负离子,它较带正电荷的碳原子要稳定得多,因此反应中心是羰基中带正电荷的碳。
所以羰基易与亲核试剂进行加成反应,发生亲核加成反应。
此外,受羰基的影响,与羰基直接相连的α-C原子上的氢原子(α-H)较活泼,能发生一系列反应。
亲核加成反应和α-H的反应是醛、酮的两类主要化学性质。
醛、酮的反应与结构关系一般描述如下:4.醛、酮的亲核加成反应反应机理:(1)与HCN的加成反应:反应范围:醛、脂肪族甲基酮。
ArCOR和ArCOAr难反应。
α-羟基腈是很有用的中间体,它可转变为多种化合物,例如:总结:含碳亲核试剂的亲核性:RC≡CNa>RLi>RMgX>HCN。
(2)与饱和NaHSO3的加成反应:产物α-羟基磺酸盐为白色结晶,不溶于饱和的NaHSO3溶液中,容易分离出来;与酸或碱共热,又可得原来的醛、酮。
故此反应可用以分离提纯醛、酮。
(3)与醇的加成反应:在强的无水酸(干燥的氯化氢)催化下,醛酮与过量的醇反应首先得到半缩醛或半缩酮,最后可生成缩醛或缩酮。
形成的缩醛或缩酮,对碱、氧化剂、还原剂都相当稳定,但在稀酸催化下可水解生成原来的醛酮,因此常作为羰基的保护方法。
醛较易形成缩醛,酮在一般条件下形成缩酮较困难,用1,2-二醇或1,3-二醇则易生成缩酮。

复旦自主招生试题复旦大学是中国知名的综合性高等教育机构,旨在培养具有创新意识和全球视野的高素质人才。
为了选拔优秀的学生,复旦大学设立了自主招生项目。
以下是一些典型的复旦大学自主招生试题,希望能帮助考生更好地准备自主招生考试。
1. 个人表现和领导能力(1) 请列举你在学校或社会活动中的个人成就,并解释你如何在领导团队或组织中发挥作用。
(2) 请描述一个你曾经遇到过的具体问题,解释你是如何解决这个问题的,并思考你从中学到了什么。
2. 学术潜力和研究兴趣(1) 请列举你在学校学习中的最骄傲的成绩和奖项,并解释你在这些学科中的研究兴趣或潜力。
(2) 请描述一个你在学术研究或实践中的项目,解释你在这个项目中的角色和所取得的成就。
3. 社会责任和公益活动(1) 请列举你在社会公益活动中的经历,并说明你对社会问题的看法和态度。
(2) 请描述一个你参与的具体公益活动,解释你对这个项目的贡献和对社会的影响。
4. 外语能力和跨文化交流(1) 请描述你的英语水平和你如何提高你的英语表达能力。
(2) 请根据你的经历,谈谈你对国际交流和跨文化交流的看法,并举例说明你在这方面的经验。
5. 自主学习和创新思维(1) 请描述一个你自主学习的经历,解释你如何培养了自主学习的能力。
(2) 请从你的角度出发,谈谈你对创新思维的理解,并举例说明你如何应用创新思维解决问题。
6. 价值观和人生目标(1) 请谈谈你的价值观和人生目标,并解释这些价值观和目标对你的影响。
(2) 请描述一个具体的情况,解释你如何遇到挫折并坚持追求目标。
以上是一些可能出现在复旦大学自主招生考试中的典型问题。
希望考生能认真思考并准备好答案,展示自己的优势和潜力。
同时,希望考生在撰写答案时能够充分发挥个人思考和表达能力,以增加自己的竞争力。
祝愿所有参加复旦大学自主招生考试的学生取得优异的成绩,实现自己的理想!。

A .溴化亚铁溶液中通人少量氯气: 2Br + Cl = Br + 2Cl H 2 S高校自主招生考试(化学)真题集萃参考答案 1.(08 北理工)在体积为 VL 的干燥烧瓶中用排空气法冲入氯化氢气体后,测得烧瓶中气体对氧气的相对密度为 1.082。
若用此气体进行喷泉实验,在喷泉停止后,进入烧瓶中的 液体的体积是( )A .VLB . 3 4 VLC . 1 2 VLD . 1 4 VL 解析 烧瓶中气体的相对平均分子质量为 1.082×32 = 34.624,根据 29× x %+36.5×(1— x %)=34.624,可求出氯化氢气体占混合气体的 3 4 ,B 正确。
2.(09 北理工)能正确反应表示下列反应的离子方程式( 2 )B .实验室氯化铁溶液制取氢氧化铁胶体:Fe + 3H 2O Fe (OH )3(胶本)+3H +C .硫酸铜溶液中加入氢氧化钡溶液: Ba + SO 42 = BaSO 4D .用湿润的醋酸铅试纸检验 H 2 S : Pb+ = PbS+2H + 解析 选项 A 氯气应先和亚铁离子反应。
选项 C 中还有氢氧化铜生成。
选项中 D 中有醋 酸生成。
B 正确。
3.(08 同济大学)舞台上产生烟雾的方法很多,其中一种方法是在硝酸铵上覆盖一些锌粉,温热之,在加几滴水,即产生大量烟。
已知参加反应的NH 4 NO 3 和 Zn 物质的量之比为1:1。
(1)写出该反应方程式。
(2)烟主要是由___________组成。
(3)若不加水,是否有其他方法令反应进行?若有,写出方法。
(4)有趣的是,若硝酸铵和锌粉潮湿,或滴加的水过多,实验又会失败。
分析原因。
解析 根据氧化还原反应原理可得: (1) NH 4 NO 3 + Zn [H 2O ]ZnO + N 2 +2H 2O(2)烟为固体颗粒,故只能为 ZnO 。
(3)只要能量达到了,就有可能发生反应。

“强基计划”针对训练-2008年北京大学自主招生化学真题1.制备KMnO4的方法是先合成K2MnO4。
(1)MnO2和KOH在O2的作用下可生成K2MnO4,写出该反应的化学方程式。
(2)K2MnO4转化为KMnO4的两种方法是①通入Cl2;②电解。
分别写出反应式。
解:(1)(2)①②2.NH4+的化合价、半径均和K+相同(近),因此铵盐溶解度和相应钾盐相近。
请各举一例说明铵盐和钾盐两种不同的性质。
解:3.室温下饱和氯水浓度约为0.09mol/dm3,其中约1/3的Cl2发生了自氧化还原反应。
增加饱和溶液中HClO浓度的一种方法是:把Cl2通入到CaCO3悬浊液。
请写出反应式并简述理由。
解:4.称取16g CuSO4、25g CuSO4·5H2O各一份,分别溶于相同量水时,一种是溶解吸热,另一种是溶解放热。
溶解放热的溶质是________________。
若测得放热量和吸热量的差值为Q,由此可以得到的数据是_____________________________。
解:5.大气中CO2等气体含量增加会导致温室效应已引起广泛关注。
回答下列问题:(1)用酿造C2H5OH作燃料,不会增加大气中CO2含量。
为什么?(2)请解释为何天然气(燃烧热为892kJ/mol)与煤(主要成分为炭,燃烧热为394kJ/mol)相比是“清洁燃料”?解:6.有机物A分子式为C4H4O4,在浓硫酸、加热下能和C2H5OH反应生成B,分子式为C8H12O4;A和HBr反应得到分子式为C4H5O4Br的C,C和水在一定条件下反应得到分子式为C4H6O5的D。
请写出A、B、C、D的结构简式。
解:7.有机物A的分子式为C2H5NO2,能和NaOH反应生成相应的钠盐,在酸性溶液中易发生氮原子的质子化反应。
(1)写出A的结构简式。
(2)两个A分子脱水得B。
请写出B的结构简式及其所含官能团的名称。
(3)请写出含有B中官能团(A中没有)且有工业意义的一种环状化合物的结构简式。

自主招生化学试题及答案一、选择题(每题2分,共10分)1. 下列物质中,属于混合物的是()。
A. 蒸馏水B. 碳酸氢钠C. 空气D. 纯碱答案:C2. 化学反应中,能量变化通常表现为()。
A. 光能B. 热能C. 电能D. 机械能答案:B3. 金属活动性顺序表中,排在氢前面的金属能与酸反应生成氢气,下列金属中,不能与稀盐酸反应生成氢气的是()。
A. 铁B. 铜C. 镁D. 锌答案:B4. 下列物质中,属于电解质的是()。
A. 蔗糖B. 酒精C. 硫酸D. 氢氧化钠答案:D5. 根据质量守恒定律,下列说法正确的是()。
A. 反应前后元素种类不变B. 反应前后原子种类不变C. 反应前后原子数目不变D. 反应前后原子质量不变答案:C二、填空题(每题2分,共10分)1. 硫酸的化学式为______。
答案:H2SO42. 氧化还原反应中,得电子的物质是______。
答案:氧化剂3. 原子核由______和______组成。
答案:质子;中子4. 实验室中常用的酸碱指示剂是______。
答案:酚酞5. 根据原子结构,原子序数等于______。
答案:核内质子数三、简答题(每题5分,共20分)1. 请简述什么是氧化还原反应。
答案:氧化还原反应是指在化学反应中,原子或离子之间发生电子转移的过程,其中一个物质失去电子被氧化,另一个物质获得电子被还原。
2. 请解释什么是化学平衡。
答案:化学平衡是指在一定条件下,可逆反应中正反应速率和逆反应速率相等,反应物和生成物浓度不再发生变化的状态。
3. 什么是摩尔质量?答案:摩尔质量是指1摩尔物质的质量,以克每摩尔(g/mol)为单位,数值上等于该物质的相对原子质量或相对分子质量。
4. 请解释什么是同位素。
答案:同位素是指具有相同原子序数但不同质量数的原子,即它们具有相同数量的质子但中子数不同。
四、计算题(每题10分,共20分)1. 已知某化合物的化学式为C2H6O,其相对分子质量为46g/mol,求该化合物中碳、氢、氧元素的质量比。

高中化学奥林匹克竞赛辅导配位化学-1998-2008年全国初赛真题 2008第1题EDTA 是乙二胺四乙酸的英文名称的缩写,市售试剂是其二水合二钠盐。
1-1.画出EDTA 二钠盐水溶液中浓度最高的阴离子的结构简式。
1-2.Ca(EDTA)2-溶液可用于静脉点滴以排除体内的铅。
写出这个排铅反应的化学方程式(用Pb 2+ 表示铅)。
1-3.能否用EDTA 二钠盐溶液代替Ca(EDTA)2-溶液排铅?为什么?1-4.Na 2[Fe(CN)5(NO)]的磁矩为零,给出铁原子的氧化态。
Na 2[Fe(CN)5(NO)]是鉴定S 2-的试剂,二者反应得到紫色溶液,写出鉴定反应的离子方程式。
解:1-1. C H 2N C H 2H 2C N H 2C CH 2H 2CCOO -COO --OOC-OOC H H (2分) (-OOCCH 2)2NCH 2CH 2N(CH 2COO -)2H H 或CH 2NH(CH 2COO -)22 得2分,质子必须在氮原子上。
1-2.Pb 2++Ca(EDTA)2-=Ca 2++Pb(EDTA)2- (1分)1-3.不能。
若直接用EDTA 二钠盐溶液,EDTA 阴离子不仅和Pb 2+反应, 也和体内的Ca 2+结合造成钙的流失(答案和原因各0.5分,共 1分)1-4.+2 (2分) [Fe(CN)5(NO)]2-+S 2-= [Fe(CN)5(NOS)]4- 配合物电荷错误不得分(1分)化合物A 是近十年开始采用的锅炉水添加剂。
A 的相对分子质量90.10,可形成无色晶体,能除去锅炉水中溶解氧,并可使锅炉壁钝化。
7-1.A 是用碳酸二甲酯和一水合肼在70o C 下合成的,收率80%。
画出A 的结构式。
7-2.写出合成A 的反应方程式。
7-3.低于135o C 时,A 直接与溶解氧反应,生成三种产物。
写出化学方程式。
7-4.高于135o C 时,A 先发生水解,水解产物再与氧反应。
“强基计划”针对训练-2006年复旦大学自主招生化学真题1.2005年11月一度造成松花江水污染的化学物质是()A.苯B.甲苯C.氯苯D.硝基苯2.已知2NO+O2=2NO2+114kJ,且不生成N2O4。
下列判断正确的是()A.升温,反应速度变快B.加压,混合物颜色变浅C.加热,混合物颜色加深D.充入N2,NO转化率增大3.可用作核反应堆减速剂(也称慢化剂)的物质是()A.HClB.H2OC.NaOHD.HNO34.烯烃C4H8混合气体经O3氧化并水解后生成0.60mol酮和1.80mol醛(其中HCHO 0.90mol),则原混合气体中,2-丁烯的体积分数为()A.0.25B.0.33C.0.40D.0.505.化学式量:NaOH=40.0,Al(OH)3=78.0,Mg(OH)2=58.0。
含0.100mol Al3+和0.100mol Mg2+的酸性溶液中加入NaOH,产生沉淀4.524g。
沉淀所消耗的NaOH的质量至少为()A.6.24gB.6.60gC.6.80gD.6.96g6.设空气中O2体积分数0.25。
N2体积分数0.75。
有水存在的条件下,氮的氧化物和一定量空气混合恰好完全反应,反应后气体体积减少一半。
则该氮的氧化物是()A.NOB.NO2C.NO和NO2 2:1混合物D.NO和NO2 1:1混合物7.KCl、NaNO3、H2O为原料制取KNO3,合理的操作步骤为()A.称量、溶解、蒸发、冷却、过滤、干燥B.称量、溶解、萃取、分液、蒸馏、干燥C.称量、溶解、蒸发、过滤、冷却、过滤、干燥D.称量、溶解、蒸发、冷却、萃取、分液、干燥8.已知H2CO3的二级电离常数为K2,a mol/L NaHCO3溶液(pH=8.3)中CO32-的浓度为()A.10-8.3a K2 mol/LB.108.3a K2 mol/LC.10-8.3a/K2 mol/LD.108.3a/K2 mol/L9.太阳中主要化学元素是()A.氢B.碳C.氧D.氮10.KMnO4和H2O2之间的化学反应:MnO4-+H2O2+H+=Mn2++O2+H2O。
化学自主招生试题
1. 简答题(共10小题,每题5分,共50分)
1)请简述离子键的形成和性质。
2)铝(Al)的原子序数为13,氧(O)的原子序数为8,请写出
二氧化铝(Al2O3)的化学式,并说明其化合物的特点。
3)什么是酸碱中和反应?请举例说明。
4)请简要描述吸附现象的原理和应用。
5)请解释有机化学中的取代反应与加成反应的区别。
6)请解释化学反应速率与反应物浓度的关系,并举例说明。
7)请简述高分子材料的特点及其应用领域。
8)请解释溶解度与食盐在水中溶解的过程。
9)请简要叙述光合作用的过程和意义。
10)简述化学反应中的能量变化及其与活化能的关系。
2. 计算题(共3小题,每题10分,共30分)
1)将10g的NaOH固体加入水中,计算所得溶液的浓度(mol/L)。
2)氨气(NH3)的摩尔质量为17g/mol,若氨气的密度为0.75g/L,求氨气的摩尔浓度。
3)氢氧化钠(NaOH)的水溶液pH值为12,求其氢离子浓度。
3. 实验题(共2小题,每题20分,共40分)
1)针对盐酸和碳酸钙的反应,请设计一个简单的实验方案,并描述实验步骤和现象。
2)请设计一种方法检测未知溶液中是否含有氯离子(Cl-),并附上实验步骤和结果分析。
4. 短文题(共1题,50分)
请根据所学化学知识,写一篇短文,阐述化学在环境保护方面的重要性,并提出你个人的建议和观点。
注意:请确保所有答案清晰、准确,并且解答完整。
提交答卷时,请认真检查,确保没有拼写错误和语法错误。
祝你成功!。
高中化学奥林匹克竞赛辅导分子结构-1998-2008年全国初赛真题2008第4题(CN)2被称为拟卤素,它的阴离子CN-作为配体形成的配合物有重要用途。
4-1.HgCl2和Hg(CN)2反应可制得(CN)2,写出反应方程式。
4-2.画出CN-、(CN)2的路易斯结构式。
4-3.写出(CN)2 (g)在O2(g)中燃烧的反应方程式。
4-4.298 K下,(CN)2(g)的标准摩尔燃烧热1095 kJ/mol,C2H2(g)的标准摩尔燃烧热1300 kJ/mol,C2H2(g)的标准摩尔生成焓为227 kJ/mol,H2O(l)的标准摩尔生成焓为-286 kJ/mol,计算(CN)2(g)的标准摩尔生成焓。
4-5.(CN)2在300~500 o C形成具有一维双链结构的聚合物,画出该聚合物的结构。
4-6.电镀厂向含氰化物的电镀废液中加入漂白粉以消除有毒的CN-,写出化学方程式(漂白粉用ClO-表示)。
解:4-1.HgCl2+Hg(CN)2=Hg2Cl2 +(CN)2(1分)4-2.C N -[]C C(各1分,共2分) 短线画成电子对同样得分;不画孤对电子不得分。
4-3.(CN)2(g)+2O2(g)=2CO2(g)+N2(g) (1分)4-4.4-5.CCNNn或CCNCCNNCCNNN(2分)画成也得2分。
但画成只得1分。
4-6.2CN -+ 5ClO -+ H 2O = 2HCO 3-+ N 2 + 5Cl - (2分)2007第1题通常,硅不与水反应,然而,弱碱性水溶液能使一定量的硅溶解,生成Si(OH)4。
1-1.已知反应分两步进行,试用化学方程式表示上述溶解过程。
1-2.早在上世纪50年代就发现了CH 5+的存在,人们曾提出该离子结构的多种假设,然而,直至 1999年,才在低温下获得该离子的振动-转动光谱,并由此提出该离子的如下结构模型:氢原子围绕着碳原子快速转动,所有C-H 键的键长相等。
复旦自主招生试题复旦大学自主招生试题自主招生旨在选拔具有综合素质和潜力的优秀学生,复旦大学自主招生试题考察的是学生的才智、思维能力和学科基础。
以下是几道典型的复旦自主招生试题,帮助大家更好地了解复旦大学自主招生的考察方向和要求。
题一:数学思维某班一共有50名学生,其中有20%的学生参加了足球队,25%的学生参加了篮球队,30%的学生参加了乒乓球队,10%的学生既参加了足球队又参加了篮球队,15%的学生既参加了足球队又参加了乒乓球队,20%的学生既参加了篮球队又参加了乒乓球队,其中没有学生同时参加了三者。
请问有多少学生一个球队都没有参加?解题思路:首先我们可以利用集合论中的容斥原理来解决这个问题。
让A表示参加足球队的学生人数,B表示参加篮球队的学生人数,C表示参加乒乓球队的学生人数,根据题意可得:A +B +C - (A ∩ B) - (A ∩ C) - (B ∩ C) + (A ∩ B ∩ C) = 50其中,我们已知 A = 0.2 * 50 = 10, B = 0.25 * 50 = 12.5(约等于13),C = 0.3 * 50 = 15。
代入上式,可以计算得到:10 + 13 + 15 - (A∩ B) - (A ∩ C) - (B ∩ C) + (A ∩ B ∩ C) = 50。
再根据已知条件,可得到(A ∩ B) = 0.1 * 50 = 5,(A ∩ C) = 0.15 * 50 = 7.5(约等于8),(B ∩ C)= 0.2 * 50 = 10,(A ∩ B ∩ C) = 0。
代入上式,可得:10 + 13 + 15 - 5 - 8 - 10 + 0 = 50。
所以,有多少学生一个球队都没有参加,即(A' ∩ B' ∩ C') = 50 - 35 = 15个学生。
因此,共有15个学生一个球队都没有参加。
题二:文学赏析以下是经典文学作品的一些摘录,请阅读并简要进行评析。
“强基计划”针对训练-2008年复旦大学自主招生化学真题
1.下列不能大量共存的一组离子是()
A.OH-、NH4+
B.Cl-、NH4+
C.Na+、K+
D.OH-、CO32-
2.下列不属于同素异形体的一组物质是()
A.石墨—金刚石
B.红磷—白磷
C.氧气—臭氧
D.青铜—黄铜
3.下列氮肥中含氮量最高的是()
A.CO(NH2)2
B.NH4NO3
C.NH4HCO3
D.NH4Cl
4.下列不属于有毒气体的是()
A.光气
B.氦气
C.氯气
D.芥子气
5.若氯原子和羟基连在同一个碳原子上不能稳定存在,则一氯丙醇的同分异构体数目为()
A.2
B.3
C.4
D.5
6.明矾在净水过程中发生的变化是()
A.氧化
B.还原
C.水解
D.中和
7.用CaH2和水反应制取H2 2.24L(标准状况),需要的CaH2质量不少于()
A.4.2g
B.4.0g
C.2.1g
D.2g
8.下列有机化合物可以形成内酯的是()
A.异丙醇
B.α-羟基酸
C.β-羟基酸
D.γ-羟基酸
9.下列化合物中含有极性共价键的是()
A.NaCl
B.KOH
C.BaO2
D.CaC2
10.当吸热反应N2O4(g)2NO2(g)达平衡后,下列判断正确的是()
A.升高温度,混合物颜色变浅
B.降低压强,混合物颜色变浅
C.添加NO2(g),混合物颜色变浅
D.降低温度,混合物颜色变浅
11.下列原子序数对应的元素不属于零族元素的是()
A.56
B.54
C.36
D.18
12.下列各组元素中性质十分相近的一组元素是()
A.H、He
B.Cl、Ca
C.Be、Mg
D.P、Cu
13.由五边形和六边形组成的C540多面体中,五边形有12个,六边形有()
A.250个
B.260个
C.270个
D.280个
14.某地区曾发生天然气泄漏,其中含有毒气体。
该有毒气体是()
A.HCN
B.Cl2
C.NO2
D.H2S
15.在1.0L 0.10mol/L H2SO4水溶液中,其浓度最接近于()
A.0.22mol/L
B.0.20mol/L
C.0.11mol/L
D.0.10mol/L
16.铅蓄电池放电反应:Pb+PbO2+2H2SO4=2PbSO4+2H2O,下列判断正确的是()
A.PbO2是氧化剂
B.Pb是氧化剂
C.Pb是正极
D.PbO2是负极
答案:
1.A
2.D
3.A
4.
5.B
6.C
7.
8.
9.B
10.
11.A
12.C
13.
14.D
15.
16.。