人教版九年级化学下册课课练基础闯关练习(含答案):9.3溶液的浓度
- 格式:doc
- 大小:498.00 KB
- 文档页数:7

饱和溶液一课一练·基础闯关知识点饱和溶液与不饱和溶液的性质1.(2017·茂名一模)在20℃时,往100 g饱和食盐溶液中,加入5 g食盐,保持不变的是( )A.溶质质量B.溶剂质量C.溶液质量D.以上皆是【解析】选D。
20℃时,往100 g饱和食盐溶液中,加入5 g食盐,食盐不再溶解,故溶质质量不变,溶剂质量不变,溶液的质量不变。
2.20℃时,100 g水中不断加入NaCl固体,充分搅拌后过滤,称量所得溶液的质量如下表所示,其中属于饱和溶液的是( )选项 A B C D加入NaCl质量(g) 5 15 30 40所得溶液质量(g) 105 115 130 136【解析】选D。
结合表格数据可知加入40 g氯化钠固体后只有36 g被溶解,所以得到的溶液一定是饱和溶液。
3.(2017·上海徐汇区二模)能证实20℃时原KNO3的溶液是饱和溶液的事实是 ( )A.降温到10℃时有KNO3晶体析出B.蒸发掉10 g水,有KNO3晶体析出C.加热到30℃后,再加入KNO3晶体仍能继续溶解D.在20℃时,向上述KNO3溶液中加入少量KNO3晶体,溶液的质量不变【解析】选D。
接近饱和的硝酸钾溶液,降温至10℃时也可能有晶体析出;蒸发掉10 g水,有KNO3晶体析出,原溶液可能是饱和溶液,也可能是接近饱和的溶液;加热到30℃后,硝酸钾的饱和溶液与不饱和溶液再加入KNO3晶体,均能继续溶解;在20℃时,向上述KNO3溶液中加入少量KNO3晶体,溶液的质量不变,说明加入的KNO3晶体没有溶解,原溶液为20℃时的饱和溶液。
4.下面关于饱和溶液的说法中,正确的是( )A.含有溶质很多的溶液B.还能继续溶解某种溶质的溶液C.不能继续溶解某种溶质的溶液D.在一定温度下,一定量的溶剂中,不能再溶解某种溶质的溶液【解析】选D。
饱和溶液是指在一定温度下,一定量的溶剂中,不能再溶解某种溶质的溶液,含有溶质很多的溶液不一定是饱和溶液。

课题3 溶液的浓度(总分:52分时间:40分钟)一、选择题(本题包括9小题,每小题2分,共18分。
每小题只有1个选项符合题意)1.向200 g溶质质量分数为10%的蔗糖溶液中加200 g水,搅拌后把所得溶液倒掉一半,剩余的溶液溶质质量分数为()A.10%B.5%C.2.5%D.20%2.配制50 g 5%的氯化钠溶液,下列说法或做法正确的是()A.将准确称取的氯化钠固体直接倒入装有水的量筒中溶解B.称量氯化钠时药品和砝码(最小的砝码为1 g)放置颠倒了,所配制溶液溶质量分数偏大C.用量筒量取水时仰视液面,所配制溶液溶质质量分数偏小D.若用稀释10%的氧化钠溶液的方法配制上述溶液,需加水30 g3.如图是某同体物质的溶解度曲线。
则t2℃时,该物质的饱和溶液中溶质的质量分数为( )A.20%B.l6.7%C.30%D.23.1%4.某同学在实验室配制480 mL 0.5mol•L﹣1 NaOH溶液以备使用。
其操作步骤如图所示,则如图操作应在图中的()(填选项字母)之间。
A.②与③B.①与②C.④与⑤D.⑤与⑥5.小兰同学配制50 g 5%的氯化钠溶液,取水时他是俯视读数的,这位同学配得的溶液质量分数()A.等于5%B.大于5%C.小于5%D.无法判断6.要配制一定质量分数的氢氧化钠溶液,正确的操作步骤是()A.称量、溶解、计算、装瓶、贴标签B.称量、计算、溶解、装瓶、贴标签C.计算、称量、溶解、装瓶、贴标签D.溶解、计算、称量、装瓶、贴标签7.如图是配制100g溶质质量分数为5%的氯化钠溶液的操作过程.以下说法错误的是()A.该实验操作顺序为③②④⑤①B.称量时如果发现指针偏向右边,应向左盘添加氯化钠C.配制该溶液需要称取5g氯化钠,量取100mL水D操作①中玻璃棒的作用是搅拌,加速溶解8.保持温度不变,小心蒸发NaCl不饱和溶液(蒸发皿中始终有溶液),则溶液中溶质的质量分数(m%)与时间(t)的关系合理的是()A. B.C. D.9.将 50g 98%的浓硫酸全部溶于水配制成 10%的稀硫酸,需要加入水的质量为()gA.400B.440C.450D.500二、填空题(本题包括7小题,共29分)10.(3分)用5%的KNO3溶液配制150g溶质质量分数为2%的硝酸钾营养液,需要加水的质量是________g;用量筒量取水时,若读数时仰视,则导致配制溶液的质量分数________(天“偏大”或“偏小”);玻璃棒在配制过程中的作用是________。

课题3溶液的浓度一选择题1.下列对于溶质的质量分数的叙述正确的是()A.一定质量溶液所含溶质的质量B.溶液中溶质质量与溶液质量之比C.1 L溶液里所含溶质的质量D.100 g溶剂里所含溶质的质量2.已知某溶液的溶质质量分数为20%,则下列比例正确的是()A.溶质质量∶溶液质量=1∶5B.溶剂质量∶溶液质量=1∶5C.溶质质量∶溶剂质量=1∶5D.溶质质量∶溶液质量=4∶53.向100 g质量分数为10%的NaOH溶液中加入12.5 g NaOH固体,完全溶解后,所得溶液中溶质质量分数为()A.12.5%B.20%C.22.5%D.25%4.如果将100 g溶质质量分数为20%的硝酸钾溶液稀释成溶质质量分数为10%的硝酸钾溶液,需加水的质量为()A.50 g B.90 g C.100 g D.200 g5.在温度不变的条件下,欲使下列溶液溶质的质量分数变为原来2倍的方法,最可行的是()A.将20 g硝酸钾饱和溶液蒸发掉10 g水B.将20 g硝酸钾不饱和溶液蒸发掉10 g水C.在10 g10%的硝酸钾溶液中,加入5 g 40%的硝酸钾溶液D.在10 g硝酸钾不饱和溶液中加入10 g硝酸钾固体6.保持温度不变,小心蒸发NaCl不饱和溶液(蒸发皿中始终有溶液),则溶液中溶质的质量分数(m%)与时间(t)的关系合理的是()7.20 ℃时,硝酸钾的溶解度为31.6 g,在此温度下,向50 g水中加入20 g硝酸钾后,所得溶液中溶质的质量分数为()A.40.0% B.30.0%C.28.6% D.24.0%8.电解水时,常在水中加入少量硫酸以增大水的导电性,若用9%的硫酸溶液50 g,通直流电进行电解水的实验,过一段时间后,硫酸的溶质质量分数变为10%,则被电解的水的质量为()A.3 g B.5 g C.7 g D.10 g9.现有一杯20 ℃时的硝酸钾饱和溶液,欲改变其溶质质量分数,下列方法可行的是()A.加入一定量的硝酸钾B.恒温蒸发部分水C.升温到60℃D.加入一定量的水10.如图为a、b、c三种不含结晶水的固体物质的溶解度曲线,下列叙述中正确的是()A.t1℃时,a、b、c饱和溶液的溶质质量分数为20%B.P点表示:t2℃时,a、b的溶液是饱和状态,c的溶液是不饱和状态C.t2℃时,a、b、c 三种物质溶液的溶质质量分数:a>b>cD.70 g a的饱和溶液从t2℃降温到t1℃时,析出晶体15 g11.X、Y、Z三种物质的溶解度曲线如图所示。

课题9.3 溶液的浓度(练)姓名:___________班级:___________考号:___________一、单选题1.关于100g 5%的NaCl溶液,下列叙述正确的是()A.100g水溶解了5g NaClB.5g NaCl溶于95g水中C.溶液中NaCl与水的质量比为1︰20D.溶液中NaCl与水的质量比为19︰1【答案】B【解析】100g 5%的NaCl溶液含有NaCl的质量为100g×5%=5g,水的质量为100g-5g=95g.溶液中NaCl 与水的质量比为5︰95=1︰19.2.对于“26%的食盐溶液”的含义解释正确的是()A.100g食盐溶液中溶解了26g食盐B.100g水中溶解了26g食盐C.将26g食盐溶解在100g水中所得的溶液D.将食盐与水按13︰50的质量比配成的溶液【答案】A【解析】正确理解“26%”的含义,“100”是指溶液的质量为100份,“26”是指食盐的质量为26份,很显然,水的质量为74份.3.用、乙两种固体的溶解度曲线如图所示,下列说法正确的是()。
A.甲的溶解度大于乙的溶解度t℃时,甲、乙饱和溶液中溶质的质量分数均为15%B.1C .2t ℃时,将甲、乙的饱和溶液降温至1t ℃,甲析出的固体一定大于乙D .2t ℃时,向30g 甲、乙中分别加入100g 水,所得溶液中溶质的质量分数甲一定大于乙【答案】D【解析】A 、比较溶解度大小须确定温度,不知温度,无法比较,说法错误;B 、饱和溶液中100%100g=⨯+容解度溶质的质量分数容解度,1t ℃时,甲、乙溶解度均为15g ,则溶质的质量分数为:15g 100%15%115g⨯<,说法错误; C 、不知饱和溶液的质量多少,无法判断析出固体质量多少,说法错误;D 、2t ℃时甲的溶解度是30g ,乙的溶解度<30g ,故向30g 甲,乙中分别加入100g 水,甲恰好完全溶解,乙溶解的质量小于30g ,所以所得溶液中溶质的质量分数甲一定大于乙,说法正确。

人教版九年级下9.3溶液的浓度一、选择题1. 某溶液的溶质质量分数为20%,则下列质量比不正确的是A.m(溶质):m(溶剂)=1:4B.m(溶质):m(溶液)=1:5C.m(溶剂):m(溶液)=4:5D.m(溶质):m(溶剂)=1:52. 按下列方法配制的溶液,其溶质质量分数为5%的是A.称取5.0g生石灰,放入95mL水中B.称取5.0g碳酸钙,放入95g水中C.量取5.0mL浓盐酸,倒入95mL水中D.称取5.0g氯化钾,溶解在95mL水中3. 如图为硫酸锌的溶解度曲线,下列说法正确的是A.20 ℃时,向100 g水中加入60 g硫酸锌,得到160 g溶液B.30 ℃时,硫酸锌饱和溶液中溶质的质量分数为60%C.将80 ℃的硫酸锌饱和溶液降温至60 ℃,溶液仍饱和D.60 ℃的硫酸锌饱和溶液,无论升温或降温,均会有固体析出4. 如图是硝酸钾固体的溶解度曲线。
下列说法错误的是A.硝酸钾的溶解度随温度的升高而增大B.可通过降低温度的方法将硝酸钾的不饱和溶液变成饱和溶液C.将t1℃时硝酸钾的饱和溶液升温到t2℃,溶质质量分数不变D.t2℃时,将105g硝酸钾的饱和溶液稀释到20%需加水的质量为100g 5. 如图是、、C三种物质的溶解度曲线,下列说法中正确的是A.的溶解度大于C的溶解度B.时水溶解物质恰好达到饱和状态C.时、、C三种物质的溶解度由大到小的顺序为、、CD.将C的饱和溶液从降到时溶液的溶质质量分数变小6. 下列关于溶液说法正确的是A.将氯化钠和汽油放入水中,充分搅拌后都能形成溶液B.把30%的硝酸钾溶液均分成两份,每份溶液的溶质质量分数为15% C.向20%C时的蔗糖饱和溶液中加入食盐,食盐不再溶解D.配制100g10%的氯化钠溶液一般经过计算、称量、量取、溶解等步骤7. 如图是A、B、C三种物质的溶解度曲线,下列分析正确的是A.A的溶解度比B大B.20℃时,A、C两种溶液中溶质的质量相等C.将A物质的饱和溶液变为不饱和溶液,溶质质量分数可能不变D.C物质的饱和溶液升温后可变成不饱和溶液8. 固体物质a、b、c的溶解度曲线如图所示。
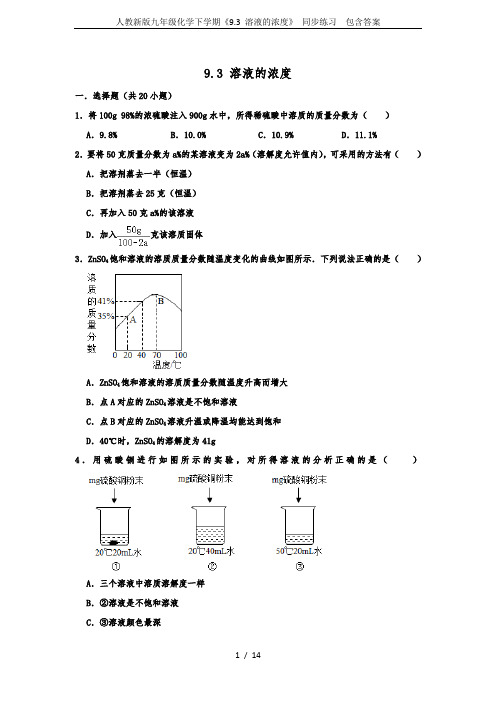
9.3 溶液的浓度一.选择题(共20小题)1.将100g 98%的浓硫酸注入900g水中,所得稀硫酸中溶质的质量分数为()A.9.8% B.10.0% C.10.9% D.11.1%2.要将50克质量分数为a%的某溶液变为2a%(溶解度允许值内),可采用的方法有()A.把溶剂蒸去一半(恒温)B.把溶剂蒸去25克(恒温)C.再加入50克a%的该溶液D.加入克该溶质固体3.ZnSO4饱和溶液的溶质质量分数随温度变化的曲线如图所示.下列说法正确的是()A.ZnSO4饱和溶液的溶质质量分数随温度升高而增大B.点A对应的ZnSO4溶液是不饱和溶液C.点B对应的ZnSO4溶液升温或降温均能达到饱和D.40℃时,ZnSO4的溶解度为41g4.用硫酸铜进行如图所示的实验,对所得溶液的分析正确的是()A.三个溶液中溶质溶解度一样B.②溶液是不饱和溶液C.③溶液颜色最深D.温度不同,无法比较①③溶液的溶质质量分数5.某溶液溶质的质量分数为20%,加入50g水后变为10%,稀释后溶液中溶质的质量是()A.50g B.10g C.100g D.40g6.溶解度为S克的某物质的饱和溶液,跟水以1:4的质量比混合后,溶液的质量百分比浓度为()A.×100% B.×100%C.% D.%7.20℃时,取四份一定质量的饱和硝酸钾溶液分别进行如下实验后,所得结论正确的是()A.保持温度不变,减少10g溶剂后,溶液中溶质的质量分数增大B.保持温度不变,加入10g溶质后,溶液中溶质的质量分数增大C.保持温度不变,减少10g溶剂后,溶质的溶解度减小D.降低至10℃后,溶质的溶解度减小8.按下列方法配制的溶液,其溶质质量分数为5%的是()A.称取5.0g氯化钾,溶解在95mL水中,充分搅拌B.称取5.0g生石灰,放入95mL水中,充分搅拌C.量取5.0mL浓盐酸,倒入95mL水中,充分搅拌D.称取5.0g二氧化锰,放入95mL水中,充分搅拌9.将50g 98%的浓硫酸溶于450g水中,所得溶液中溶质的质量分数为()A.9.8% B.10.2% C.10.8% D.19.6%10.某同学对下表中的溶解度数据分析后,得出的结论正确的是()温度/℃0 20 40 60KCl的溶解度/g 27.6 34.0 40.0 45.5KNO3的溶解度/g 13.3 31.6 63.9 110Ca(OH)2的溶解度/g 0.18 0.16 0.14 0.11A.硝酸钾的溶解度最大B.降温可将不饱和的Ca(OH)2溶液变为饱和溶液C.40℃时,饱和的氯化钾溶液溶质质量分数为40%D.当KNO3中混有少量KCl时,可以用冷却热饱和溶液的方法提纯11.下列说法正确的是()A.根据质量守恒定律,2gH2跟8gO2完全反应,可得到10H2OB.用含Fe2O385%的赤铁矿160t,理论上可生产100t含杂质4.8%的生铁C.各取10g镁粉和锌粉,分别与足量的盐酸完全反应,镁粉产生的H2多,说明镁的金属活动性比锌强D.将l0gCuSO4•5H2O与90gH2O混合,固体完全溶解,可得100g溶质的质量分数为10%的CuSO4溶液12.下列有关水和溶液的说法错误的是()A.水是由氢元素和氧元素组成B.生活中可用煮沸的方法降低水的硬度C.外界条件不改变,溶质不会从溶液中分离出来D.饱和溶液溶质的质量分数一定大于不饱和溶液溶质的质量分数13.下列关于溶液的说法错误的是()A.与乳化作用相比,溶解能使物质混合得更均匀B.20℃时,50g水中溶解了15g的硝酸钾,则20℃时硝酸钾的溶解度是30gC.一定温度下,固体物质的溶解度不随水的质量改变而改变D.硝酸钾的饱和溶液恒温蒸发部分水后,剩余溶液溶质质量分数不变14.压强为101kPa下,硝酸钾和氨气在不同温度下的溶解度如下表。
9.3 溶液的浓度一.选择题(共25小题)1.如图所示,20℃时100g硫酸铜饱和溶液中,分别加入下列物质后,相关分析错误的是()A.溶质质量:Ⅰ=Ⅲ>ⅡB.溶剂质量:Ⅰ>Ⅲ>ⅡC.溶液质量:Ⅰ>Ⅱ=ⅢD.溶质质量分数:Ⅰ<Ⅱ=Ⅲ2.下列有关溶液组成的说法,正确的是()A.溶质质量分数是溶质质量与溶剂质量的比值B.饱和溶液降温后,一定有溶质结晶析出C.饱和溶液中有晶体析出后,溶质质量分数减小D.10%的NaCl溶液的浓度一定比5%的NaCl溶液的浓度大3.ZnSO4饱和溶液的溶质质量分数随温度变化的曲线如图所示。
说法正确的是()A.M点对应的ZnSO4溶液是不饱和溶液B.N点对应的ZnSO4溶液升温或降温均都可能析出晶体C.ZnSO4饱和溶液的溶质质量分数随温度升高而增大D.40℃时,ZnSO4的溶解度为41g/100g水4.下列说法正确的是()A.某硝酸钾溶液在20℃时是饱和的,当其他条件不变,温度升高到50℃时,该溶液也一定是饱和溶液B.稀溶液一定是不饱和溶液C.在一定温度下,同一种溶质的饱和溶液的溶质质量分数比不饱和溶液的大D.在一定温度下,同一种溶质饱和溶液的溶质质量比不饱和溶液的大5.关于如图所示过氧化氢溶液说法错误的是()A.500g溶液中含溶质30gB.500mL溶液的质量为550gC.500mL溶液中溶质与溶剂的质量比为3:7D.取出 50mL溶液,溶质质量分数仍为30%6.现有一杯50℃的饱和硝酸钾溶液,欲改变其溶质质量分数,下列方法可行的是()A.加入一定量的硝酸钾B.恒温蒸发部分水C.升温到80℃D.降温到20℃7.用下列方法配制的溶液,其溶质质量分数为5%的是()A.称取5.0g氯化钾,溶解在95mL水中,充分搅拌B.称取5.0g生石灰,放入95mL水中,充分搅拌C.量取5.0mL浓盐酸,倒入95mL水中,充分搅拌D.称取5.0g碳酸钙,放入95mL水中,充分搅拌8.对 100 克溶质质量分数为 10%的某物质的溶液,分别进行如下操作:①加入 10g 水②加入 10g 同种溶质,且完全溶解③加入溶质质量分数为 10%的同种溶质的溶液 10g ④蒸发掉 10g 水,无晶体析出。
人教版初三化学溶液的浓度过关测试含答案解析一、初中化学溶液的浓度选择题1.向t℃时饱和的Na2CO3溶液中加入ng无水Na2CO3,会析出mgNa2CO3·10H2O,则(m-n)的值为()A.饱和溶液失去水的质量B.饱和溶液失去溶质的质量C.饱和溶液失去水和溶质的质量之和D.其数值为0,即溶液质量不变【来源】广西贺州市莲塘镇第一初级中学2019年第一次适应性训练化学试题2.右图是A、B、C三种物质的溶解度曲线。
下列说法错误的是A.C的溶解度随温度的升高而减小B.t2℃时A、B、C的溶解度大小为A=B>CC.t2℃A、B、C的饱和溶液降温到t1℃时,A、C两溶液中溶质的质量分数相等D.t1℃时,A的饱和溶液中溶质质量分数为20%【来源】2016届江苏省扬州市邗江区九年级第一次模拟考试化学试卷(带解析)3.甲、乙两种物质的溶解度曲线如图所示。
下列说法正确的是()A.a1℃时甲的饱和溶液,升温至a2℃时仍是饱和溶液B.乙的溶解度随温度的升高而增大C.相同温度时,甲的溶解度一定大于乙的溶解度D.分别将甲、乙的饱和溶液从a2℃将至a1℃时,所得溶液中溶质的质量分数相等【来源】沪科版(遵义专版)2018届九年级化学:期末测试卷4.下图是A、B、C三种物质的溶解度曲线,下列分析不正确的是()A.50℃时A、B、C三种物质的溶解度由大到小的顺序是A>B>CB.50℃时把50gA放入50g水中能得到A的饱和溶液,其中溶质与溶剂的质量比为1:2 C.将C的饱和溶液变为不饱和溶液,采用降温的方法D.将50℃时A、B、C三种物质的饱和溶液降温至20℃时,这三种溶液的溶质质量分数的大小关系是B>A=C【来源】2013年初中毕业升学考试(湖北孝感卷)化学(带解析)5.甲、乙两种物质的溶解度曲线如图1所示。
下列说法中正确的是A.t1℃时,甲饱和溶液的溶质质量分数大于乙饱和溶液B.t2℃时,甲、乙饱和溶液的溶质质量分数都为30%C.t2℃时,甲、乙的饱和溶液分别降温至t1℃,甲溶液饱和,乙溶液不饱和D.t2℃时,质量相同的甲、乙饱和溶液分别升温至t3℃,为达饱和状态,需加入甲的质量大于乙【来源】2015年初中毕业升学考试(福建厦门卷)化学(带解析)6.甲、乙两种固体物质(均不含结晶水)的溶解度曲线如图所示,下列说法错误的是()A.t2℃时,将甲、乙的两种饱和溶液分别降温到t1℃,所得溶液都是饱和溶液B.t1℃时,向50g水中加入甲可得80g饱和溶液,则乙在该温度下的溶解度为60g C.甲中混有少量乙时,可用降温结晶的方法提纯甲D.t2℃时,将等质量的甲、乙两种溶液分别降温到0℃,甲溶液的溶质质量分数一定小于乙溶液的溶质质量分数【来源】2017年初中毕业升学考试(黑龙江哈尔滨卷)化学(带解析)7.将100g 质量分数为20%的硝酸钾溶液稀释为5%的硝酸钾溶液,需要加水的质量为()A.100g B.200g C.300g D.400g【来源】2016届广东省广州市南沙区九年级一模化学试卷(带解析)8.20℃时,往100g硝酸钾溶液中加入20g硝酸钾,充分搅拌,硝酸钾部分溶解。
人教版初三化学溶液的浓度练习题及解析一、初中化学溶液的浓度选择题1.海水晒盐提取食盐晶体后留下的母液叫卤水,卤水中除含NaCl外,还含有MgCl2、MgSO4等物质。
它们的溶解度曲线如图所示。
下列说法正确的是()A.0℃时,三种物质的饱和溶液中,溶质质量分数最大的是MgSO4B.三种物质的溶解度都随温度升高而不断增大C.将卤水加热到80℃以上蒸发水分,逐渐析出的晶体是NaCl和MgSO4D.20℃时,向40gNaCl固体和40gMgCl2固体中分别加入100g水充分溶解后,两种溶液均能达到饱和状态【来源】2016年初中毕业升学考试(四川德阳卷)化学(带解析)2.a、b两种固体物质(均不含结晶水)的溶解度曲线如图所示,在t1℃时,将a、b两种物质各60g分别加入100水中,充分溶解后,下列有关叙述不正确的是()A.t1℃时,得到的两种溶液均为饱和溶液B.将所配制的a、b两种溶液从t1℃同步降温,a析出的晶体比b多C.t2℃时a的溶解度比b大D.将所得的两种溶液温度升高到t2℃时,a溶液的溶质质量分数大于b溶液的溶质质量分数【来源】哈尔滨市道外区2017—2018学年度上学期九年级期末调研测试化学试卷3.下图是A、B、C三种物质的溶解度曲线,下列分析不正确的是()A.50℃时A、B、C三种物质的溶解度由大到小的顺序是A>B>CB.50℃时把50gA放入50g水中能得到A的饱和溶液,其中溶质与溶剂的质量比为1:2 C.将C的饱和溶液变为不饱和溶液,采用降温的方法D.将50℃时A、B、C三种物质的饱和溶液降温至20℃时,这三种溶液的溶质质量分数的大小关系是B>A=C【来源】2013年初中毕业升学考试(湖北孝感卷)化学(带解析)4.根据下表信息,相关说法正确的是()溶解度/g温度/℃NaCl KCl NH4Cl KNO32036.034.037.231.64036.640.045.863.96037.345.555.2110A.20℃时,NaCl 的溶液度为 36.0B.40℃时,KCl 饱和溶液的溶质质量分数为 40%C.40℃时,向 100g 水中加入 50gNH4Cl 充分溶解,溶液质量为 145.8gD.60℃时降温到 20℃时,KNO3和 KCl 的饱和溶液析出晶体较多的是 KNO3【来源】2017年初中毕业升学考试(四川成都卷)化学(带解析)5.a,b两种物质的溶解度曲线如下图所示.下列说法不正确的是A .将℃时b的饱和溶液加水可变为不饱和溶液B.将℃时a的饱和溶液降温至℃,溶液质量不变C.℃时,两种物质的饱和溶液中溶质质量分数a bD.将℃时a、b的饱和溶液分别降温至℃,两溶液的溶质质量分数相等【来源】2015年初中毕业升学考试(北京卷)化学(带解析)6.甲、乙两种固体物质(均不含结晶水)的溶解度曲线如图所示,下列说法错误的是()A.t2℃时,将甲、乙的两种饱和溶液分别降温到t1℃,所得溶液都是饱和溶液B.t1℃时,向50g水中加入甲可得80g饱和溶液,则乙在该温度下的溶解度为60g C.甲中混有少量乙时,可用降温结晶的方法提纯甲D.t2℃时,将等质量的甲、乙两种溶液分别降温到0℃,甲溶液的溶质质量分数一定小于乙溶液的溶质质量分数【来源】2017年初中毕业升学考试(黑龙江哈尔滨卷)化学(带解析)7.氯化铵和硝酸钾溶解度曲线如图所示,下列叙述正确的是( )A.50℃时,氯化铵的溶解度大于硝酸钾B.a℃时,氯化铵与硝酸钾溶液的质量分数相等C.将60℃的硝酸钾饱和溶液降温会变为不饱和溶液D.40℃时,50g水中加入50g硝酸钾,充分搅拌,得到质量分数约为39%的硝酸钾溶液【来源】2015届山东省枣庄市薛城舜耕中学九年级学业水平模拟化学试卷(带解析) 8.右图是a、b、c 三种物质的溶解度曲线,下列分析不正确的是A.t2℃时,a、b、c三种物质的溶解度由大到小的顺序是a>b>cB.t2℃时,将50ga物质放入100g水中充分溶解恰好得到a的饱和溶液(a物质不含结晶水) C.将t2℃时a、b、c三种物质的饱和溶液降温至t1℃时,所得溶液的溶质质量分数关系b >c=aD.将c的饱和溶液变为不饱和溶液,可采用降温的方法【来源】[首发]山东省枣庄市薛城区2017届九年级中考模拟(5月)化学试题9.下列叙述正确的是()A.温度升高时,物质的溶解度增大B.凡是均一、透明的液体就是溶液C.浓溶液不一定是饱和溶液,稀溶液也不一定是不饱和溶液D.20℃时36g氯化钠溶于100g水中,恰好达到饱和,此溶液中溶质的质量分数是36%【来源】2019年内蒙古呼伦贝尔市三岔河中学中考化学模拟试卷(4月份)10.化学与生活密切相关,下列饮品中属于溶液的是A.牛奶B.白酒C.豆浆D.咖啡【来源】【区级联考】江苏省无锡市惠山区2019届九年级一模化学试题11.常温下向一定质量的石灰石中逐滴加入稀盐酸,充分反应(忽略挥发)。
9.3溶液的浓度同步习题一.选择题1.若将某溶液的溶质质量分数增大一倍,可采用的方法是(设均未有晶体析出)()A.将溶剂蒸发掉一半B.将溶液倒出一半C.将溶质的质量增加一倍D.将溶剂的质量减少至原溶液质量的一半2.有40g 5%的硝酸钾溶液,若将其质量分数增大到10%,应采用的方法是()A.把溶剂蒸发掉一半B.加入40g溶质质量分数为15%的硝酸钾溶液C.把溶液倒掉20gD.加入2g硝酸钾固体3.下列有关溶液及溶解度的说法正确的是()A.同一种溶质的水溶液,饱和溶液中溶质的质量分数一定大于不饱和溶液中溶质的质量分数B.在T℃时,某物质A的溶液,若蒸发掉5克水时,析出A(不含结晶水)2克;若蒸发掉10克水时,析出A 5克,则T℃时,A的溶解度为40克C.室温下,5mL水和5mL酒精混合后总体积为10mLD.现要配制10%的稀硫酸2940g,用98%的浓硫酸进行稀释,需加水2640g4.要配制0.5%的苯甲酸溶液,下述方法正确的是()A.称取0.5g苯甲酸,溶于100g水中B.称取5g苯甲酸,溶于995g水中C.称取50g苯甲酸,溶于950g水中D.称取0.5g苯甲酸,溶于1000g水中5.下图中能正确反映图中所描述的变化事实的是()A.接近饱和的氯化钠溶液中加入氯化钠固体B.不饱和的硝酸钾溶液升温C.饱和的硝酸钾溶液中加水D.加热蒸发酒精溶液6.使100g 20%的KNO3溶液变为10%的溶液,可以采用的方法是()A.加入80g水B.加水使溶液质量为200gC.倒出50g溶液D.加入10g KNO3,完全溶解7.压强为101kPa下,硝酸钾和氨气在不同温度下的溶解度如下表。
下列说法正确的是()温度℃10203060溶解度/g KNO320.931.645.8110NH3705644.520A.两种物质的溶解度均随温度升高而增大B.20℃时,KNO3饱和溶液中溶质的质量分数为31.6%C.60℃的KNO3饱和溶液降温至30℃,有晶体析出D.NH3的溶解度只与温度大小有关8.下列关于溶液的说法中正确的是()A.不饱和溶液转化为饱和溶液,溶液中溶质的质量分数肯定增大B.饱和溶液一定是浓溶液,不饱和溶液一定是稀溶液C.5g某物质溶解在95g水中,所得溶液中该溶质的质量分数不一定是5%D.一定温度下某物质的饱和溶液,肯定不能再溶解任何物质了9.某物质在20℃时的溶解度为20g/100g水,在20℃时将20g该物质投入到80g水中充分溶解,则该物质溶液中溶质质量分数为()A.25%B.20%C.16.7%D.无法计算10.20℃时,氯化钠(NaCl)溶解于水的实验数据如表所示,则下列叙述正确的是()实验序号水的质量(g)加入NaCl的质量(g)溶液的质量(g)①10212②10313③10413.6④10513.6A.①所得溶液的溶质质量分数为20%B.②所得溶液是饱和溶液C.20℃时,氯化钠的溶解度是36g/100g水D.③④溶液的溶质质量分数不相等二.填空题11.现有100g溶质的质量分数为8%的硝酸钾溶液,若要使溶液中溶质的质量分数增大一倍,可加入或蒸发。
溶液的浓度一课一练·基础闯关知识点溶质质量分数的意义与基本计算1.(2017·商丘一模)下列关于“10%的硝酸钾溶液”含义的说法中,错误的是( )A.100 g水中溶解了10 g硝酸钾B.100 g硝酸钾溶液中有10 g硝酸钾C.将10 g硝酸钾溶于90 g水中所得的溶液D.将硝酸钾与水按1∶9的质量比配制的溶液【解析】选A。
10%的硝酸钾溶液表示的是在100 g溶液中含有10 g硝酸钾,即90 g水中溶解10 g硝酸钾,其中硝酸钾与水的质量比为1∶9。
2.室温时,分别向含有100 mL水的M、N两个烧杯中加入5 g、10 g硫酸铜,如图所示。
则下列说法正确的是( )A.M烧杯中溶液的颜色浅,溶质质量分数大B.M烧杯中溶液的颜色深,溶质质量分数小C.N烧杯中溶液的颜色深,溶质质量分数大D.N烧杯中溶液的颜色浅,溶质质量分数小【解析】选C。
向含有100 mL水的M、N两个烧杯中分别加入5 g、10 g硫酸铜,M中含有的溶质少,则溶液颜色浅,溶质质量分数小,N中含有的溶质多,溶液颜色深。
3.将100 g 10%的硝酸钾溶液与200 g 10%的硝酸钾溶液混合后,不发生改变的是( )A.溶质的量B.溶剂的量C.溶质质量分数D.溶液总量【解析】选C。
将100 g 10%的硝酸钾溶液与200 g 10%的硝酸钾溶液混合后,溶质质量、溶剂质量、溶液的质量都增加了,但溶质质量分数不变,还是10%。
4.(2017·株洲中考)除质量分数以外,人们有时也用体积分数来表示溶液的浓度。
例如,52%的饮用白酒就是指每100体积的饮用白酒中含有52体积的乙醇。
下列溶液的浓度属于用体积分数来表示的是( ) A.0.9%的生理盐水 B.5%的葡萄糖注射液C.10%的氢氧化钠溶液D.75%的医用酒精【解析】选D。
溶质质量分数是最常用的溶液组成的表示方法,除此之外还可以用体积分数来表示。
A、B、C选项中溶液中的溶质都是固体,常用溶质质量分数表示溶液的组成,D选项中的溶质为液态的酒精,可用体积分数来表示溶液的组成。
5.(2017·莆田涵江区质检)向一定量的10%的硝酸钾溶液中加入少量氯化钠,搅拌至完全溶解,此时所得溶液中硝酸钾的质量分数与原溶液中硝酸钾的质量分数相比较,其变化是( )A.不变B.变小C.变大D.无法判断【解析】选B。
向溶质质量分数为10%的硝酸钾溶液里加入少量氯化钠并完全溶解后,所得溶液的质量增加了,而溶质硝酸钾的质量不变,所以硝酸钾的质量分数将减小。
6.保持温度不变,小心蒸发NaCl的不饱和溶液(蒸发皿中始终有溶液),则溶液中溶质的质量分数(m%)与时间(t)的关系合理的是( )【解析】选A。
本题主要考查溶质质量分数,掌握溶质质量分数的含义是解题的关键。
氯化钠溶液蒸发水分,由不饱和溶液变为饱和溶液的过程,溶剂质量减小,溶液中溶质质量分数(m%)增大,当氯化钠饱和溶液再蒸发水分时,仍为饱和溶液,溶质的质量分数不再变化。
7.(2017·海口一模)已知20℃时100 g水中最多能溶解36 g氯化钠,20℃时向100 g水中加50 g氯化钠,充分溶解后,所得溶液中溶质的质量分数为( )A.36%B.50%C.33.3%D.26.5%【解析】选D。
20℃时向100 g水中加50 g氯化钠,充分溶解后,有36 g氯化钠溶解,所得溶液中溶质的质量分数为×100%≈26.5%。
8.(2017·临沂中考)工业上常用红锌矿(主要含ZnO)和18%~25%的稀硫酸为原料制取硫酸锌。
(1)硫酸锌中硫元素和氧元素的质量比是____________。
(2)100 g溶质质量分数为98%的浓硫酸配制成溶质质量分数为20%的稀硫酸,需要水的质量是____________g。
【解析】(1)ZnSO4中硫元素和氧元素的质量比为32∶(16×4)=1∶2。
(2)溶液稀释前后溶质的质量不变,设加入水的质量为x,则有100 g×98%=(100 g+x)×20%,x=390 g。
答案:(1)1∶2 (2)390知识点溶液稀释的计算1.(2017·郴州苏仙区期中)溶液在用水稀释前后,保持不变的是( )A.溶质的质量B.溶剂的质量C.溶液的质量D.溶质的质量分数【解析】选A。
溶液在用水稀释的过程中,溶质的质量不变,溶剂的质量增加,溶液的质量增加,溶质的质量分数减小。
2.某溶液溶质的质量分数为20%,加入50 g水后变为10%,则稀释后溶液中溶质的质量是( )A.5 gB.10 gC.20 gD.50 g【解析】选B。
设稀释前溶液的质量为x,根据溶液稀释前后溶质的质量不变,列式x×20%=(50 g+x)×10%,解得x=50 g,稀释后溶液中溶质的质量为50 g×20%=10 g。
3.要将100 kg质量分数为10%的过氧乙酸消毒液变为溶质质量分数为25%,需要蒸发水分的质量是( )A.40 kgB.60 kgC.80 kgD.25 kg【解析】选B。
设需要蒸发水分的质量为x,根据溶液蒸发前后溶质的质量相等,100 kg×10%=(100 kg-x)×25%,解得x=60 kg。
4.(2017·广州白云区一模)把质量分数为20%的氢氧化钾溶液100 g,加水稀释到1 000 g,其质量分数为( )A.0.02%B.0.2%C.2%D.20%【解析】选C。
设稀释后溶液的质量分数为x,根据溶液稀释前后,溶质的质量不变,则100 g×20%=1 000 g×x,x=2%。
5.质量分数为10%的盐酸5 g,加水稀释至250 g后取出10 g,则此10 g溶液中溶质的质量分数是( )A.0.2%B.0.5%C.1%D.2%【解析】选A。
根据加水稀释时,溶液中溶质质量不变,加水稀释至250 g,溶液中溶质的质量分数=×100%=0.2%,又因溶液具有均一性,所以取出的10 g溶液中溶质的质量分数也是0.2%。
6.50℃时,将12 g硝酸钾溶于48 g水中,其溶质质量分数为______,将此溶液分为三等份:(1)取第一份溶液,将温度升高10℃(无水分损失),所得溶液的溶质质量分数为________。
(2)取第二份溶液,使其溶质质量分数变为原来的2倍,需加入硝酸钾晶体______g,或者蒸发______g水。
(3)取第三份溶液,使其溶质质量分数变为原来的一半,需加水______g。
【解析】50℃时,将12 g硝酸钾溶于48 g水中,所得溶液中溶质的质量分数为×100%=20%,将溶液分成三等份时,溶液的溶质质量分数不变,每份溶液中溶质的质量为4 g,溶液的质量为20 g。
(1)将溶液升高温度时,因溶质和溶剂都没有变化,所以溶质质量分数不变。
(2)使其溶质质量分数变为原来的2倍,则溶质质量分数变为40%,则设加入硝酸钾的质量为x,×100%=40%,x=g≈6.67 g;设蒸发水的质量为y,×100%=40%,y=10 g。
(3)使其溶质质量分数变为原来的一半,即溶质的质量分数为10%,设加入水的质量为z,×100%=10%,z=20 g。
答案:20% (1)20% (2)6.67 10 (3)207.葡萄糖(化学式:C6H12O6)是生命体所需能量的主要来源。
有一瓶葡萄糖溶液,部分标签如图所示,请计算:(1)配制这瓶葡萄糖溶液,需要固体葡萄糖的质量为______g。
(2)要把这瓶葡萄糖溶液加水稀释为2%的葡萄糖溶液,需要水的质量为______________g。
【解析】(1)这瓶葡萄糖溶液的质量为500 g,溶质质量分数为5%,配制这瓶葡萄糖溶液,需要固体葡萄糖的质量为500 g×5%=25 g。
(2)设需要加水的质量为x,根据溶液稀释前后,溶质的质量不变,则(500 g+x)×2%=25 g,x=750 g。
答案:(1)25 (2)750知识点有关溶质质量分数的综合考查1.有100 g 10%的盐酸溶液,要使其溶质质量分数增大一倍,应采取的方法是( )A.把溶液的量倒掉一半B.溶质的质量增大一倍C.将100 g 10%的盐酸与200 g 25%的盐酸混合D.蒸发掉溶剂的质量是原溶液质量的一半【解析】选C。
A选项,溶液具有均一性,把溶液的量倒掉一半,其溶质质量分数不变,故A错误;B选项,根据溶质质量分数=×100%可知,溶质的质量增大一倍,因溶液的质量也增加,因此溶质质量分数增大不到一倍,故B错误;C选项,将100 g 10%的盐酸与200 g 25%的盐酸混合,溶质质量分数为×100%=20%,故C正确;D选项,蒸发时先挥发出来的是氯化氢气体,故D错误。
2.(2017·东营一模)下列说法正确的是( )A.15℃时,硝酸钾的溶解度是25 g,15℃时饱和溶液的质量分数为20%B.24%的氢氧化钠溶液取出一半其溶质质量分数为12%C.饱和溶液中析出晶体后,溶质的质量分数一定减小D.饱和溶液升高温度一定变成不饱和溶液【解析】选A。
15℃时,硝酸钾的溶解度是25 g,15℃时饱和溶液的质量分数为×100%=20%;溶液具有均一性,24%的氢氧化钠溶液取出一半其溶质质量分数仍为24%;恒温蒸发溶剂的方法,饱和溶液析出晶体后,溶质的质量分数不变;有些物质如氢氧化钙的溶解度随温度的升高而减小,饱和溶液升高温度不能变成不饱和溶液。
3.(2017·重庆中考A卷)合成氨工业中,常用碳酸钾溶液吸收产生的二氧化碳得到碳酸氢钾,反应的化学方程式为K2CO3+CO2+H2O2KHCO3。
现向碳酸钾溶液中通入二氧化碳,恰好完全反应,得到溶质的质量分数为10%的溶液50 g,试计算:(1)碳酸钾中钾元素、碳元素、氧元素的质量比为________。
(2)若把该50 g溶液,稀释为质量分数为4%的溶液,需要加入水的质量。
(3)原碳酸钾溶液中溶质的质量分数(计算结果精确到0.1%)。
【解析】(1)碳酸钾中钾元素、碳元素、氧元素的质量比为(39×2)∶12∶(16×3)=13∶2∶8。
(2)根据稀释前后溶质的质量不变,可以计算加入水的质量。
(3)根据化学方程式,由碳酸氢钾的质量可以分别计算碳酸钾及二氧化碳的质量,从而可以计算原碳酸钾溶液中溶质的质量分数。
答案:(1)13∶2∶8(2)设需要加水的质量为m,则(50 g+m)×4%=50 g×10% m=75 g(3)设原碳酸钾溶液中碳酸钾的质量为x,恰好反应时,需二氧化碳质量为yK2CO3+CO2+H2O2KHCO3138 44 200x y 50 g×10%=x=3.45 g=y=1.1 g原碳酸钾溶液的质量为50 g-1.1 g=48.9 g则原碳酸钾溶液中溶质的质量分数为≈7.1%答:原碳酸钾溶液中溶质的质量分数为7.1%。