最新化学计算题专项练习经典(word)
- 格式:doc
- 大小:300.00 KB
- 文档页数:9

【化学】初三化学化学计算题专项训练及答案一、有关化学式的计算1、计算硝酸铵(NH₄NO₃)中氮元素的质量分数。
解:硝酸铵中氮元素的相对原子质量总和为:$14×2 = 28$硝酸铵的相对分子质量为:$14×2 + 1×4 + 16×3 = 80$氮元素的质量分数为:$\frac{28}{80}×100\%= 35\%$答:硝酸铵中氮元素的质量分数为 35%。
2、已知氧化铁(Fe₂O₃)的化学式,求其中铁元素与氧元素的质量比。
解:氧化铁中铁元素与氧元素的质量比为:$(56×2) :(16×3) = 112 : 48 = 7 : 3$答:氧化铁中铁元素与氧元素的质量比为 7 : 3。
二、有关化学方程式的计算1、加热分解 63g 高锰酸钾,可以得到多少克氧气?解:设可以得到氧气的质量为 x。
$2KMnO₄\stackrel{\triangle}{=\!=\!=} K₂MnO₄+ MnO₂+ O₂↑$$316 32$$63g x$$\frac{316}{32} =\frac{63g}{x}$$x =\frac{32×63g}{316} ≈ 06g$答:加热分解 63g 高锰酸钾,可以得到 06g 氧气。
2、用氢气还原氧化铜,要得到 32g 铜,需要多少克氢气?解:设需要氢气的质量为 y。
$H₂+ CuO \stackrel{\triangle}{=\!=\!=} Cu +H₂O$$2 64$$y 32g$$\frac{2}{64} =\frac{y}{32g}$$y =\frac{2×32g}{64} = 1g$答:需要 1g 氢气。
3、实验室用 100g 含碳酸钙 80%的大理石与足量的稀盐酸反应,能制得多少克二氧化碳?解:大理石中碳酸钙的质量为:$100g×80\%= 80g$设生成二氧化碳的质量为 z。

题型一:化学式的计算一、春天是流感的多发季节,民间有很多治疗流感的土方法,其中多吃大蒜能预防感冒.大蒜中的大蒜素硫化丙烯是杀菌的有效成分,1千克大蒜中含大蒜素125克,已知大蒜素由C、H、S三种元素组成,相对分子质量为74,其中碳元素质量分数48.6%,氢元素质量分数8。
1%,求:(1)大蒜素硫化丙烯属于____________(选填“有机物”或“无机物”)(2)1千克大蒜中含硫元素质量为多少克?(3)硫化丙烯的化学式为____________.二、我国民间有端午节挂艾草的习俗.艾草含有丰富的黄酮素(化学式为:C15H10O2),有很高的药用价值.请回答:(1)黄酮素的相对分子质量为_________.(2)黄酮素中碳、氢元素的质量比为_________(填最简比).(3)11.1g黄酮素中含碳元素的质量为_________g.三.某火力发电厂常用石灰石浆吸收废气中的二氧化硫,以防止空气污染。
(1)补全其反应原理的化学方程式:2CaCO3+O2+2SO2=2CaSO4+2X .其中X的化学式为______.(2)若该发电厂每天要处理含有3.2吨二氧化硫的废气,计算每天至少需含碳酸钙90%的石灰石多少吨才能满足处理废气所需?(写出计算过程,保留1位小数)四。
舟山虾蟹资源丰富,利用虾蟹等甲壳动物的废弃甲壳开发生产的可溶性甲壳素,是研制生物医药、化妆品等新产品的重要原料。
但甲壳素生产过程排放的废液中含有盐酸,对环境会造成严重污染.如图是某工厂所用盐酸容器上标签的部分内容,请仔细阅读后计算:(1)已知甲壳素的化学式为(C8H13NO5)n,它由______种元素组成.(2)甲壳素中碳、氢、氮、氧元素的质量比为_________.(3)取上述20%盐酸10ml,加水稀释至100ml,问稀释后的稀盐酸中含溶质多少克?题型二:质量分数的计算五、某同学为了测定一瓶过氧化氢溶液中溶质的质量分数,在如图甲所示发生装置的锥形瓶内加入二氧化锰0.5g,在分液漏斗内加入该过氧化氢溶液25g.完全反应后,称得发生装置内剩余物质的总质量为24.7g.请回答:(1)若要测量产生的气体体积,则应选_________(选填“乙图”或“丙图”)所示装置收集气体,且要慢慢地上下移动量筒,使量筒内外液面高度相同,读取量筒的气体体积.(2)请列式计算该过氧化氢溶液中溶质的质量分数.六、我校科学兴趣小组考察了钱塘江附近一家企业的污水处理情况,在考察过程中收集到如下数据:①该企业排放的污水主要成分是盐酸,提取未经处理的污水水样,用pH试纸测得pH=3;②处理污水步骤之一是:污水进入中和池进行中和处理,所用的材料是较经济的石灰水;③提取经过处理后可排放的水样,测得pH在7.0左右.根据上述提供的资料,回答下列问题:(1)这种考察属于____________调查(填“直接"或“间接”);(2)要测出污水的酸碱度,可选用____________;(3)经计算得知pH=3的污水中,盐酸的质量分数为0.00365%,现假设中和池中有1。

化学计算题专练(22道题)1.(9分)小明为了测定某钙片中碳酸钙的质量分数,用如图装置进行如下实验:①取研碎后的钙片4克,导入气密性良好的锥形瓶中,然后在分液漏斗中加入适量的稀盐酸,置于电子天平上测出装置总质量。
②打开活塞,滴入足量稀盐酸后关闭活塞,待气泡不再冒出时,测出反应后装置总质量。
③整理相关数据如表所示,计算出钙片中碳酸钙的质量分数。
(1)该实验中,对装置中的固态干燥剂的性质有何要求?。
(2)反应前容器内是空气(密度为ρ1),反应后全部是二氧化碳(密度为ρ2),则反应前后容器(容积为V)内的气体质量差为m为。
(用字母表示,反应物的体积忽略不计)(3)小明查阅有关数据后,计算出反应前后容器内的气体质量差m为0.22克,结合表中数据,计算该钙片中碳酸钙的质量分数。
(钙片中的其它成分不与盐酸反应)2.某环保小组监测到一湿法冶铜厂排放的废水中含有硫酸和硫酸铜两种污染物,为测定该废水中各污染物的含量,给冶铜厂提供处理废水的参考,环保小组的同学进行了以下实验。
取废水500g,向其中加入溶质质量分数为20%的氢氧化钠溶液。
测得沉淀质量与所加入的氢氧化钠溶液的质量关系如下图:根据所得数据计算:(1)500g该废水中硫酸铜的质量。
(2)该废水中硫酸的溶质质量分数。
3.某化学兴趣小组为了测定一批石灰石样品中碳酸钙的质量分数,取用10.0 g石灰石样品,将40.0g稀盐酸分为4次加入样品中(石灰石样品中所含的杂质不溶于水和盐酸),充分反应后经过滤、干燥等操作,最后称量,得实验数据如下:请计算:Array(1)从以上数据可知,这四次实验中,第次石灰石样品中碳酸钙完全反应;第 1 页(2)该石灰石样品碳酸钙的质量分数是;(3)10.0 g稀盐酸与10.0 g石灰石样品作用,得到溶质的质量分数是多少?(写出计算过程)4.实验室有一瓶标签被腐蚀的盐酸,小丽为了测定溶液中溶质的质量分数,在烧杯中配制了8g 10%的NaOH溶液.然后往烧杯中滴加该盐酸.反应过程中溶液的pH与滴入盐酸的质量关系如图所示.请回答下列问题:(1)配制了8g 10%的NaOH溶液,需要水的质量为;(2)计算该盐酸的溶质质量分数;(写出计算过程)(3)当滴入4g盐酸时,烧杯内溶液中钠元素的质量为g.5.科学实验提倡绿色环保,对实验装置进行微型化改进是一条很好的途径。

化学计算题专项练习经典经典一、中考化学计算题1.有一份锌粉与铜粉的混合物样品,为确定其组成,某同学将32.5g样品加入100g稀硫酸中,恰好完全反应,放出气体的质量与反应时间的关系如图所示。
试求:(1)样品中金属铜的质量是____g。
(2)所用稀硫酸的溶质质量分数____(写出计算过程)。
【答案】19.519.6%【解析】混合物中只有锌能够和稀硫酸反应生成氢气,题目给出了氢气的质量,所以可以根据氢气的质量和对应的化学方程式求算参加反应的锌的质量和消耗的稀硫酸中溶质的质量,进而求算铜的质量和硫酸中溶质的质量分数。
设参加反应的锌的质量为x,所消耗的硫酸中的溶质的质量为y。
Zn+ H2SO4 = ZnSO4 + H2↑65 98 2x y 0.4g659820.4x y g==x=13gy=19.6g混合物中铜的质量为32.5g-13g=19.5g所以稀硫酸中溶质的质量分数为19.6g0010019.600 100g⨯=答:(1)样品中金属铜的质量是19.5g。
(2)所用稀硫酸中溶质的质量分数为19.6%。
2.现有一份氧元素质量分数为 89.5%的过氧化氢溶液,加入 MnO2充分反应后,得到液体的质量为 90g(不考虑操作过程中液体的损失),则生成氧气的质量为________________g(精确到小数点后 1 位)。
【答案】 5.2【解析】解法一:设生成氧气的质量为x,过氧化氢溶液的质量为y,根据反应前后氧元素的质量不变可得关系式:①y-90g=x,②y89.5%=x+90g100%,x=5.2g,答:生成氧气的质量为5.2g。
解法二:可根据反应前后氢元素的质量不变进行分析解答,则:根据题意过氧化氢溶液的质量=90g 100%(1-89.5%),生成氧气的质量=90g 100%(1-89.5%)-90g=5.2g,答:生成氧气的质量为5.2g。
3.某化学兴趣小组同学对含有Na2SO4杂质的Na2CO3固体样品进行了以下实验探究。

一、计算题专题〔1〕气体表达型:4.〔2021.鄂州市〕〔5分〕为测定某石灰石样品中1.〔2021.徐州市〕(7分)医学上常用双氧水来清洗碳酸钙的含量,取克于烧杯中再向其中参加稀盐酸创口和局部抗菌。
小美同学为了测定一瓶医用双氧水溶液克,恰好完全反响〔杂质不反响〕,反响后烧杯中物的溶质质量分数,取该双氧水69g放入烧杯中,然后参加质总质量为克。
2g二氧化锰,完全反响后,称得烧杯内剩余物质的总质〔1〕生成CO2的质量。
量为。
请答复以下问题;〔2〕求石灰石样品中碳酸钙的质量分数〔写出计〔1〕二氧化锰在反响中的作用是,生成的算过程〕。
氧气为g。
〔2〕该双氧水溶液的溶质质量分数。
〔写出计算过程〕〔2021.河南省〕称取12.5g石灰石(主要成分是CaCO3,杂质不参加反响)放人烧杯中,向其中参加50g稀盐酸,二者恰好完全反响。
反响结束后称量烧杯中剩余物质的总质量为58.1g(不包括烧杯的质量,且气体的溶解忽略不计)。
试计算石灰石中杂质的质量分数。
5.〔2021.鸡西市〕为测定某黄铜样品中锌的含量,某同学称取20g黄铜〔铜和锌的合金〕样品于烧杯中,向其中参加稀硫酸至不再产生气泡为止,共消耗100g质量分数为9.8%的稀硫酸,请计算:(1)该黄铜样品中锌的质量。
(2)反响后所得溶液的溶质质量分数〔计算结果保留0.1%〕。
〔2021.达州市〕〔7分〕26g黄铜〔Cu-Zn合金〕与100g稀硫酸在烧杯中恰好完全反响,反响后测得烧杯中剩余物的总质量为克。
求:⑴黄铜中铜的质量分数;⑵反响后所得溶液中溶质质量分数。
〔计算结果精确到%〕〔2021.沈阳市〕〔6分〕黄铜是铜和锌的合金,可以用来制造机器、电器零件及日常用品。
为了测定某黄铜样品中铜的质量分数,取20g该样品向其中参加一定量的10%的稀硫酸,恰好完全反响,产生氢气。
请解答一下问题:〔1〕黄铜属于材料;〔2〕该黄铜样品中铜的质量分数;〔3〕完全反响后所得溶液的质量分数。

化学计算题中考题集锦(word)一、中考化学计算题1.现有l00g 8%的NaOH溶液,通过计算回答下列有关问题:(1)若用该溶液吸收CO2,最多可以生成Na2CO3多少克?____(写出详细计算过程)(2)当NaOH全部转化成为Na2CO3后,Na2CO3还会继续与CO2、H2O发生反应:Na2CO3+CO2+H2O=2NaHCO3,直至Na2CO3完全反应完。
请在如图画出利用l00g8%的NaOH 溶液吸收CO2与生成NaHCO3的曲线。
____(3)现有三种溶液:①100g8%NaOH溶液、②100g8%NaOH溶液吸收CO2转化为Na2CO3溶液、③100g8%NaOH溶液吸收过量CO2转化为NaHCO3溶液,分别用相同质量分数的硫酸与上述三种溶液恰好完全反应,需要的硫酸的质量_____(选填“相等”或“不相等”),原因是_____。
【答案】10.6g 相等三种溶液中所含的钠元素质量相等,与硫酸反应产生的Na2SO4质量相等,故消耗同种硫酸的质量相等【解析】【详解】(1)100g8%的NaOH溶液中含NaOH的质量=100g×8%=8g(2)设碳酸钠的质量为x,与氢氧化钠反应的二氧化碳的质量为y,碳酸氢钠的质量为z,和碳酸钠反应的二氧化碳的质量为a根据2NaOH+CO2=Na2CO3+H2O和 Na2CO3+CO2+H2O=2NaHCO3,可得关系式为:22323 2NaOH~CO~Na CO CO~2NaHCO8044106441688g y x a z804410644168====8g y x a zx=10.6gy=4.4gz =16.8ga=4.4g利用l00g8%的NaOH溶液吸收CO2与生成NaHCO3的曲线,起点4.4、拐点(8.8,16.8)。
如图:(3)三种溶液中所含的钠元素质量相等,根据钠元素守恒和硫元素守恒,可知与硫酸反应产生的Na2SO4质量相等,故消耗同种硫酸的质量相等。

计算题专项训练1.将镁条在氧气中燃烧,完全反响消耗氧气的质量为〔〕2.在反响A+3B==2C+3D中,A和B的相对分子质量为7:8,当与一定量B恰好完全反响后,生成,那么C的质量为〔〕3.将16g高锰酸钾放在试管中加热,反响后称得剩余物质得质量为,那么剩余物质是〔〕2MnO42和K2MnO44和K2MnO42、K2MnO4和KMnO44.点燃H2、N2和O2的混合气体20g,完全反响后生成18g水,那么剩余气体不可能是〔〕、N2和O的混合气体 B.N和O的混合气体2222D.H和N混合气体2225.在一个密闭容器中放入X、Y、Z、Q四种物质,在一定条件下发生化学反响,一段时间后,测得有关数据如下,那么关于此反响的认识错误的选项是〔〕A.反响后物质X的质量为15g物质X Y Z QB.反响中Y、Q的质量比为6:5反响前质量/g202137C.物质Y一定是单指反响后质量/g未测32112D.物质Z可能是该反响的催化剂6.在实验室制取氧气时,取MnO2和KClO3的固体混合物,加热至不再产生气体为止,收集到一定质量的氧气。
某化学兴趣小组欲求得所制氧气的质量,他们讲加热后的剩余物冷却到一定温度后,通过屡次加水测定剩余物质质量的方法即可求出。
水的质量与剩余固体的质量见下表:〔MnO2是不溶于水的黑色固体粉末〕〔1〕表中m值为。
编号1234〔2〕所制的氧气的质量。
加水的质量/g1*******剩余固体的质量/g m3 7.如今,有些城市使用二甲醚作为公交车的燃料,有效地解决了公交车冒黑烟的问题。
二甲醚燃烧的化学方程式可表示为:CabO d〔二甲醚〕222。
H+3O2CO+3HO请根据计算答复:〔1〕a=,b=,d=。
〔2〕23g二甲醚充分燃烧需要氧气质量多少克?生成CO2质量多少克?〔3〕假设用大理石和稀盐酸反响,制取与〔 2〕等质量的CO2,需质量分数为85%的大理石多少?8.高温加热10g碳酸钙,一段时间后停止加热,测得剩余固体中钙元素的质量分数为50%。
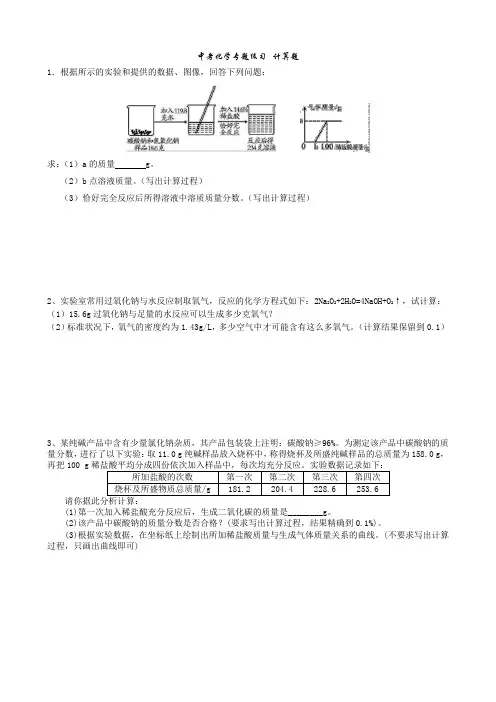
中考化学专题练习--计算题1.根据所示的实验和提供的数据、图像,回答下列问题:求:(1)a的质量 g。
(2)b点溶液质量。
(写出计算过程)(3)恰好完全反应后所得溶液中溶质质量分数。
(写出计算过程)2、实验室常用过氧化钠与水反应制取氧气,反应的化学方程式如下:2Na2O2+2H2O=4NaOH+O2↑,试计算:(1)15.6g过氧化钠与足量的水反应可以生成多少克氧气?(2)标准状况下,氧气的密度约为1.43g/L,多少空气中才可能含有这么多氧气。
(计算结果保留到0.1)3、某纯碱产品中含有少量氯化钠杂质,其产品包装袋上注明:碳酸钠≥96%。
为测定该产品中碳酸钠的质量分数,进行了以下实验:取11.0 g纯碱样品放入烧杯中,称得烧杯及所盛纯碱样品的总质量为158.0 g,再把100 g(1)第一次加入稀盐酸充分反应后,生成二氧化碳的质量是________g。
(2)该产品中碳酸钠的质量分数是否合格?(要求写出计算过程,结果精确到0.1%)。
(3)根据实验数据,在坐标纸上绘制出所加稀盐酸质量与生成气体质量关系的曲线。
(不要求写出计算过程,只画出曲线即可)4.工业盐酸中通常溶有少量的FeCl3而呈黄色,小红为测定某工业盐酸中HCl的含量进行如下实验:取某工业盐酸l00g,滴加一定溶质质量分数的NaOH溶液,测得加入NaOH溶液质量与反应生成的沉淀质量关系如图所示。
请回答下列问题:(1)FeCl3与NaOH恰好完全反应时,生成沉淀的质量是________g。
(2)计算氢氧化钠溶液的溶质质量分数。
(写出计算过程)(3)该工业盐酸中HCl的质量分数是_________。
5、钙是人体中的常量元素,缺钙时可通过食用保健药剂来增加摄入量。
某补钙药剂主要成分为碳酸钙,现将100g盐酸分成5等份,逐次加到用40g该药剂制成的粉末中(其他成分不与盐酸反应),得到部分数据与图象。
请根据有关信息回答问题:序号第1次第2次第3次第4次第5次加入盐酸的质量/g 20 20 20 20 20剩余固体的质量/g 35 30 25 20 a(1)a的数值为________,该品牌补钙药剂中CaCO3的质量分数是_________。


【化学】化学计算题练习题 (word )一、中考化学计算题1.某合金可能由铜与镁、锌中的一种组成,现欲测定其组成,进行如下实验:取该合金样品30g 放入烧杯中,让后将200g 溶质质量分数为19.6%的稀硫酸平均分四次依次加入该烧杯中,每次均充分反应。
实验数据如下:请计算:(1)该合金中铜的质量分数为 。
(2)该合金除铜外,另一种金属是 。
(写出过程) (3)第三次加入稀硫酸充分反应后,所得溶液中溶质的质量分数。
【答案】(1)30% ; (2)另一种金属应该是锌(详见解析过程) (3)28.6% 【解析】 【分析】 【详解】(1)由第一次加入50g 的稀硫酸合金的质量减少了6.5g ,第二次再加50g 稀盐酸时,合金的质量又减少6.5g ,所以得出每加入50g 的稀硫酸合金的质量就会减少6.5g ,说明50g 的稀硫酸和6.5g 的合金恰好完全反应,最后加入50g 稀硫酸时减少的质量只有1.5g ,所以剩余物质的质量即为铜的质量,该合金中铜的质量分数为=9g100%30%30g⨯= (2)由50g 的稀硫酸和6.5g 的合金确好完全反应,求出金属的相对原子质量 设:另一种金属为M ,相对原子质量为x 。
2442x 986.5g 50g M + H SO =MSO +19.6%H ⨯↑x 6.5g =9850g 19.6%⨯ x=65;所以该金属是锌; (3)第三次后剩余固体的质量为10.5g ,因此反应掉的物质的质量即为30g-10.5g=19.5g ,由19.5g 锌的质量求出反应生成的硫酸锌的质量,反应后溶液的质量=锌的质量+稀硫酸的质量-氢气的质量设:第三次反应后生成硫酸锌的质量为y ,氢气质量为z 。
2442981612150g 19.Zn + H S 6%yO =ZnSO +H z↑⨯98150g 19.6%=161y ⨯ y=48.3g ; 98150g 19.6%=2z⨯ z=0.6g 第三次加入稀硫酸充分反应后,所得溶液中溶质的质量分数=48.3g100%28.6%19.5g+150g-0.6g⨯≈2.实验室有一瓶碳酸钙和氯化钙粉末组成的均匀混合物,小科用相同溶质质量分数的稀盐酸和该混合物反应(所得溶液均为不饱和溶液),四组实验数据记录如下表,请分析计算:(1)反应后,稀盐酸还有剩余的是第________组; (2)求混合物中碳酸钙和氯化钙的质量之比________; (3)求表中a 的值为________; (4)求表中m 的值____。

最新化学计算题中考经典题型带答案(word)一、中考化学计算题1.将20.0g稀盐酸逐滴加入到10.0g溶质质量分数为40%的氢氧化钠溶液中,边滴加边搅拌,随着稀盐酸的滴加,溶液的pH变化情况如图所示,溶液的温度变化如表所示(不考虑反应过程中热量散失)反应时间0 10 20 30 40 5060(s)溶液温度20.5 20.6 20.7 20.8 20.920.8 20.7(℃)(1)当稀盐酸与氢氧化钠溶液恰好完全反应时,溶液的温度是_____℃(2)计算稀盐酸中溶质的质量分数_________(精确到0.1%)【答案】20.936.5%【解析】【分析】根据图表可知当反应时间为40秒时,溶液的温度最高,所以当40秒时,反应恰好完全反应。
当pH为7的时候,恰好完全反应,根据氢氧化钠的质量可以求出盐酸的质量分数。
【详解】(1)因为中和反应是放热反应,所以温度最高时恰好完全反应,所以恰好完全反应时的温度从表上可知为20.9℃(2)设参加反应的盐酸的质量为xx=3.65g36.5%所以参加反应的盐酸的质量是36.5%。
2.我国化工专家侯德榜的“侯氏制碱法”为世界制碱工业做出了突出的贡献,工业上用侯氏制碱法制得的纯碱中含有一定量的氯化钠杂质。
现称取只含氯化钠杂质的纯碱样品11g,全部溶解在50g水中,当加入稀盐酸64.4g时,恰好完全反应,所得溶液的质量为121g。
试求:(1)该纯碱样品的纯度_________________。
(2)所得溶液中溶质的质量分数_________。
【答案】96.4% l0%【解析】【分析】纯碱中碳酸钠与稀盐酸反应放出二氧化碳,根据质量守恒定律,利用反应前后物质总质量差即反应放出二氧化碳的质量;根据反应的化学方程式,计算出纯碱中碳酸钠的质量和反应后溶液中溶质氯化钠的质量。
【详解】反应放出的CO2的质量为:64.4g+50g+11g-121g=4.4g设参加反应的Na2CO3质量为x,生成NaCl的质量为yNa2CO3+2HCl=2NaCl+H2O+CO2↑106 117 44x y 4.4g10611744==x y 4.4g解之得 x=10.6g,y=11.7g(1)碳酸钠纯度=10.6g100%11g≈96.4%;(2)纯碱样品中NaCl的质量=11g-10.6g=0.4g反应后溶液中NaCl的质量为=11.7g+0.4g=12.1g反应后溶液中NaCl的质量分数=12.1g121g×100%=10%答:(1)该纯碱样品的纯度约为96.4%;(2)所得溶液中溶质的质量分数为10%。
最新人教版中考化学 化学计算题专题复习练习(含解析)(word )一、中考化学计算题1.请根据如图所示的实验过程和提供的数据计算。
(1)a 、b 的数值分别为_____、_____。
(2)合金中锌的质量分数为_____。
(3)第二次加入ag 14.6%的稀盐酸充分反应后所得溶液中溶质的质量分数。
_____(写出计算过程,计算结果精确至0.1%) 【答案】50 8.5 90% 24.2% 【解析】 【分析】 【详解】解:(1)由题意可知,第一次和第二次加入稀盐酸后锌有剩余,稀盐酸完全反应,即2ag14.6%的稀盐酸消耗锌粒15g ﹣2g =13g ;故b =15g ﹣13g2=8.5g ;由题意可知: 22+=+65736.514.6%Zn 2HCl ZnCl H g ag ↑⨯65 6.57314.6%g ag =⨯ a =50(2)合金中锌的质量分数为15 1.515g gg- ×100%=90%;(3)设第二次加入ag 14.6%的稀盐酸充分反应后所得溶液中溶质的质量为x ,生成氢气质量为y ,22+=Zn 2HCl Zn +6513621l 52C H g gxy↑-651362152g g x y==- x =27.2g y =0.4g第二次加入ag 14.6%的稀盐酸充分反应后所得溶液中溶质的质量分数:27.2(152)5020.4gg g g g-+⨯-×100%≈24.2%。
答案:(1)50;8.5;(2)90%;(3)第二次加入ag 14.6%的稀盐酸充分反应后所得溶液中溶质的质量分数为24.2%。
2.某炼铝工厂想测定铝土矿中A12O 3的含量,将矿石粉碎(其中杂质不溶于水,不与酸反应,且不含铝元素),进行如下实验,第一步反应的物质质量关系如坐标图所示:(1)上述实验过程中发生反应的化学方程式是_____;(2)根据已知条件列出求解第一步实验铝土矿中参加反应的A12O 3质量(x)的比例式_____ (3)铝土矿样品中A12O 3的含量_____;(4)坐标图中B 点所示溶液中溶质的化学式是_____;(5)在第二步实验结束后所得溶液中溶质的质量分数是_____(6)用1700t 此铝土矿冶炼得到540t 的铝,则在冶炼中,铝土矿的利用率是_____。
最新中考化学化学计算题20篇(附带答案解析)(word)一、中考化学计算题1.将一定质量的NaCl和Na2SO4 固体混合物完全溶于水后,加入一定质量分数的BaCl2溶液208g,恰好完全反应,过滤,得到23.3g沉淀,经测定滤液中含氯元素的质量为21.3g (不考虑过滤过程中物质质量的损失)。
计算:(1)所加BaCl2溶液的溶质质量分数_______。
(2)原固体混合物中Na2SO4的质量________。
(3)原固体混合物中NaCl的质量__________。
【答案】10% 14.2g 23.4g【解析】【分析】由题可知生成硫酸钡的质量是23.3g,根据化学方程式列比例求出Na2SO4的质量,BaCl2的质量,由化学式求出BaCl2中氯元素的质量,可得出原固体混合物中NaCl中氯元素的质量,从而求得NaCl的质量;【详解】设BaCl2的质量是xg,Na2SO4的质量是yg,Na2SO4+BaCl2=2NaCl+BaSO4↓142 208 233y x 23.3g142/y=208/x=233/23.3gy=14.2g,x=20.8gBaCl2溶液的溶质质量分数==10﹪BaCl2中氯元素的质量=g=7.1g原固体混合物中NaCl中氯元素的质量=21.3g-7.1g=14.2g原固体混合物中NaCl的质量=14.2g=23.4g2.化学实验小组的同学为了研究某公共场所铁制护栏锈蚀程度,取12.8g已生锈的铁护栏(假设其成分只有Fe和Fe2O3,不含其它杂质),加入到120g一定浓度的稀盐酸中,充分反应,测得产生气体质量与稀盐酸质量关系如图所示。
请回答问题:(1)发生复分解反应的化学方程式为_____。
(2)根据已知信息列出求解参加反应的铁的质量(X )的比例式_____。
(3)铁护栏中氧化铁的质量分数为_____。
(4)若用质量分数36.5%的浓盐酸配制120g 上述稀盐酸,需要浓盐酸与水的质量比为_____。
最新初三化学化学计算题题20套(带答案)一、中考化学计算题1 .向13. 6g 碳酸钠和氯化钠的固体混合物滴加稀盐酸,所加稀盐酸质量与生成气体质量 的关系如图所示。
计算:T 气体的质量gkj ____ ,° 73盐酸的质量£■(1)固体混合物中碳酸钠的质量。
(2)该稀盐酸中溶质的质量分数。
(3)恰好完全反应时所得的溶液中溶质的质量分数。
(计算结果精确至 0.1%)【答案】(1) 1。
. 6 克(2) 10% (3) 17 . 9% 【解析】试题分析:设固体混合物中 Na2c 。
3的质量为X,稀盐酸中溶质的质量为 y,反应生成NaCI的质量为z 。
Na2c03+ 2HCI ="='• 2NaCI + HO + CO2 t 106 2 x . 333 2 x 585 44 x y z 4 4g 得x=10 . 6克106 = 44 J 4.4s恰好完全反应时所得的溶液溶质质量分数为:11. 7g-13. 6g —10.6g——— --------- x 100°G=17.9%73E -13.6E -4. 4?WBIWB考点:根据化学方程式的计算物质的质量分数2 .将14.06g 粗还原铁粉(假设粗还原铁粉中杂质仅含少量Fe x C)与足量稀硫酸反应,得到0.48gH2 (FexC 与稀硫酸反应不产生吨)。
若将相同质量的粗还原铁粉在氧气流中完全73117 <9_444.4g_ ____ 444.4s得♦二克 ■得;z ・lL7克稀盐酸中溶质的质量分数为:7;y -X100S=10%反应,得到0.22gCO2 .试通过计算确定:(1)此粗还原铁粉中单质铁的质量(2)此粗还原铁粉中杂质FexC的化学式。
【答案】13.44g Fe2c【解析】【分析】【详解】若将14.06g还原铁粉(含少量Fe x C)在氧气流中加热,得到0.22gCO2,碳元素的质量12=0.22gx —=0.06g44(1)将相同质量的还原铁粉与足量硫酸反应,得到0.48gH2,设消耗铁的质量为X。
初三化学化学计算题专项训练及答案一、有关化学式的计算1、计算相对分子质量相对分子质量等于化学式中各原子的相对原子质量总和。
例 1:计算硫酸(H₂SO₄)的相对分子质量。
解:氢(H)的相对原子质量约为 1,硫(S)的相对原子质量约为32,氧(O)的相对原子质量约为 16。
硫酸的相对分子质量= 2×1 + 32 + 4×16 = 98练习 1:计算碳酸钙(CaCO₃)的相对分子质量。
答案:钙(Ca)的相对原子质量约为 40,碳(C)的相对原子质量约为 12,氧(O)的相对原子质量约为 16。
碳酸钙的相对分子质量= 40 + 12 + 3×16 = 1002、计算物质组成元素的质量比物质中各元素的质量比等于各元素的相对原子质量乘以原子个数之比。
例 2:计算水(H₂O)中氢元素和氧元素的质量比。
解:氢元素的相对原子质量约为1,氧元素的相对原子质量约为16。
水(H₂O)中氢元素和氧元素的质量比=(2×1)∶(1×16)=1∶8练习 2:计算二氧化碳(CO₂)中碳元素和氧元素的质量比。
答案:碳元素的相对原子质量约为 12,氧元素的相对原子质量约为16。
二氧化碳(CO₂)中碳元素和氧元素的质量比=(1×12)∶(2×16)= 3∶83、计算物质中某元素的质量分数某元素的质量分数=(该元素的相对原子质量×原子个数÷相对分子质量)×100%例 3:计算硝酸铵(NH₄NO₃)中氮元素的质量分数。
解:氮(N)的相对原子质量约为 14,氢(H)的相对原子质量约为 1,氧(O)的相对原子质量约为 16。
硝酸铵的相对分子质量= 14×2 + 1×4 + 16×3 = 80氮元素的质量分数=(14×2÷80)×100% = 35%练习 3:计算尿素CO(NH₂)₂中氮元素的质量分数。
最新化学计算题专项练习(word)一、中考化学计算题1.某化学兴趣小组的同学在实验室配制溶质质量分数为8%的氢氧化钠溶液,并用其测定某稀盐酸中溶质的质量分数。
下图表示用该氢氧化钠溶液与10g某稀盐酸发生反应时溶液温度的变化情况。
试计算稀盐酸中溶质的质量分数。
【答案】14.6%【解析】试题分析:由于中和反应放热,故随着反应的进行,溶液的温度逐渐升高,直至反应恰好完全,溶液温度达到最高,故根据图示可判断,当加入氢氧化钠那溶液的质量为20g时,反应恰好完全解:分析图知与10g稀盐酸恰好完全反应的氢氧化钠质量为:20g×8%=1.6g设稀盐酸中溶质的质量为xNaOH+HCl=NaCl+H2O40 36.51.6g x40:1.6g=36.5:xx=1.46g稀盐酸中溶质的质量分数为:1.46g/10g=14.6%答:稀盐酸中溶质的质量分数为14.6%考点:根据化学方程式计算2.我国化工专家侯德榜的“侯氏制碱法”为世界制碱工业做出了突出的贡献,工业上用侯氏制碱法制得的纯碱中含有一定量的氯化钠杂质。
现称取只含氯化钠杂质的纯碱样品11g,全部溶解在50g水中,当加入稀盐酸64.4g时,恰好完全反应,所得溶液的质量为121g。
试求:(1)该纯碱样品的纯度_________________。
(2)所得溶液中溶质的质量分数_________。
【答案】96.4% l0%【解析】【分析】纯碱中碳酸钠与稀盐酸反应放出二氧化碳,根据质量守恒定律,利用反应前后物质总质量差即反应放出二氧化碳的质量;根据反应的化学方程式,计算出纯碱中碳酸钠的质量和反应后溶液中溶质氯化钠的质量。
【详解】反应放出的CO2的质量为:64.4g+50g+11g-121g=4.4g 设参加反应的Na2CO3质量为x,生成NaCl的质量为y Na2CO3+2HCl=2NaCl+H2O+CO2↑106 117 44x y 4.4g10611744==x y 4.4g解之得 x=10.6g,y=11.7g(1)碳酸钠纯度=10.6g100%11g≈96.4%;(2)纯碱样品中NaCl的质量=11g-10.6g=0.4g反应后溶液中NaCl的质量为=11.7g+0.4g=12.1g反应后溶液中NaCl的质量分数=12.1g121g×100%=10%答:(1)该纯碱样品的纯度约为96.4%;(2)所得溶液中溶质的质量分数为10%。
最新化学计算题单元测试(word版附答案)经典一、中考化学计算题1.某石化厂有一种石油产品含有质量分数为4.9%的残余硫酸,过去他们都是用NaOH溶液来清洗这些硫酸。
请你计算:(1)若要清洗1000kg的这种石油产品,需要_____kg的NaOH。
(2)该石化厂进行了技术改造,采用Ca(OH)2中和这些残余硫酸。
每处理1000kg这种产品,他们可以节约多少经费_____?请你写出具体的计算过程。
工业级的NaOH和Ca(OH)2的最新市场批发价如下表:试剂Ca(OH)2NaOH价格(元/kg) 1.00 6.00(3)请你在图中画出氢氧化钠和氢氧化钙处理1000kg该石油产品时,残余硫酸溶质的质量变化曲线;氢氧化钠用虚线表示,氢氧化钙用实线表示。
_____(请你注明具体的坐标)【答案】40 203元【解析】【详解】1000kg的这种石油产品所含硫酸的质量为1000kg×4.9%=49kg设消耗的氢氧化钠的质量为x,消耗的氢氧化钙的质量为y根据2NaOH+H2SO4=Na2SO4+2H2O和Ca(OH)2+H2SO4=CaSO4+2H2O可得关系式为242 2NaOH H SO Ca(OH)809874x49kg y::809874==x49kg yx=40kgy=37kg每处理1000kg这种产品,他们可以节约经费为6.00元/kg×40kg-1.00元/kg×37kg=203元图中画出用氢氧化钠和氢氧化钙处理1000kg该石油产品时,残余硫酸溶质的质量变化曲线;氢氧化钠用虚线“…”表示,氢氧化钙用实线“一”表示,答:(1)若要清洗1000kg的这种石油产品,需要 40kg的NaOH。
(2)该石化厂进行了技术改造,采用Ca(OH)2中和这些残余硫酸。
每处理1000kg这种产品,他们可以节约203元经费。
(3)残余硫酸溶质的质量变化曲线;氢氧化钠用虚线“…”表示,氢氧化钙用实线“一”表示,2.我国化工专家侯德榜发明了侯氏制碱法,为世界制碱工业作出了突出贡献。