4 第二章 合成的抗感染药
- 格式:ppt
- 大小:3.56 MB
- 文档页数:85


药物化学在抗感染药物研发中的应用药物化学是研究药物分子结构与性质之间相互关系的学科,广泛应用于药物研发领域。
随着细菌耐药性的不断增强,抗感染药物的研发变得尤为重要。
药物化学在抗感染药物研发中发挥关键作用。
本文将探讨药物化学在抗感染药物研发中的应用。
一、药物化学的意义和作用药物化学是一门综合性学科,涉及有机合成、药物设计与合成、药物分析等多个方面。
它的意义在于探索药物分子与靶标之间相互作用的规律,为药物研发提供指导。
在抗感染药物研发中,药物化学的作用不可忽视。
通过药物化学的手段,可以合成出具有高效、低毒副作用的抗感染药物。
二、抗感染药物研发的挑战抗感染药物研发面临着诸多挑战。
一方面,细菌不断产生耐药性,已有的抗生素逐渐失去了对感染的治疗效果。
另一方面,抗感染药物的研发周期长、成本高、成功率低。
因此,寻找新的抗感染药物成为迫切的需求。
三、药物化学在抗感染药物研发中的策略在抗感染药物研发中,药物化学起到了重要的推动作用。
以下为药物化学在抗感染药物研发中的策略:1. 靶向细菌的关键酶活性:通过药物化学的方法,可以设计和合成特异性靶向细菌关键酶活性的抑制剂。
这些抑制剂可以阻断细菌关键酶的活性,从而达到抗菌的目的。
2. 合成新的化合物结构:药物化学可以通过合成新的化合物结构,改变药物分子的性质,增强其抗菌活性和选择性。
通过这种方式,可以寻找到更加有效的抗感染药物。
3. 结构修饰和优化:通过结构修饰和优化,药物化学可以提高药物的药效和安全性。
这一策略在抗感染药物研发中尤其重要,因为药物需要在受感染部位起到高效杀菌作用,并且避免对宿主产生毒副作用。
4. 组合用药策略:药物化学可以通过组合用药策略,将不同的抗菌药物进行合理的组合,以增强药效和防止多重耐药性的产生。
药物化学可以设计和合成适合组合用药的化合物,提高治疗效果。
四、实例分析以抗MRSA感染为例,药物化学在研发抗MRSA感染药物的过程中发挥了重要作用。
通过药物化学的手段,可以设计出特异性靶向MRSA细菌的抑制剂,并通过合成新的化合物结构,改善药物的药效。


阿莫西林 (Amoxicillin) 抗感染药物阿莫西林 (Amoxicillin) 抗感染药物阿莫西林(Amoxicillin)是一种广泛使用的抗感染药物,是青霉素类抗生素的一种。
它通过抑制细菌细胞壁的合成,从而阻止细菌的生长和繁殖,对许多细菌引起的感染起到治疗作用。
下面我们将从阿莫西林的作用机制、适应症和副作用等方面来介绍这一抗感染药物。
一、作用机制阿莫西林通过干扰细菌细胞壁的合成来发挥其抗感染作用。
它能抑制细菌壁合成所需的转肽酶,导致细菌细胞壁的脱水和破裂,进而使细菌失去保护,最终导致细菌的死亡。
这种作用机制使得阿莫西林能广泛应用于治疗细菌感染。
二、适应症阿莫西林可用于治疗多种细菌引起的感染,包括但不限于:1. 上呼吸道感染:如鼻窦炎、扁桃体炎等。
2. 下呼吸道感染:如支气管炎、肺炎等。
3. 泌尿生殖系统感染:如尿道炎、性传播疾病等。
4. 皮肤和软组织感染:如蜂窝组织炎、痤疮等。
5. 消化系统感染:如胃肠炎、阑尾炎等。
在使用阿莫西林治疗感染时,医生会针对具体情况确定用药剂量和疗程。
请严格按照医生的指示使用药物,不得自行调整剂量或停药。
三、副作用阿莫西林通常是安全有效的,但使用中仍可能出现一些副作用,如:1. 胃肠道反应:如恶心、呕吐、腹泻等。
2. 过敏反应:如皮疹、荨麻疹等。
3. 严重过敏反应:如药疹、药热综合征等,需立即停药并就医。
4. 肝功能损害:如肝酶升高、黄疸等,需密切观察。
在使用阿莫西林时,如果出现上述或其他不适症状,应及时告知医生或药师,以便调整治疗方案。
四、注意事项在使用阿莫西林时,需注意以下几点:1. 运用药物前,需告知医生关于过敏史、其他疾病史以及正在使用的其他药物。
2. 在医生的指导下使用药物,严格按照医嘱用药,不可随意增减剂量或停药。
3. 对于儿童、孕妇、哺乳期妇女和老年人,应特别谨慎使用,并根据医生的建议确定剂量和疗程。
4. 阿莫西林与某些药物可能存在相互作用,如抗凝药物、甲苯磺丁脲和其他抗菌药物等。

毕业生考试习题库(适用于药学专业)药物化学第一章绪论一、选择题(单选)1。
药物化学的研究对象是()A。
天然药物 B. 生物药物C。
化学药物D。
中药材E。
中成药2。
硝苯地平的作用靶点为( )A。
受体B。
酶 C. 离子通道D。
核酸E。
基因二、配比选择题[5-9]A。
药品通用名B。
INN名称 C. 化学名 D. 商品名 E. 俗名5.对乙酰氨基酚( )6。
泰诺()7.Paracetamol ()8。
N-(4-羟基苯基)乙酰胺( )9.醋氨酚()第二章合成抗感染药一、选择题(单选)1.磺胺类药物的作用机制是抑制()A.二氢叶酸合成酶B.二氢叶酸还原酶C.叶酸合成酶D.叶酸还原酶 E. DNA回旋酶2。
下列具有三氮唑结构的抗真菌药物有()A。
酮康唑B。
氟康唑C。
克霉唑D。
两性霉素E。
咪康唑3。
属于开环核苷类的抗病毒药物是( )A。
阿昔洛韦B。
利巴韦林C。
齐多夫定D。
盐酸金刚烷胺E。
阿糖腺苷4。
下面哪个药物为抗菌增效剂()A。
磺胺甲噁唑B。
呋喃妥因C。
盐酸小檗碱D。
甲氧苄啶E。
诺氟沙星5。
在喹诺酮类抗菌药构效关系中,为抗菌活性不可缺少的部分是() A.1-位氮原子无取代B.3—位上有羧基和4—位是羰基C.5 位的氨基D.7 位杂环取代基团E.8 位的氟原子6。
磺胺甲噁唑(SMZ)和甲氧苄啶(TMP)代谢拮抗叶酸生物合成通路( )A.都作用于二氢叶酸还原酶B.都作用于二氢叶酸合成酶C.前者作用于二氢叶酸还原酶,后者作用于二氢叶酸合成酶D.前者作用于二氢叶酸合成酶,后者作用于二氢叶酸还原酶E.干扰细菌对叶酸的摄取7. 利福平的化学结构属于下列哪一种( )A。
大环羧酸类B。
氨基糖甙类C。
大环内酰胺类D. 环状多肽类E. 大环内酯类8。
下列哪个药物结构中含有叠氮基团 ( )A. 利巴韦林B. 齐多夫定 C 。
阿昔洛韦 D 。
特比萘芬 E 。
克霉唑9. 与乙胺嘧啶属同一结构类型,作用机制也相似的药物为 ( )A. 磺胺甲恶唑 B 。

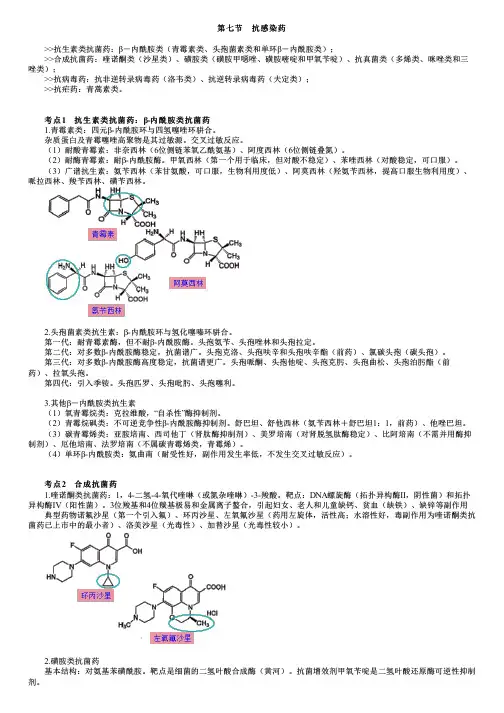
第七节 抗感染药 >>抗生素类抗菌药:β-内酰胺类(青霉素类、头孢菌素类和单环β-内酰胺类); >>合成抗菌药:喹诺酮类(沙星类)、磺胺类(磺胺甲噁唑、磺胺嘧啶和甲氧苄啶)、抗真菌类(多烯类、咪唑类和三唑类); >>抗病毒药:抗非逆转录病毒药(洛韦类)、抗逆转录病毒药(夫定类); >>抗疟药:青蒿素类。
考点考点1 抗生素 抗生素类抗菌药:类抗菌药:β-内酰胺类内酰胺类抗菌药抗菌药 1.青霉素类:四元β-内酰胺环与四氢噻唑环骈合。
杂质蛋白及青霉噻唑高聚物是其过敏源。
交叉过敏反应。
(1)耐酸青霉素:非奈西林(6位侧链苯氧乙酰氨基)、阿度西林(6位侧链叠氮)。
(2)耐酶青霉素:耐β-内酰胺酶。
甲氧西林(第一个用于临床,但对酸不稳定)、苯唑西林(对酸稳定,可口服)。
(3)广谱抗生素:氨苄西林(苯甘氨酸,可口服,生物利用度低)、阿莫西林(羟氨苄西林,提高口服生物利用度)、哌拉西林、羧苄西林、磺苄西林。
2.头孢菌素类抗生素:β-内酰胺环与氢化噻嗪环骈合。
第一代:耐青霉素酶,但不耐β-内酰胺酶。
头孢氨苄、头孢唑林和头孢拉定。
第二代:对多数β-内酰胺酶稳定,抗菌谱广。
头孢克洛、头孢呋辛和头孢呋辛酯(前药)、氯碳头孢(碳头孢)。
第三代:对多数β-内酰胺酶高度稳定,抗菌谱更广。
头孢哌酮、头孢他啶、头孢克肟、头孢曲松、头孢泊肟酯(前药)、拉氧头孢。
第四代:引入季铵。
头孢匹罗、头孢吡肟、头孢噻利。
3.其他β-内酰胺类抗生素 (1)氧青霉烷类:克拉维酸,“自杀性”酶抑制剂。
(2)青霉烷砜类:不可逆竞争性β-内酰胺酶抑制剂。
舒巴坦、舒他西林(氨苄西林+舒巴坦1:1,前药)、他唑巴坦。
(3)碳青霉烯类:亚胺培南、西司他丁(肾肽酶抑制剂)、美罗培南(对肾脱氢肽酶稳定)、比阿培南(不需并用酶抑制剂)、厄他培南、法罗培南(不属碳青霉烯类,青霉烯)。
(4)单环β-内酰胺类:氨曲南(耐受性好,副作用发生率低,不发生交叉过敏反应)。


新型抗感染药赛来昔布的合成新工艺作者:姚德勇,王巧玲来源:《中国医药导报》2010年第16期[摘要] 目的:研究一步法制备赛来昔布的合成方法。
方法:以异丙醇为溶剂,对甲基苯乙酮与三氟乙酸乙酯为原料缩合得到1-(4-甲基苯基)-4,4,4-三氟-1,3-丁二酮,直接与对磺胺基苯肼盐酸盐在溶剂脱水环合。
结果:本法总收率达83%。
结论:赛来昔布新合成方法切实可行。
[关键词] 赛来昔布;环氧化酶;合成[中图分类号] R914.5[文献标识码]A [文章编号]1673-7210(2010)06(a)-029-02New synthesis technology about celecoxib of a new anti-inflammatoryYAO Deyong, WANG Qiaoling(Qingdao Continent Pharmaceutical Co., Ltd., Qingdao 266061, China)[Abstract] objective: To improve the one stage synthetic method of celecoxib. Methods: In isopropyl alcohol, the condensation of 4-methylacetophenone with ethyl trifluoroacetate by means of sodium methoxide gives 1-(4-methylphenyl)-4, 4, 4-trifluorobutane which was cyclodehydrated with (4-sulfamoylphenyl) hydrazine hydrochloride to give celecoxib. Results: The total yield reached up to around 83%. Conclusion: The new synthesis process of celecoxib is practicable.[Key words] Celecoxib; Cyclooxygenase; Synthesis赛来昔布(Celecoxib)是一种新型抗感染药,用于治疗类风湿性关节炎和骨关节炎等炎症性疾病。