13-1 准静态过程 功 热量【热力学】
- 格式:pptx
- 大小:637.74 KB
- 文档页数:4








热力学基础一、基本要求1. 理解功、热量及准静态过程的概念。
2. 掌握热力学第一定律,能分析计算理想气体等容、等压、等温过程和绝热过程中的功、热量、内能改变量;理解循环过程概念及卡诺循环的特征,并能计算效率和致冷系数。
3. 了解可逆过程、不可逆过程及卡诺定理。
4. 了解热力学第二定律及其统计意义。
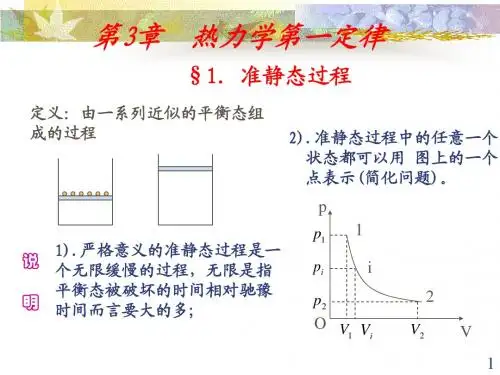
二、主要内容1. 准静态过程:过程进行的每一时刻,系统的状态都无限接近平衡态。
准静态过程可以用状态图上的曲线表示。
2. 热力学第一定律(1) 热力学第一定律的数学表达式Q=E 2 - E 1 +W对微分过程为dQ=dE +d W热力学第一定律的实质是能量守恒与转换定律在热现象中的应用,其内容表示系统吸收的热量一部分转换为系统的内能,一部分对外做功。
(2) 准静态过程系统对外做功:d W=pd V ,W=⎰12V V pd V(3) 热量:系统和外界之间或两个物体之间由于温度不同而交换的热运动量,热量也是过程量。
一定摩尔的某种物质,在某一过程中吸收的热量,)(C m12m c,T T M Q -=(4) 摩尔热容:1mo1物质温度变化1K 所吸收或放出的热量,定义式为 dTQd m,=m c C 其中m 为1mo1 物质吸热。
摩尔定容热容:CV , m =摩尔定压热容:Cp, m =理想气体的摩尔热容:CV, m =,Cp, m =Cp, m =CV, m + 摩尔热容比:=3. 热力学第一定律对理想气体等值过程和绝热过程的应用,详见表1 表1 d =0 =恒量=恒量p =恒量mmmM m T1nMm T1nCV, m =Cp, m =4. 循环过程(1)循环过程的特征是E =0热循环:系统从高温热源吸热,对外做功,向低温热源放热,致效率为== 1—致冷循环:系统从低温热源吸热,接受外界做功,向高温热源放热,致冷系数为==(2)卡诺循环:系统只和两个恒温热源进行热交换的准静态循环过程。
卡诺热机的效率为= 1—卡诺致冷机的致冷系数为三、习题与解答1、 如图所示,一定量的空气,开始在状态A ,其压强为2.0×105Pa ,体积为2.0 ×10-3m 3 ,沿直线AB 变化到状态B 后,压强变为1.0 ×105Pa ,体积变为3.0 ×10-3m 3 ,求此过程中气体所作的功.解 S ABCD =1/2(BC +AD)×CD 故 W =150 J2、 汽缸内储有2.0mol 的空气,温度为27 ℃,若维持压强不变,而使空气的体积膨胀到原体积的3倍,求空气膨胀时所作的功. 解 根据物态方程11RT pV v =, 则作功为()J 1097.92231112⨯===-=RT pv V V p W v3、64g 氧气(可看成刚性双原子分子理想气体)的温度由0℃升至50℃,〔1〕保持体积不变;(2)保持压强不变。

§13.1~13. 213.1 如图所示,当气缸中的活塞迅速向外移动从而使气体膨胀时,气体所经历的过程【C 】(A) 是准静态过程,它能用p ─V 图上的一条曲线表示(B) 不是准静态过程,但它能用p ─V 图上的一条曲线表示(C) 不是准静态过程,它不能用p ─V 图上的一条曲线表示(D) 是准静态过程,但它不能用p ─V 图上的一条曲线表示分析:从一个平衡态到另一平衡态所经过的每一中间状态均可近似当作平衡态(无限缓慢)的过程叫做准静态过程,此过程在p-V 图上表示一条曲线。
题目中活塞迅速移动,变换时间非常短,系统来不及恢复平衡,因此不是准静态过程,自然不能用p -V 图上的一条曲线表示。
13.2 设单原子理想气体由平衡状态A ,经一平衡过程变化到状态B ,如果变化过程不知道,但A 、B 两状态的压强,体积和温度都已知,那么就可以求出:【B 】(A ) 体膨胀所做的功; (B ) 气体内能的变化;(C ) 气体传递的热量; (D ) 气体的总质量。
分析:功、热量都是过程量,除了与系统的始末状态有关外,还跟做功或热传递的方式有关;而内能是状态量,只与始末状态有关,且是温度的单值函数。
因此在只知道始末两个状态的情况下,只能求出内能的变化。
对于答案D 而言,由物态方程RT PV ν=可以计算气体的物质的量,但是由于不知道气体的种类,所以无法计算气体总质量。
13.3 一定量的理想气体P 1、V 1、T 1,后为P 2、V 2、T 2, 已知V 2>V 1, T 2<T 1,以下说法哪种正确?【D 】(A ) 不论经历什么过程,气体对外净作功一定为正值;(B ) 不论经历什么过程,气体对外界净吸热一定为正值;(C ) 若是等压过程,气体吸的热量最少;(D ) 若不知什么过程,则W 、Q 的正负无法判断。
分析:功和热量都是过程量,他们除了与系统的始末状态有关外,还跟经历的过程方式有关,所以A 、B 选项不正确。