分析化学——滴定分析1
- 格式:docx
- 大小:37.09 KB
- 文档页数:2

概述一、络合滴定中的滴定剂:络合滴定法:以络合反应为基础的滴定分析方法称为络合滴定法。
络合剂:在络合反应中,提供配位原子的物质称为配位体,即络合剂。
无机络合剂:⑴无机络合剂的分子或离子大都是只含有一个配位原子的单齿配位体,它们与金属离子的络合反应是逐级进行的;⑵络合物的稳定性多数不高,因而各级络合反应都进行得不够完全;⑶由于各级形成常数彼此相差不大,容易得到络合比不同的一系列络合物,产物没有固定的组成,从而难以确定反应的计量关系和滴定终点。
2、有机络合剂:⑴有机络合剂分子中常含有两个或两个以上的配位原子,称之为多齿配位体。
⑵与金属离子络合时可以形成具有环状结构的螯合物,在一定的条件下络合比是固定的。
⑶生成的螯合物稳定,络合反应的完全程度高,能得到明显的滴定终点。
三氨羧络合剂:它是一类含有氨基二乙酸—N(CH2COOH)2基团的有机化合物,其分子中含有氨氮和羧氧两种配位能力很强的配位原子。
能够用于络合滴定的反应,必须具备下列条件:一、形成的络合物要相当稳定,K形≥108,否则不易得到明显的滴定终点。
二、在一定反应条件下,络合数必须固定(即只形成一种配位数的络合物)。
三、反应速度要快。
四、要有适当的方法确定滴定的计量点。
二、EDTA及其二钠盐的性质:乙二胺四乙酸是含有羧基和氨基的螯合剂,能与许多金属离子形成稳定的螯合物。
在化学分析中,它除了用于络合滴定以外,在各种分离、测定方法中,还广泛地用作掩蔽剂。
乙二胺四乙酸简称EDTA或EDTA酸,常用H4Y表示。
白色晶体,无毒,不吸潮。
在水中难溶。
在22℃时,每100毫升水中能溶解0.02克,难溶于醚和一般有机溶剂,易溶于氨水和NaOH溶液中,生成相应的盐溶液。
一、EDTA的结构:在水溶液中,其以双偶极离子存在。
当H4Y溶解于酸度很高的溶液中,它的两个羧基可再接受H+而形成H6Y,这样EDTA就相当于六元酸,有六级离解平衡。
Ka1 Ka2 Ka3 Ka4 Ka5 Ka610-0.90 10-1.60 10-2.00 10-2.67 10-6.16 10-10.26由于EDTA酸在水中的溶解度小,通常将其制成二钠盐,一般也称EDTA或EDTA二钠盐,常以Na2H2Y·2H2O形式表示。

分析化学滴定分析滴定分析是一种常用的分析化学方法,主要用于测定溶液中其中一种物质的含量或浓度。
它通过添加一种已知浓度的试剂(称为滴定试剂),使之与待测溶液中所需测定的物质发生化学反应,根据化学反应的滴定终点,即溶液发生可观察的变化,比如颜色变化、电位变化或沉淀的出现,确定滴定的终点,从而计算出被滴定物质的浓度。
滴定分析在实际应用中广泛用于酸碱中和反应、氧化还原反应、络合反应等。
其中最常见的滴定反应是酸碱滴定反应。
酸碱滴定分析的基本原理是根据酸、碱之间的中和反应来测定溶液中酸或碱的浓度。
其常用的滴定试剂有强酸和强碱,如盐酸、硫酸、氢氧化钠等。
在进行酸碱滴定分析时,首先需要准备两种溶液,一个是待测溶液,一个是滴定试剂。
待测溶液的浓度通常是未知的,而滴定试剂的浓度通常是已知的。
滴定试剂以滴定管逐滴加入待测溶液中,同时不断搅拌溶液,直到滴定终点出现。
滴定终点是指溶液中化学反应发生完全,可观察到的物理变化出现,如颜色突变或电位突变。
滴定过程中需要注意一些重要的实验技巧。
首先,滴定试剂的浓度要适当选择,以使其与被测物质充分反应。
其次,要进行试剂的标定,即确定滴定试剂的准确浓度。
这可以通过溶液的标定反应来实现,即反应滴定试剂与已知浓度的物质,根据反应的化学计量关系计算出滴定试剂的浓度。
再次,滴定过程中要注意控制滴定液的滴加速度,以免产生误差。
最后,在靠近滴定终点时,要慢慢地滴加试剂,以避免过量滴定,从而影响结果的准确性。
滴定分析具有准确度高、操作简便、结果可靠等优点,因此被广泛应用于实际分析中。
例如,酸碱滴定法可以用于测定水样中的酸度或碱度,从而评估水质的好坏。
氧化还原滴定法可以用来测定溶液中其中一种物质的氧化或还原能力,如测定食品中的抗氧化剂含量。
络合滴定法可以用来测定金属离子的浓度,如测定水中的钙离子含量。
总的来说,滴定分析是一种重要的分析化学方法,常用于测定溶液中其中一种物质的含量或浓度。
其原理简单,操作方便,准确度高,广泛应用于实际分析和实验室研究中。







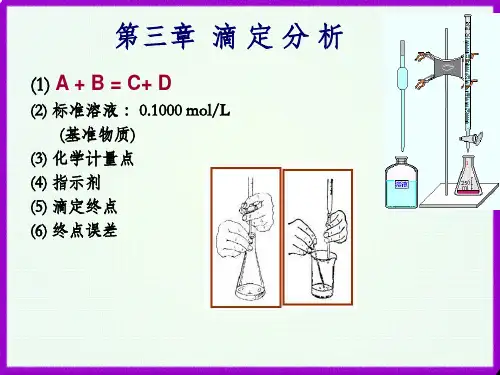
滴定分析原理
滴定分析是一种化学分析方法,用于确定溶液中某种物质的含量。
其原理是利用化学反应的定量关系,通过加入一种已知浓度的试剂溶液(称为滴定试剂)与待测溶液进行反应,确定反应终点的时刻,从而推算出待测溶液中所含物质的浓度。
滴定分析基于滴定方程,滴定方程是描述反应物质之间定量关系的数学表达式。
通过实验,确定滴定方程中的反应物物质的化学计量比,可以定量计算待测溶液中所含物质的浓度。
滴定分析通常需借助指示剂来帮助确定反应终点,指示剂是一种受酸碱条件影响而改变颜色的物质。
当反应接近终点时,滴定试剂的添加会导致溶液颜色发生明显变化,此时滴定停止。
根据滴定试剂的用量,结合滴定方程,可以计算出待测溶液中所含物质的浓度。
滴定分析的精确度受滴定试剂和指示剂的选择、反应条件(如温度、pH值等)以及实验操作的精细程度等因素影响。
为了提高滴定分析的准确性,通常需要进行标定实验,即利用已知浓度的标准溶液进行滴定,得到标定曲线或修正因子,以消除实验误差。
总的来说,滴定分析是一种重要的定量化学分析方法,广泛应用于各个领域,如环境监测、食品检测、药物分析等。
通过合理选取试剂、指示剂和仪器设备,准确操作滴定分析实验,可以高效地确定溶液中某种物质的浓度,为科学研究和工业生产提供有力支持。
分析化学——滴定分析1
分析化学——滴定分析1
滴定分析是一种常用的定量分析方法,广泛应用于分析化学领域。
其中,酸碱滴定法是滴定分析中的一种常见方法,用于测定溶液中酸碱度的
浓度。
酸碱滴定法的基本原理是,在滴定过程中,通过加入一溶液中碱(酸)
溶液的滴加,来使酸碱反应完全进行,从而确定酸碱溶液的浓度。
这一过
程中,通常需要使用作为指示剂的物质,其颜色会与溶液的酸碱度有关,
以判定滴定终点。
滴定分析中,常见的酸碱指示剂有酚酞、溴酚蓝、溴甲蓝等,它们的
酸碱变色范围与所滴定的溶液的酸碱度变化范围对应。
例如,酚酞是一种
经典的指示剂,它在酸性溶液中呈现红色,在碱性溶液中呈现黄色。
因此,当滴定溶液的酸度逐渐减小,接近中性的时候,加入的酚酞指示剂会由红
色转变为黄色,这就表明滴定终点已经达到,即反应完全进行。
在进行酸碱滴定分析时,实验中通常需要采取以下步骤:
1.准备滴定溶液:确定所需测定酸碱度的溶液体积和滴定液体积比例,准备好待测溶液和滴定液。
2.取定量的待测溶液进入烧杯中,添加适量的酸碱指示剂。
3.使用滴定管将滴定液加入待测溶液中,一滴一滴地滴加,同时轻轻
摇动烧杯,以促使反应充分进行。
4.当颜色变化接近滴定终点的指示剂要求时,减缓滴定速度,进行逐
滴滴定。
5.当颜色变化到达滴定终点时,滴定停止,记录滴加的滴定液体积。
6.重复实验,取平均值,计算溶液的酸碱浓度。
酸碱滴定法的关键在于确定滴定终点。
滴定终点的判断可以通过观察
颜色变化、定性判断,或者使用仪器来测定。
例如,可以使用电位计来测
定酸碱溶液的电位变化,从而确定滴定终点。
需要注意的是,在酸碱滴定分析中,滴定过程必须进行充分,并且滴
定液的浓度和体积要仔细计算,以确保结果的准确性。
此外,选择合适的
酸碱指示剂也是非常重要的,它应与所测定的溶液酸碱度变化范围相匹配。
总之,酸碱滴定法是一种常用的分析化学方法,用于测定溶液中的酸
碱度浓度。
在实验中,需要准确控制滴定液的加入量和速度,确定滴定终点,并选择适合的酸碱指示剂,以保证结果的准确性。