分析化学四大滴定总结
- 格式:pdf
- 大小:134.24 KB
- 文档页数:2

分析化学四大滴定总结
定性分析化学中的四大滴定,也就是碱度滴定、水的氢离子滴定、质
量滴定(定量滴定)和酸度滴定,是实验室中最基本的定性分析化学方法,用于化学分析当中不同物质的含量测定和种类鉴定。
一、碱度滴定
碱度滴定是指测定溶液的碱离子的含量,即溶液中氢离子浓度的定量
测定,是通过酸度滴定时,将酸离子与碱离子结合,反应形成盐类,消耗酸,使pH值变化,从而测定溶液中碱离子的含量的一种化学滴定方法。
碱度滴定根据反应物是否有色不同,可分为标准的无色滴定和常用的有色
滴定两种类型。
碱度滴定通常用于分析碱性物质的含量,例如碱的溶液,
如NaOH溶液、KOH溶液等。
二、水的氢离子滴定
水的氢离子滴定(也称氢离子滴定)是在水样中测定溶液中氢离子的
含量的一种滴定,是一种实验室中常用的化学分析滴定方法。
水的氢离子
滴定是通过测定溶液中氢离子的浓度来评价溶液的碱度的,它是以硫酸铜
为滴定剂,采用titration程序,以滴定曲线的路径从而测定水质当中氢
离子含量的一种滴定方法。
三、质量滴定
质量滴定,也称定量滴定,是指以一定的量的容量或重量的质量,测
定溶液中其中一种物质的含量的一种化学分析滴定方法。


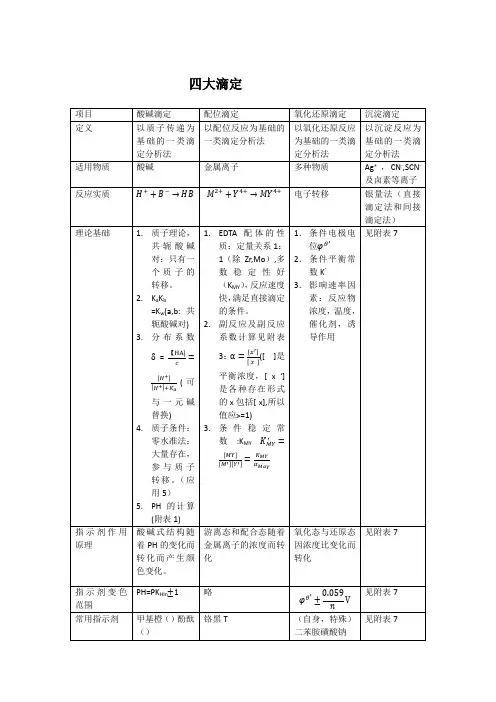
分析化学四大滴定总结一、酸碱滴定原理酸碱滴定法是以酸、碱之间质子传递反应为基础的一种滴定分析法。
基本反应H++ OH- = H2O滴定曲线与直接滴定的条件强碱滴定强酸强碱滴定弱酸强酸滴定弱碱cK a≥10-8cK b≥10-8多元酸的滴定混合酸的滴定多元碱的滴定c o K a1≥10-9c o K b1≥10-9K b1/K b2>104液基准物质无水碳酸钠、硼酸邻苯二甲酸氢钾、苯甲酸应用硼酸的测定、铵盐的测定、克氏定发、酸酐和醇类的测定等酸碱溶液pH计算一元弱酸两性物质二元弱酸缓冲物质理定分析方法。
基本反应M+Y=MY配合物的稳定常数酸效应αY(H)干扰离子效应αY(N)溶液酸度越大,αY(H)越大,表示酸效应引起的副反应越严重。
αY(H)=1+β1[H+] +β2[H+] ²+β3[H+] ³+β4[H+]⁴+βⁿ [H+] ⁿ[Y]越小,αY(N)越大,表示干扰离子效应引起的副反应越严重。
金属离子的配位效应αM(OH)、αM(L)及总副反应αMY的总副反应αY条件稳定常数K’MYαM越小,αY越小,K’MY越小,配合物稳定性越大滴定条件准确直接滴定的条件K’MY≥10-6分别滴定的条件K’MY≥10-6,△lgK≥5配位剂1.无机配位剂 2.有机配位剂:EDTA、CyDTA、EGTA、EDTP等指示剂铬黑T、二甲酚橙、钙指示剂、PAN等指示剂原理指示剂游离态与配合态颜色不同影响滴定突跃范围因素1.金属离子浓度的影响:K’MY一定时,CM越大,ΔpM’越大2.条件稳定常数的影响:CM一定时,K’MY越大,ΔpM’越大3.酸度的影响:pH越小,αY(H)越大,K’MY越小,ΔpM’越小4.其他辅助配位剂的影响:CL越大,αM(L)越大,K’MY越小,ΔpM’越小用掩蔽和解蔽的方法进行滴定常用掩蔽方法配位掩蔽法沉淀掩蔽法氧化还原隐蔽法解蔽法应用测定石灰石中CaO、测定Ga2+、Mg2+Bi3+、Zr4+、Th4+的滴定测定Cu2+、Zn2+、条件电极电位条件对电极电位的影响离子强度副反应酸度一般忽略离子强度的影响,一般用浓度代替活度酸度变化直接影响电对的电极电位条件平衡常数滴定反应条件影响反应速率的因素1.反应物浓度2.温度3.催化剂4.诱导作用滴定化学计量点前化学计量点时化学计量点后曲线与终点的测定指示剂氧化还原指示剂、自身指示剂、专属指示剂预处理预氧化、预还原,除去有机物:干法灰化。

四大滴定比较与总结滴定是化学分析常用的一种分析方法,主要用于测定溶液中其中一种物质的含量。
四大滴定是指电位滴定、自动滴定、嗅觉滴定和颜色滴定。
这四种滴定方法各有特点,下面将对它们进行比较与总结。
1.电位滴定电位滴定是通过测定电位的变化来判断滴定终点的方法。
它的优点是滴定速度快、灵敏度高,可以实现自动控制。
电位滴定需要使用较贵的电位计仪器,因此成本较高。
2.自动滴定自动滴定是指通过电动滴定器进行滴定操作,滴定剂的滴定过程由机器自动完成。
自动滴定优点是操作简便、准确度高,可以提高实验效率。
然而,需要注意的是机器操作所需的技术支持较高,且设备价格相对较高。
3.嗅觉滴定嗅觉滴定是通过嗅觉来判断滴定终点的方法。
这种方法不需要任何仪器设备,简便易行。
嗅觉滴定的缺点是主观性较强,准确度较低,且对于不同人来说灵敏度差异较大。
4.颜色滴定颜色滴定是通过颜色的变化来判断滴定终点的方法。
它的优点是操作简便,可观察到直观的颜色变化,使滴定过程更为直观。
而且,现有的颜色滴定剂相对较多,可根据不同的滴定物质选择合适的颜色指示剂。
然而,颜色滴定对于滴定终点的判断常常不够准确,需要较丰富的经验和实践。
综上所述,四大滴定方法各有优缺点。
电位滴定能够实现自动化、快速高灵敏度的滴定分析,但所需设备价格较高。
自动滴定操作简单准确,但设备价格相对较高且需要技术支持。
嗅觉滴定方法简单易行,但主观性较高,准确度较低。
颜色滴定直观易懂,但滴定终点判断较为主观,需要经验和实践。
在实际应用中,选择滴定方法要根据具体的实验需求和条件来确定。
对于要求快速高灵敏度的滴定分析,电位滴定是更合适的选择。
对于操作简便准确度要求较高的滴定,可以考虑自动滴定方法。
对于便捷性要求较高且不需要太高准确度的滴定分析,可以使用嗅觉滴定法。
而颜色滴定方法则适用于对经验要求较高、对实验结果准确度不要求过高的分析。

四大滴定总结分析化学中的四大滴定即:酸碱滴定,氧化还原滴定,配位滴定,沉淀滴定。
一酸碱滴定1原理酸碱滴定法是以酸、碱之间质子传递反应为基础的一种滴定分析法。
基本反应为H+ + OH- = H2O也称中和法,是一种利用酸碱反应进行容量分析的方法用酸作滴定剂可以测定碱,用碱作滴定剂可以测定酸,这是一种用途极为广泛的分析方法。
[2]2滴定曲线强碱滴定弱酸滴定反应为:以NaOH液(0.1000moL/L滴定20.00ml醋酸(HAc,0.1000mol/L)用NaOH滴定HOAc的滴定曲线为例,滴定曲线如下图:滴定开始前 pH=2.88滴入NaOH 液19.98ml时 pH=7.75化学计量点时 pH=8.73滴入NaOH液20.02ml时 pH=9.70指示剂的选择(1)只能选择碱性指示剂(酚酞或百里酚酞等),不能选用酸性范围内变色的指示剂(如甲基橙、甲基红等)。
因为突跃范围较小,pH值在7.75~9.70之间;计量点在碱性区。
(2)弱酸被准确滴定的判决是C·Ka>10-8。
因为Ka愈大,突跃范围愈大。
而Ka<10-8时,已没有明显突跃,无法用指示剂来确定终点;另外,酸的浓度愈大,突跃范围也愈大。
3酸碱指示剂用于酸碱滴定的指示剂,称为酸碱指示剂。
是一类结构较复杂的有机弱酸或有机弱碱,它们在溶液中能部分电离成指示剂的离子和氢离子(或氢氧根离子),并且由于结构上的变化,它们的分子和离子具有不同的颜色,因而在pH不同的溶液中呈现不同的颜色。
常用类型指示剂名称范围酸色中性色碱色甲基橙 3.1-4.4 红橙黄甲基红4.4-6.2 红橙黄溴百里酚蓝 6.0-7.6 黄绿蓝酚酞 8.2-10.0 无色浅红红紫色石蕊 5.0-8.0 红紫蓝4影响滴定结果的因素⑴读数:滴定前俯视或滴定后仰视(偏大)滴定前仰视或滴定后俯视(偏小)⑵未用标准液润洗滴定管(偏大);未用待测溶液润洗滴定管(偏小)⑶用待测液润洗锥形瓶(偏大)⑷滴定前标准液滴定管尖嘴有气泡,滴定后尖嘴气泡消失(偏大)⑸不小心将标准液滴在锥形瓶的外面(偏大)⑹指示剂(可当作弱酸)用量过多(偏小)⑺滴定过程中,锥形瓶振荡太剧烈,有少量液滴溅出(偏小)⑻开始时标准液在滴定管刻度线以上,未予调整(偏小)⑼碱式滴定管(量待测液用)或移液管内用蒸馏水洗净后直接注入待测液(偏小)⑽移液管吸取待测液后,悬空放入锥形瓶,少量待测液洒在外面(偏小)⑾滴定到指示剂颜色刚变化,就是到了滴定终点(偏小)⑿锥形瓶用蒸馏水冲洗后,不经干燥便直接盛待测溶液(无影响)⒀滴定接近终点时,有少量蒸馏水冲洗锥形瓶内壁(无影响)(14)滴定时待测液滴定管尖嘴有气泡,滴定后尖嘴气泡消失(偏小)二配位滴定2滴定曲线。
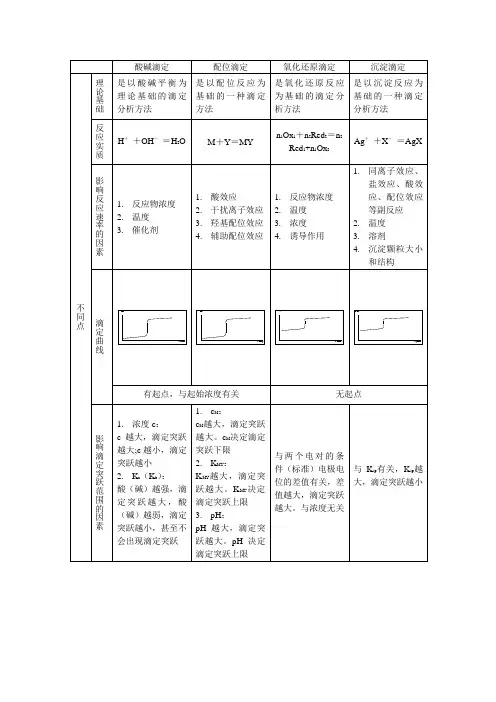

酸碱中和滴定一、酸碱中和滴定原理1.定义:用已知物质旳量浓度旳酸(或碱)来测定未知物质旳量浓度旳碱(或酸)旳试验措施。
2. 酸碱中和滴定原理(1)实质:H+ +OH-= H2O(2)原理:在中和反应中使用一种已知物质旳量浓度旳酸(或碱)溶液与未知物质旳量浓度旳碱(或酸)溶液完全中和,测出两者所用旳体积,根据化学方程式中酸碱物质旳量比求出未知溶液旳物质旳量浓度。
(3)关键:①精确测定两种反应物旳溶液体积;②保证原则液、待测液浓度旳精确;③滴定终点旳精确鉴定(包括指示剂旳合理选用)(4)酸、碱指示剂旳选择二、中和滴定所用仪器酸式滴定管、碱式滴定管、锥形瓶、铁架台、滴定管夹、烧杯等三、试剂:原则液、待测液、指示剂;指示剂旳作用:①原则液:已知精确物质旳量浓度旳酸或碱溶液;②待测液:未知物质旳量浓度旳酸或碱溶液①酸式滴定管用于盛装酸性、中性或强氧化性溶液,不能盛装碱性溶液或者氢氟酸(它们易腐蚀玻璃)。
②碱式滴定管用于盛装碱性溶液,不能盛装酸性和强氧化性溶液(它们易腐蚀橡胶)。
③通过指示剂旳颜色变化来确定滴定终点。
④指示剂旳选择:变色要敏捷、明显,一般强酸滴定强碱用甲基橙,强碱滴定强酸用酚酞。
四、中和滴定旳操作(以原则盐酸滴定NaOH 为例)Ⅰ、准备:(1)滴定管:————精确到小数点后两位如:24.00mL 、23.38mL①检查酸式滴定管与否漏水②洗涤滴定管后要用原则液洗涤2~3次,并排除管尖嘴处旳气泡③注入原则液至“0”刻度上方2~3cm 处④将液面调整到“0”刻度(或“0”刻度如下某一刻度)(2)锥形瓶:只用蒸馏水洗涤,不能用待测液润洗Ⅱ、滴定:(4)滴定滴定管夹在夹子上,保持垂直右手持锥形瓶颈部,向同一方向作圆周运动而不是前后振动左手控制活塞(或玻璃球),注意不要把活塞顶出Ⅲ、计算:每个样品滴定2~3次,取平均值求出成果。
Ⅳ、注意点:①滴速:滴加速度先快后慢,背面可半滴,当靠近终点时,应一滴一摇同步眼睛注视锥形瓶内溶液颜色变化. 直至溶液颜色变化,且30S 内颜色不复原,此时再读数。

分析化学四大滴定总结1. 介绍滴定是化学分析中常用的一种定量分析方法,通过滴定液与待测物反应的化学反应达到定量的目的。
在分析化学中,有四种常用的滴定方法,分别是酸碱滴定、氧化还原滴定、络合滴定和沉淀滴定。
本文将对这四种滴定方法进行详细介绍和总结。
2. 酸碱滴定酸碱滴定是通过酸碱中和反应进行定量分析的方法。
常用的滴定指示剂包括酚酞、甲基橙等。
在酸碱滴定中,滴定液通常是一种浓度已知的酸或碱溶液,待测物为酸或碱溶液。
滴定过程中,通过观察指示剂的颜色变化来判断滴定终点。
酸碱滴定的一般步骤如下:1.准备滴定液和待测物溶液。
2.取一定数量的待测物溶液放入滴定瓶中。
3.准备滴定管和取靶。
4.滴定管中加入一定量的滴定液。
5.滴定管中的滴定液滴入待测物溶液中,同时搅拌。
6.当颜色变化出现,滴定终点达到。
7.记录加入的滴定液的体积。
3. 氧化还原滴定氧化还原滴定是通过氧化还原反应进行定量分析的方法。
在氧化还原滴定中,常用的滴定指示剂有二茂铁和碘化钾淀粉溶液。
滴定液和待测物之间的氧化还原反应可以通过观察指示剂的颜色变化来判断滴定终点。
氧化还原滴定的一般步骤如下:1.准备滴定液和待测物溶液。
2.取一定数量的待测物溶液放入滴定瓶中。
3.准备滴定管和取靶。
4.滴定管中加入一定量的滴定液。
5.滴定管中的滴定液滴入待测物溶液中,同时搅拌。
6.当颜色变化出现,滴定终点达到。
7.记录加入的滴定液的体积。
4. 络合滴定络合滴定是通过络合反应进行定量分析的方法。
常用的滴定指示剂有硫氰酸铁、二甲基黄等。
滴定液和待测物之间的络合反应可以通过观察指示剂的颜色变化来判断滴定终点。
络合滴定的一般步骤如下:1.准备滴定液和待测物溶液。
2.取一定数量的待测物溶液放入滴定瓶中。
3.准备滴定管和取靶。
4.滴定管中加入一定量的滴定液。
5.滴定管中的滴定液滴入待测物溶液中,同时搅拌。
6.当颜色变化出现,滴定终点达到。
7.记录加入的滴定液的体积。
5. 沉淀滴定沉淀滴定是通过生成沉淀反应进行定量分析的方法。

分析化学四大滴定总结分析化学是研究物质成分和性质的科学,其中滴定是常用的定量分析方法之一、在滴定中,有四种常用的滴定方法被称为“四大滴定”,分别是酸碱滴定、氧化还原滴定、络合滴定和沉淀滴定。
下面将对这四种滴定方法进行详细的介绍和分析。
1.酸碱滴定:酸碱滴定是根据物质的酸碱性质进行滴定的一种方法。
它通过在酸性或碱性介质中,用一种酸或碱溶液滴定另一种碱或酸溶液,以酸碱中和点的发生来确定物质的浓度。
酸碱滴定方法简单、准确,广泛应用于环境监测、药物分析、食品检测等领域。
2.氧化还原滴定:氧化还原滴定是通过氧化还原反应进行滴定的一种方法。
在这种滴定中,被滴定溶液中的氧化还原体与滴定试剂发生氧化还原反应,反应发生到等量点时,可通过指示剂显示出等量点的位置。
氧化还原滴定广泛应用于药物分析、环境监测等领域。
3.络合滴定:络合滴定是通过金属离子与配体之间的化学反应进行滴定的一种方法。
金属离子与配体结合形成络合物,滴定试剂添加之后会与嘌呤等指示剂形成分子或离子配合物,通过颜色的改变来确定等量点。
络合滴定方法用于测定金属离子或配体的浓度,广泛应用于环境监测、地质矿产等领域。
4.沉淀滴定:沉淀滴定是通过沉淀反应进行滴定的一种方法。
在滴定过程中,滴定试剂与被滴定物质反应生成沉淀,滴定至产生等量沉淀时,滴定终点出现。
沉淀滴定可用于测定硬度、氯离子、硫酸根离子等物质的浓度,常用于水质检测、环境检测等领域。
四大滴定方法各有其特点和应用范围。
酸碱滴定适用于测定酸碱度、酸度和碱度;氧化还原滴定适用于测定氧化还原体、氧化还原电位等;络合滴定适用于测定金属离子或配体的浓度;沉淀滴定适用于测定沉淀物的浓度等。
这些滴定方法在分析化学中起着重要的作用,为定量分析提供了可靠的手段。
总结起来,四大滴定是分析化学中常用的滴定方法。
酸碱滴定、氧化还原滴定、络合滴定和沉淀滴定分别通过酸碱性质、氧化还原性质、络合反应和沉淀反应进行滴定,它们分别用于测定各种物质的浓度和性质。

四大滴定总结四大滴定方法的比较酸碱中和滴定是一种基于酸碱质子传递反应的分析方法,反应方程式为酸+碱=盐+水。
配位滴定是一种基于络合反应(形成配合物)的分析方法,反应方程式为M+Y=MY。
氧化还原滴定是一种基于氧化还原反应的分析方法,反应方程式为Ox+ne=Red。
沉淀滴定是一种利用沉淀反应进行容量分析的方法,反应方程式为Ag+X=AgX+﹣。
对于多元弱酸的滴定,条件稳定常数K’MY≥10-8,两点对的电位差大于0.4V并且反应的进行程度达99.9%时,选择性好。
影响滴定分析的因素包括浓度、Ka、条件稳定常数、pH、反应物浓度、温度、催化剂、酸度和共存离子指示剂。
指示剂的选择应考虑变色点、变色范围和变色原理。
常用指示剂包括甲基橙、酚酞、甲基红、铬黑T、二甲酚橙、磺基水杨酸和PAN等。
不同的指示剂指示终点的方法不同,常用的滴定方法有莫尔法、佛尔哈德法和法扬司法。
在滴定分析中,常用的计算方法包括计算pH值、条件稳定常数、电极电势、浓度积和样品中物质所占含量等。
氮的测定常用的方法包括蒸馏法、定氮和甲醛法。
混合碱的测定常用的方法包括双指示剂法和氯化钡法。
本文将介绍几种常见的化学分析方法,包括锌、钙、镁、高锰酸钾法、碘量法、重铬酸钾法、溴酸钾法、岩盐中可溶性氯离子的测定、银的测定以及混合离子的测定。
锌是一种重要的金属元素,其测定方法主要包括原子吸收光谱法、电感耦合等离子体发射光谱法和荧光光谱法等。
其中,原子吸收光谱法是一种常用的方法,通过反应定量进行测定,具有反应速度快、化学计量关系明确等优点。
钙和镁是人体所需的重要元素,其测定方法主要包括滴定法、分光光度法和原子吸收光谱法等。
其中,滴定法是一种简便易行的方法,适用于样品量较小的情况。
高锰酸钾法是一种常用的氧化剂,可用于有机物的氧化反应。
其测定方法主要是通过滴定法进行,反应速度快,且具有较高的准确度。
碘量法是一种常用的测定物质中碘含量的方法,其原理是通过氧化还原反应将碘转化为离子态,然后用滴定法进行测定。
分析化学四大滴定总结分析化学四大滴定总结滴定分析法又称为容量分析法,是一种简便、快速和应用广泛的定量分析方法,在常量分析中有较高的准确度。
这其中又有重要的四大滴定方法。
以下是店铺整理的分析化学四大滴定总结,欢迎查看。
一、酸碱滴定原理:利用酸和碱在水中以质子转移反应为基础的滴定分析方法。
可用于测定酸、碱和两性物质。
其基本反应为H﹢+OH﹣=H2O也称中和法,是一种利用酸碱反应进行容量分析的方法。
用酸作滴定剂可以测定碱,用碱作滴定剂可以测定酸,这是一种用途极为广泛的分析方法。
最常用的酸标准溶液是盐酸,有时也用硝酸和硫酸。
标定它们的基准物质是碳酸钠Na2CO3。
方法简介:最常用的碱标准溶液是氢氧化钠,有时也用氢氧化钾或氢氧化钡,标定它们的基准物质是邻苯二甲酸氢钾KHC8H4O6或草酸H2C2O·2H2O:OH+HC8H4O6ˉ→C8H4O6ˉ+H2O如果酸、碱不太弱,就可以在水溶液中用酸、碱标准溶液滴定。
离解常数 A和Kb是酸和碱的强度标志。
当酸或碱的浓度为0.1M,而且A或Kb大于10-7时,就可以准确地滴定,一般可准确至0.2%。
多元酸或多元碱是分步离解的,如果相邻的离解常数相差较大,即大于104,就可以进行分步滴定,这种情况下准精确度不高,误差约为1%。
盐酸滴定碳酸钠分两步进行:﹢ˉCO32-+H→HCO3HCO3ˉ+H﹢→CO2↑+H2O相应的滴定曲线上有两个等当点,因此可用盐酸来测定混合物中碳酸钠和碳酸氢钠的含量,先以酚酞(最好用甲酚红-百里酚蓝混合指示剂)为指示剂,用盐酸滴定碳酸钠至碳酸氢钠,再加入甲基橙指示剂,继续用盐酸滴定碳酸氢钠为二氧化碳,由前后消耗的盐酸的体积差可计算出碳酸氢钠的含量。
某些有机酸或有机碱太弱,或者它们在水中的溶解度小,因而无法确定终点时,可选择有机溶剂为介质,情况就大为改善。
这就是在非水介质中进行的酸碱滴定。
有的非酸或非碱物质经过适当处理可以转化为酸或碱。
酸碱中和滴定一、 酸碱中和滴定原理1•定义:用已知物质的量浓度的酸(或碱)来测定未知物质的量浓度的碱(或酸)的实验方 法。
2. 酸碱中和滴定原理(1) 实质:H ++0H 一 = H 2O(2) 原理:在中和反应中使用一种已知物质的量浓度的酸(或碱)溶液与未知物质的量浓 度的碱(或酸)溶液完全中和,测出二者所用的体积,根据化学方程式中酸碱物质的量比求 出未知溶液的物质的量浓度。
(3) 关键:① 准确测定两种反应物的溶液体积; ② 确保标准液、待测液浓度的准确;③ 滴定终点的准确判定(包括指示剂的合理选用)(4 )酸、碱指示剂的选择 二、 中和滴定所用仪器酸式滴定管、碱式滴定管、锥形瓶、铁架台、滴定管夹、烧杯等三、 试剂:标准液、待测液、指示剂;指示剂的作用: ① 标准液:已知准确物质的量浓度的酸或碱溶液; ② 待测液:未知物质的量浓度的酸或碱溶液 ③ 通过指示剂的颜色变化来确定滴定终点。
④ 指示剂的选择:变色要灵敏、明显,一般强酸滴定强碱用甲基橙, 强碱滴定强酸用酚酞。
四、 中和滴定的操作(以标准盐酸滴定NaOH 为例)I 、准备:(1 )滴定管: ----- 精确到小数点后两位如: 24.00mL 、23.38mL① 检验酸式滴定管是否漏水② 洗涤滴定管后要用标准液洗涤 2~3次,并排除管尖嘴处的气泡 ③ 注入标准液至 “0刻度上方2~3cm 处① 酸式滴定管用于盛装酸性、 中性或强氧化性溶液,不能盛装碱 性溶液或者氢氟酸(它们易腐蚀玻 璃)。
② 碱式滴定管用于盛装碱性 溶液,不能盛装酸性和强氧化性溶 液(它们易腐蚀橡胶)④ 将液面调节到 “0刻度(或“ 0刻度以下某一刻度) (2)锥形瓶:只用蒸馏水洗涤,不能用待测液润洗n 、滴定:(4)滴定滴定管夹在夹子上,保持垂直右手持锥形瓶颈部,向同一方向作圆周运动而不是前后振动 左手控制活塞(或玻璃球),注意不要把活塞顶出 川、计算:每个样品滴定 2~3次,取平均值求出结果。
一、酸碱滴定
原
理
酸碱滴定法是以酸、碱之间质子传递反应为基础的一种滴定分析法。
基
本
反
应
H++ OH- = H2O
滴定曲线与直接滴定的条件
强碱滴定强酸强碱滴定弱酸强酸滴定弱碱
cK a≥10-8
cK b≥10-8多元酸的滴定混合酸的滴定多元碱的滴定
c o K a1≥10-9
K a1/K a2>104
两种弱酸混合:
c o K b1≥10-9
K b1/K b2>104
C HA K HA≥10-9
c HA K HA/c HB K HB>104
指
示
剂
酚酞、甲基橙酚酞、百里酚蓝甲基红、溴甲酚绿
指
示
剂
原
理
指示剂在不同pH下颜色不同
影响滴定突跃范围因素1.Ka:Ka越小,滴定突跃范围越小,甚至不会出现滴定突跃,Ka影响的是滴定曲线的前半部分
2.滴定剂浓度:浓度越小,滴定突跃范围范围越小
标准溶液酸标准溶液碱标准溶液HCl NaOH
基
准
物
质
无水碳酸钠、硼酸邻苯二甲酸氢钾、苯甲酸应硼酸的测定、铵盐的测定、克氏定发、酸酐和醇类的测定等。