酸碱盐的鉴别
- 格式:ppt
- 大小:2.14 MB
- 文档页数:22

酸碱盐怎么区分有哪些通性碱盐区分方法:1、看电离:电离时生成的阳离子全部是氢离子的就是酸,电离时生成的阴离子全部是氢氧根离子的就是碱,由金属离子或铵根离子与酸根离子形成的就是盐。
2、看化学式:一般酸的左边都只有一个元素H,右边是一个非金属原子或者一个原子团,如HCl,其左边是H,右边是非金属原子Cl,又如H2SO4、HNO3、H3PO4等。
酸碱盐怎么区分碱盐区分方法:1、看电离电离时生成的阳离子全部是氢离子的就是酸,电离时生成的阴离子全部是氢氧根离子的就是碱,由金属离子或铵根离子与酸根离子形成的就是盐。
2、看化学式一般酸的左边都只有一个元素H,右边是一个非金属原子或者一个原子团,如HCl,其左边是H,右边是非金属原子Cl,又如H2SO4、HNO3、H3PO4等。
碱左边是一个金属原子,右边是原子团OH,比如NaOH、Mg(OH)2、Fe(OH)3等。
盐左边是一个金属原子,右边是一个非金属原子或者一个原子团,其实可以看为酸的右边和碱的左边所组成,比如NaCl、Na2SO4、Na3PO4等。
酸碱盐的通性酸的通性:酸+酸碱指示剂酸+金属——盐+氢气酸+金属氧化物——盐+水酸+碱——盐+水酸+盐——新酸+新盐碱的通性:碱+酸碱指示剂碱+非金属氧化物碱+酸——盐+水碱+盐——新碱+新盐盐没有通性。
酸碱盐溶解性口诀酸类多数都易溶,硅酸微溶是独种。
碱类钾钠钡铵溶,钙是微溶余不溶。
硫酸铅钡沉水中,微溶钙银与亚汞。
盐类溶有钾钠铵,外加易溶硝酸盐。
碳酸能溶钾钠铵,其余俱沉水中间。
盐酸沉淀银亚汞,还有微溶氯化铅。


酸、碱、盐的鉴别(一)
班级:实验小组:姓名:
实验要求:学会用简单的方法来鉴别一些常见的酸碱盐物质。
实验用品:试管(15*150)6个,试管架,试管刷,标签纸。
废液缸,湿抹布。
量筒(10ml),pH试纸,吸水纸,玻璃片(或表面皿),玻璃棒、滴管(放在250ml的烧杯中) ,石蕊试液,酚酞试液,饱和碳酸钠溶液,硫酸铜溶液。
1:4稀盐酸、0.5M NaOH溶液、食盐溶液随机编号A、B、C(均盛放在细口瓶中)
酸、碱、盐的鉴别(一)
班级:实验小组:姓名:
实验要求:学会用简单的方法来鉴别一些常见的酸碱盐物质。
实验用品:试管(15*150)6个,试管架,试管刷,标签纸。
废液缸,湿抹布。
量筒(10ml),pH试纸,吸水纸,玻璃片(或表面皿),玻璃棒、滴管(放在250ml的烧杯中) ,石蕊试液,酚酞试液,饱和碳酸钠溶液,硫酸铜溶液。
1:4稀盐酸、0.5M NaOH溶液、食盐溶液随机编号A、B、C(均盛放在细口瓶中)。


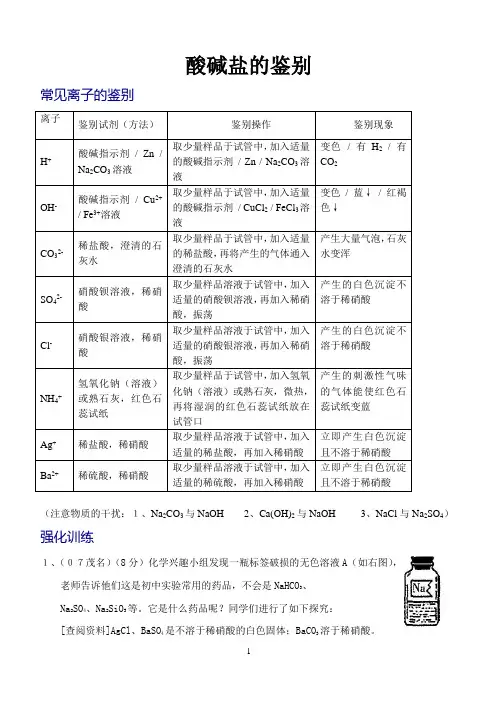
酸碱盐的鉴别常见离子的鉴别离子鉴别试剂(方法)鉴别操作鉴别现象H+酸碱指示剂/ Zn /Na2CO3溶液取少量样品于试管中,加入适量的酸碱指示剂/ Zn / Na2CO3溶液变色/ 有H2/ 有CO2OH-酸碱指示剂/ Cu2+/ Fe3+溶液取少量样品于试管中,加入适量的酸碱指示剂/ CuCl2 / FeCl3溶液变色/ 蓝↓/ 红褐色↓CO32-稀盐酸,澄清的石灰水取少量样品于试管中,加入适量的稀盐酸,再将产生的气体通入澄清的石灰水产生大量气泡,石灰水变浑SO42-硝酸钡溶液,稀硝酸取少量样品溶液于试管中,加入适量的硝酸钡溶液,再加入稀硝酸,振荡产生的白色沉淀不溶于稀硝酸Cl-硝酸银溶液,稀硝酸取少量样品溶液于试管中,加入适量的硝酸银溶液,再加入稀硝酸,振荡产生的白色沉淀不溶于稀硝酸NH4+氢氧化钠(溶液)或熟石灰,红色石蕊试纸取少量样品于试管中,加入氢氧化钠(溶液)或熟石灰,微热,再将湿润的红色石蕊试纸放在试管口产生的刺激性气味的气体能使红色石蕊试纸变蓝Ag+稀盐酸,稀硝酸取少量样品溶液于试管中,加入适量的稀盐酸,再加入稀硝酸立即产生白色沉淀且不溶于稀硝酸Ba2+稀硫酸,稀硝酸取少量样品溶液于试管中,加入适量的稀硫酸,再加入稀硝酸立即产生白色沉淀且不溶于稀硝酸(注意物质的干扰:1、Na2CO3与NaOH2、Ca(OH)2与NaOH 3、NaCl与Na2SO4)强化训练1、(07茂名)(8分)化学兴趣小组发现一瓶标签破损的无色溶液A(如右图),老师告诉他们这是初中实验常用的药品,不会是NaHCO3、Na2SO4、Na2SiO3等。
它是什么药品呢?同学们进行了如下探究:[查阅资料]AgCl、BaSO4是不溶于稀硝酸的白色固体;BaCO3溶于稀硝酸。
(1)小明:我猜想A是__________溶液。
(填化学式)[实验验证]取A溶液放入试管中,滴加硝酸银和硝酸的混合液。
若有白色沉淀生成,则猜想正确。


酸碱盐怎么区分酸碱盐区分口诀:阳离子只有H+的,全是酸。
阴离子只有OH-的,全是碱。
盐,除了酸碱,再除去有机物(像甲烷,乙烯,乙炔,苯,甲苯,乙醛等)的化合物就全是盐。
酸的定义:化学上是指在水溶液中电离时产生的阳离子都是是氢离子的化合物。
碱指在水溶液中电离出的阴离子全部都是OH-的物质;在酸碱质子理论中碱指能够接受质子的物质;在酸碱电子理论中,碱指电子给予体。
盐是指一类金属离子或铵根离子(NH4+)与酸根离子或非金属离子结合的化合物。
酸、碱、盐的溶解性是判断复分解反应能否发生的一个重要依据,酸碱盐溶解度记忆口诀:钾钠铵盐硝酸盐,全部都属可溶盐。
硫酸盐不溶钡和铅;酸易溶,碱难溶。
氯化物不溶银亚汞,碳酸盐,多不溶。
酸碱盐有哪些化学性质1、酸的化学性质酸溶液能跟酸碱指示剂起反应,紫色石蕊试液遇酸变红,无色酚酞试液遇酸不变色。
显色的物质是指示剂;酸能跟多种活泼金属起反应,通常生成盐和氢气。
只有位于金属活动性顺序表中氢前面的金属才能与稀酸反应,产生氢气。
位于氢后的金属不能与稀酸反应,但能与浓硫酸和浓硝酸反应;酸能跟碱性氧化物反应,生成盐和水;酸能跟一些盐反应,生成新酸和新盐;酸跟碱起中和反应,生成盐和水。
2、碱的化学性质与酸发生中和反应;碱可以和一些非金属氧化物反应;使紫色石蕊变蓝;使无色酚酞变红;碱可以和一些盐反应,生成新盐和新碱等。
3、盐的化学性质在金属活动性顺序里,只有排在前面的金属,才能把排在后面的金属从它们的盐溶液里置换出来;盐跟一些金属起反应,一般能生成另一种盐和另一种金属;盐跟酸起反应,一般生成另一种盐和另一种酸;盐跟碱起反应,一般生成另一种盐和另一种碱;盐和盐的反应,两种盐起反应一般生成另外两种盐。



快速判别酸碱盐的方法:酸:第一个字母为H,不是水和双氧水就是酸碱:最后两个字母是OH盐:其他的为盐指出下列物质中那些是酸?那些是碱?那些是盐?NaHCO3KOH HNO3K2CO3NaNO3H2CO3Mg(OH)2从这个故事里,结合书本,你对食盐的作用了解了多少?1 重要的调味品2 人体正常生理不可缺少的物质3 日常生活中用来腌制食品4 工业的原料:氯---碱工业粗盐提纯的步骤:1称量(左物右码)2溶解3过滤:过滤的要点(一贴二低三靠)4蒸发:(是否需要把水全部蒸干再熄灭酒精灯?)5称量6计算产率在溶解过滤蒸发中都用到了玻璃棒,它的作用分别是什么?溶解:搅拌,加速固体的溶解过滤:引流蒸发:防止液体受热不均匀,液滴飞溅碳酸钠(Na 2CO 3 ) 碳酸氢钠(NaHCO 3 ) 碳酸钙(CaCO 3) 碳酸钠(Na 2CO 3 ) 碳酸氢钠(NaHCO 3 ) 碳酸钙(CaCO 3) 用于生产玻璃、造纸、纺织、洗涤剂碳酸钠 主 要 用 途 名 称碳酸钙与盐酸反应CaCO3+2HCl=CaCl2+H2O+CO2↑请书写出碳酸钠、碳酸氢钠与盐酸反应的化学方程式Na2CO3+2HCl=2NaCl+H2O+CO2↑NaHCO3+HCl=NaCl+H2O+CO2↑组成里含有CO32-(或HCO3-)离子的盐,都能跟盐酸反应生成二氧化碳气体,利用此反应可以检验盐的组成中是否含有CO32-(或HCO3-)复分解反应:由两种化合物互相交换成分,生成另外两种化合物的反应CaCO3+2HCl=CaCl2+H2O+CO2↑KOH+HCl=KCl+H2ONa2CO3+Ca(OH)2=2NaOH+CaCO3复分解反应条件:基本反应类型比较: 反应物与生成物都是两种,且都是单质和化合物反应物只有一种而生成物有多种, 即“一变多” 反应物为多种而生成物只有一种,即“多变一” 特 征 AB + C →A+BC AB →A+B+…… A+B →AB 类 型 由一种单质与一种化合物反应,生成另一种单质与另一种化合物的反应 由一种物质生成两种或两种以上其它物质的反应 由两种或两种以上物质生成另一种物质的反应 定 义 置 换 反 应 分 解 反 应 化 合 反 应。
酸碱盐怎么区分
区分酸碱盐的方法口诀:阳离子全是H+的化合物是酸,阴离子全是OH-的化合物是碱,金属离子和酸根离子组成的化合物是盐。
酸:电离时生成的阳离子全部是氢离子(H+)的化合物叫做酸,或者溶于水并能释放质子形成H3O+(水合氢离子)的物质也是酸。
如盐酸、硫酸、碳酸、硝酸等。
酸的通性:酸溶液能与酸碱指示剂反应、酸+碱性氧化物=盐+水等。
碱:在水溶液中电离出的阴离子全部都是OH-的物质是碱。
如氢氧化锂、氢氧化钠、氢氧化铷、氢氧化铯、氢氧化钫等。
碱的通性:碱溶液能跟酸碱指示剂起反应,紫色石蕊试液遇碱变蓝,无色酚酞试液遇碱变红。
盐:金属离子或铵根离子(NH4+)与酸根离子或非金属离子结合的化合物是盐。
如氯化钠,硝酸钙,硫酸亚铁和乙酸铵硫酸钙,氯化铜,醋酸钠等。
盐的通性:有些盐有微弱的腐蚀性,溶液的酸碱度根据盐的性质判定,能与某些酸,碱,盐反应,还能和其他某些化合物反应。