2016高考化学二轮复习 专题13 钠、镁、铝及其化合物课件
- 格式:ppt
- 大小:1.20 MB
- 文档页数:10





2020届高考化学二轮复习专项测试专题十三考点二镁、铝及其化合物的性质(2)1、镁、铝能够在空气中稳定存在的原因是( )A.性质不活泼,不与空气中的成分反应B.镁、铝与氧气反应的速率极慢C.经过了特殊工艺处理D.与氧气反应在表面形成了氧化物保护膜2、将镁、铝、硅的混合物分为等质量的两份。
一份跟足量的NaOH溶液反应。
另一份跟足量H一样多。
则镁与硅物质的量之比为( )的盐酸反应,最终产生的2A.2:1 B.4:1 C.1:1 D.3:13、某兴趣小组在实验室用Al、稀H2SO4、NaOH溶液制备1摩尔Al(OH)3。
设计如下三种方案: 方案Ⅰ:向Al中加入NaOH溶液,至Al刚好完全溶解,得溶液①。
向溶液①中加硫酸至刚好沉淀完。
过滤、洗涤、干燥。
方案Ⅱ:向Al中加入硫酸,至Al刚好完全溶解,得溶液②。
向溶液②中加NaOH溶液至刚好沉淀完。
过滤、洗涤、干燥。
方案Ⅲ:将Al按一定比例分为两份,按前两方案先制备溶液①和溶液②。
然后将两溶液混和。
过滤、洗涤、干燥。
下列说法不正确的是( )A.三种方案转移电子数一样多B.方案Ⅲ所用硫酸的量最少C.方案Ⅲ比前两个方案更易控制酸碱的加入量D.采用方案Ⅲ时,用于制备溶液①的Al占总量的0.254、将镁铝合金溶于100mL稀硝酸中,产生1.12L NO气体(标准状况),向反应后的溶液中加入NaOH溶液,加入10mL时开始产生沉淀,加入60mL时沉淀最多,继续加入至70mL时沉淀量不再变化。
据此判断下列说法不正确的是( )A.沉淀最大质量为4.08gB.原溶液中c(HNO3)=2.6mol/LC.m(Mg):m(Al)=8:9D.氢氧化钠溶液浓度为3mol/L5、Al 2O 3是合成气直接制备二甲醚反应催化剂的主要成分之一。
工业上用铝土矿(含Fe 2O 3及其他不反应的杂质)制备较高纯度Al 2O 3的主要工艺流程有很多步骤,下列操作步骤中最恰当的组合是( ) ①加盐酸溶解 ②加烧碱溶液溶解 ③过滤④通入过量CO 2生成Al(OH)3沉淀 ⑤加入盐酸生成Al(OH)3沉淀 ⑥加入过量烧碱溶液 ⑦洗涤并锻烧A.①⑥③④③⑦B.②③④③⑦C.②③⑤③⑦D.①③⑤③⑦ 6、将镁铝合金溶于100mL 稀硝酸中,产生1.12L NO 气体(标准状况),向反应后的溶液中加入NaOH 溶液,产生沉淀情况如图所示。
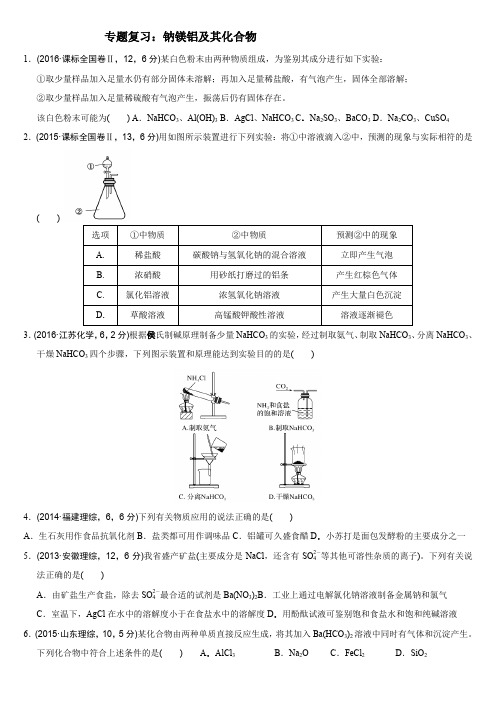
专题复习:钠镁铝及其化合物1.(2016·课标全国卷Ⅱ,12,6分)某白色粉末由两种物质组成,为鉴别其成分进行如下实验:①取少量样品加入足量水仍有部分固体未溶解;再加入足量稀盐酸,有气泡产生,固体全部溶解;②取少量样品加入足量稀硫酸有气泡产生,振荡后仍有固体存在。
该白色粉末可能为() A.NaHCO3、Al(OH)3 B.AgCl、NaHCO3 C.Na2SO3、BaCO3 D.Na2CO3、CuSO4 2.(2015·课标全国卷Ⅱ,13,6分)用如图所示装置进行下列实验:将①中溶液滴入②中,预测的现象与实际相符的是()3.(2016·江苏化学,6,2分)根据侯氏制碱原理制备少量NaHCO3的实验,经过制取氨气、制取NaHCO3、分离NaHCO3、干燥NaHCO3四个步骤,下列图示装置和原理能达到实验目的的是()4.(2014·福建理综,6,6分)下列有关物质应用的说法正确的是()A.生石灰用作食品抗氧化剂B.盐类都可用作调味品C.铝罐可久盛食醋D.小苏打是面包发酵粉的主要成分之一5.(2013·安徽理综,12,6分)我省盛产矿盐(主要成分是NaCl,还含有SO2-4等其他可溶性杂质的离子)。
下列有关说法正确的是()A.由矿盐生产食盐,除去SO2-4最合适的试剂是Ba(NO3)2B.工业上通过电解氯化钠溶液制备金属钠和氯气C.室温下,AgCl在水中的溶解度小于在食盐水中的溶解度D.用酚酞试液可鉴别饱和食盐水和饱和纯碱溶液6.(2015·山东理综,10,5分)某化合物由两种单质直接反应生成,将其加入Ba(HCO3)2溶液中同时有气体和沉淀产生。
下列化合物中符合上述条件的是() A.AlCl3B.Na2O C.FeCl2D.SiO27.(2013·山东理综,9,5分)足量下列物质与相同质量的铝反应,放出氢气且消耗溶质物质的量最少的是( )A .氢氧化钠溶液B .稀硫酸C .盐酸D .稀硝酸8.(2016·浙江理综,27Ⅰ,6分)化合物Mg 5Al 3(OH)19(H 2O)4可作环保型阻燃材料,受热时按如下化学方程式分解:2Mg 5Al 3(OH)19(H 2O)4=====△27H 2O ↑+10MgO +3Al 2O 3(1)写出该化合物作阻燃剂的两条依据________。



