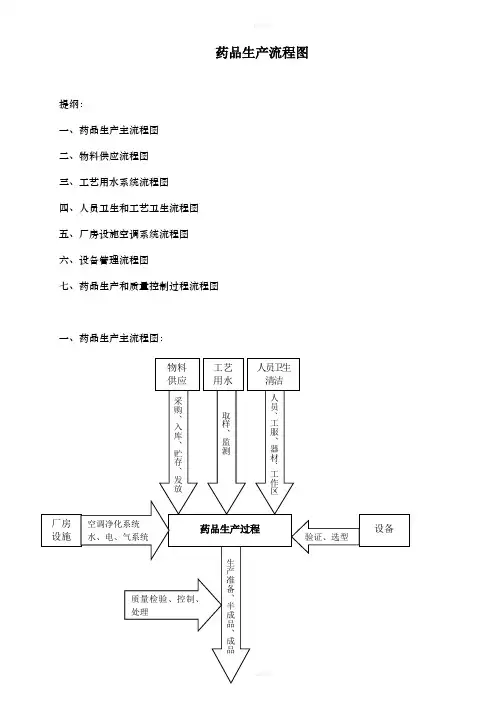
药品生产、质量控制过程流程图
- 格式:doc
- 大小:49.50 KB
- 文档页数:1

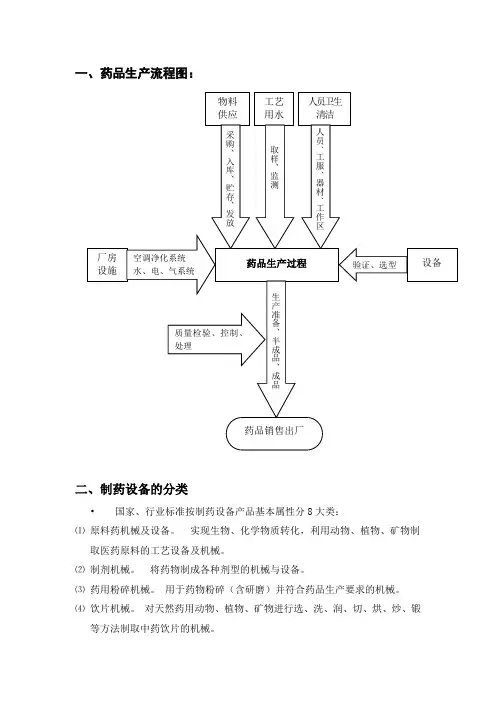
一、药品生产流程图:二、制药设备的分类•国家、行业标准按制药设备产品基本属性分8大类:⑴原料药机械及设备。
实现生物、化学物质转化,利用动物、植物、矿物制取医药原料的工艺设备及机械。
⑵制剂机械。
将药物制成各种剂型的机械与设备。
⑶药用粉碎机械。
用于药物粉碎(含研磨)并符合药品生产要求的机械。
⑷饮片机械。
对天然药用动物、植物、矿物进行选、洗、润、切、烘、炒、锻等方法制取中药饮片的机械。
⑸制药用水设备。
采用各种方法制取制药用水的设备。
⑹药品包装机械。
完成药品包装过程以及与包装过程相关的机械与设备。
⑺药用检测设备。
检测各种药物制品或半制品质量的仪器与设备。
⑻其他制药机械及设备。
执行非主要制药工序的有关机械与设备。
•其中制剂机械按剂型分14类:⑴剂机械。
将原料药与辅料经混合、造粒、压片、包衣等工序制成各种形状片剂的机械与设备。
⑵针剂机械。
将药液制作成安瓿针剂的机械与设备。
⑶生素粉、水针剂机械。
将粉末药物或药液制作成玻璃瓶抗生素粉、水针剂的机械与设备。
⑷液剂机械。
将药液制作成大剂量注射剂的机械与设备。
⑸胶囊剂机械。
将药物充填于空心胶囊内制作成硬胶囊剂的机械与设备。
⑹胶囊(丸)剂机械。
将药液先裹于明胶膜内的制剂机械与设备。
⑺剂机械。
将药物细粉或浸膏与赋形剂混合,制成丸剂的机械与设备。
⑻膏剂机械。
将药物与基质混匀,配制成软膏,定量灌装于软管内的制剂机械与设备。
⑼剂机械。
将药物与基质混合,制成栓剂的机械与设备。
⑽服液剂机械。
将药液制成口服液剂的机械与设备。
⑾膜剂机械。
将药物浸透或分散于多聚物薄膜内的制剂机械与设备。
⑿雾剂机械。
将药液和抛射剂灌注于耐压容器中,制作成药物以雾状喷出的制剂机械与设备。
⒀眼剂机械。
将药液制作成滴眼药剂的机械与设备。
⒁水、糖浆剂机械。
将药液制作成酊水、糖浆剂的机械与设备。
三、原料药生产设备生物制药反应过程设备。

目录目录 (1)四查十对操作流程 (2)调剂差错管理流程 (3)药品召回程序流程图 (4)门诊处方调剂流程图 (5)中心药房工作流程图 (6)模糊医嘱的澄清流程 (7)住院药房(门诊药房)药品效期管理流程 (8)药库工作流程图 (9)药库药品效期管理流程 (10)假、劣药品,调剂药品导致人身伤害处置流程图 (11)突发事件药事管理应急预案流程 (12)突发事件药品供应应急预案流程图 (13)特殊使用抗菌药物应用流程 (14)药品采购流程图 (14)备用药品管理流程图 (15)麻、精、高危药品管理流程 (17)科室急救备用药品领用、补充工作流程 (18)输液反应处置流程 (19)细菌耐药监测与预警管理流程 (20)四查十对操作流程调剂人员对科别、姓名、年龄查处方对临床诊断对药品性状、 用法用量对药名、剂型、规格、数量 查药品 查配伍禁忌 查用药合理性 发药人员对药名、规格、剂量、用法与处方内容是否相查药品对姓名、年龄,并交待用法及注意事项对药品有无变质、是否超过有效期对与处方内容是否相符 查标签(药袋)查药品查姓名、年龄调剂差错管理流程报告部门负责人报药剂科主任报医务办严重事件填写报告事件处理核对相关处方和药品查找患者发现差错药品召回程序流程图(一级24h 内)(二级7d 内) NOYESYes)药剂科各部门负责接收退回的药品,通知各科室停止销售和使用, 填写《药品召回登记表》,报告质量管理人员当使用被召回药品不会对治疗或患者的健康造成不良影响时,应采用二级召回当继续使用被召回药品将对治疗或患者的健康造成不良影响时,应采用一级召回反馈到投诉人或医院药品质量管理领导小组收到存在安全隐患可能的信息药品安全隐患的调查 召回决定/确定召回等级制定召回计划/通告发放启动召回是否存在药品安全隐患的评估质量安全与管理小组组织召回质量控制小组调查评估报告和召回计划上报 汇总药品召回登记表,召回实施情况定期上报医院药品质量领导小组, 召回总结报告召回产品的处理如需销毁,报医院药品质量安全领导小组,由药监部门监督销毁 质量控制小组总结报告,上报医院药品质量领导小组验收/取样待处理药库负责接收各药房撤架和患者退回的药品,按《药剂科退药制度》的规定办理手续并记录,统一、专人妥善保管。
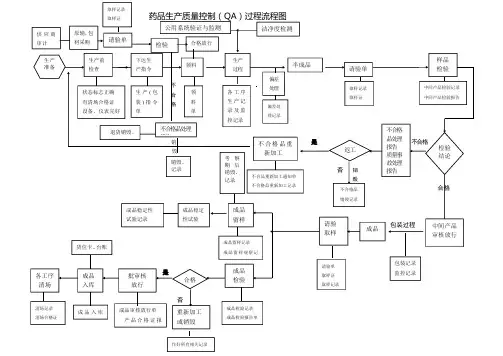
不合格销是不合格毁否销毁合格包装过程是否药品生产质量控制(QA)过程流程图生产准备生产前检查下达生产指令生产过程偏差处理样品检验检验结论返工成品成品留样生产(包装)指令单各工序生产记录及监控记录偏差处理记录半成品请验单取样记录取样证中间产品检验记录中间产品检验报告中间产品审核放行请验取样请验单取样证取样记录成品稳定性试验成品稳定性试验记录成品检验成品检验记录成品检验报告单成品留样记录成品留样观察记批审核放行合格成品入库成品审核放行单产品合格证报重新加工或销毁作好所有相关记录成品入库不合格品处理报告质量事故处理报告不合格品销毁记录不合格品重新加工不合品重新加工通知单不合格品重新加工记录状态标志正确有清场合格证设备、仪表完好领料领料单各工序清场清场记录清场合格证包装记录监控记录货位卡、台账洁净度检测公用系统验证与监测考察期后销毁、记录供应商审计原辅,包材采购请验单取样记录取样证检验合格放行不合格品处理报告退货销毁、销毁、记录文件产品质量标准省级以上药品检验报告单组织机构代码证税务登记证书应为合法有效版本审计:公司每年对所选择供应商进行审计(现场审计、非现场审计)并出具公司质量部的审计报告,具体按供应商审计管理标准内容进行。
每年未应制定出下年度的合格供应商目录,并受权人签字确认,分发至物料部门采购部门,质量部存档1.按以上目录内先择相应0购入材料的供应商,并签定购销合同及质量保证协议书同货存档,再进行采购。
1采购到位的合法材料,在进入库前进行初验,填写初验记录。
合格后进行待验区,做好状态标示及货位卡,填写请验单,请验质量部。
2.取样员取样应填写取样单、取样证、带好取样器具取样,并做好取样记录,填好货位卡的取样量。
物料部门应在取样前后做好取样车使用记录。
取过样的物料应放至最上层,生产时应先出。
1.取样后按时效进行分样检验(检验原始记录、检验台账(合格与不合格)、试剂领用、配制记录(毒剧试剂的领用、配制、销毁记录)、标准品、液领用、配制记录、标定复标记录、检验仪器使用记录、检定菌传代与使用销毁记录)并出具报告单(一式三份)。
1.目的
2.范围
3.职责
4.内容
4.1生产处方
4.1.1名称
通用名:
汉语拼音名:
英文名:
4.1.2产品代号
4.1.3有效期、贮藏
4..1.4产品剂型、规格、批量
4.1.5原辅料清单
4.2 生产操作要求
4.2.1生产工艺流程图(见附表)
4.2.2主要设备和仪器及相应操作方法4.2.3生产工艺操作步骤及技术参数
4.2.4中间控制
4.2.5生产过程产量限度及物料平衡
4.2.6 原辅料、包装容器、中间产品、侍包装产品、包装材料贮存条件
4.2.7生产场所环境情况(洁净级别、温度、湿度)
4.2.8环境卫生要求及采取措施
4.2.9工艺卫生要求及采取措施
4.2.10个人卫生要求及采取措施
4.3包装操作要求
4.3.1包装规格
4.3.2包装材料清单
4. 3.3包装开始前对工作场所进行检查
4. 3.4灯检
4.3.5贴标
4.3.6包装
4. 3.7有效期。
贮藏条件。
4.3.8包装中间控制方法及合格标准
4.3.9包装工序物料平衡
4.3.10原辅材料消耗定额
4.3.11包装材料消耗定额
4.3.12动力消耗定额
4.4质量标准及相应检验操作方法
4.4.1成品及半成品质量标准及相应检验操作方法
4.4.2原辅料、溶剂质量标准及相应检验操作方法
4.4.3成品包装容器、包装成料规格及质量标准及相应检验操作方法
5.安全与劳动保护
6.劳动组织、岗位定员、工时定额、生产周期
7.经济技术指标计算。

药品业务流程SANY标准化小组 #QS8QHH-HHGX8Q8-GNHHJ8-HHMHGN#药品业务流转规程第一业务经营部分一、药品采购流转规程 1二、药品采退流转规程 3三、药品销售流转规程 4四、药品销退流转规程 7五、专项药品(透析液、麻药)销售流转规程 8第二质量管理部分一、质量管理制度编制、修订、审批、撤销及检查、考核流转规程 11二、药品进货质量审核流转规程 13三、药品检查验收流转规程 17四、药品出库储存质量流转规程 20五、药品在库养护流转规程 21六、药品销售质量审核流转规程 24七、药品出库复核质量流转规程 27八、药品拆零拼箱发货流转规程 29九、药品采购退货质量流转规程 30十、药品销售退货质量流转规程 32十一、不合格药品确认和处理流转规程 34十二、药品报损、报溢流转规程 38十三、报损药品销毁流转规程 41第三药品储存部分一、药品入库流转规程 43二、药品出库流转规程 43三、药品在库管理流转规程 44第四药品运输部分一、本市送货流转规程 45二、外埠集装箱发运流转规程 45三、铁路零担发运流转规程 46四、汽车送货流转规程 47五、外埠快件发运流转规程 47六、特快专递发运流转规程 48七、邮局发运流转规程 48八、铁路下站流转规程 49九、民航、汽车到达流转规程 49十、其他到货流转规程(厂家、驻京办事处、业务单位调剂品种) 50第一业务经营部分一、药品采购流转规程(一)流程图8、调剂品种由分公司提出申请,通知采购员,由采购员按采购管理权限与供应商进行药品的调剂。
其他流程与药品采购流程相同。
9、不备库存的调剂品种,只需验收员填写验收数据及临时仓位。
二、药品采退流程图(一)流程图(二)药品采退流程描述1、采购人员对种种原因发生采退确定退回供应厂商需要出库退厂的药品,在系统中制作采购退货电子预报单并通知供应厂商。
2、采购中心打印一式两联负入库单并转财务记应付帐和商品帐。


目录目录 (1)四查十对操作流程 (2)调剂差错管理流程 (3)药品召回程序流程图 (4)门诊处方调剂流程图 (5)中心药房工作流程图 (6)模糊医嘱的澄清流程 (7)住院药房(门诊药房)药品效期管理流程 (8)药库工作流程图 (9)药库药品效期管理流程 (10)假、劣药品,调剂药品导致人身伤害处置流程图 (11)突发事件药事管理应急预案流程 (12)突发事件药品供应应急预案流程图 (13)特殊使用抗菌药物应用流程 (14)药品采购流程图 (14)备用药品管理流程图 (15)麻、精、高危药品管理流程 (17)科室急救备用药品领用、补充工作流程 (18)输液反应处置流程 (19)细菌耐药监测与预警管理流程 (20)四查十对操作流程调剂人员对科别、姓名、年龄查处方对临床诊断对药品性状、 用法用量对药名、剂型、规格、数量 查药品 查配伍禁忌 查用药合理性 发药人员对药名、规格、剂量、用法与处方内容是否相查药品对姓名、年龄,并交待用法及注意事项对药品有无变质、是否超过有效期对与处方内容是否相符 查标签(药袋)查药品查姓名、年龄调剂差错管理流程报告部门负责人报药剂科主任报医务办严重事件填写报告事件处理核对相关处方和药品查找患者发现差错药品召回程序流程图(一级24h 内)(二级7d 内) NOYESYes)药剂科各部门负责接收退回的药品,通知各科室停止销售和使用, 填写《药品召回登记表》,报告质量管理人员当使用被召回药品不会对治疗或患者的健康造成不良影响时,应采用二级召回当继续使用被召回药品将对治疗或患者的健康造成不良影响时,应采用一级召回反馈到投诉人或医院药品质量管理领导小组收到存在安全隐患可能的信息药品安全隐患的调查 召回决定/确定召回等级制定召回计划/通告发放启动召回是否存在药品安全隐患的评估质量安全与管理小组组织召回质量控制小组调查评估报告和召回计划上报 汇总药品召回登记表,召回实施情况定期上报医院药品质量领导小组, 召回总结报告召回产品的处理如需销毁,报医院药品质量安全领导小组,由药监部门监督销毁 质量控制小组总结报告,上报医院药品质量领导小组验收/取样待处理药库负责接收各药房撤架和患者退回的药品,按《药剂科退药制度》的规定办理手续并记录,统一、专人妥善保管。