高一化学核素
- 格式:pdf
- 大小:1.29 MB
- 文档页数:9

高一化学核素知识点核素是指具有确定质子数和中子数的同位素,可以通过核反应进行转化,存在于核反应中的核素称为反应物,参与反应但未被转化的核素称为中间体,通过核反应转化成其他核素的核素称为产物。
一、核素符号核素符号由元素化学符号和质量数构成,元素化学符号一般用拉丁字母表的第一个字母大写来表示,质量数在元素符号的左上角标注,质子数在元素符号的右下角标注,如氢的核素符号为^1H,碳-12的核素符号为^12C。
二、同位素和同位素符号同位素是指具有相同质子数但质量数不同的核素,同位素符号的元素化学符号后面用连字符的方式接上质量数,如氢的同位素有氘和氚,分别表示为^2H和^3H。
三、放射性核素和稳定核素根据核素的稳定性,可以将核素分为放射性核素和稳定核素。
放射性核素具有不稳定核结构,会自发地发生核衰变释放粒子或电磁辐射,最终转化成其他核素。
稳定核素则具有相对稳定的核结构,不会自发发生核衰变。
例如,铀-238是一种放射性核素,而碳-12是一种稳定核素。
四、核反应和核方程式核反应是指由于核的结构变化导致的反应过程。
核方程式用于表示核反应的化学方程式,由反应物核素符号和产物核素符号组成,反应物写在箭头的左侧,产物写在箭头的右侧。
核方程式中需保证质量数和电荷数在反应前后相等。
例如,氢的核融合反应方程式可以表示为:^1H + ^1H → ^2H + e+ + ν其中,ν表示中微子,e+表示正电子。
五、核衰变和半衰期核衰变是指放射性核素发生自发性核转换的过程,常见的核衰变方式包括α衰变、β衰变和γ衰变。
α衰变是指放射性核素放出一个α粒子,质量数减少4、质子数减少2。
β衰变是指放射性核素放出一个β粒子,质量数不变、质子数增加1。
γ衰变是指放射性核素发射γ射线,不改变质量数和质子数。
半衰期是指放射性核素衰变为其半衰期的一半所需的时间。
不同放射性核素具有不同的半衰期,半衰期的长短决定了放射性核素的放射强度和放射性活度。
常见的放射性核素如铀-238的半衰期为45.7亿年,碳-14的半衰期为5730年。








高中化学中的核素教案模板
一、教学目标:
1. 理解核素的概念
2. 掌握核素的表示方法和命名规则
3. 了解核素的放射性及应用
二、教学重点:
1. 核素的定义和表示方法
2. 核素的放射性及应用
3. 核素的命名规则
三、教学步骤:
1. 核素的概念(5分钟)
a. 引入核素的概念
b. 解释核素和同位素的关系
2. 核素的表示方法和命名规则(15分钟)
a. 介绍核素的表示方法:表示方式、符号、质子数、中子数和质量数
b. 解释核素的命名规则:元素符号+质量数
3. 核素的放射性及应用(15分钟)
a. 讲解核素的放射性现象及产生原因
b. 探讨核素在医学、工业和农业等领域的应用
4. 练习与检测(15分钟)
a. 完成核素相关习题
b. 进行核素相关知识测验
五、课后作业:
1. 复习核素的表示方法和命名规则
2. 思考核素在生活中的应用,并写下自己的见解和观点
六、教学反思:
通过本节课的教学,学生是否能够掌握核素的表示方法和命名规则?是否能够理解核素的
放射性及应用?是否能够在日常生活中理解核素的重要性和作用?通过学生的表现和反馈,及时调整教学方法和内容,提高教学效果。
高一化学核素知识点一、物质的分类金属:na、mg、al单质非金属:s、o、n酸性氧化物:so3、so2、p2o5等氧化物碱性氧化物:na2o、cao、fe2o3氧化物:al2o3等纯盐氧化物:co、no等天量含氧酸:hno3、h2so4等物按酸根分无氧酸:hcl强酸:hno3、h2so4、hcl酸按高低分后弱酸:h2co3、hclo、ch3cooh化一元酸:hcl、hno3合按电离出的h+数分二元酸:h2so4、h2so3物多元酸:h3po4强碱:naoh、ba(oh)2物按高低分后质弱碱:nh3?h2o、fe(oh)3碱一元碱:naoh、按电离出来的ho-数分二元碱:ba(oh)2多元碱:fe(oh)3正盐:na2co3盐酸式盐:nahco3碱式盐:cu2(oh)2co3溶液:nacl溶液、稀h2so4等搭悬浊液:泥水混合物等合乳浊液:油水混合物物胶体:fe(oh)3胶体、淀粉溶液、烟、雾、有色玻璃等二、分散系相关概念1、集中系则:一种物质(或几种物质)以粒子形式集中至另一种物质里所构成的混合物,泛称为集中系则。
2、分散质:分散系中分散成粒子的物质。
3、分散剂:集中质集中在其中的物质。
4、分散系的分类:当分散剂是水或其他液体时,如果按照分散质粒子的大小来分类,可以把分散系分为:溶液、胶体和浊液。
分散质粒子直径小于1nm的分散系叫溶液,在1nm-nm之间的分散系称为胶体,而分散质粒子直径大于nm的分散系叫做浊液。
下面比较几种集中系则的相同:分散系溶液胶体浊液集中质粒子单个小分子或离子许多小分子集合体或高分子非常大数目的分子集合体三、胶体2、胶体的分类:①根据分散质微粒组成的状况分类:例如:胶体胶粒就是由许多等小分子涌入一起构成的微粒,其直径在1nm~nm之间,这样的胶体叫做粒子胶体。
又例如:淀粉属于高分子化合物,其单个分子的直径在1nm~nm范围之内,这样的胶体叫做分子胶体。
②根据分散剂的状态划分:例如:烟、云、雾等的分散剂为气体,这样的胶体叫作气溶胶;agi溶胶、溶胶、溶胶,其分散剂为水,分散剂为液体的胶体叫作液溶胶;有色玻璃、烟水晶均以液态为分散剂,这样的胶体叫作固溶胶。
高一下册化学核素知识点核素是指具有特定核子数和质子数的同位素。
在化学中,核素的了解对于理解元素的性质、反应以及核反应的平衡等方面具有重要意义。
下面将介绍高一下册化学中的一些核素知识点。
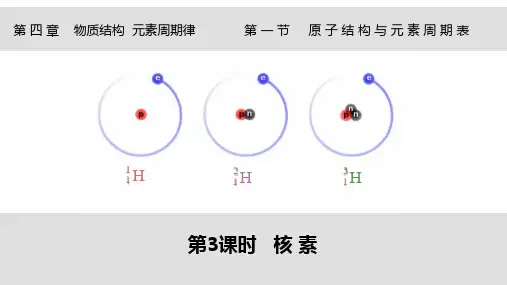
1. 氢(H-1)氢是元素周期表上最简单的元素,其原子核由一个质子组成。
在自然界中,氢的最丰富的同位素是氘(H-2)和氚(H-3)。
氘核中有一个中子,氚核中有两个中子。
氘和氚具有不同的物理性质和化学性质,因此在实际应用中具有广泛的用途。
2. 碳(C-12,C-14)碳是元素周期表上的第6号元素,其原子核由6个质子和6个中子组成。
自然界中存在两种主要的碳同位素,即稳定的C-12和放射性的C-14。
C-14具有放射性,其半衰期为5730年。
因此,C-14常用于测定古物的年代和地质年代。
3. 铀(U-235,U-238)铀是元素周期表上的第92号元素,其原子核由92个质子和不同数量的中子组成。
铀有两种自然存在的同位素,即U-235和U-238。
U-235是放射性同位素,可以发生裂变,广泛应用于核能反应堆和核武器。
U-238是稳定的同位素,但可以通过中子俘获转变成放射性的钚(Pu-239)。
4. 铀系列衰变铀系列衰变是一系列从铀开始,经过多个核素连续衰变直至稳定同位素的过程。
铀系列衰变产生了一系列的放射性同位素,包括镭(Ra-226)、钋(Po-210)等。
这些同位素在核能研究、医学和工业等领域有广泛应用。
5. 放射性同位素的应用放射性同位素在科学研究、医学和工业等方面具有广泛应用。
例如,放射性同位素碘-131(I-131)可用于治疗甲状腺疾病;锶-90(Sr-90)用于癌症治疗;钴-60(Co-60)被用作肿瘤治疗中的辐照源等。
总结:通过对高一下册化学中的核素知识点的了解,我们可以看到核素作为同位素的特殊类别,在化学研究和实际应用中具有重要作用。
从氢的同位素到铀系列衰变,不同的核素在核能反应、放射治疗、古物年代测定等方面都发挥着关键作用。