立体化学基础培训课件
- 格式:ppt
- 大小:6.92 MB
- 文档页数:102







第16讲《立体化学基础》高中化学奥林匹克竞赛辅导讲座第16讲立体化学基础【竞赛要求】有机立体化学基本概念。
构型与构象。
顺反异构(trans-、cis-和Z-、E-构型)。
手性异构。
endo-和exo-。
D,L构型。
【知识梳理】从三维空间结构研究分子的立体结构,及其立体结构对其物理性质和化学性质的影响的科学叫立体化学。
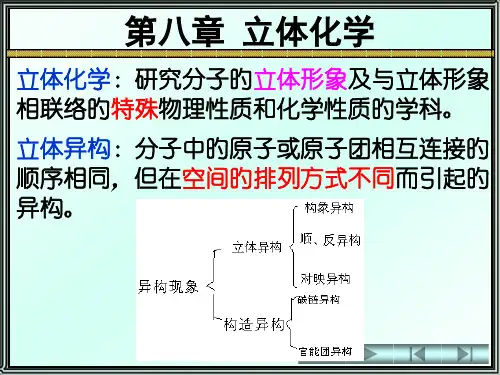
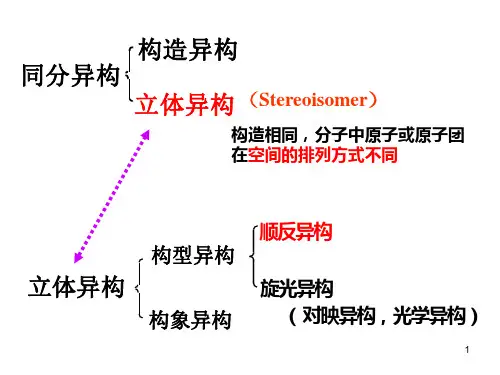
一、异构体的分类按结构不同,同分异构现象分为两大类。
一类是由于分子中原子或原子团的连接次序不同而产生的异构,称为构造异构。
构造异构包括碳链异构、官能团异构、位置异构及互变异构等。
另一类是由于分子中原子或原子团在空间的排列位置不同而引起的异构,称为立体异构。
立体异构包括顺反异构、对映异构和构象异构。
二、立体异构(一)顺反异构分子中存在双键或环等限制旋转的因素,使分子中某些原子或基团在空间位置不同,产生顺反异构现象。
双键可以是C=C、C=N、N=N。
双键产生顺反异构体的条件是双键两端每个原子所连二基团或原子不同。
a b如:顺反异构的构型以前用顺�C 和反�C 表示。
如:H H CH3 H C = C C = CCH3 H CH3 CH3顺�C 2 �C 丁烯反�C 2 �C 丁烯a b c ca b c cc c a ba dc d但顺反异构体的两个双键碳原子上没有两个相同的取代基用这种命名法就无能为力。
如: H3C CH2CH3C = CH CH(CH3)2系统命名法规定将双键碳链上连接的取代基按次序规则的顺序比较,高序位基在双键同侧的称Z型,反之称E型。
如上化合物按此规定应为E型。
命名为E �C 4 �C 甲基�C 3 �C 已基�C 2 �C 戊烯。
所谓“次序规则”,就是把各种取代基按先后次序排列的规则。
(1)原子序数大的优先,如I>Br>Cl>S>P>F>O>N>C>H,未共用电子对为最小;(2)同位素质量数大的优先,如D>H;(3)二个基团中第一个原子相同时,依次比较第二、第三个原子;(4)重键,如:分别可看作:(5)当取代基的结构完全相同,只是构型不同时,则R>S,Z>E。
