2015 《中国药典》无菌检查法修订解析
- 格式:ppt
- 大小:1.08 MB
- 文档页数:37

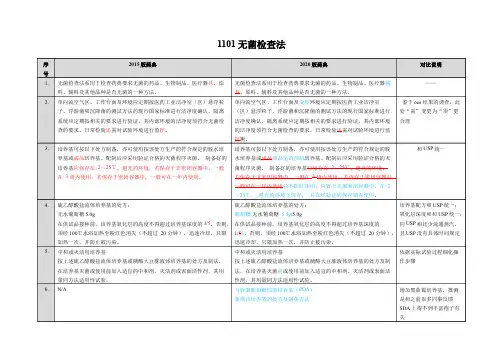
1101 无菌检查法无菌检查法系用于检查药典要求无菌的药品、生物制品、医疗器具、原料、辅料及其他品种是否无菌的一种方法。
若供试品符合无菌检查法的规定,仅表明了供试品在该检验条件下未发现微生物污染。
无菌检查应在无菌条件下进行,试验环境必须达到无菌检查的要求,检验全过程应严格遵守无菌操作,防止微生物污染,防止污染的措施不得影响供试品中微生物的检出。
单向流空气区、工作台面及环境应定期按医药工业洁净室(区)悬浮粒子、浮游菌和沉降菌的测试方法的现行国家标准进行洁净度确认。
隔离系统应定期按相关的要求进行验证,其内部环境的洁净度须符合无菌检查的要求.日常检验还需对试验环境进行监控。
培养基硫乙醇酸盐流体培养基主要用于厌氧菌的培养,也可用于需氧菌培养;胰酪大豆胨液体培养基用于真菌和需氧菌的培养。
培养基的制备及培养条件培养基可按以下处方制备,亦可使用按该处方生产的符合规定的脱水培养基或成品培养基。
配制后应采用验证合格的灭菌程序灭菌。
制备好的培养基应保存在2~25℃、避光的环境,若保存于非封闭容器中,一般在3周内使用;若保存于密闭容器中,一般可在一年内使用。
1. 硫乙醇酸盐流体培养基胰酪胨15.0g 氯化钠2.5g酵母浸出粉5。
0g 新配制的0。
1% 刃天青溶液1。
0ml无水葡萄糖5。
0g 琼脂0.75gL-胱氨酸0.5g 水1000ml硫乙醇酸钠0.5g(或硫乙醇酸) (0。
3ml)除葡萄糖和刃天青溶液外,取上述成分混合,微温溶解,调节pH为弱碱性,煮沸,滤清,加入葡萄糖和刃天青溶液,摇匀,调节pH,使灭菌后在25℃的pH值为7。
1±0.2。
分装至适宜的容器中,其装量与容器高度的比例应符合培养结束后培养基氧化层(粉红色)不超过培养基深度的1/2。
灭菌。
在供试品接种前,培养基氧化层的高度不得超过培养基深度的1/5,否则,须经100℃水浴加热至粉红色消失(不超过20分钟),迅速冷却,只限加热一次,并防止污染。

2015版中国药典微生物检查方法及培养基变更参照1.无菌检查法1.1变更内容1.1.1无菌检查方面,使用胰酪胨大豆肉汤(胰酪胨大豆液体培养基/大豆酪蛋白肉汤培养基)取代改良马丁培养基与硫乙醇酸盐流体培养基配合进行细菌和真菌的全面微生物检测。
1.1.2菌液制备环节,使用胰酪胨大豆肉汤、胰酪胨大豆琼脂取代营养肉汤、营养琼脂进行金黄色葡萄球菌、铜绿假单胞菌、枯草芽孢杆菌和大肠埃希氏菌的菌液制备。
1.1.3菌液制备环节,使用沙氏葡萄糖液体培养基、沙氏葡萄糖琼脂培养基取代改良马丁培养基、改良马丁琼脂进行白色念珠菌和黑曲霉菌液的制备,同时对沙氏葡萄糖液体培养基、沙氏葡萄糖琼脂的配方进行了变更。
1.1.4适用性试验中,胰酪胨大豆肉汤使用枯草芽孢杆菌、白色念珠菌和黑曲霉进行灵敏度检查;硫乙醇酸盐流体培养基使用金黄色葡萄球菌、大肠埃希氏菌、生孢梭菌、铜绿假单胞菌进行灵敏度检查。
1.2培养基信息2010版2015版无菌检查/菌液制备——硫乙醇酸盐流体培养基无菌检查/菌液制备——改良马丁培养基菌液制备——改良马丁琼脂培养基菌液制备——营养肉汤菌液制备——营养琼脂无菌检查——0.5%葡萄糖肉汤培养基供试品制备——0.1%蛋白胨水培养基无菌检查/菌液制备——硫乙醇酸盐流体培养基无菌检查/菌液制备——胰酪胨大豆肉汤菌液制备——胰酪胨大豆琼脂菌液制备——沙氏葡萄糖琼脂菌液制备——沙氏葡萄糖肉汤无菌检查——0.5%葡萄糖肉汤培养基供试品制备——0.1%蛋白胨水培养基供试品制备——pH7.0氯化钠—蛋白胨缓冲液1.3参考文件(国家药典委员会—中国药典2015版附录征求意见稿—1101无菌检查法)http://w w /cms/new scenter/new s/000603.html2.非无菌产品微生物限度检查2.1变更内容2.1.1供试品制备环节,除了pH7.0氯化钠—蛋白胨缓冲液、pH6.8磷酸盐缓冲液、pH7.6磷酸盐缓冲液外,添加了pH7.2磷酸盐缓冲液和胰酪胨大豆肉汤。




讲义五:2015年版版中国药典四部增修订情况第一篇:讲义五:2015年版版中国药典四部增修订情况2015 年版《中国药典》四部增修订概况2015年版《中国药典》已于2015年6月5日由国家食品药品监督管理总局正式颁布。
2015年版《中国药典》最大的变动之一是将原药典各部附录整合,并与药用辅料标准单立成卷,首次作为《中国药典》第四部,解决了长期以来药典各部共性检测方法重复收录、彼此之间方法不协调、不统一、不规范,给药品检验实际操作带来不便的问题。
2015年版《中国药典》四部内容包括凡例、通则和药用辅料,药典通则涵盖了通用性要求、检验方法、指导原则以及试剂和标准物质等药品标准的共性要求,是药典标准的基础,不但反映了我国药品质量控制整体状况和药品检验技术水平;同时也对规范药品研究、生产、检验、加强药品监管发挥重要作用。
现就2015年版《中国药典》四部整体情况简要介绍如下。
1.2015 年版《中国药典》四部增修订整体情况2015 年版《中国药典》四部收载通则总数317个;将药典一部、二部、三部制剂整合后共计38个;检测方法附录287个,其中新增通则28个(检定方法通则27个、制剂通则1个),整合通则63个,修订通则67 个;新增生物制品总论3个;指导原则共计30个,其中新增15个,修订10个。
辅料收载总数约270个品种,其中新增137 个,修订97个,不收载2个。
2.2015 年版《中国药典》四部主要特点2.1 整体提升质控水平《中国药典》凡例、通则、总论是药典的重要组成部分,对药品标准的检测方法和限度进行总体规定,对药典以外的其他药品国家标准具同等效力。
通过对2010年版《中国药典》相关内容的全面增修订,全面完善了药典标准基本共性规定(表2),从整体上提升对药品质量控制的要求,形成了以凡例为统领,通则为同类药品基本准则、各论作为基本要求的药典标准体例。
药品标准控制更加全面化、系统化、规范化。
2.2 药典标准体系更加完善 2015年版《中国药典》四部首次纳入“国家药品标准物质通则”以及“国家药品标准物质制备指导原则”、“药包材通用要求”和“药用玻璃材料和容器”等指导原则,进一步完善了药用辅料和药包材通用性要求,从影响药品质量的等各方面,包括原料药及其制剂、药品标准物质、药用辅料和药包材的制定控制要求,形成了全面、完善的药典标准体系。




1101 无菌检查法无菌检查法系用于检查药典要求无菌的药品、生物制品、医疗器具、原料、辅料及其他品种是否无菌的一种方法。
若供试品符合无菌检查法的规定,仅表明了供试品在该检验条件下未发现微生物污染。
无菌检查应在无菌条件下进行,试验环境必须达到无菌检查的要求,检验全过程应严格遵守无菌操作,防止微生物污染,防止污染的措施不得影响供试品中微生物的检出。
单向流空气区、工作台面及环境应定期按医药工业洁净室(区)悬浮粒子、浮游菌和沉降菌的测试方法的现行国家标准进行洁净度确认。
隔离系统应定期按相关的要求进行验证,其内部环境的洁净度须符合无菌检查的要求。
日常检验还需对试验环境进行监控。
培养基硫乙醇酸盐流体培养基主要用于厌氧菌的培养,也可用于需氧菌培养;胰酪大豆胨液体培养基用于真菌和需氧菌的培养。
培养基的制备及培养条件培养基可按以下处方制备,亦可使用按该处方生产的符合规定的脱水培养基或成品培养基。
配制后应采用验证合格的灭菌程序灭菌。
制备好的培养基应保存在2~25℃、避光的环境,若保存于非封闭容器中,一般在3周内使用;若保存于密闭容器中,一般可在一年内使用。
1. 硫乙醇酸盐流体培养基胰酪胨15.0g 氯化钠2.5g酵母浸出粉 5.0g 新配制的0.1% 刃天青溶液1.0ml无水葡萄糖 5.0g 琼脂0.75gL-胱氨酸0.5g 水1000ml硫乙醇酸钠0.5g(或硫乙醇酸)(0.3ml)除葡萄糖和刃天青溶液外,取上述成分混合,微温溶解,调节pH为弱碱性,煮沸,滤清,加入葡萄糖和刃天青溶液,摇匀,调节pH,使灭菌后在25℃的pH值为7.1±0.2。
分装至适宜的容器中,其装量与容器高度的比例应符合培养结束后培养基氧化层(粉红色)不超过培养基深度的1/2。
灭菌。
在供试品接种前,培养基氧化层的高度不得超过培养基深度的1/5,否则,须经100℃水浴加热至粉红色消失(不超过20分钟),迅速冷却,只限加热一次,并防止污染。
中国药典2015版⽆菌检查⽅法适⽤性试验(直接接种法)*********公司*********产品⽆菌检查⽅法适⽤性试验1、样品信息2、培养基及试剂3、菌种基本信息:4、菌液制备:2.1接种⾦黄⾊葡萄球菌、⼤肠埃希菌、枯草芽孢杆菌的新鲜培养物⾄胰酪⼤⾖胨培养基中或胰酪⼤⾖胨脂培养基上,30~35℃培养18~24⼩时,培养物⽤0.9%⽆菌氯化钠溶液制成每1ml含菌数⼩于100cfu的菌悬液。
2.2接种⽣孢梭菌的新鲜培养物⾄硫⼄醇酸盐流体培养基中,30~35℃培养18~24⼩时,培养物⽤0.9%⽆菌氯化钠溶液制成每1ml含菌数⼩于100cfu的菌悬液。
2.3接种⽩⾊念珠菌的新鲜培养物⾄沙⽒葡萄糖液体培养基或沙⽒葡萄糖琼脂斜⾯培养基上,20~25℃培养24~48⼩时,培养物⽤0.9%⽆菌氯化钠溶液制成每1ml 含菌数⼩于100cfu的菌悬液。
2.4接种⿊曲霉菌的新鲜培养物接种⾄沙⽒葡萄糖琼脂斜⾯培养基上,20~25℃培养5~7天,加⼊3~5ml含0.05%(ml/ml)聚⼭梨酯80的0.9%⽆菌氯化钠溶液,将孢⼦洗脱。
然后,采⽤适宜的⽅法吸出孢⼦悬液⾄⽆菌试管内,⽤含0.05%(ml/ml)聚⼭梨酯80的0.9%⽆菌氯化钠溶液制成每1ml含菌数⼩于100cfu的菌孢⼦悬液。
6、⽆菌检查直接接种法⽅法适⽤性试验6.1供试品制备:描述供试品制备过程(主要为每个样品的取样部位及⽤量)。
6.2试验组:取装量为 ml硫⼄醇酸盐流体培养基,接种规定的供试品量(同6.1),并接种⼩于100cfu的⾦黄⾊葡萄球菌;⼤肠埃希菌、⽣孢梭菌、枯草芽孢杆菌、⽩⾊念珠菌、⿊曲霉按照上述步骤操作,其中⼤肠埃希菌、⽣孢梭菌加⼊硫⼄醇酸盐流体培养基,枯草芽孢杆菌、⽩⾊念珠菌、⿊曲霉加⼊胰酪⼤⾖胨液体培养基。
6.3对照组:取装量为 ml硫⼄醇酸盐流体培养基3管,分别接种⼩于100cfu的⾦黄⾊葡萄球菌、⼤肠埃希菌、⽣孢梭菌;取相同装量的胰酪⼤⾖胨培养基3管,分别接种⼩于100cfu枯草芽孢杆菌、⽩⾊念珠菌、⿊曲霉。