植物核蛋白和细胞器蛋白提取方法
- 格式:pdf
- 大小:163.61 KB
- 文档页数:3

植物蛋白质提取方法汇总(本人经验总结)一、植物组织蛋白质提取方法1、根据样品重量(1g样品加入3.5ml提取液,可根据材料不同适当加入),准备提取液放在冰上。
2、把样品放在研钵中用液氮研磨,研磨后加入提取液中在冰上静置(3-4小时)。
3、用离心机离心8000rpm40min4℃或11100rpm20min4℃4、提取上清液,样品制备完成。
蛋白质提取液:300ml1、1Mtris-HCl(PH8)45ml2、甘油(Glycerol)75ml3、聚乙烯吡咯烷酮(Polyvinylpolypyrrordone)6g这种方法针对SDS-PAGE,垂直板电泳!二、植物组织蛋白质提取方法氯醋酸—丙酮沉淀法1、在液氮中研磨叶片2、加入样品体积3倍的提取液在-20℃的条件下过夜,然后离心(4℃8000rpm 以上1小时)弃上清。
3、加入等体积的冰浴丙酮(含0.07%的β-巯基乙醇),摇匀后离心(4℃8000rpm 以上1小时),然后真空干燥沉淀,备用。
4、上样前加入裂解液,室温放置30分钟,使蛋白充分溶于裂解液中,然后离心(15℃8000rpm以上1小时或更长时间以没有沉淀为标准),可临时保存在4℃待用。
5、用Brandford法定量蛋白,然后可分装放入-80℃备用。
药品:提取液:含10%TCA和0.07%的β-巯基乙醇的丙酮。
裂解液:2.7g尿素0.2gCHAPS溶于3ml灭菌的去离子水中(终体积为5ml),使用前再加入1M 的DTT65ul/ml。
这种方法针对双向电泳,杂质少,离子浓度小的特点!当然单向电泳也同样适用,只是电泳的条带会减少!三、组织:肠黏膜目的:WESTERN BLOT检测凋亡相关蛋白的表达应用TRIPURE提取蛋白质步骤:含蛋白质上清液中加入异丙醇:(1.5ml每1mlTRIPURE用量)倒转混匀,置室温10min离心:12000 g,10min,4度,弃上清加入0.3M盐酸胍/95%乙醇:(2ml每1mlTRIPURE用量)振荡,置室温20min离心:7500g,5 min,4度,弃上清重复0.3M盐酸胍/95%乙醇步2次沉淀中加入100%乙醇2ml充分振荡混匀,置室温20 min离心:7500g,5min,4度,弃上清吹干沉淀1%SDS溶解沉淀离心:10000g,10min,4度取上清-20度保存(或可直接用于WESTERN BLOT)存在的问题:加入1%SDS后沉淀不溶解,还是很大的一块,4度离心后又多了白色沉定,SDS结晶?测浓度,含量才1mg/ml左右。

植物蛋白质提取方法总汇一、植物组织蛋白质提取方法1、根据样品重量(1g 样品加入3.5ml 提取液,可根据材料不同适当加入),准备提取液放在冰上。
2、把样品放在研钵中用液氮研磨,研磨后加入提取液中在冰上静置(3-4 小时)。
3、用离心机离心8000rpm40min4 C或11100rpm20min4 °C4、提取上清液,样品制备完成。
蛋白质提取液:300ml1 、1Mtris-HCl (PH8)45ml2、甘油(Glycerol )75ml3、聚乙烯吡咯烷酮(Polyvinylpolypyrrordone )6g这种方法针对SDS-PAGE垂直板电泳!二、植物组织蛋白质提取方法氯醋酸—丙酮沉淀法1 、在液氮中研磨叶片2、加入样品体积3倍的提取液在-20 C的条件下过夜,然后离心(4 C 8000rpm以上1 小时)弃上清。
3、加入等体积的冰浴丙酮(含0.07%的3 -巯基乙醇),摇匀后离心(4C 8000rpm 以上1 小时),然后真空干燥沉淀,备用。
4、上样前加入裂解液,室温放置30 分钟,使蛋白充分溶于裂解液中,然后离心(15C 8000rpm以上1小时或更长时间以没有沉淀为标准),可临时保存在 4 C待用。
5、用Brandford法定量蛋白,然后可分装放入-80 C备用。
药品:提取液:含10%TCA和0.07%的3 -巯基乙醇的丙酮。
裂解液:2.7g尿素0.2gCHAPS 溶于3ml灭菌的去离子水中(终体积为5ml),使用前再加入1M的DTT65ul/ml。
这种方法针对双向电泳,杂质少,离子浓度小的特点!当然单向电泳也同样适用,只是电泳的条带会减少!三、组织:肠黏膜目的:WESTERN BLO检测凋亡相关蛋白的表达应用TRIPURE提取蛋白质步骤:含蛋白质上清液中加入异丙醇:(1.5ml每ImITRIPURE用量)倒转混匀,置室温10min离心:12000 g,10min,4 度,弃上清加入0.3M盐酸胍/95 %乙醇:(2ml每ImITRIPURE用量)振荡,置室温20min离心:7500g ,5 min ,4 度,弃上清重复0.3M 盐酸胍/95 %乙醇步2 次沉淀中加入100%乙醇2ml充分振荡混匀,置室温20 min离心:7500g ,5min,4 度,弃上清吹干沉淀1 % SDS溶解沉淀离心:10000g,10min ,4 度取上清-20 度保存(或可直接用于WESTERN BLO)T存在的问题:加入1%SDS后沉淀不溶解,还是很大的一块,4度离心后又多了白色沉定,SDS结晶?测浓度,含量才1mg/ml左右。

用200毫摩每升的tris-cl 和62.5毫摩每升的tris-cl,我们研究室一般用100毫摩每升的tris-cl,pH 8.0 .另外,最好加150毫摩每升的NaCl,用来分离以弱电荷结合到多糖上的蛋白。
2我提的蛋白难溶,请问怎么解决?1、请问这是为什么呢?怎么解决?2、溶解时是先在100℃沸水浴后在涡旋吗?3、涡旋时产生大量泡沫,对蛋白有影响吗?4、是在常温溶解还是在4℃?或-20℃?5、一般溶解需要多长时间?怎样才算溶解充分了?我也是做植物叶片的,建议你可以用TCA-丙酮沉淀,方法如下:1、在液氮中研磨叶片30min,加PVP,和石英砂2、加入样品体积3倍的提取液(丙酮溶液1)在-20℃的条件下过夜,然后离心(4℃10000rpm以上1小时)弃上清。
3. 每份加入9ml丙酮溶液II,捣碎沉淀,常温振动混匀,-20℃沉淀1h;10000rpm,4℃离心15min,弃上清.4. 每份加入9ml丙酮溶液II,常温振动混匀,-20℃沉淀1h;10000rpm,4℃离心15min,弃上清.5. 每份加入9ml 80%丙酮溶液III, 常温振动混匀,-20℃沉淀1h, 10000rpm,4℃离心15min,弃上清6.干燥成硬块,磨成粉磨-20℃保存待用。
第二个问题:37度水浴第三个问题:涡旋时产生大量泡沫,没有影响第四个问题:37度溶解第五个问题1个小时,中间混匀数次出现这种情况是很正常的,要是全部都溶了倒是不太正常。
用沉淀法浓缩蛋白都存在一个变性的问题,在具体的操作过程中,有一部分蛋白变性了,所以会不溶解。
操作的时候尽量保持低温!溶解的时候可以在常温下,蛋白变成粉末后,立即加1*SDS上样缓冲液,用加样器吹打,大约5分钟就好,可以用来进行下一步的实验了。
也可以在4度溶解过夜。
涡旋时产生大量泡沫,个人认为影响不大一般溶解半个小时就很充分了,但仍会有很多不溶物!可以离心弃掉!丙酮沉淀之后要干燥,这个过程一定不要时间太长,不然样品干燥得过了,就很难溶了。

提取细胞核蛋白的步骤:1.向培养细胞的平皿中加入少量(保证在1.5ml TUBE内能放下)冷PBS(或1*D-Hanks)2.,用细胞刮刀尽可能多的刮下细胞,收集到1.5ml的离心管中。
在预冷的离心机中,4度,1000rcf,1-3分钟,沉降细胞。
为尽可能多的获得细胞,可将一次离心后的上清再重复刮细胞一次;2. 将细胞重悬于cell lysis buffer中(加入体积106细胞/200uL,体积估计方法还是没确定,should be sufficient; 一般就是一个10cm平皿加1ml cell lysis buffer),添加蛋白酶抑制剂;先破细胞膜,得到细胞核(没有用B DOUNCE);冰上放置(不震荡,可偶尔用枪轻吹)30分钟至1小时(此时核膜没有破,有核染色为证),充分裂解;cell lysis buffer:5mM PIPES pH 8.0 85mM KCL, 0.5% NP40, 1% protein inhibitor;3. 4度,1000rcf,20分钟,上清为胞质蛋白(蛋白浓度比较低,如需要检测,建议先浓缩一下),沉淀为细胞核;此时可以将沉淀冻存于-70℃;4. 将沉淀重悬于100-200 ul nucleai lysis buffer(体积视目的蛋白表达丰度而定,一般50-100ul)中,添加蛋白酶抑制剂,冰上放置30分钟至1小时(每5分钟震荡一次),充分裂解;可以观察到沉淀慢慢消失,溶液变澄清;nucleai lysis buffer:成分同SDS lysis buffer;50mM Tris-Cl pH 8.1, 10mM EDTA, 1% SDS, 1% protein inhibitor;5. 四度,最大转速离心,10分钟以上(尽可能沉淀完全),上清即为细胞核蛋白;(此文档部分内容来源于网络,如有侵权请告知删除,文档可自行编辑修改内容,供参考,感谢您的配合和支持)编辑版word。

植物全蛋白提取方法:TCA丙酮沉淀法、Tris-HC1法、Trizol沉淀法提取法。
1 TCA丙酮沉淀法基于蛋白在酸或疏水条件下变性使蛋白浓缩并去除污染物原理的TCA丙酮沉淀法,最早用于小麦蛋白的提取,是目前提取植物蛋白的常用方法之一。
具有降低次生代谢物质的干扰、减少蛋白降解等优点。
TCA能有效地抑制蛋白酶对蛋白质的水解作用,保证在制样过程中蛋白质不被降解;丙酮溶液能除去样品中的酚类及色素等干扰物质,同时实验过程中采用的高速离心办法能较好地去除多糖的影响。
然而该方法的一个最大缺点是蛋白质很难重新溶解,而且样品中的非蛋白成分很难除去,可能会丢失膜蛋白和疏水性蛋白,导致2-DE图谱上有明显的横纵条纹。
在研磨样品时加入聚乙烯吡咯烷酮(PVP)或交联聚乙烯基吡咯烷酮(PVPP)用来吸附样品中富含的酚、醌类物质。
它们能通过疏水键与酚类形成复合物,离心可以去除该复合物。
然而,TCA丙酮沉淀法中与蛋白共沉淀的污染物在随后的有机溶剂清洗步骤中通常难以去除,可以通过振荡和延长蛋白沉淀在裂解缓冲液中温育时间的方法来增加蛋白的溶解能力。
在提取的过程中同时加入了TCA、β-巯基乙醇及DTT 3 种药剂可以更好的抑制蛋白质的水解及去除干扰物质。
TCA丙酮提取法耗时少且容易操作,一般作为植物蛋白提取的初始方案,该方法常用于幼嫩组织中蛋白的提取,对更为复杂的植物组织该方法并非最佳选择。
但该方法还是在植物蛋白的提取中占有重要位置,很多木本植物的样品应用该方法效果很好,如鹅掌楸叶片、巴东木莲的雌蕊柱头、槟榔叶片、银杏叶片及枝条、茶树叶片及芽、红豆杉的愈伤组织、石斛叶片等。
草本植物中的大豆叶片、生菜叶片、黄瓜叶片、番茄子叶、龙胆花芽、灰木相思叶片等应用该方法都获得了较清晰的2-DE图谱。
TCA protein precipitation protocolStock Solutions: 100% (w/v) Trichloroacetic acid (TCA)recipe: dissolve 500g TCA (as shipped) into 350 ml dH2O, store at RT.Precipitation Protocol:1. Add 1 volume of TCA stock to 4 volumes of protein sample.i.e. in 1.5ml tube with maximum vol., add 250µl TCA to 1.0ml sample.2. Incubate 10 min at 4°C.3. Spin tube in microcentrifuge at 14K rpm, 5 min.4. Remove supernatant, leaving protein pellet intact. Pellet should be formed from whitish,fluffy ppt.5. Wash pellet with 200µl cold acetone.6. Spin tune in microfuge at 14K rpm, 5min.7. Repeat steps 4-6 for a total of 2 acetone washes.8. Dry pellet by placing tube in 95°C heat block for 5-10 min to drive off acetone.9. For SDS-PAGE, add 2X or 4X sample buffer (with or without bME) and boil smaple for10 min in 95°C herat block before loading smaple onto polyacrylamide gel.2 Trizol沉淀法与TCA 丙酮沉淀法相比,Trizol沉淀蛋白质的方法可有效地除去色素、酚类等干扰电泳的化学物质,特别是对植物样品中高丰度蛋白——Rubisco1,5-二磷酸核酮糖羧化酶/加氧酶(Ribulose-1,5-bisphosphate carboxylase/oxygenase,通常简写为RuBisCO)。

一、植物组织蛋白质提取方法1、根据样品重量(1g样品加入3.5ml提取液,可根据材料不同适当加入),准备提取液放在冰上。
2、把样品放在研钵中用液氮研磨,研磨后加入提取液中在冰上静置(3-4小时)。
3、用离心机离心8000rpm40min4℃或11100rpm20min4℃4、提取上清液,样品制备完成。
蛋白质提取液:300ml1、1Mtris-HCl(pH8)45ml2、甘油(Glycerol)75ml3、聚乙烯吡咯烷酮(Polyvinylpolypyrrordone)6g这种方法针对SDS-PAGE,垂直板电泳!二、植物组织蛋白质提取方法氯醋酸―丙酮沉淀法1、在液氮中研磨叶片2、加入样品体积3倍的提取液在-20℃的条件下过夜,然后离心(4℃8000rpm以上1小时)弃上清。
3、加入等体积的冰浴丙酮(含0.07%的β-巯基乙醇),摇匀后离心(4℃8000rpm以上1小时),然后真空干燥沉淀,备用。
4、上样前加入裂解液,室温放置30分钟,使蛋白充分溶于裂解液中,然后离心(15℃8000rpm以上1小时或更长时间以没有沉淀为标准),可临时保存在4℃待用。
5、用Brandford法定量蛋白,然后可分装放入-80℃备用。
药品:提取液:含10%TCA和0.07%的β-巯基乙醇的丙酮。
裂解液:2.7g 尿素0.2gCHAPS溶于3ml灭菌的去离子水中(终体积为5ml),使用前再加入1M的DTT65μl/ml。
这种方法针对双向电泳,杂质少,离子浓度小的特点!当然单向电泳也同样适用,只是电泳的条带会减少!三、组织:肠黏膜目的:WESTERN BLOT检测凋亡相关蛋白的表达应用TRIPURE提取蛋白质步骤:含蛋白质上清液中加入异丙醇:(1.5ml每1mlTRIPURE用量)倒转混匀,置室温10min离心:12000 g,10min,4度,弃上清加入0.3M盐酸胍/95%乙醇:(2ml每1mlTRIPURE用量)振荡,置室温20min离心:7500g,5 min,4度,弃上清重复0.3M盐酸胍/95%乙醇步2次沉淀中加入100%乙醇2ml充分振荡混匀,置室温20 min离心:7500g,5min,4度,弃上清吹干沉淀1%SDS溶解沉淀离心:10000g,10min,4度取上清-20度保存(或可直接用于WESTERN BLOT)存在的问题:加入1%SDS后沉淀不溶解,还是很大的一块,4度离心后又多了白色沉定,SDS结晶?测浓度,含量才1mg/ml左右。
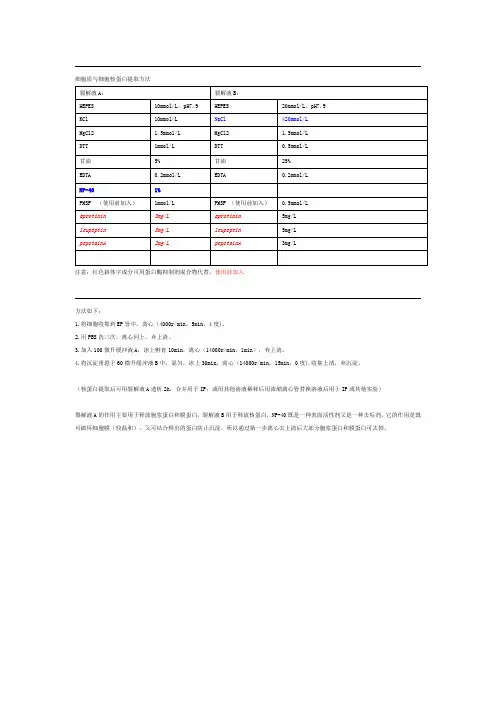
细胞质与细胞核蛋白提取方法
注意:红色斜体字成分可用蛋白酶抑制剂混合物代替,使用前加入
方法如下:
1.将细胞收集到EP管中,离心(4000r/min,5min,4度)。
2.用PBS洗三次,离心同上,弃上清。
3.加入100微升缓冲液A,冰上孵育10min,离心(14000r/min,1min),弃上清。
4.将沉淀重悬于60微升缓冲液B中,混匀,冰上30min,离心(14000r/min,15min,0度),收集上清,弃沉淀。
(核蛋白提取后可用裂解液A透析2h,合并用于IP;或用其他溶液稀释后用浓缩离心管替换溶液后用于IP或其他实验)
裂解液A的作用主要用于释放胞浆蛋白和膜蛋白,裂解液B用于释放核蛋白,NP-40既是一种表面活性剂又是一种去垢剂,它的作用是既可破坏细胞膜(较温和),又可结合释出的蛋白防止沉淀,所以通过第一步离心去上清后大部分胞浆蛋白和膜蛋白可去掉。


植物蛋白质提取方法总汇一、植物组织蛋白质提取方法1、根据样品重量(1g样品加入3.5ml提取液,可根据材料不同适当加入),准备提取液放在冰上。
2、把样品放在研钵中用液氮研磨,研磨后加入提取液中在冰上静置(3-4小时)。
3、用离心机离心8000rpm40min4℃或11100rpm20min4℃4、提取上清液,样品制备完成。
蛋白质提取液:300ml1、1Mtris-HCl(PH8)45ml2、甘油(Glycerol)75ml3、聚乙烯吡咯烷酮(Polyvinylpolypyrrordone)6g这种方法针对SDS-PAGE,垂直板电泳!二、植物组织蛋白质提取方法氯醋酸—丙酮沉淀法1、在液氮中研磨叶片2、加入样品体积3倍的提取液在-20℃的条件下过夜,然后离心(4℃8000rpm以上1小时)弃上清。
3、加入等体积的冰浴丙酮(含0.07%的β-巯基乙醇),摇匀后离心(4℃8000rpm以上1小时),然后真空干燥沉淀,备用。
4、上样前加入裂解液,室温放置30分钟,使蛋白充分溶于裂解液中,然后离心(15℃8000rpm以上1小时或更长时间以没有沉淀为标准),可临时保存在4℃待用。
5、用Brandford法定量蛋白,然后可分装放入-80℃备用。
药品:提取液:含10%TCA和0.07%的β-巯基乙醇的丙酮。
裂解液:2.7g尿素0.2gCHAPS 溶于3ml灭菌的去离子水中(终体积为5ml),使用前再加入1M的DTT65ul/ml。
这种方法针对双向电泳,杂质少,离子浓度小的特点!当然单向电泳也同样适用,只是电泳的条带会减少!三、组织:肠黏膜目的:WESTERN BLOT检测凋亡相关蛋白的表达应用TRIPURE提取蛋白质步骤:含蛋白质上清液中加入异丙醇:(1.5ml每1mlTRIPURE用量)倒转混匀,置室温10min离心:12000 g,10min,4度,弃上清加入0.3M盐酸胍/95%乙醇:(2ml每1mlTRIPURE用量)振荡,置室温20min离心:7500g,5 min,4度,弃上清重复0.3M盐酸胍/95%乙醇步2次沉淀中加入100%乙醇2ml充分振荡混匀,置室温20 min离心:7500g,5min,4度,弃上清吹干沉淀1%SDS溶解沉淀离心:10000g,10min,4度取上清-20度保存(或可直接用于WESTERN BLOT)存在的问题:加入1%SDS后沉淀不溶解,还是很大的一块,4度离心后又多了白色沉定,SDS结晶?测浓度,含量才1mg/ml左右。

细胞核蛋白分离提取方法
1.将培养皿内的培养基倒去,用预冷的1xPBS洗两遍后,每盘加入
2.5ml1xPBS,放在冰上;
2.用细胞刮讲细胞刮下,移至15ml离心管,再用2.5ml1xPBS清洗培养皿一次,共5ml;
3.1500g离心5min,倒去上清,移入1.5ml离心管中,再每管加入800ul1xPBS清洗一次;
4.每管加入低渗bufferA(1M HEPES,1M KCL,100mMEDTA,100mM EGTA)(buffer:蛋白酶抑制剂:1M DTT=1000:10:1)200ul(原500ul),冰上静置15min裂解;
5.每管加入25ul 10%NP-40,涡旋10s;
6.1500g4℃离心10min,上清为细胞质蛋白,收集至新的离心管中;
7.每管加入500ul bufferA清洗沉淀,离心速度约2000g;
8.每管加入RIPA buffer(buffer:蛋白酶抑制剂:1M DTT=1000:10:1)50ul,吹散沉淀颗粒,4℃震荡15min,其间每隔5min重新吹散一次,使其充分裂解;
9.14000rpm4℃离心15min,上清为细胞核蛋白,收集至新离心管中。

植物蛋白质提取关键点:a、种子研磨充分 b、蛋白质尽量溶解 c、蛋白质尽量沉淀所需药品:NaCl、C2H5OH、(NH4)2SO4、NaOH、H Cl、CH3COOH﹑Na2SO4﹑冰水注:Na2SO4,芒硝,禁与强酸、铝、镁相配。
药品溶解度:NaCl,36g[20℃]; (NH4)2SO4,76.7g[25℃]; Na2SO4, 19.5g[20℃]其中溶解蛋白质的常用中性盐是NaCl、(NH4)2SO4、Na2SO4、Mg2SO4等①、盐析法﹕原理:蛋白质在水溶液中的溶解度取决于蛋白质分子表面离子周围的水分子数目,亦即主要是由蛋白质分子外周亲水基团与水形成水化膜的程度以及蛋白质分子带有电荷的情况决定的。
蛋白质溶液中加入中性盐后,由于中性盐与水分子的亲和力大于蛋白质,致使蛋白质分子周围的水化层减弱乃至消失。
同时,中性盐加入蛋白质溶液后由于离子强度发生改变,蛋白质表面的电荷大量被中和,更加导致蛋白质溶解度降低,之后蛋白质分子之间聚集而沉淀。
由于各种蛋白质在不同盐浓度中的溶解度不同,不同饱和度的盐溶液沉淀的蛋白质不同,从而使之从其他蛋白中分离出来。
简单的说就是将硫酸铵、硫化钠或氯化钠等加入蛋白质溶液,使蛋白质表面电荷被中和以及水化膜被破坏,导致蛋白质在水溶液中的稳定性因素去除而沉淀。
步骤:溶解蛋白质→离心→取上清液,盐析(低温)→离心沉淀蛋白质→透析②﹑等电点法(本方法中最好不要用Na2SO4):原理:在等电点时,蛋白质分子以两性离子形式存在,其分子净电荷为零(即正负电荷相等),此时蛋白质分子颗粒在溶液中因没有相同电荷的相互排斥,分子相互之间的作用力减弱,其颗粒极易碰撞、凝聚而产生沉淀,所以蛋白质在等电点时,其溶解度最小,最易形成沉淀物。
等电点时的许多物理性质如黏度、膨胀性、渗透压等都变小,从而有利于悬浮液的过滤。
步骤:溶解蛋白质→离心→取上清液,调节PH,析出蛋白质→离心沉淀蛋白质→ 透析③、有机溶剂法:原理:有机溶剂能降低溶液的电解常数,从而增加蛋白质分子上不同电荷的引力,导致溶解度的降低;另外,有机溶剂与水的作用,能破坏蛋白质的水化膜,故蛋白质在一定浓度的有机溶剂中的溶解度差异而分离的方法,称“有机溶剂分段沉淀法”,它常用于蛋白质或酶的提纯。
植物组织蛋白质提取方法•相关推荐植物组织蛋白质提取方法用200毫摩每升的tris-cl 和62.5毫摩每升的tris-cl,我们研究室一般用100毫摩每升的tris-cl,pH 8.0 .另外,最好加150毫摩每升的NaCl,用来分离以弱电荷结合到多糖上的蛋白。
2我提的蛋白难溶,请问怎么解决?1、请问这是为什么呢?怎么解决?2、溶解时是先在100℃沸水浴后在涡旋吗?3、涡旋时产生大量泡沫,对蛋白有影响吗?4、是在常温溶解还是在4℃?或-20℃?5、一般溶解需要多长时间?怎样才算溶解充分了?我也是做植物叶片的.,建议你可以用TCA-丙酮沉淀,方法如下:1、在液氮中研磨叶片30min,加PVP,和石英砂2、加入样品体积3倍的提取液(丙酮溶液1)在-20℃的条件下过夜,然后离心(4℃10000rpm以上1小时)弃上清。
3. 每份加入9ml丙酮溶液II,捣碎沉淀,常温振动混匀,-20℃沉淀1h;10000rpm,4℃离心15min,弃上清.4. 每份加入9ml丙酮溶液II,常温振动混匀,-20℃沉淀1h;10000rpm,4℃离心15min,弃上清.5. 每份加入9ml 80%丙酮溶液III, 常温振动混匀,-20℃沉淀1h, 10000rpm,4℃离心15min,弃上清6.干燥成硬块,磨成粉磨-20℃保存待用。
第二个问题:37度水浴第三个问题:涡旋时产生大量泡沫,没有影响第四个问题:37度溶解第五个问题1个小时,中间混匀数次出现这种情况是很正常的,要是全部都溶了倒是不太正常。
用沉淀法浓缩蛋白都存在一个变性的问题,在具体的操作过程中,有一部分蛋白变性了,所以会不溶解。
操作的时候尽量保持低温!溶解的时候可以在常温下,蛋白变成粉末后,立即加1*SDS上样缓冲液,用加样器吹打,大约5分钟就好,可以用来进行下一步的实验了。
也可以在4度溶解过夜。
涡旋时产生大量泡沫,个人认为影响不大一般溶解半个小时就很充分了,但仍会有很多不溶物!可以离心弃掉!丙酮沉淀之后要干燥,这个过程一定不要时间太长,不然样品干燥得过了,就很难溶了。
植物蛋白质提取方法总汇一、植物组织蛋白质提取方法1、根据样品重量(1g样品加入3.5ml提取液,可根据材料不同适当加入),准备提取液放在冰上。
2、把样品放在研钵中用液氮研磨,研磨后加入提取液中在冰上静置(3-4小时)。
3、用离心机离心8000rpm40min4℃或11100rpm20min4℃4、提取上清液,样品制备完成。
蛋白质提取液:300ml1、1Mtris-HCl(PH8) 45ml2、甘油(Glycerol)75ml3、聚乙烯吡咯烷酮(Polyvinylpolypyrrordone)6g这种方法针对SDS-PAGE,垂直板电泳!二、植物组织蛋白质提取方法氯醋酸—丙酮沉淀法1、在液氮中研磨叶片2、加入样品体积3倍的提取液在-20℃的条件下过夜,然后离心(4℃8000rpm以上1小时)弃上清。
3、加入等体积的冰浴丙酮(含0.07%的β-巯基乙醇),摇匀后离心(4℃8000rpm以上1小时),然后真空干燥沉淀,备用。
4、上样前加入裂解液,室温放置30分钟,使蛋白充分溶于裂解液中,然后离心(15℃8000rpm 以上1小时或更长时间以没有沉淀为标准),可临时保存在4℃待用。
5、用Brandford法定量蛋白,然后可分装放入-80℃备用。
药品:提取液:含10%TCA和0.07%的β-巯基乙醇的丙酮。
裂解液:2.7g尿素0.2gCHAPS 溶于3ml灭菌的去离子水中(终体积为5ml),使用前再加入1M的DTT65ul/ml。
这种方法针对双向电泳,杂质少,离子浓度小的特点!当然单向电泳也同样适用,只是电泳的条带会减少!三、组织:肠黏膜目的:WESTERN BLOT检测凋亡相关蛋白的表达应用TRIPURE提取蛋白质步骤:含蛋白质上清液中加入异丙醇:(1.5ml每1mlTRIPURE用量)倒转混匀,置室温10min离心:12000 g,10min,4度,弃上清加入0.3M盐酸胍/95%乙醇:(2ml每1mlTRIPURE用量)振荡,置室温20min离心: 7500g,5 min,4度,弃上清重复0.3M盐酸胍/95%乙醇步2次沉淀中加入100%乙醇 2ml充分振荡混匀,置室温20 min离心: 7500g,5min,4度,弃上清吹干沉淀1%SDS溶解沉淀离心:10000g,10min,4度取上清-20度保存(或可直接用于WESTERN BLOT)存在的问题:加入1%SDS后沉淀不溶解,还是很大的一块,4度离心后又多了白色沉定,SDS结晶?测浓度,含量才1mg/ml左右。
植物膜蛋白提取方法说实话植物膜蛋白提取这事,我一开始也是瞎摸索。
我试过超声破碎法来提取。
就像敲鸡蛋,想把里头的东西弄出来那种感觉。
把植物组织放在缓冲液里,然后用超声仪来破碎细胞。
可是我发现这种法子很容易把膜也给弄破喽,得到的膜蛋白纯度不咋高,好多其他乱七八糟的东西都混进去了。
这就好比炒菜的时候把不该放的调料都倒进去了,最后味道全乱套了。
后来呢,我又尝试了差速离心法。
这就像挑豆子,把大的小的分开那样。
先把植物组织破碎后,通过不同的离心速度把细胞器啊什么的和膜蛋白分离开。
开始的时候我老是掌握不好离心速度和时间,要么离心速度不够,那些东西分不开,要么就是离心太久了,把想要的膜蛋白都给弄丢了一部分。
经过好多次的尝试,我才慢慢摸准了一点规律。
比如说,先低速度短时间离心去掉那些大的残渣,然后再逐步提高离心速度和延长时间来纯化膜蛋白。
我有段时间还听别人说密度梯度离心法好使。
这方法有点像从水里分层捞东西。
就是用不同浓度的溶液形成一个密度梯度,然后离心,让膜蛋白在适合它密度的那个层面停下来,这样和其他物质分离开。
但是这个方法操作起来比较麻烦,各种溶液的配制就要很精确,我就老在这上面出错,溶液配不对后续根本得不到像样的结果。
还有就是用化学试剂来提取。
比如说表面活性剂。
这就跟用清洁剂去油污有点像,表面活性剂能把膜蛋白从细胞膜上给“扒拉”下来。
不过这化学试剂的种类和浓度可得选好了,选错了就像洗衣粉放太多把衣服都洗坏了似的,膜蛋白的活性啥的就全没了。
我就在选择表面活性剂的种类和浓度上栽过跟头,试了好多种,结果都不理想,不是蛋白没有提取出来就是提取出来的蛋白变性了失去活性了。
如果是新手上路的话,我觉得差速离心法可以先试试,毕竟相对来说比较直白一点,虽然可能会碰到不少问题,但是在调整离心速度和时间的过程中可以慢慢学习。
可千万别像我刚开始的时候,只知道按照书上的数值来,实际情况和书上可能有差别,要多做尝试才行。
在操作的全过程里,实验设备的清洁也很重要。
核蛋白提取方法
以下是 8 条关于核蛋白提取方法的内容:
1. 嘿,你知道吗?核蛋白提取就像是一场精细的寻宝游戏!比如说,你要从一堆复杂的细胞混合物中准确找到那个珍贵的核蛋白。
想象一下,拿着小工具一点点去探索、挖掘,那可真是个挑战呢!
2. 哇塞,核蛋白提取可得小心谨慎呀!就如同在小心翼翼地构建一座精美的城堡,稍有不慎可能就全塌了。
就像那次我和小伙伴一起做实验,一点小疏忽,哎呀,前功尽弃啦!
3. 核蛋白提取这事儿啊,真不是随随便便就能搞定的!这就好比登山,爬得越高越难,但到达山顶看到的风景也越美呀!当成功提取出核蛋白的那一刻,那种成就感,简直无与伦比!
4. 嘿呀,核蛋白提取可不能马虎哦!这简直跟解一道超级复杂的谜题一样,每一个步骤都要仔细思考。
有次我们做到一半才发现之前有个地方弄错了,这不是让人哭笑不得嘛!
5. 核蛋白提取啊,就像是在茫茫大海中寻找那根特定的针!困难重重但又让人充满斗志。
我曾经看到别人做成功后开心的样子,哇,我也发誓一定要搞定!
6. 啊哟喂,核蛋白提取这工作可不容易啊!它就像一场激烈的比赛,和那些复杂因素竞争。
有次朋友在提取时遇到难题,那着急上火的样子,我现在都还记得呢!
7. 核蛋白提取呀,这可是个技术活!好比雕琢一件艺术品,得精心打磨每一个细节。
我们一起做实验时都会互相提醒,生怕出一点纰漏呢!
8. 核蛋白提取绝对不是轻松的事儿,但只要掌握方法,也就没那么难啦!就像划船过河,一开始觉得很难,等熟练了就能轻松到达对岸啦。
所以,大家别害怕,大胆去尝试呀!
我的观点结论:核蛋白提取虽然有难度,但只要我们认真对待,仔细钻研,就一定能够成功提取出核蛋白!。