高等有机化学习题(1)
- 格式:doc
- 大小:426.00 KB
- 文档页数:4

高职有机化学试题及答案一、选择题(每题2分,共20分)1. 以下哪种化合物属于芳香烃?A. 甲烷B. 乙炔C. 苯D. 乙醇答案:C2. 有机化学中,一个碳原子最多可以形成多少个共价键?A. 2B. 3C. 4D. 5答案:C3. 以下哪个反应是加成反应?A. 酯化反应B. 消去反应C. 取代反应D. 氧化反应答案:B4. 以下哪种物质是高分子化合物?A. 葡萄糖B. 蛋白质C. 水D. 甲醇答案:B5. 以下哪种化合物是手性分子?A. 乙醇B. 甲醇C. 丙醇D. 丁醇答案:D6. 以下哪个是有机反应的催化剂?A. 硫酸B. 硝酸C. 盐酸D. 氢氧化钠答案:A7. 以下哪种化合物含有碳碳双键?A. 甲烷B. 乙烷C. 乙烯D. 乙炔答案:C8. 以下哪种物质是天然高分子化合物?A. 聚氯乙烯B. 聚苯乙烯C. 纤维素D. 聚丙烯答案:C9. 以下哪种反应是消除反应?A. 酯化反应B. 水解反应C. 消去反应D. 取代反应答案:C10. 以下哪种化合物是氨基酸?A. 葡萄糖B. 甘油C. 丙氨酸D. 尿素答案:C二、填空题(每空2分,共20分)11. 有机化学中,碳原子的价电子数是________。
答案:412. 芳香族化合物通常含有一个或多个________环。
答案:苯13. 一个碳原子最多可以连接________个氢原子。
答案:414. 有机化学反应中,催化剂的作用是________。
答案:加速反应速率15. 一个有机分子中,如果存在四个不同的基团连接到同一个碳原子上,这种碳原子称为________。
答案:手性中心16. 有机化学中,取代反应是指一个原子或原子团被另一个原子或原子团________。
答案:取代17. 有机化学中,酯化反应是指醇与________反应生成酯和水。
答案:酸18. 有机化学中,消去反应是指有机分子在一定条件下失去小分子(如水、卤化氢等),生成________。
答案:不饱和化合物19. 有机化学中,高分子化合物是指相对分子质量在________以上的有机化合物。

高等有机化学试题及答案文库高等有机化学试题及答案文库________________________________高等有机化学是一门重要的理论和应用结合的科学,它不仅是药物研究的基础,而且也是重要的工业原料和产品制造工艺的基础。
对于初学者来说,需要通过不断的练习来巩固学习成果。
一、有机化学试题及解析1、下列关于有机物分子式正确的是()A、乙烯C2H2B、乙醇CH2OHC、乙醛CH2OD、乙酸C2H3O2正确答案:A、B、C、D2、下列关于构象正确的是()A、乙烯具有均相异构象B、乙醇具有对映异构象C、乙醛具有对映同构象D、乙酸具有均相同构象正确答案:A、B、C3、下列关于有机物的反应性正确的是()A、甲醛可以通过加氢反应得到甲醇B、乙醛可以通过加氢反应得到乙醇C、丙酸可以通过加氢反应得到丙醇D、甲酸可以通过加氢反应得到乙醇正确答案:A、B、C4、下列关于有机物的性质正确的是()A、甲醛是一种无色气体B、乙醇是一种清澈无色液体C、丙酸是一种混浊的无色液体D、甲酸是一种无色固体正确答案:A、B、D二、有机化学试题及解析进阶1、下列关于芳香族化合物正确的是()A、苯可以与甲酸反应得到对甲苯胺B、乙醛可以通过氧化反应得到甲醛C、苯乙酮可以与甲酸反应得到对甲基苯胺D、苯乙酮可以通过氧化反应得到乙醛正确答案:A、C2、下列关于芳香族化合物性质正确的是()A、苯是一种无色气体B、乙醇是一种清澈无色液体C、苯乙酮是一种混浊的无色液体D、对甲基苯胺是一种无色固体正确答案:A、C、D3、下列关于有机物的合成方法正确的是()A、甲基胺可以通过Fischer-Tropsch合成法合成B、乙酸可以通过Friedel-Crafts反应合成C、甲基胺可以通过Friedel-Crafts反应合成D、乙酸可以通过Fischer-Tropsch合成法合成正确答案:B、C4、下列关于有机物的催化剂正确的是()A、甲基胺合成所需要的催化剂是金属钴B、乙酸合成所需要的催化剂是金属银C、甲基胺合成所需要的催化剂是金属铜D、乙酸合成所需要的催化剂是金属钛正确答案:A、B三、有机化学实验室实践1、下列实验室中常用仪器正确的是()A、真空泵B、真空测定仪C、气体流量计D、真空干燥仪E、真空分子泵F、气体分析仪G、浊度仪正确答案:A、B、C、D、E、F2. 下列实验室中常用试剂正确的是()A. 硝酸盐试剂B. 氢氧化物试剂C. 碘试剂D. 过氧化物试剂正确答案:A, B, C, D。


⾼等有机化学习题⾼等有机化学习题第⼀章化学键⼀、⽤共振轮说明下列问题1)联本中的C 1-C 2键长为什么⽐⼄烷中的键长短?联苯的硝化反应为什么主要发⽣在2-位和4-位?联苯的共振结构式可表是如下:(1)由共振结构式可以看出C 1-C 2键有双键结构的贡献,故⽐⼄烷的C 1-C 2键短。
(2)由共振结构式可以看出邻对位负电荷相对集中,故有利于发⽣硝化反应。
2)⽅酸为什么是强酸?(强于硫酸)⽅酸的共振结构式可表是如下:对吗?由⽅酸的共振结构式可以看出⽅酸的电⼦离域效果更好。
⼆、试推测6,6-⼆苯基富烯的亲电取代发⽣于哪个环,哪个位置?亲核取代发⽣于哪个环,哪个位置?6,6-⼆苯基富烯的共振式如下:由6,6-⼆苯基富烯的共振式可以看出,亲电取代发⽣在五元环的2位上,⽽亲核取代发⽣在苯环的2位上。
三、计算烯丙基正离⼦和环丙烯正离⼦π分⼦轨道的总能量,并⽐较两者的稳定性。
烯丙基正离⼦有两个电⼦在成键轨道上其总能量为 E 烯丙基正离⼦=2E 1=2(α+1.414β)=2α+2.828β11'OH OOO OO HOOOO HO OOH OOO O S O OH OOS OO O H O S O O O HOS O O OH环丙烯正离⼦有两个电⼦在成键轨道上其总能量为E 环丙烯正离⼦=2E 1=2(α+2β)=2α+2β能量差值为E 烯丙基正离⼦- E 环丙烯正离⼦=(2α+2.828β)- (2α+2β)=0.828β因此,环丙烯正离⼦⽐烯丙基正离⼦稳定。
四、⽤HMO 法分别说明烯丙基负离⼦和环丙烯负离⼦的电⼦排布和成键情况,并⽐较两者稳定性。
五、简要说明1)吡咯和吡啶分⼦的极性⽅向相反,为什么?吡咯分⼦中氮原⼦给出⼀对为共⽤电⼦参与了共轭分⼦的⼤π键,也就是电⼦从氮原⼦流向五员环,⽽吡啶分⼦中氮原⼦只拿出⼀个电⼦参与共轭,并且氮原⼦的电负性⼤于碳原⼦使电⼦流向氮原⼦的⽅向。
因此,两个分⼦的极性正好相反。


《高等有机化学高等有机化学》》例题及详解例11 试解释为什么氯甲烷的极性大于氯苯的极性。
CH3Cl>Clµ = 1.86 D (气态)µ = 1.70 D (气态)解:原因在于CH3Cl中只有-I s效应存在,而在PhCl中同时有p-π共轭效应和-I s 效应存在,且p-π共轭效应与-I s效应方向相反,导致PhCl的偶极矩小于CH3Cl。
ClCH另外,PhCl中C-Cl键的偶极矩方向和CH3Cl分子中的偶极矩方向一样,均是由C→Cl,故可以得出这样的结论,在氯苯分子中,σ键电子在很大程度上向Cl偏移,且要比由于Cl原子的未共用p电子对苯环共轭所引起的向苯环的p电子偏移要大。
例2 试解释下列化合物的偶极矩差别原因:1.CH2=CH-CH=O > CH3CH2CH=O(µ=2.88D) (µ=2.49D)2.CH3CH2-Cl > CH2=CH-Cl(µ=2.05D) (µ=1.66D)解:1.丙烯醛中主要为+C效应;丙醛中主要为+Is效应。
2.氯乙烷中主要为-Is 效应,氯乙烯中则同时存在+C效应与-Is效应。
例33 从下列反应的相对速率数据,可得出什么结论?R CH2Br+N R H2C N BrR H CH3CH2CH3(CH3)2CH (CH3)3C相对速率 1 1.66 1.48 1.34 1.35 解:从表中数据可知,当R为供电基时,反应较快,如果仅考虑+Is效应,则无法解释这一结果。
实际上,此处起主要作用的是R与苯环的σ-π超共轭效应。
由于CH3的C-H键最多,故其σ-π超共轭效应最强,而(CH3)3C最弱,这样就较好地揭示了上述现象。
例44 试解释下列化合物的碱性大小顺序: N(CH 3)2N,N-二甲基苯胺(pKa = 5.06)<N苯并奎宁环(pKa = 7.79)N <奎宁环(pKa = 10.58)解:在N,N-二甲基苯胺中由于p-π共轭,导致N 原子上电子云密度下降,碱性最小。

⾼等有机化学课后习题第⼀章习题1. ⽤共振式说明苯甲醚分⼦中甲氧基的邻/对位效应。
2. ⽐较下列各组化合物的酸性⼤⼩并予以解释。
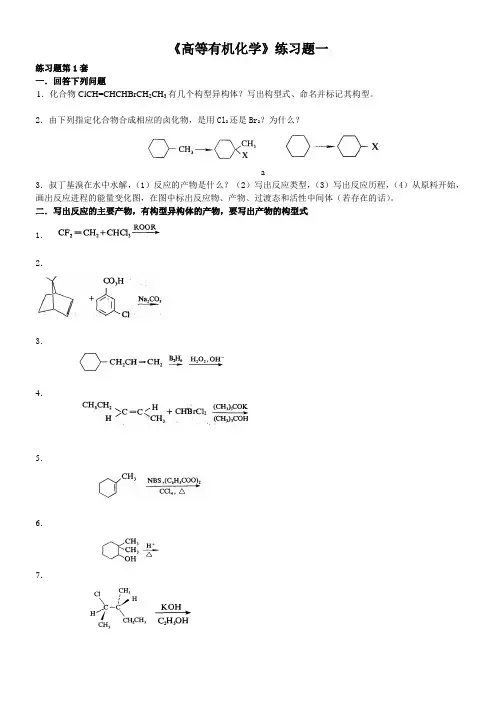
(1) HOCH2CH2COOH 和CH3CH(OH)COOH (2)⼄酸、丙⼆酸、⼄⼆酸和甲酸(3) COOHNO 2和COOHHO(4)H 2C CH 2H 3C CH 3HC CH 、和3. ⽐较碱性。
H 2N(1) CH 3CH 2NH 2 和(2)NH 2HO NH 2O 2N和(3)N HN和⽐较C-Br 键断裂的难易次序和CH 3CH 2CHCH 2CH 3CH 3OCHCH 2CH 3CH 3CH 2CHCF 2CF 3在极性条件下,、4.5. 下列共振式哪⼀个贡献⼤,为什么?C C C C OAB6. 在亲核加成反应中ArCH 2COR 和ArCOR 哪⼀个活性⾼,为什么?7. 解释酸性⼤⼩。
COOH<COOH(1)COOH COOH(2)>8. 为什么ArCOR 被HI 断裂时,得到的产物是RI 和ArOH ,⽽不是ROH 和ArI 。
9. 下列反应中⼏乎不会⽣成PhCH 2CBr(CH 3)2,为什么?PhCH 2CH(CH 3)2 + Br 2 PhCHBrCH(CH 3)2 + HBr10. ⽐较拗CH 3COCH 2COCH 3和CH 3COCH 2COOC 2H 5的酸性,并简要说明原因。
11. 为什么胺的碱性⼤于酰胺?12. 羧酸及其衍⽣物的亲核取代反应活性为什么是RCOCl>(RCO)2O>RC OOR’~RCOOH>RCONH 2。
13.为什么顺丁烯⼆酸的p K a1⽐反丁烯⼆酸⼩,p K a2却正相反?14. 排列下列化合物与HCN反应的活性顺序。
NO2CHO(H3C)2N CHOCHO CHOCl(1)(2)(3)(4)15. 五元杂环⽐苯更易进⾏亲电取代,为什么?第⼆章习题1. 2-丁烯的顺反异构体,分别经稀、冷、碱性KMnO4⽔溶液氧化后,为什么⽣成的2,3-丁⼆醇都不能测出旋光度?2. (R)-CH3CH2CH2CHDI在丙酮NaI溶液中共热,试解释下属现象,①化合物外消旋化;②有过量NaI128存在下,外消旋化速度是同位素交换的两倍;3. 请根据下述现象,为反应H2C CH OC2H5 + H2O C2H5OH + CH3CHO提出反应机理:(1)该反应符合普通的酸催化反应.(2)⽔解反应速度在⽔中⽐在重⽔中快1.9倍.(3)如果⽤同位素标记的⽔进⾏⽔解,所得⼄醇不含18O.(4)若在D2O中进⾏⽔解,只在⼄醛中出现⼀个D.第4章习题1.完成下列反应。

高等有机化学试题及答案一、选择题(每题2分,共20分)1. 下列哪个反应不是亲核取代反应?A. 醇的硫酸酯化B. 格氏试剂与醛酮的加成C. 卤代烃的水解D. 羟醛缩合反应答案:B2. 以下哪个化合物不能发生E1反应?A. 2-丁醇B. 1-丁醇C. 3-戊醇D. 2-戊醇答案:B3. 以下哪个化合物具有芳香性?A. 环己烯B. 苯C. 环戊二烯D. 环丁烯答案:B4. 以下哪个反应属于消除反应?A. 醇的脱水B. 酯的水解C. 卤代烃的氢化D. 醛的氧化答案:A5. 以下哪个化合物是手性分子?A. 乙烯B. 环己烷C. 2-丁醇D. 丙酮答案:C6. 以下哪个反应是自由基反应?A. 羟醛缩合B. 格氏试剂与醛酮的加成C. 卤代烃的自由基取代D. 酯化反应答案:C7. 以下哪个化合物是烯醇?A. 苯酚B. 乙醇C. 丙酮D. 丙烯答案:D8. 以下哪个反应是亲电加成反应?A. 氢氧化钠与卤代烃的反应B. 卤代烃的水解C. 溴与烯烃的加成D. 格氏试剂与醛的反应答案:C9. 以下哪个化合物是芳香族化合物?A. 环己酮B. 苯酚C. 环己醇D. 环己烷答案:B10. 以下哪个化合物是炔烃?A. 乙烯B. 乙炔C. 丙烯D. 丙烷答案:B二、填空题(每空2分,共20分)11. 有机化合物的命名通常遵循______的规则。
答案:IUPAC12. 亲核取代反应中,亲核试剂首先______被取代基团。
答案:攻击13. E2反应中,离去基团与亲核试剂的离去是______的。
答案:协同14. 芳香性化合物通常具有______个π电子。
答案:4n+215. 手性分子是指具有______的分子。
答案:非超posable镜像16. 烯醇是烯烃的______形式。
答案:烯醇式17. 自由基反应的特点是反应过程中存在______。
答案:自由基18. 亲电加成反应中,亲电试剂首先______不饱和键。
答案:攻击19. 芳香族化合物是指含有苯环的______化合物。
高等有机化学习题参考答案(注:本答案仅供参考,错误和不足之处敬请指正)Chapter 1 Effect of Substituted in Organic molecule1. 试判断下列各对基团,那一个具有强的-I 效应(即强的吸电子诱导效应): 答案:(1) -COOH > -COO -(2) C HN O CH 3<C H N N(CH 3)2CH 3+(3) C OCH 3 > C CH 2CH 3, (4) SO 2H <SO 3H 1(5) OCH 3 > SCH 3 (6) C H C H CH 3 <C C CH 3(7) N (CH 3)2 > P(CH 3)2(8) Si(CH 3)3 <Si(CH 3)2(9)N(CH 3)3+>NH 2 (10) CN > CH 2NH 2 (11) SiCH 3 <Cl(12) C C CH 3 , >C H C H CH 3与(6)同(13)>(14) NO 2>NO 2(15)O 2SCH 3<O 2SBr2. 指出下列各对酸中哪一个酸性强 答案:(1) H 3NCH 2CH 2COOH > HOCH 2CH 2COOH (2) HC C COOH >H 2C C H COOH(3) C 6H 5COCH 2COOH > C 6H 5CHOHCH 2COOH(4)C 4H 9CHCOOCOOH n<CCCH 3CH 3CH 3CH 3COOHOOC分子内氢键(5)COOHOH > COOH OH分子内氢键(6) BrCH 2CH 2COOH < CH 3CHBrCOOH(7)(H 3C)2CH 2CHCOOH>H 2CC HCH 2COOH(8) HC C COOH > SCOOH(9) CH 2(COOH)2 >HOOCH C COOCl(10) CH 3OCH 2CH 2COOH < CH 3SCH 2CH 2COOH 分子内氢键 (11) CH 3SCH 2COOH < CH 3SO 2COOH(12)OHCCOOH>COOHCHO(13)OHC(CH 3)3(H 3C)3C<OHC(CH 3)3CH 3(H 3C)3C(14) H 3COCOOH >OCH 3(15) C 6H 5CH 2SeH < H 3CSeH3. 预料以下各对化合物,何者具有更强的酸性? 答案:(1) CH 3NO 2 < (CH 3)2CHNO 2 (互变为酸式时的稳定性比较) (2) CH 2(SO 2C 6H 5)2 > CH 2(SOC 6H 5)2 (3)H 3CCH(C 6H 5)2> (C 6H 5)2CHCH 2C 6H 5(4) CH 3COCH 2COOCH 3 > CH 3COCH 2CONH 2(5) CH 3COCH 2COCH 2F < CH 3COCHFCOCH 3(6)NOCH 3<NO H 3C(7)SO 2O 2S >OO(8) NO 2CH 3CH 3H 3C >NO 2CH 3H 3CCH 3(场效应)(9)CH3>CH3(10) CH(C 6H 5)2< CH(C 6H 5)2(11) (CH 3)2Se < (CH 3)2O(12) <4. 解释以下现象:(1). 杯烯 (Calcene) 的偶极距很大,μ= 5.6 D.(答案:同时满足两个环的4n+2规则)(2). 吡咯 μ = 1.80 D ,吡啶 μ = 2.25 D ,且极性相反,如图:NN H(答案:孤对电子的排列方向)5. 比较下列化合物的碱性的强弱:NN(CH 3)2N(C 2H 5)2NH 2N答案:1>4>3>2>56. 9,10-二氢蒽-1-羧酸(A )和9,10-乙撑蒽-1-羧酸(B )的酸性取决于8-位上取代基X的性质。
第一章电子效应及酸碱理论1. 比较下列化合物亲电加成反应的活性顺序并加以解释。
解:由于分子中存在给电子超共轭效应,所以超共轭效应越强,给电子效应越强,电子云密度越大,亲电加成反应活性越强。
2. 比较下列芳香烃亲电取代反应的活性顺序并加以解释。
解:给电子的超共轭效应越强,苯环上电子云密度越大,反应活性越强。
同时由于空间效应的影响。
反应活性依次为:2>3>4>13. 比较下列碳正离子的稳定性并加以解释。
解:超共轭效应的影响。
4. 写出下列化合物与氯化氢的加成产物,并解释.解:从两个方面考虑,一是电子效应的存在,二是碳正离子的稳定性。
苯乙烯加成产物满足马氏规则,主要是生成的苄基碳正离子比较稳定的原因。
5. 比较下列化合物碱性强弱,并解释。
解:从电子效应考虑,吸电子诱导效应使酸性增强,共轭效应使碱性减弱。
3>1>4>2第二章立体化学1. 指出下面化合物那些互为对映异构体,那些为非对映异构体,并用R/S法命名下列化合物。
2. 用D/L法命名下列化合物3. 将下列透视式转化为不同的Fischer投影式(最小基团分别在横键或竖键上),并对不同构型用R、S法命名。
第三章有机活性中间体作业1:比较下列碳正离子的稳定性解:(3)>(1)>(2)作业2:写出下面反应的历程解:先质子化再脱水,不发生重排,因为苄基正离子比较稳定。
作业3. 解释说明碳正离子与碳负离子的稳定性顺序真好相反的原因。
解:由电子效应和超共轭效应解释,关键是对电荷的分散!作业4. 写出下面反应历程解题思路:作业5. 比较下列自由基的稳定性顺序解题思路:作业6. 写出下面反应的主要产物并命名解题思路:作业7. 写出下面反应的历程第四章:亲核取代反应1.完成下面反应并写出机理2.写出羟基乙胺(H2NCH2CH2OH)与过量环氧乙烷的反应历程。
3.对下面反应提出合理解释4.比较下列各组化合物的亲核性的强弱RSNa>RONa ; P(CH3)3 > N(CH3)3 ; CH3CH2SH < CH3CH2T eH第五章芳烃的取代反应1.判断下面化合物是否具有芳香性解:(1)利用双键修正法可知共有14个π电子,符合“4n+2”规则,具有芳香性。
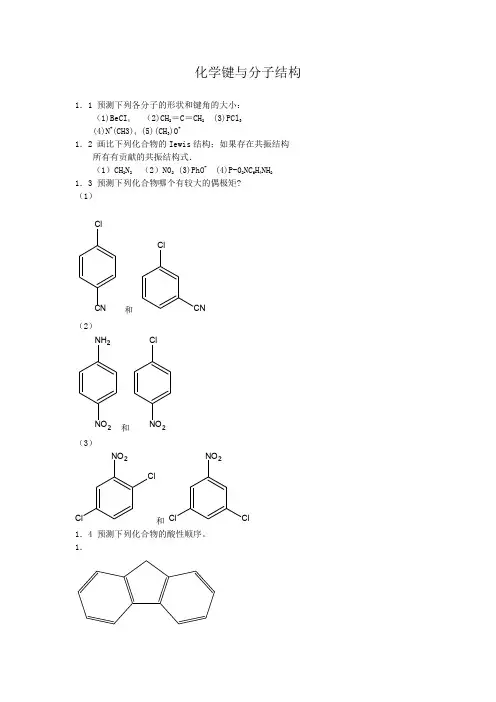
化学键与分子结构1.1 预测下列各分子的形状和键角的大小:(1)BeCI4(2)CH2=C=CH2(3)PCl3(4)N+(CH3)4 (5)(CH3)O+1.2 画比下列化合物的Iewis结构;如果存在共振结构所有有贡献的共振结构式.(1)CH2N2(2)N02(3)PhO- (4)P-02NC6H4NH21.3 预测下列化合物哪个有较大的偶极矩? (1)C lCN和C lCN(2)N H2NO2和C l NO2(3)C l NO2C l和C lNO2C l1.4 预测下列化合物的酸性顺序。
1.3.1.5 顺式与反式丁烯二酸的第一级和第二级电力常数如下:HCO 2HCO 2HHHCO 2HHHO 2CK 1=1.17×10-2K 1=9.3×10-4K 2=2.6×10-7 K 2=2.9×10-5 试说明其原因1.6 下列化合物是否有芳香性? (1)2,4,6-环庚三烯-1-羧酸(2)(3)NMe2NMe21.7 对气相正碳离子热力学稳定性的有效热力学测量是测定反应R 3C+H -→R 3CH 的△H 值。
CH 3+、CH 2F +、CHF 2-、和CF 3-的△H 值分别是312kcal ·mol -1,290kcal ·mol -1,284kcal ·mol -1和299kcal ·mol -1。
试合理地解释这些结果。
1.8下列各组化合物能否形成分子间氢键?若有的话,请画出分子间氢键。
(1)HCN 和HCN (2)HCHO 和HCHO (3)HCHO 和H 2O (4)Cl -和H 2O(5)OH COOH和丙酮 (6)HOCH 2CH2NH 2和HOCH 2CH 2NH 2(7)CH 3Br 和H 2O1.1(1)线性(2)三个碳原子呈线型,氢位于相互垂直的平面上(3)棱锥型,键角约105~110°(4)正四面体(5)棱锥型,键角约105~110°。
高等有机化学试题一、选择题1. 下列化合物中,哪一个是芳香化合物?A. 丙烯醛B. 环己酮C. 苯酚D. 戊酸2. 格氏反应中通常使用的金属卤化物不包括以下哪一项?A. 溴乙基镁B. 氯化锂C. 碘化钠D. 溴化铜3. 哪一个反应不是碳-碳键形成反应?A. 狄尔斯-阿尔德反应B. 威廉逊合成C. 卤代烃的亲核取代反应D. 弗林斯反应4. 在酸碱催化下,以下哪种化合物最难发生酯化反应?A. 乙醇B. 乙酸酯C. 醋酸D. 苯甲酸5. 以下哪个反应是立体特异性的?A. 克莱森缩合B. 羟醛缩合C. 狄尔斯-阿尔德反应D. 威廉逊合成二、填空题1. 在有机化学中,___________原则是指在形成新的σ键时,新的π键必须处于共面状态。
2. 有机分子中的手性中心是指一个碳原子连接着四个不同的取代基,这种现象也被称为___________。
3. 酮类化合物可以通过___________还原反应转化为二级醇。
4. 在有机合成中,常常使用___________试剂来保护羟基。
5. 弗林斯试剂是用来检测___________基团的存在。
三、简答题1. 请简述威廉逊合成反应的原理及其应用。
2. 描述克莱森缩合反应的基本步骤,并给出一个实际应用的例子。
3. 解释为什么芳香化合物相比于非芳香化合物更加稳定,并举例说明。
四、合成题请根据所给的起始原料和试剂,设计合成路线,目标化合物为苯乙酸。
起始原料:苯酚,二氧化碳试剂:氢氧化钠,氯化亚砷,硫酸五、论述题论述有机光化学在现代有机合成中的应用及其重要性。
江西理工大学研究生考试高等有机试卷及参考答案一单项选择题本大题共10题,每小题3分,共30分1.下列结构中,所有的碳均是SP2杂化的是 A2.下列自由基稳定性顺序应是 D① CH33C·② CH3CHC2H5③ Ph3C·④ CH3CH2·A. ①>③>②>④B. ①>③>④>②C. ③>①>④>②D. ③>①>②>④3.下列化合物中酸性最强的是 BA. CH3CH2COOHB. Cl2CHCOOHC. ClCH2COOHD. ClCH2CH2COOH4.下列化合物最易发生S N1反应的是 AA. CH33CClB. CH3ClC. CH3CH2CH2ClD. CH32CHCl5.下列羰基化合物亲核加成速度最快的是 C6.下列化合物中具有手性碳原子,但无旋光性的是 B7.化合物:①苯酚②环己醇③碳酸④乙酸,酸性由大到小排列为 BA、①>③>②>④B、④>③>①>②C、④>②>①>③D、②>①>③>④8. 3-甲基-1-溴戊烷与KOH-H2O主要发生 C 反应A、E1B、S N1C、S N2D、E29.下列化合物中为内消旋体的是 D10.下列几种构象最稳定的是 B二写出下列反应的主要产物;本大题共4题,每小题2分,共8分1.答案:2.COOC2H5+NBS(PhCOO)2CCL4,回流答案:3.答案:4.答案:三.写出下列亲核取代反应产物的构型式,反应产物有无旋光性并标明R或S构型,它们是SN1还是SN2本大题共6分答案:R型,有旋光性.SN2历程.无旋光性,SN1历程.四.写出下列反应机理;本大题共3题,每小题10分,共30分1.答案:2.答案:3.答案:五简要回答下列问题;本大题共4题,每小题4分,共16分1..为什么叔卤烷易发生 SN1 反应,不容易发生 SN2 反应答:单分子亲核取代 SN1 反应分两步进行,第一步决定反应速度,中间体为碳正离子,由于烃基是供电子基,叔碳正离子的稳定性大于仲碳正离子和伯正离,子,因而叔卤烷易发生 SN1 反应;双分子亲核取代 SN2 反应一步进行,空间位阻决定反应速度,由于叔卤烷空间位阻大,因而叔卤烷不易发生 SN2 反应;2.叁键比双键更不饱和,为什么亲电加成的活性还不如双键大答:叁键碳原子sp杂化,双键碳原子sp2杂化;电负性Csp>Csp 2; σ键长sp-sp<sp2-sp2叁键中形成两个π键的 p 轨道交盖的程度比在双键中更大,结合更紧密;故不易发生给出电子的亲电加成反应;3.当下列化合物进行乙酸解时,A比B快1014倍,比C快1012倍;答:三元环参与的结果,A的三元环电子云参与促进反应发生,C的三元环电子云不参与,B的三元环电子云阻止反应发生;4.试比较下列相对反应速度的大小,并解释原因;C2H5OCH2Cl CH3-CH2-CH2-CH2-Cl C2H5O-CH2CH2Cl A B C答:A>B>C ,当中心碳原子与杂原子直接相连时,反应速率明显增大,当杂原子与中心碳原子相连时,所形成的正碳离子,因共轭效应而被稳定;六. 将以下各组化合物,按照不同要求排列成序本大题共10分⑴水解速率⑶进行SN2反应速率:① 1-溴丁烷 2,2-二甲基-1-溴丁烷 2-甲基-1-溴丁烷 3-甲基-1-溴丁烷② 2-环戊基-2-溴丁烷 1-环戊基-1-溴丙烷溴甲基环戊烷⑷进行SN1反应速率:①3-甲基-1-溴丁烷 2-甲基-2-溴丁烷 3-甲基-2-溴丁烷②苄基溴α-苯基乙基溴β-苯基乙基溴答案:⑴水解速率:⑵与 AgNO3 -乙醇溶液反应的难易程度:⑶进行SN2反应速率:① 1-溴丁烷>3-甲基-1-溴丁烷>2-甲基-1-溴丁烷>2,2-二甲基-1-溴丁烷②溴甲基环戊烷>1-环戊基-1-溴丙烷>2-环戊基-2-溴丁烷⑷进行SN1反应速率:①2-甲基-2-溴丁烷>3-甲基-2-溴丁烷>3-甲基-1-溴丁烷②α-苄基乙基溴>苄基溴>β-苄基乙基溴。
F.A.C a r e y-最全最完备的高等有机化学习题-详细解答与分析-完美版work Information Technology Company.2020YEARChapter 1 Effect of Substituted in Organic molecule1. 试判断下列各对基团,那一个具有强的-I 效应(即强的吸电子诱导效应):(1) -COOH , -COO -(2) C HN O CH 3 , C H N N(CH 3)2CH 3+(3) C OCH 3 , C CH 2CH 3, (4) SO 2H ,SO 3H(5) OCH 3 , SCH 3 (6)C H C H CH 3 ,C C CH 3(7) N (CH 3)2 , P(CH 3)2(8) Si(CH 3)3 ,Si(CH 3)23(9) N(CH 3)3+,NH 2 (10)CN , CH 2NH 2 (11) SiCH 3 ,Cl (12) C C CH 3 ,C H C H CH 3(13),(14) NO 2,NO 2 (15)O 2SCH 3, O 2SBr2. 指出下列各对酸中哪一个酸性强 (1) H 3NCH 2CH 2COOH , HOCH 2CH 2COOH (2) HC C COOH ,H 2C C H COOH(3) C 6H 5COCH 2COOH , C 6H 5CHOHCH 2COOH(4)C 4H 9CHCOOn,C C CH 3CH 3CH 3CH 3COOHOOC(5) COOH OH,COOH OH(6) BrCH 2CH 2COOH , CH 3CHBrCOOH(7) (H 3C)2CH 2CHCOOH ,H 2CC HCH 2COOH(8) HC C COOH , SCOOH(9) CH 2(COOH)2 ,HOOCH CCOOCl(10)CH 3OCH 2CH 2COOH , CH 3SCH 2CH 2COOH (11)CH 3SCH 2COOH ,CH 3SO 2COOH (12)OHCCOOH,COOHCHO(13)OHC(CH 3)3(H 3C)3C ,OHC(CH 3)3CH 3(H 3C)3C(14) H 3COCOOH , OCH 3COOH(15) C 6H 5CH 2SeH ,H 3CSeH3. 预料以下各对化合物,何者具有更强的酸性? (1) CH 3NO 2 ,(CH 3)2CHNO 2 (2) CH 2(SO 2C 6H 5)2 ,CH 2(SOC 6H 5)2(3) H 3CCH(C 6H 5)2,(C 6H 5)2CHCH 2C 6H 5(4) CH 3COCH 2COOCH 3 ,CH 3COCH 2CONH 2(5) CH 3COCH 2COCH 2F ,CH 3COCHFCOCH 3(6)NOCH 3,NO H 3C(7) SO 2O 2S,OO(8) NO 2CH 3CH 3H 3C ,NO 2CH 3H 3CCH 3(9)CH3,CH3(10) CH(C 6H 5)2,CH(C 6H 5)2(11)(CH)3Se , (CH 3)2O(12) ,4.解释以下现象:(1). 杯烯 (Calcene) 的偶极距很大,μ= 5.6 D.(2). 吡咯 μ = 1.80 D ,吡啶 μ = 2.25 D ,且极性相反,如图:NN H5.比较下列化合物的碱性的强弱:N N(CH3)2N(C2H5)2NH2N6.9,10-二氢蒽-1-羧酸(A)和9,10-乙撑蒽-1-羧酸(B)的酸性取决于8-位上取代基X的性质。
ProblemⅠ
Write the IUPAC name for the following structures
1.4-Ethyl-5-methyl octane
2.5-(3-Pentenyl)-3,6,8-decatriene-1-yne
3.Bicyclo[12,2,2]octadeca-14,16(1)diene
4.5-methyl spiro[2,4]heptane
5.4-Phenyl-2-naphthol
6.1-methyl-1,2-ethanediol
7.Magnesium di(1-propanolate)
8.2-Hexen-4-ynedioic acid
9.2,4,5-trioctanetriane
10.Methyl 3-ethyl-5-phenyl heptanoate
11.5,9,12,15,21-pentaoxaheptacosane-1,27-diol
12.1,2-Cyclohexane dicarboxylic anhydride
13.azocine
14.6H-1,2,5-Thidiazine
15.N-Methyl-N-propylpentylamine OR Methyl penthyl propyl ammonium
16.1H-pyrazolo[4,3-d]oxazole
17.4H-[1,3] oxathiolo[4,5-b]pyrrole
Write the systematic name for the following structures
18.azine Hexahydrozine azole azolidone 1,2-Diazine 1,3-Diazine 1,3-Diazole
1,2-oxazole oxin Thiole
ProblemⅡ
Write the systematic name for the following structures
1.3-bromo-2-(propenyl)-2,4-hexadienoic acid
2.1-Ethoxy-6-octen-1-yne-3,5-dione
3.4-chloro-2-methyl-2-cyclohexenol
4.(2-methyl)butyl 3-bromo-2-hydroxy-2-methyl 3-butenate
5.1,3,5-Naphthalene triacetic acid
6.5-(4-Hydroxy-1-butynyl)-2-nonen-6-yne
7.2-Amino-5-bromo diphenylamine
8.4,5-Dichloro-2-(4-chloro-2-hydroxy methyl-5-oxo-3-hexenyl)-1-cyclohexane carboxylic acid
9.N-(2,3-Dimethybutyl)-3,5-dihydroxy-3-ethyl pentanamide
10.2-Ethyl-4-ethyl amino-2-methyl-3-oxobutanal
11.2-hydroxy-1-(2-hydroxy-5methyl-1-phenylazo) Naphthalene-4-sulfonic acid
12.Methyl 3-{4-[2-hydroxy-3-(1-methyl ethyl)amino propoxy]}benzenepropanoate
Problem Ⅲ 1. Solution 1
CH 3
+Cl-F CH 3Cl +F △H =-105KJmol -1
△H f
146.5
-51.1
-88.1
78.5
Solution 2
Cl-F
Cl + F
DH Cl-F =△H f (Cl )+△H f (F )-△H f (Cl-F)
=250.9KJmol -1
CH 3
+Cl-F CH 3Cl +F
DH
250.9
355.9
△H =-105KJmol -1
2.
C 6H 5
C 6H 5(Liminting rate step)
+
(CN)2C=C(CN)2
C 6H 5
6H 5
(CN)2(CN)2
C 6H 5
6H 5
C 6H 5
6H 5
3.
C 6H 5
H
N 6H 5C 6H 5N NH 2+ C 6H 5N
N
N
C 6H 5N
fast
C 6H 5+ N 2C 6H 5+ C 6H 5N NH 2
fast
6H 6
+ C 6H 5N=NH
4.
Cl
CH3NH-
3
3
- Cl
CH3
3
NH2
CH3
+
CH3 H2N
5.
(1) It is the first order isotopic effect K H/K D=6.76
(2) It is a E2 reaction reaction
6
(1)A (2)A
7.
d[prod.]
dt = k2[A-][HA],
d[A-]
dt
= 0=k1[HA][B] - k2[A-][HA] - k-1[A-1][BH+]
[A-] =
k1[HA][B]
k2[HA] + k-1[BH+]So
d[prod.]
dt
=
k1k2[HA]2[B]
k2[HA] + k-1[BH+]
for the general base catalysis, k2>>k-1
d[prod.]
dt =
k1k2[HA]2[B]
k2[HA]
= k1[HA][B]
for the specific base catalysis, k2<<k-1
d[prod.]
dt =
k1k2[HA]2[B]
k-1[BH+]
but K b =[BH+][OH-]
[B]
OH- is a specific base in the reaction
So d[prod.]
dt =
k1k2[HA]2[OH-]
k-1k b
Proble mⅣ
1.σm-IO2 = -3.50 + 4.2 = 0.70
σp-IO2 = -3.44 + 4.2=0.76
σp-x
σm-x for m-NO2 ,for p-NO2 2.
3.
(1)ρ< 0
(2)ρ> 0
(3)ρ< 0
(4)ρ< 0
(5)ρ> 0
4.
(1) pk a(p-Cl) = pk a–σp-Cl
(2) pk a(p -Cl) = pk a -ρσp-Cl
= pk a -ρσp-NO2
(3) pk a(p -NO
2)。