常见盐和化学肥料
- 格式:doc
- 大小:113.00 KB
- 文档页数:7

第十一单元盐化肥教材知识梳理知识点一:常见的盐及其用途1.日常生活中所说的盐,通常指食盐(主要成分是);而化学中的盐是指一类组成里含有和的化合物。
2. 是重要的调味品。
它还有很多的用途,例如医疗上的,农业上用它来,还可以作为化工原料,还可以腌制食品延长保存时间。
公路上的积雪也可以用来消除等。
3. 是一种工业用盐,有毒、有咸味,外形与食盐相似,人若误食会引起。
4.碳酸钠俗称或。
在工业上,碳酸钠广泛用于玻璃、造纸、纺织和洗涤剂的生产等。
我国制碱工业的先驱— 发明了侯氏制碱法,这里的碱是指纯碱— (写化学式)。
5.天然存在的或的主要成分就是碳酸钙,它们都是重要的。
碳酸钙还可用作。
6.碳酸氢钠俗称。
碳酸氢钠是焙制糕点所用的的主要成分之一。
在医疗上,它是治疗的一种药剂。
碳酸氢钠跟碳酸钠一样能跟酸反应产生二氧化碳和水。
但碳酸氢钠又不同于碳酸钠的性质是:能产生碳酸钠、二氧化碳和水。
知识点二:复分解反应及其发生的条件7.两种互相交换成分,生成另外两种化合物的反应叫做反应。
只有当两种化合物互相交换成分,生成物中有生成时,复分解反应才可以发生。
8.常见沉淀:(写出其化学式)(1)蓝色沉淀:;(2)红褐色沉淀:;(3)既不溶于水也不溶于酸的白色沉淀:、;(4)溶于酸且能与酸反应产生气体的白色沉淀:、;(5)溶于酸且能治疗胃酸过多的白色沉淀:、。
9. 分析下列三个化学反应,回答问题①BaCO3+2HCl=BaCl2+H2O+CO2↑②K2CO3+2HNO3=2KNO3 + H2O+CO2↑③Na2CO3+H2SO4=Na2SO4+H2O+CO2↑(1)BaCO3、K2CO3、Na2CO3三种不同物质中,都含有的离子是,我们把这类盐叫做碳酸盐;(2)总结规律:碳酸盐能与酸反应生成气体;此外碳酸氢盐也能与酸发生反应生成该气体,例如蒸馒头揉面时需加入适量的,因为面团经过发酵后会产生乳酸等有机酸,与其反应生成二氧化碳气体,不但能除去面团中的酸味,还会使蒸出的馒头松软多孔。

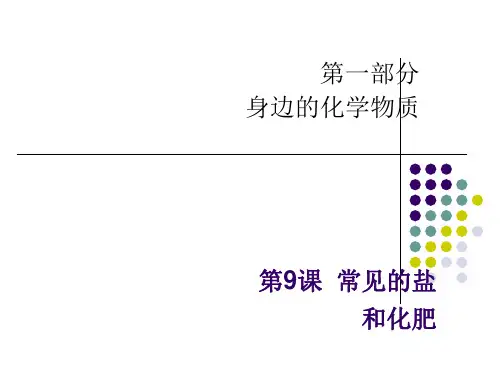






2021届中考化学专题复习考点测试《常见的盐化肥》专题班级姓名学号一、知识梳理1.盐的性质和用途(1)定义:由(或)和构成的化合物。
名称、化学式俗称物理性质主要用途氯化钠的主要成分色固体,溶于水作,配制,融雪剂等碳酸钠色固体,溶于水用于玻璃、造纸、纺织、洗涤剂的生产等碳酸氢钠色固体,溶于水糕点的的主要成分之一,医疗上用于治疗等碳酸钙、的主要成分色固体,溶于水作建筑材料,工业上制取等硫酸铜色固体,溶于水后形成色的溶液检验,农业生配制等含Cu2+的盐溶液含Fe2+的盐溶液含Fe3+的盐溶液高锰酸钾溶液1.盐溶液的酸碱性:大多数盐溶液呈性;但Na2CO3溶液呈性。
2.某些盐的热不稳定性:NaHCO3 ∆ CaCO3 高温3.盐+金属=新盐+新金属(基本反应类型属于反应)Fe + CuSO4 = Cu + AgNO3 =4.盐+酸=新盐+新酸(基本反应类型属于反应)Na2CO3 + HCl = Ba(NO3)2 + H2SO4=5.盐+碱=新盐+新碱(基本反应类型属于反应)FeCl3 + NaOH= MgCl2 + Ca(OH)2 =6.盐+盐=新盐+新盐(基本反应类型属于反应)NaCl+ AgNO3 = CaCl2 + Na2CO3 =2.复分解反应(1)定义:两种化合物,生成另外两种化合物的反应。
反应类型酸+金属氧化物酸+碱酸+盐碱+盐盐+盐反应物的条件反应物要溶于水生成物的条件生成物中有或或,满足一个条件即可(3)常见的难溶物:①难溶性碱:(蓝色)、(红褐色)、、(白色)。
②难溶性盐酸盐:;难溶性硫酸盐:;难溶性碳酸盐:、。
3.化学肥料种类常用化肥作用氮肥尿素、碳酸氢铵、氯化铵、硝酸铵等促进植物茎、叶生长茂盛,叶色,提高蛋白质含量磷肥磷矿粉[Ca3(PO4)2]、过磷酸钙等促进作物生长、根系发达,增强抗寒能力,促进作物穗粒钾肥草木灰主要成分、氯化钾、硫酸钾等促进植物茎秆粗硬,增强抗病虫害和抗能力复合肥硝酸钾、磷酸二氢铵同时均匀地供给作物几种养分氮肥钾肥磷肥NH4HCO3NH4Cl K2SO4KCl 磷矿粉等1.看颜色色固体色固体2.闻气味气味气味3.溶于水溶于水溶于水4.加碱研磨气味气味二、考点透视考点1 常见盐的俗称和用途例1 下列说法正确的是()A.NaHCO3俗称苏打B.CaCO3可用作补钙剂C.Na2CO3俗称火碱D.K2CO3属于复合肥例2 下列有关物质用途的说法,不正确的是()A.氯化钠可用作食品调味剂B.碳酸氢钠可用来治疗胃酸过多C.生石灰可作为食品干燥剂D.铁制容器可用来盛装波尔多液考点2 常见盐的性质例3下列各组固体物质,不能用水鉴别的是()A.KNO3、KCl B.CaCO3、CaCl2C.CuSO4、Na2SO4D.NH4NO3、CaO例4现有一包不纯的Na2SO4粉末,可能含有CaCO3、CuCl2、Ba(NO3)2、NaOH、NaCl中的一种或几种。
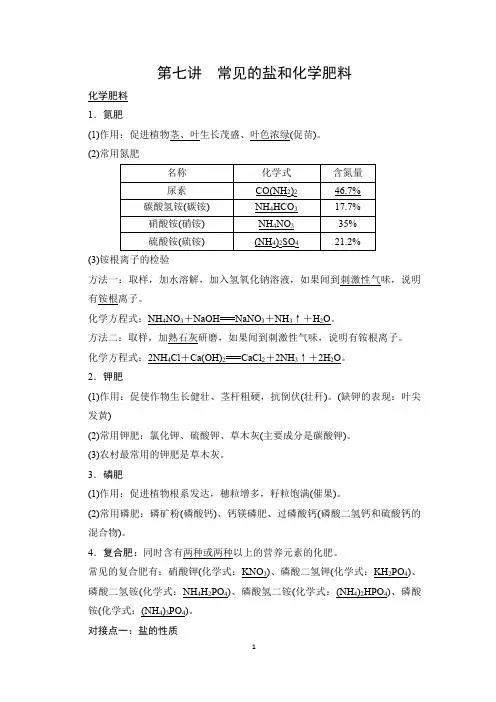
第七讲常见的盐和化学肥料化学肥料1.氮肥(1)作用:促进植物茎、叶生长茂盛、叶色浓绿(促苗)。
(2)常用氮肥(3)铵根离子的检验方法一:取样,加水溶解,加入氢氧化钠溶液,如果闻到刺激性气味,说明有铵根离子。
化学方程式:NH4NO3+NaOH===NaNO3+NH3↑+H2O。
方法二:取样,加熟石灰研磨,如果闻到刺激性气味,说明有铵根离子。
化学方程式:2NH4Cl+Ca(OH)2===CaCl2+2NH3↑+2H2O。
2.钾肥(1)作用:促使作物生长健壮、茎杆粗硬,抗倒伏(壮秆)。
(缺钾的表现:叶尖发黄)(2)常用钾肥:氯化钾、硫酸钾、草木灰(主要成分是碳酸钾)。
(3)农村最常用的钾肥是草木灰。
3.磷肥(1)作用:促进植物根系发达,穗粒增多,籽粒饱满(催果)。
(2)常用磷肥:磷矿粉(磷酸钙)、钙镁磷肥、过磷酸钙(磷酸二氢钙和硫酸钙的混合物)。
4.复合肥:同时含有两种或两种以上的营养元素的化肥。
常见的复合肥有:硝酸钾(化学式:KNO3)、磷酸二氢钾(化学式:KH2PO4)、磷酸二氢铵(化学式:NH4H2PO4)、磷酸氢二铵(化学式:(NH4)2HPO4)、磷酸铵(化学式:(NH4)3PO4)。
对接点一:盐的性质【例1】(2013·滨州)碳酸氢钠是一种重要的盐类物质,在生活中用途广泛。
小滨同学设计了实验,以探究碳酸氢钠的化学性质。
[探究实验1]碳酸氢钠溶液的酸碱性[实验方案]取少量该固体加入试管中,加适量水溶解,再滴入几滴酚酞试液,振荡。
现象:溶液变成浅红色.由此得出结论____________________________;[探究实验2]能与酸反应[实验方案]取少量该固体加入试管中,滴加稀盐酸,现象为_________________________________________________________________;[探究实验3]碳酸氢钠的热稳定性[实验方案]用如图所示装置进行实验现象:充分加热后,大试管口有水珠出现,管底有白色固体残留,小试管中澄清石灰水变浑浊。

考点09 盐和化肥1.盐及其化学性质:本考点常以选择题和填空与简答题的形式进行考查,考查的命题点有:碳酸钠、碳酸氢钠、碳酸钙的性质;盐的通性等。
2.化学肥料:本考点常以选择题的形式进行考查,考查的命题点有:判断化学肥料的种类、铵态氮肥的特性、结合生活实例来选择合适的化学肥料等。
1.认识盐的概念及生活中常见的盐;2.认识氯化钠在生活中的用途及海水晒盐;认识Na2CO3、NaHCO3、CaCO3的存在与用途。
3.学会运用复分解反应发生的条件;4.掌握盐的化学性质;5.认识化肥的概念和肥料三要素及其作用;一、常见的盐;二、盐的化学性质;三、化肥;考向一:常见的盐一、盐1、盐定义:金属离子(或NH4+)和酸根离子的化合物。
2、盐的分类:依据组成盐的阳离子和酸根的种类进行分类(1)根据阳离子的不同,盐可以分为钠盐、钾盐、镁盐、铵盐等(如氯化钠为钠盐)。
(2)根据酸根的不同,盐可以分为硫酸盐、碳酸盐、盐酸盐等(如氯化钠为盐酸盐)。
3、盐的溶解性规律:①钾盐、钠盐、铵盐、硝酸盐都可溶;②盐酸盐只有氯化银不可溶;③硫酸盐只有硫酸钡不可溶;④碳酸盐只溶钾、钠、铵,剩下都不溶。
注意:AgCl、BaSO4不仅不溶于水,而且不溶于稀硝酸。
七种常见沉淀:AgCl↓BaSO4↓Cu(OH)2↓F e(OH)3↓Mg(OH)2↓BaCO3↓CaCO3↓4、几种常见的盐(1)、氯化钠(NaCl)1)氯化钠是食盐的主要成分。
白色固体,熔、沸点较高,易溶于水,其溶解度受温度的影响不大。
2)用途:调味、腌渍食品,生理盐水,制钠、氯气、氢氧化钠、盐酸、纯碱等。
在自然界中分布很广泛,海水中含有大量氯化钠。
(2)碳酸钠(Na2CO3)1)俗名:纯碱、苏打2)纯碱不是碱,是盐;白色粉末、易溶于水,水溶液显碱性。
我国著名化学家侯德榜在改进纯碱的生产方面,作出了巨大贡献,创立侯氏制碱法(联合制碱法)。
3)用途:玻璃、造纸、纺织和洗涤剂的生产等。
九年化学盐化肥知识点与重点酸碱盐在中考中是必考的知识点之一,方程式也比较难懂,同学们要下苦功夫去克服这部分内容,那么这部分内容具体的资料,你想了解吗?小编整理了相关资料,希望能帮助到您。
初中化学重点知识盐和化肥生活中常见的盐一、常见的盐1、盐的分类:钠盐:NaCl、Na2CO3、Na2SO4等。
碳酸盐:Na2CO3、CaCO3、K2CO3等。
氯化物:NaCl、KCl、FeCl2等。
2、盐溶液的酸碱性:并非所有的盐溶液都是中性的。
①强酸强碱盐和弱酸弱碱盐呈中性:NaCl、KNO3、CaSO4等。
②强酸弱碱盐呈酸性:NH4Cl、NH4NO3、CuSO4等。
③弱酸强碱盐呈碱性: Na2CO3、NaHCO3、K2CO3等。
3利与弊:、物理性质和用途:俗称物理性质用途NaCl食盐白色晶体易溶于水①作调味品,腌制食物;②医疗上配制生理盐水;③农业上选种;④工业原料;⑤消除道路积雪。
Na2CO3纯碱苏打白色粉末易溶于水工业上用于玻璃、造纸、纺织和洗涤剂的生产;食品工业等。
NaHCO3小苏打白色粉末易溶于水焙制糕点所用的发酵粉;医疗上,治疗胃酸过多(胃溃疡患者禁用)。
CaCO3白色粉末难溶于水建筑材料、补钙剂4、化学性质:①盐与金属反应:盐 + 金属 = 新盐 + 新金属 (置换反应) Fe + CuSO4 = FeSO4 + Cu②盐与酸反应:盐 + 酸 = 新盐 + 新酸 (复分解反应) Na2CO3 + 2HCl = 2NaCl + H2O + CO2↑③盐与碱反应:盐 + 碱 = 新盐 + 新碱 (复分解反应)Na2CO3 + Ca(OH)2 = CaCO3↓ + 2NaOH④盐与盐反应:盐 + 盐 = 两种新盐 (复分解反应)CaCl2 + Na2CO3 = CaCO3↓ + 2NaCl5、粗盐提纯:①提纯原因:粗盐中含有多种可溶性杂质(MgCl2、CaCl2)和不溶性杂质(泥沙等)。
②提纯步骤:溶解、沉淀、过滤、蒸发等。
【中考化学】盐和化肥知识点梳理归纳!1、盐的概念:由金属阳离子(或NH4+)和酸根阴离子组成的化合物;或者能解离出金属离子(或NH4+)和酸根离子的化合物。
碳酸钠晶体Na2CO3·10H2O(纯净物),俗称天然碱、石碱、口碱。
风化:常温时在空气中放置一段时间后,失去结晶水而变成粉末。
(化学变化)Na2CO3·10H2O= Na2CO3+10H2O3、2Na H CO3Na2CO3+ H2O+ CO2↑NaHCO3+HCl===NaCl+ H2O+ CO2↑3、粗盐提纯——去除不溶性杂质,得到的精盐中还含有氯化镁、氯化钙等可溶性杂质。
4、碳酸钠、碳酸氢钠、碳酸钙的化学性质1)、碳酸钙的化学性质:①与酸的反应:2HCl + CaCO3 = CaCl2 + H2O + CO2↑②高温分解:CaCO3CaO + CO2 ↑2)、碳酸钠的化学性质:(这两个反应可用于检验NaOH是否变)①与酸的反应: 2HCl + Na2CO3 = 2NaCl + H2O + CO2↑②与碱溶液的反应;Ca(OH)2 + Na2CO3 = CaCO3↓ + 2NaOH3)、碳酸氢钠的化学性质:与酸的反应;HCl + NaHCO3 = NaCl + H2O + CO2↑4)、检验溶液中存在CO32-的方法:⑴取样少许与试管中,加入稀HCl,若有无色气泡产生,然后将该气体通入澄清石灰水中,石灰水变浑浊,则证明存在CO32-2HCl + CaCO3 = CaCl2 + H2O + CO2↑Ca(OH) 2 + CO2 ==== CaCO 3↓+ H2 O⑵加入石灰水或Ba(OH)2溶液,若溶液变浑浊,然后加入稀盐酸浑浊消失,则存在CO32-Ca(OH)2+Na2CO3=CaCO3↓+2NaOH2HCl +CaCO3 = CaCl2+ H2O+CO2↑⑶加入CaCl2或Ca(NO3)2溶液,若液体变浑浊,则有存在CO32-CaCl2+ Na2CO3= CaCO3↓+2NaClCa(NO3)2+ Na2CO3= CaCO3↓+2Na(NO3)25、盐的性质(1)盐的溶解性钾钠铵硝全可溶,碳酸钡钙银不溶;硫酸钡和氯化银,不溶水来不溶酸;镁铝亚铁和铁铜,五碱均不溶于水;氢氧化钙硫酸钙,微溶于水要记牢。
生活中常见的盐1、常见的盐定义:能解离出____________________________的化合物。
注:此时的盐不是指食盐,食盐的主要成分是NaCl。
物质俗称物理性质用途氯化钠________ _____粉末,水溶液有___味,溶解度受温度影响_____(1)作调味品(2)作防腐剂(3)消除积雪(降低雪的熔点)(4)制生理盐水碳酸钠Na2CO3 _____(因水溶液呈碱性)、____________粉末状固体,__溶于水用于玻璃、造纸、纺织、洗涤、食品工业等碳酸氢钠NaHCO3 _____________晶体,___溶于水制糕点所用的发酵粉医疗上,治疗胃酸过多碳酸钙1、大理石,石灰石的主要成分是________________2、大理石是____色______体,_______溶于水。
3、碳酸钙煅烧和盐酸反应的方程式分别为:________________________ _______________________________________2、精盐提纯——去除不溶性杂质,得到的精盐。
(1)、实验步骤:溶解、过滤、蒸发(2)、实验仪器实验步骤实验仪器其中玻璃棒的作用溶解烧杯、玻璃棒过滤铁架台(带铁圈)、漏斗、烧杯、玻璃棒蒸发铁架台(带铁圈)蒸发皿、酒精灯、玻璃棒过滤蒸发注意:①蒸发皿是可以直接加热的仪器,液体体积不能超过蒸发皿2/3.②溶解时用玻璃棒搅拌,目的是加快溶解。
③加热时用玻璃棒搅拌,防止局部温度过高造成液滴飞溅④待蒸发皿中出现较多固体时停止加热,利用余热使滤液蒸干,不能将滤液完全蒸干才停止加热。
3、碳酸钠Na2CO3碳酸钠_____俗名______或_____。
碳酸钠属于_____,因其溶于水后显____性,所以俗称_____。
广泛用于玻璃、造纸、纺织和洗涤剂生产等。
(1)物理性质:____粉末固体,____溶于水,溶解时放热,水溶液能使无色酚酞溶液变__色。
注意:Na2CO3 是一种盐,其溶液显碱性,pH>7,滴入无色酚酞溶液变红,此知识点是常考点。
常见的盐 化学肥料一、中考复习要求1、知道食盐、硫酸铜、碳酸钠和碳酸钙的物理性质和主要用途。
记忆某些盐的颜色以及在水中的溶解性。
2、正确描述食盐、硫酸铜、碳酸钠和碳酸钙的某些化学性质,记住反应现象,会熟练书写有关反应的化学方程式。
3、简单了解结晶水和结晶水合物的概念,知道结晶水合物具有风化现象。
41、常见的盐(1)氯化钠(NaCl ,俗称 ) 色晶体, 溶于水,有 味,有较高的熔点和沸点,纯净NaCl 不潮解,因含杂质而易潮解。
海水中含有大量食盐,可用 方法把食盐从海水中结晶分离出来。
食盐是重要的化工原料,可制盐酸、氢氧化钠、金属钠等,食盐还与人类的生理活动有着密切的关系,家庭常用它作调味品和防腐剂,生理食盐水中含NaCl0.9%。
(2)硫酸铜(CuSO 4)无水硫酸铜是 色固体, 溶于水,水溶液呈 色。
硫酸铜晶体(CuSO 4·5H 2O )是无水硫酸铜结合一定量结晶水形成的结晶水合物,俗称 或 ,硫酸铜晶体在常温干燥的空气中,失去结晶水而风化。
加热的条件下很易失去结晶水得到无水硫酸铜。
CuSO 4·5H 2O = CuSO 4 + 5H 2O硫酸铜有毒,农业上配制波尔多液杀菌剂,工业上制备多种含铜化合物的原料。
(3)碳酸钠(Na 2CO 3)碳酸钠俗称 ,是 色粉沫状固体, 易溶于水,水溶液呈碱性。
碳酸钠晶体是一种 色结晶水合物(化学式为 ),俗称 ,常温下干燥的空气中 风化。
碳酸钠是重要的化工产品,是造纸、玻璃、肥皂、洗涤剂、纺织、制革、制取氢氧化钠等工业的重要原料。
(4)碳酸钙(CaCO 3)碳酸钙是 色固体, 溶于水,比较坚硬,白垩、石灰石、大理石的主要成份是碳酸钙。
石灰石用作建筑材料,是烧制生石灰和水泥的主要原料。
工业上利用石灰石烧制生石灰的化学方程式为: 。
2、常见盐在水中的溶解性规律(1)钾盐、钠盐、铵盐、硝酸盐都溶于水。
(2)硫酸盐中:BaSO 4不溶,CaSO 4 、Ag 2SO 4微溶,其余均可溶。
第21讲常见的盐和化学肥料1.(2011年广东广州)下列关于化肥的说法正确的是()。
A.过磷酸钙[Ca(H2PO4)2和CaSO4的混合物]属于氮肥B.凡施用过化肥的蔬菜都会危害健康C.硫酸钾与熟石灰混合、研磨,能闻到刺激性的气味D.合理施用化肥能提高农作物的产量2.(2011年广东揭阳)钾肥具有增强农作物抗病虫害和抗倒伏能力的功能。
下列化肥中具有此功能的是()。
A.尿素[CO(NH2)2]B.氯化钾(KCl)C.硫酸铵[(NH4)2SO4]D.磷矿粉[Ca3(PO4)2]3.(2011年广东佛山)学习化学时可用下图描述某些相互关系,下列选项正确的是()。
4.(2012年重庆)在A+B―→盐+水的反应中,A和B不可能...是()。
A.HCl和NaOH B.CO2和NaOHC.H2SO4和Fe2O3D.H2SO4和BaCl25.(2012年山东泰安)钾肥能提高农作物抗倒伏、抗病虫害的能力。
小明家的水稻出现了倒伏现象,应施用的肥料是()。
A.Ca(H2PO4)2B.NH4H2PO4C.CO(NH2)2D.KCl6.(2012年四川雅安)以下几种常见化学肥料中属于复合肥的是()。
A.硫酸钾(K2SO4)B.磷酸二氢钾(KH2PO4)C.磷矿粉[有效成分Ca3(PO4)2]D.尿素[CO(NH2)2]7.(2012年四川泸州)KNO3是农业上常用的一种化肥,KNO3中氮元素的化合价是()。
A.+3 B.+4C.+5 D.+28.(2012年北京)某固体粉末可能由氢氧化钠、氢氧化钙、碳酸钠和碳酸钙中的一种或几种组成,现进行如下实验:①取少量固体加入足量的水,搅拌,有不溶物;②过滤,向滤液中加入盐酸,有气泡产生。
下列对固体粉末成分的判断中,不正确...的是()。
A.一定有碳酸钠B.可能有氢氧化钠C.一定有碳酸钙D.可能有氢氧化钙9.酸、碱、盐在工农业生产和日常生活中的广泛应用,促进了人类文明的进步和社会的可持续发展。
下列有关酸、碱、盐的生产或应用的说法不合理...的是()。
A.将草木灰(含K2CO3)与氯化铵混合施用B.纯碱既可从内陆盐湖提取,又可用“侯氏联合制碱法”生产C.用石灰乳与硫酸铜溶液混合配制防治植物病害的波尔多液D.汽车或电动车的蓄电池中用到的硫酸溶液是由浓硫酸稀释而成10.(2012年四川德阳)下列各组物质在溶液中能大量共存且形成无色溶液的是()。
A.NaCl、BaCl2、Na2CO3B.KNO3、HCl、CaCl2C.H2SO4、FeCl3、NaNO3D.NaOH、HNO3、NH4NO311.(2012年广东肇庆)下图是某化肥包装袋上的部分说明。
(1)碳酸氢铵保存时的注意事项是________________________。
(2)将碳酸氢铵和氢氧化钙混合研磨会发生反应,并可闻到刺激性气味。
请写出该反应的化学方程式:_________________________________________________;闻到的刺激性气味气体是氨气,它能使湿润的红色石蕊试纸变________色。
12.(2010年广东湛江)小红家从农贸市场买回一包化肥,化肥包装上的标签如下图所示,请回答下列问题。
富家牌优质化肥(NH4HCO3)含氮量为20.3%(1)该化肥是由__________种元素组成的。
(2)该化肥中N、H两种元素的质量比是__________。
(3)该化肥的含氮量应该是__________(结果保留到0.1%),说明此标签有错误。
13.(2012年四川资阳)化学在工农业生产中的应用较为广泛。
(1)合理使用氮肥、磷肥、钾肥是农业增产的重要手段,下列属于复合肥的是________(填序号)。
①尿素[CO(NH2)2];②硫酸钾(K2SO4);③磷酸二氢铵(NH4H2PO4);④硝酸铵(NH4NO3)。
(2)不同农作物的生长适应酸碱性不同的土壤。
经测定某土壤的pH为5.6,该土壤为______性土壤(填“酸”或“碱”)。
(3)可用适量的稀盐酸除去锅炉里的水垢[主要成分为CaCO3、Mg(OH)2],用化学方程式表示其反应之一:__________________________________________________________;稀盐酸选用适量而不是过量,是因为________________________________________。
14.(2012年湖南株洲)有一包白色固体粉末可能由NH4Cl、Na2CO3、BaCl2、CuSO4、NaCl中的一种或几种组成。
为了确定其组成,小东做了以下实验:①取少量白色粉末于研钵中,加入少量的熟石灰粉末混合,研磨,没有闻到氨味;②另取少量白色粉末加入适量的水,出现白色浑浊,静置后,上层清液无色;③小心倒掉上层清液,向沉淀中加入稀硝酸,白色沉淀完全溶解,并有无色无味的气体产生。
由以上实验可推断:(1)这包白色固体中肯定存在________________,肯定不存在_____________________;(2)写出②中出现白色浑浊的化学方程式:_____________________________________。
15.(2012年广东湛江)下图是初中化学常见物质间的转化关系(反应条件和部分产物已略去),其中A为钠盐,B、C常温下是无色气体,X、Y均为黑色粉末,D为红色金属单质,F在常温下为液态氧化物。
试回答下列问题:(1)已知A含有三种元素,则A的俗名是__________;F的化学式为__________。
(2)上述物质转化过程中,B+X→C所属的反应类型是______________。
(3)指出C的一种用途:________________________;写出C+Y→D的化学方程式:____________________________________。
(4)若反应E→F为中和反应,则E的化学式为______。
16.(2012年江苏南京)实验室有三瓶化肥未贴标签,只知道它们分别是碳酸氢铵(NH4HCO3)、氯化铵(NH4Cl)和尿素[CO(NH2)2]中的一种。
为鉴别三种化肥,某同学分别取少量样品编号为A、B、C,并进行如下实验(此处箭头表示得出实验结论)。
根据上述实验回答:(1)写出三种化肥的名称:A__________;B__________;C__________。
(2)如果实验Ⅱ中B、C两种样品没有另取,对实验结果________(填“有”或“无”)影响。
(3)常温下如要鉴别B、C两种样品,________(填“能”或“不能”)采取闻气味的方法。
(4)由实验和查阅资料可知,人们在施用铵态氮肥时,若遇到碱性物质,会使铵态氮肥转化为氨气,氨气进入大气后与雨水作用,可能形成“碱雨”。
“碱雨”中碱的化学式为____________。
17.(2012年四川达州)草木灰是一种常见的农家肥料,其主要成分是碳酸钾(K2CO3);硫酸铵[(NH4)2SO4]是一种氮肥。
为了给农民朋友提供技术指导,小明对这两种肥料作了相关性质的探究。
【友情提示】碳酸钾与纯碱具有相似的化学性质。
【实验探究】完成以下各题。
变废为宝,还起到了改良酸性土壤的作用。
②草木灰和硫酸铵能否混合使用?________(填“能”或“否”)。
【知识拓展】若要鉴别失去标签的碳酸钾和硫酸铵固体,下列试剂不可用的是________。
A .水 B .稀盐酸 C .氯化钡溶液 D .无色酚酞溶液18.(2012年江苏连云港)我国制碱工业的先驱侯德榜将制碱与制氨结合起来的联合制碱法,为纯碱和氮肥工业技术的发展做出了杰出的贡献。
其生产工艺流程示意图如下:(1)粗盐水中主要含有Ca 2+、Mg 2+、SO 2-4等杂质离子,工业上常加入稍过量的NaOH 溶液、Na 2CO 3溶液、BaCl 2溶液及适量的盐酸等除杂、精制。
则加入试剂合理的顺序为____________________(只写一种情况)、盐酸。
加盐酸的作用是(用化学方程式表示):__________________________,____________________________。
(2)制碱原理为:NaCl +CO 2+NH 3+H 2O===NaHCO 3↓+NH 4Cl ,该反应原理可看作是由①CO2+NH3+H2O===NH4HCO3和②NaCl+NH4HCO3===NaHCO3↓+NH4Cl两个反应加合而成,则其反应类型为______________。
(3)X的化学式为________。
(4)Y是滤液中的最主要成分,Y与Ca(OH)2反应的产物之一可用于循环使用,该产物的名称为______,Y的化学式为________,写出Y的一种用途:______________。
19.(2012年江苏盐城)某兴趣小组对食用纯碱和食用小苏打两种粉末进行以下探究。
【查阅资料】(1)探究两者水溶液酸碱性的差异。
小明分别向等浓度的两种溶液中滴入酚酞溶液,发现两者都变______色,但食用纯碱溶液中颜色更深,由此推测__________溶液碱性可能更强。
小欢认为要比较两种溶液的碱性强弱,可直接用________进行测定。
(2)验证两种粉末的稳定性。
在老师的指导下,该小组按下图装置进行实验操作,观察到________(填“甲”或“乙”)烧杯中澄清石灰水变浑浊,试管中发生反应的化学方程式为:___________________________,装置中棉花的作用是________________________________。
第21讲常见的盐和化学肥料【中考演练】答案1.D解析:合理施用化肥能提高农作物的产量。
2.B3.B解析:X、Y是相交关系,溶质和溶液、复分解反应和中和反应彼此都是包含关系,原子核和电子是并列关系。
4.D解析:H2SO4和BaCl2生成新盐和新酸。
5.D 6.B7.C8.C解析:氢氧化钙和碳酸钠也能生成碳酸钙。
9.A解析:草木灰(含K2CO3)显碱性,与铵盐混合会发生反应生成氨气,降低肥效,A不合理。
10.B 解析:A 中BaCl 2与Na 2CO 3,D 中NaOH 与HNO 3都会发生反应;而C 中FeCl 3为黄色。
11.(1)密封保存,防潮防晒(2)NH 4HCO 3+Ca(OH)2===CaCO 3+2H 2O +NH 3↑ 蓝 12.(1)4 (2)14∶5 (3)17.7% 13.(1)③ (2)酸(3)CaCO 3+2HCl===CaCl 2+H 2O +CO 2↑或Mg(OH)2+2HCl===MgCl 2+2H 2O 过量的稀盐酸会与锅炉中的金属铁发生反应,损坏锅炉14.(1)Na 2CO 3和BaCl 2 CuSO 4和NH 4Cl (2)Na 2CO 3+BaCl 2===BaCO 3↓+2NaCl 15.(1)纯碱(苏打) H 2O (2)化合反应(3)作燃料 CuO +CO=====△Cu +CO 2 (4)NaOH16.(1)尿素 碳酸氢铵 氯化铵 (2)无 (3)能 (4)NH 3·H 2O 17.[实验探究] ②变蓝 碱 酸③产生大量气泡 2HCl +K 2CO 3===2KCl +CO 2↑+H 2O ④产生白色沉淀,有刺激性气味的气体生成 [交流共享]否 [知识拓展]C18.(1)NaOH 、BaCl 2、Na 2CO 3(或BaCl 2、NaOH 、Na 2CO 3,或BaCl 2、Na 2CO 3、NaOH) NaOH +HCl===NaCl +H 2O Na 2CO 3+2HCl===2NaCl +CO 2↑+H 2O (2)复分解反应 (3)CO 2 (4)氨气 NH 4Cl 作氮肥19.(1)红 食用纯碱(或Na 2CO 3) pH 试纸 (2)乙 2NaHCO 3=====△Na 2CO 3+CO 2↑+H 2O 防止加热时小苏打(或NaHCO 3)粉末进入导管。