铁和铜及其化合物知识点
- 格式:doc
- 大小:88.00 KB
- 文档页数:5


高中化学【铁、铜及其化合物】基础知识一、铁及其化合物1. 知识网络构建2. 重要反应必练写出下列反应的方程式,是离子反应的写出离子方程式。
①Fe高温下和水蒸气的反应:________________________②Fe2O3和Al在高温下反应:_________________________③Fe2O3和CO的反应:_________________________________④Fe和过量稀HNO3的反应:_____________________________⑤过量铁粉和稀HNO3的反应:____________________________⑥FeCl3溶液和Cu的反应:____________________________⑦FeCl3溶液和KSCN溶液的反应:______________________⑧FeO和稀HNO3的反应:___________________________⑨Fe3O4和稀HCl的反应:_________________________⑩Fe3O4和稀HNO3的反应:___________________________⑪Fe(OH)2和稀HNO3的反应:____________________________⑫Fe(OH)2长时间置于空气中:__________________________⑬FeCl2溶液中通入Cl2:__________________________⑭FeCl2溶液中加入NaClO:__________________________⑮FeCl2溶液中加入等物质的量的Na2O2:______________⑯FeCl2溶液中加入HNO3:_________________⑰FeCl2溶液中加入酸性KMnO4溶液:______________________⑱Fe(OH)3与HI的反应:____________________________⑲Fe2(SO4)3溶液中通入SO2气体:_____________________⑳FeCl3溶液中通入H2S气体:_____________________○21FeI2和少量Cl2反应:_______________________○22FeI2和过量Cl2反应:______________________3. 实验现象强化记忆①铁丝在氧气中燃烧的现象___________________。

第12讲 铁铜及其化合物一 铁的位置和物理性质1.铁及其化合物间的主线Fe―→⎩⎪⎨⎪⎧FeO Fe 2O 3Fe 3O 4―→⎩⎨⎧Fe OH2Fe OH 3―→⎩⎨⎧FeSO 4·7H 2OFeCl 32.铁及其化合物间的转化关系3.铁元素的变价 (1)单质铁①生成+2价:铁与S 、H +、Cu 2+、I 2等反应生成+2价。
如:Fe +SFeS 、Fe +Cu 2+===Fe 2++Cu 。
①生成+3价:铁与Cl 2、Br 2等反应生成+3价。
如2Fe +3Cl 2=====点燃2FeCl 3。
①生成+2、+3价:铁与H 2O 、O 2反应生成Fe 3O 4。
3Fe +4H 2O(g)=====高温Fe 3O 4+4H 2。
①铁与HNO 3反应:当Fe 过量生成+2价,3Fe +8H ++2NO -3===3Fe 2++2NO +4H 2O ; 当Fe 不足时生成+3价,Fe +4H ++NO -3===Fe 3++NO +2H 2O 。
(2)铁的化合物:FeO 、Fe 3O 4、Fe 2O 3、Fe(OH)2、Fe(OH)3、Fe 2+、Fe 3+等。
+2价铁具有还原性,与强氧化性物如HNO 3、Cl 2等发生氧化还原反应: 如:3FeO +10HNO 3===3Fe(NO 3)3+NO +5H 2O 。
+3价铁具有氧化性,与强还原性物质, 如:HI 、Fe 、Cu 、I -、S 2-等发生氧化还原反应,如:Fe 2O 3+6HI===2FeI 2+I 2+3H 2O,2Fe 3++Cu===2Fe 2++Cu 2+。
特别强调:①Fe 与一般酸反应生成Fe 2+,与酸的量无关,但Fe 与稀HNO 3反应时最终铁的价态与铁的量有关。
①铁与硫蒸气反应生成的是FeS 而不是Fe 2S 3;铁与碘蒸气反应生成的是FeI 2而不是FeI 3。
4.铁的氧化物特别强调:①FeO 、Fe 3O 4、Fe 2O 3与硝酸反应时均生成Fe 3+。

Fe 铜、铁及其化合物一、铁及其化合物1.物理性质:银白色,具有金属光泽;质地较软,有良好的导电性、延展性。
密度7.86 g/cm 3,熔沸点较高。
位置:第四周期,第Ⅷ 族 2.化学性质:(1)与非金属反应 Fe+S (I 2)FeS (FeI 2) 4Fe+3O 22Fe 3O 4 2Fe+3Cl 2(Br 2)2FeCl 3弱氧化剂 Fe 3+、H +、I 2、S 、铁后的金属阳离子(置换)… 强氧化剂 Cl 2、Br 2、HNO 3、浓H 2SO 4、MnO 4-(H +) … (2)与水反应 3Fe + 4H 2O(g)Fe 3O 4 + 4 H 2 ↑(置换)注意:铁在常温下不会和水发生反应,但在水和空气中O 2和CO 2的共同作用下,铁却很容易被腐蚀(生锈/电化学腐蚀) (3) 与酸反应a.与非氧化性酸反应 Fe +2H +== Fe 2++ H 2 b.与氧化性酸反应c.常温下,铁在冷浓硫酸,浓硝酸中发生钝化d.与浓硫酸反应:2Fe +6 H 2SO 4(浓)Fe 2(SO 4)3 +3SO 2 +6 H2Oe.与稀硝酸反应:①当Fe 少量时,离子方程式为:Fe + 4H ++ NO 3-== Fe 3++NO↑+2H 2O②当Fe 过量时,,离子方程式为:3Fe+8H ++2NO 3-== 3Fe 2++2NO↑+4H 2O ③当1:4<n( Fe) :n (HNO 3)<3:8 时,此情况下,Fe 3+和Fe 2+共存。
(4)与盐溶液反应:2Fe 3++ Cu = 2Fe 2++ Cu 2+ Fe + 2Fe 3+ = 3 Fe 2+ Fe + Cu 2+ = Fe 2++ Cu3.铁的氧化物FeO Fe 2O 3 Fe 3O 4 铁的化合价 +2 +3 +2、+3 颜色、状态黑色粉末红棕色粉末 黑色晶体 俗名 铁红 磁性氧化铁 水溶性 不溶于水 不溶于水 不溶于水氧化物类别碱性氧化物碱性氧化物Fe 2+Fe 3+与非氧化性酸反应FeO+2H + =Fe2+ +H2O Fe2O3+6H + =2Fe3+ +3H2O Fe3O4+8H + =2Fe3+ + Fe2++4H2O与还原剂反应(H2、CO、Al等) FeO+CO Fe+CO2Fe2O3+3CO2Fe+3CO23Fe3O4+8Al9Fe+4Al2O3用途用作红色油漆和涂料;赤铁矿是炼铁原料注:3FeO+10HNO3(稀)=3Fe(NO3)3+NO↑+5H2O4、铁的氢氧化物(1)Fe(OH)2的制备Fe(OH)2易被氧化,在制备时应注意:①FeSO4晶体中不能有 Fe3+;②配制后的FeSO4溶液中要加入少量铁粉;③配制溶液的蒸馏水以及所用NaOH溶液均须煮沸以除去其中溶解的氧气;实验:FeSO4溶液中加NaOH.①现象:生成白色沉淀,后又迅速转变为灰绿色,最后生成红褐色②Fe2+容易被氧化,所以FeSO4溶液要新配制.③为了防止滴加NaOH时带入空气,可将吸收NaOH的长滴管伸入FeSO4溶液液面下,再挤出NaOH溶液.④为了防止Fe2+被氧化,还可以向盛有FeSO4溶液的试管中加入少量煤油或其它密度比水小但不溶于水的有机物以隔绝空气.化学方程式: FeSO4 + 2NaOH = Fe(OH)2↓+Na2SO4 Fe2++ 2OH -= Fe(OH)2↓(白色)4Fe(OH)2 + O2 + 2H2O = 4Fe(OH)3(红褐色)(白色→灰绿色→红褐色)(2)Fe(OH)3的制备实验:FeCl3溶液中加NaOH溶液.①现象:生成红褐色沉淀②化学方程式:FeCl3+3NaOH= Fe(OH)3↓+3NaCl Fe 3++ 3OH -= Fe(OH)3↓(红褐色)③热稳性:Fe(OH)3对热不稳定,受热能失去水生成红棕色的Fe2O3粉末.化学方程式: 2Fe(OH)3Fe2O3 +3H2O[小结]难溶性或微溶性的碱受热不稳定,容易分解。


第8讲铁、铜及其重要化合物【考纲要求】1.了解铁单质及化合物的颜色.状态及性质。
2.通过合金材料了解铜及化合物的性质。
3.能用氧化还原反应的规律探究铁的化合物之间的相互转化。
4.能掌握氢氧化铁胶体制备,能列举合金材料的应用。
【自学反馈】1、铁及其重要化合物(1)铁的氧化物的比较化学式FeO Fe2O3Fe3O4俗称—铁红磁性氧化铁色态黑色粉末红棕色粉末黑色晶体价态+2 +3 1/3+2价,2/3+3价水溶性不溶不溶不溶与酸的反应FeO+2H+===Fe2++H2O遇氧化性酸生成Fe3+盐Fe2O3+6H+===2Fe3++3H2OFe3O4+8H+===Fe2++2Fe3++4H2O与CO的反应高温FexOy+yCO===xFe+yCO2(2)Fe2+和Fe3+ 的比较Fe2+Fe3+水合离子颜色浅绿色棕黄色氧化还原性既有氧化性,又有还原性只有氧化性水解性Fe2+ +2H2O←→Fe(OH)2+2H+Fe3+ +3H2O←→Fe(OH)3+3H+与碱的反应Fe2+ +2OH—=== Fe(OH)2↓Fe3+ +3OH—=== Fe(OH)3↓(3)Fe(OH)2与Fe(OH)3的比较Fe(OH)2Fe(OH)3颜色状态白色固体红褐色固体水溶性不溶不溶稳定性易氧化为Fe(OH)3,空气中加热得不到FeO较稳定:∆Fe(OH)3== Fe2O3+3H2O与酸的反应Fe(OH)2+2H+=== Fe2+ +3H2O Fe(OH)3+3H+=== Fe3+ +3H2O制法在隔绝O2的条件下Fe2+与碱反应Fe3+与碱反应(4)铁三角:(5)检验Fe3+.常用方法有:A.向未知溶液滴入少量KSCN溶液呈血红色。
B.向未知溶液滴入少量苯酚溶液呈紫色。
C.向未知溶液中滴入少量NaOH溶液呈红褐色。
D.检验Fe+.是向未知溶液滴入少量KSCN溶液呈无色,继续滴入少量氯水呈血红色。
2、铜及其重要化合物1.2Cu+S ==== Cu2S2.Cu+2H2SO4(浓) ===== CuSO4+SO2↑+H2O3. CuSO4+Zn ==== ZnSO4+ Cu CuSO4+Fe ==== FeSO4+ Cu4. CuCl2+Fe ==== FeCl2+ Cu CuCl2 ===== Cu+Cl25. Cu+Cl2 ===== CuCl26. 2Cu+O2+H2O+CO2 ===== Cu2(OH)2CO37. Cu2(OH)2CO3 ===== 2CuO+CO2↑+H2O↑8. 2Cu+O2 ==== 2CuO9. CuO+CO ==== Cu+CO2 CuO+H2 ==== Cu+H2O10. Cu(NO3)2+Zn ==== Zn(NO3)2+Cu11. 3Cu+8HNO3 (稀) ==== 3Cu(NO3)2+2NO↑+4H2O12. CuO+2HNO3 ==== Cu(NO3)2+H2O13. 2Cu( NO3)2 ==== CuO+4NO2↑+O2↑14. Cu(NO3)2+2NaOH ==== Cu(OH)2↓+2NaNO315. Cu(OH)2+2HNO3 ==== Cu(NO3)2+2H2O16. 2 Cu(OH)2+R-CHO—→R- COOH+ Cu2O↓+2H2O17. Cu(OH)2 ==== CuO+H2O【例题解析】[例1]下列物质发生反应时其离子方程式正确的是()A.铁与三氯化铁溶液反应:Fe+Fe3+=2Fe2+B.足量的氯气通入溴化亚铁溶液中:2Fe2++4Br-+3Cl2=2Fe3++2Br2+6Cl-C. Fe(OH)3跟盐酸反应:Fe(OH)3+3H+=Fe3++3H2OD. FeS跟稀哨酸反应:FeS+2H+=Fe2++H2S[例2]在烧制砖瓦时,用粘土做成的坯经过烘烧后,铁的化合物转化成而制得红色砖瓦。

铜及其化合物知识点铜是一种常见的金属元素,化学符号为Cu。
它具有良好的导电性和导热性,因此被广泛应用于电子、建筑和工业领域。
以下是一些关于铜及其化合物的知识点:- 物理性质:铜具有金属光泽,呈红褐色。
它的熔点为1083摄氏度,沸点为2567摄氏度。
铜是柔软的,并且具有良好的延展性和可塑性。
物理性质:铜具有金属光泽,呈红褐色。
它的熔点为1083摄氏度,沸点为2567摄氏度。
铜是柔软的,并且具有良好的延展性和可塑性。
- 化学性质:铜在常温下相对稳定,不容易被空气和水腐蚀。
然而,它会与一些酸和氧化剂发生反应,生成相应的化合物。
化学性质:铜在常温下相对稳定,不容易被空气和水腐蚀。
然而,它会与一些酸和氧化剂发生反应,生成相应的化合物。
- 铜离子:在化学反应中,铜原子往往失去2个电子,形成Cu2+离子。
这种离子具有蓝色,并且在化合物中起着重要的作用。
铜离子:在化学反应中,铜原子往往失去2个电子,形成Cu2+离子。
这种离子具有蓝色,并且在化合物中起着重要的作用。
- 铜的化合物:铜可以形成多种化合物,包括氧化物、硫化物、氯化物和硝酸铜等。
这些化合物在工业上有广泛的应用,如颜料、杀菌剂和催化剂等。
铜的化合物:铜可以形成多种化合物,包括氧化物、硫化物、氯化物和硝酸铜等。
这些化合物在工业上有广泛的应用,如颜料、杀菌剂和催化剂等。
- 应用领域:铜广泛应用于电子行业,如电线、导线和电路板等。
此外,它还用于建筑和装饰,如屋顶、管道和雕塑等。
应用领域:铜广泛应用于电子行业,如电线、导线和电路板等。
此外,它还用于建筑和装饰,如屋顶、管道和雕塑等。
以上是关于铜及其化合物的一些基本知识点。
了解铜的性质和应用领域,有助于我们更好地理解和应用这种重要的金属元素。
铜及其化合物知识点铜是一种常见的金属元素,化学符号为Cu。
它具有良好的导电性和导热性,因此被广泛应用于电子、建筑和工业领域。
以下是一些关于铜及其化合物的知识点:- 物理性质:铜具有金属光泽,呈红褐色。

铁、铜及其重要化合物中的知识要点1.铁元素在周期表中的位置:第四周期、第VIII族;电子排布式:1s22s22p63s23p63d64s22.铜元素在周期表中的位置:第四周期、第I B族;电子排布式:1s22s22p63s23p63d104s13.铁丝在氧气中燃烧的现象:火星四射,生成黑色固体。
方程式:3Fe+2O2=Fe3O44.铁丝在氯气中燃烧的现象:产生棕黄色烟。
方程式:2Fe+3Cl2=2FeCl35.Fe与Br2反应:2Fe+3Br2=2FeBr36.Fe与I2反应:Fe+I2=FeI27.铁粉与硫粉混合加热的现象:生成黑色固体。
方程式:Fe+S=FeS8.稀HNO3与少量的铁反应:4HNO3(稀)+Fe = Fe(NO3)3+NO↑+2H2O9.稀HNO3与过量的铁反应:8HNO3(稀)+3Fe = 3Fe(NO3)2+2NO↑+4H2O10.铁不能与冷水、热水反应,但在水和空气中的O2、CO2等共同作用下,铁很容易被腐蚀。
在高温下,铁能与水蒸气发生反应,现象是红热的铁与水蒸气反应放出气体,蒸发皿中产生大量肥皂泡,点燃肥皂泡可听到爆鸣声,反应后,试管中固体仍呈黑色。
化学方程式:3Fe+4H2O(g)=Fe3O4+4H211.FeO与稀HNO3反应:3FeO+10HNO3=3Fe(NO3)3+NO↑+5H2O12.Fe3O4与热的浓盐酸反应:Fe3O4+8HCl(浓)=2FeCl3+FeCl2+4H2O13.Fe(OH)2的制备:在FeSO4溶液中加入NaOH溶液(1)现象:生成白色絮状沉淀,若在溶液中有氧气则迅速转变成灰绿色,最后生成红褐色沉淀。
(2)有关的方程式:FeSO4+2NaOH=Fe(OH)2↓+Na2SO4; 4Fe(OH)2+O2+2H2O=4Fe(OH)3(3)注意事项:①FeSO4溶液必须是新制备的并放入铁粉,以防止Fe2+被氧化成Fe3+;②加热煮沸NaOH溶液以除去溶液中的氧气;③为了防止滴加NaOH溶液时带入空气,可将吸收NaOH的长滴定管伸入到FeSO4溶液液面以下,再挤出NaOH溶液;④为了防止Fe2+被氧化,还可以向盛有FeSO4溶液的试管中加入少量煤油或其它密度比谁小的但不溶于水的有机物以隔绝空气,进行液封。

铜及其化合物知识点讲解一、铜的性质1.物理性质:铜是一种红色的金属,具有良好的延展性和导电性。
它的密度为8.96克/立方厘米,熔点为1083℃,沸点为2595℃。
2.化学性质:铜在常温下稳定,但受空气中的氧气和湿气影响会逐渐变成深绿色的“铜绿”。
铜的最常见化合价为+1和+2,在化合物中可以形成氧化物、硫化物、氯化物等多种化合物。
二、铜的应用1.电工行业:由于铜具有良好的导电性和导热性,广泛用于电线、电缆、变压器线圈等电工设备中。
铜导线具有较低的电阻率和较高的传导性能,可以保证电能的有效输送。
2.冶金工业:铜是一种重要的冶金原料,广泛用于制造铜合金、铜管、铜板等冶金产品。
铜合金具有优异的力学性能和耐腐蚀性,被广泛应用于航空、航天、汽车、电子等领域。
3.化工行业:铜盐是广泛应用的铜化合物。
铜硫酸盐、铜乙酸盐等广泛用于农业杀菌剂、兽药、木材防腐等领域。
铜催化剂也是许多有机合成反应中的重要催化剂。
4.装饰工艺品:铜和铜合金具有美观的外观和良好的加工性能,被广泛用于制作工艺品、雕塑、钟表等装饰品。
三、铜的主要化合物1.氧化物:铜氧化物包括氧化亚铜(Cu2O)和氧化铜(CuO)。
氧化亚铜是一种红色固体,被广泛应用于染料工业和电池制造等领域。
氧化铜是一种黑色固体,也具有一定的应用价值。
2.硫化物:铜硫化物包括二硫化二铜(Cu2S)和硫化铜(CuS)。
二硫化二铜是一种黑色结晶固体,用作染料和催化剂。
硫化铜是一种绿色结晶固体,具有一定的应用价值。
3.氯化物:铜氯化物主要有氯化亚铜(CuCl)和氯化铜(CuCl2)。
氯化亚铜是一种白色结晶固体,在化学分析中常用作试剂。
氯化铜是一种绿色结晶固体,是一种重要的化工原料。
总结:铜及其化合物是人类生活和工业生产中不可或缺的重要物质。
铜具有良好的导电性和导热性,被广泛应用于电工设备和冶金工业。
铜化合物则具有多种应用,如染料工业、农药、化工原料等。
深入了解铜及其化合物的性质和应用,有助于推动相关领域的发展和创新。
一、铁的结构和性质铁是26号元素,位于第四周期第Ⅷ族,属于过渡元素。
原子结构示意图:主要化合价:+2,+32.铁在金属的分类中属于黑色金属,重金属,常见金属。
纯净的铁是光亮的银白色金属,密度为7.86g/㎝3,熔沸点高,有较好的导电、传热性,能被磁铁吸引,也能被磁化。
还原铁粉为黑色粉末。
3.铁是较活泼的金属元素,在金属活动性顺序表中排在氢的前面。
①跟非金属反应:点燃点燃△3Fe+2O2 == Fe3O4 2Fe+3Cl2 ==2FeCl3 Fe+S== FeSFe+I2= FeI2②跟水反应:3Fe+4H2O= Fe3O4+4H2↑③跟酸作用:Fe+2H+=Fe2++H2↑(遇冷浓硝酸、浓硫酸钝化;与氧化性酸反应不产生H2,且氧化性酸过量时生成Fe3+)④与部分盐溶液反应:Fe+Cu2+=Fe2++Cu Fe+2Fe3+=3Fe2+ 。
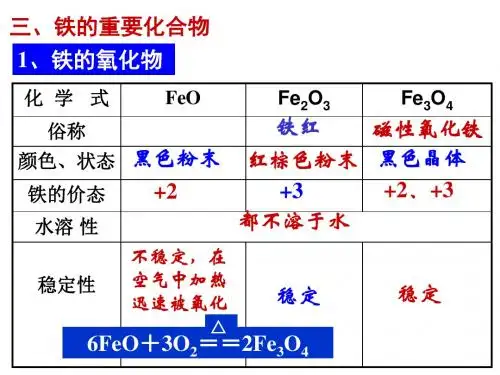
)二、铁的氧化物和氢氧化物1.铁的氧化物的比较铁的氧化物FeO Fe2O3 Fe3O4俗称铁红磁性氧化铁色、态黑色粉末红棕色粉末黑色晶体铁的价态+2 +3 +2、+3水溶性难溶于水稳定性不稳定性6FeO+O2=2Fe3O4 稳定稳定与酸的反应FeO+2H+=Fe2++H2O Fe2O3+6H+=2Fe3++3H2 Fe3O4+8H+=2Fe3++Fe2++4H2O 与CO的反应FexOy+yCO=xFe+yCO2制取高温熔融,过量的铁与氧气反应2Fe+O2=2FeO Fe(OH)3的分解2Fe(OH)3=Fe2O3+3H2O 铁在氧气中燃3Fe+2O2=Fe3O4 2.铁的氢氧化物的比较Fe(OH)2 Fe(OH)3物理性质白色,难溶于水的固体红褐色,难溶于水的固体化学性质(1)与非氧化性强酸反应Fe(OH)2+2H+=Fe2++2H2O Fe(OH)3+3H+=Fe3++3H2O(2)与氧化性酸反应3Fe(OH)2+10HNO3=3Fe(NO3)3+NO↑+8H2O(3)空气中放置被氧化4Fe(OH)2+2H2O+O2=4Fe(OH)3 受热分解2Fe(OH)3=Fe2O3+3H2O制备①煮沸蒸馏水,赶走溶解的氧气将NaOH溶液滴入Fe2(SO4)3溶液中②煮沸NaOH溶液,赶走溶解的氧气 Fe3++3OH-=Fe(OH)3↓③配制FeSO4溶液,加少量的还原铁粉④用长滴管将NaOH溶液送入FeSO4溶液液面以下Fe2++2OH-=Fe(OH)2↓1. Fe3O4是复杂的化合物,经研究证明,在Fe3O4晶体中有1/3的Fe是+2价,有2/3的Fe是+3价,可看成FeO·Fe2O3,实际应写成Fe(FeO2)2,即铁酸亚铁盐,不是一般的氧化物。
铁和铜及其化合物知识点总结1、铁、铜性质① 2Fe + 3Cl22FeCl3② 2Fe + 3Br2 == 2FeBr3③ Fe + I2 == FeI2④ 3Fe + 2O2Fe3O4 ( +2价占1/3,+3价占2/3) ① Cu + O22CuO② Cu + Cl2CuCl2③ 2Cu + S Cu2S3Fe + 4H2O(g) Fe3O4 + 4H2↑2、铁及其化合物的主要反应:①氯化铁溶液中加入铁粉(除去氯化亚铁中的氯化铁):2FeCl3 + Fe == 3FeCl22Fe3+ + Fe == 3Fe2+②铁与硫酸铜反应(湿法炼铜):Fe + CuSO4 == FeSO4 + Cu Fe + Cu2+ == Fe2+ + Cu③氯化亚铁溶液中滴加氯水(除去氯化铁中的氯化亚铁):2FeCl2 + Cl2 == 2FeCl32Fe2+ + Cl2 == 2Fe3+ + 2Cl-④氢氧化亚铁在空气中变质:4Fe(OH)2 + O2 + 2H2O == 4Fe(OH)3⑤铜与氯化铁反应(用氯化铁腐蚀铜电路板):2FeCl3 + Cu == 2FeCl2 + CuCl22Fe3+ + Cu == 2Fe2+ + Cu2+3、Fe2+与Fe3+的相互转化:(1)Fe2+ → Fe3+:Fe2+与强氧化剂(如Cl2、Br2、O2、HNO3、KMnO4、浓H2SO4、H2O2等)反应时,被氧化成Fe3+:如:2Fe2+ + Cl2 == 2Fe3+ + 2 Cl−3Fe2+ + 4H+ + NO3− == 3Fe3+ + 2H2O + NO↑(2)Fe3+ → Fe2+:Fe3+与还原剂(如Zn、Fe、Cu、S2−、I−、H2S等)反应时,被还原成Fe2+:如:Fe + 2Fe3+ == 3Fe2+Cu + 2Fe3+ == Cu2+ + 2Fe2+2I− + 2Fe3+ == I2 + 2Fe2+4、Fe3+(黄色)的检验:实验①:向FeCl3溶液中加入几滴KSCN溶液,溶液显血红色Fe3+ + 3SCN− == Fe(SCN)3(血红色溶液)实验②:向FeCl3溶液加入NaOH溶液,有红褐色沉淀Fe3+ + 3OH− == Fe(OH)3↓Fe2+(浅绿色)的检验:实验①:向FeCl2溶液加入NaOH溶液Fe2+ + 2OH− == Fe(OH)2↓(白色)4Fe(OH)2 + O2 + 2H2O == 4Fe(OH)3(红褐色)实验②:加入KSCN溶液,无现象,再加入适量氯水,溶液显血红色1。
铁及其化合物知识点
一.化学性质:
1.与非金属反应 4Fe+3O2 2Fe3O4 2Fe+3Cl2(Br2) 2FeCl3
2.与水反应3Fe + 4H2O(g) Fe3O4 + 4 H2↑(置换)
3 与酸反应
1)与非氧化性酸反应 Fe +2H+== Fe2+ + H2
2)与氧化性酸反应
a)常温下,铁在冷浓硫酸,浓硝酸中发生钝化
b)与浓硫酸反应:2Fe +6 H2SO4(浓)Fe2(SO4)3 +3SO2 +6 H2O
4.与盐反应2Fe 3++ Cu = 2Fe 2++ Cu 2 Fe + 2Fe3+ = 3 Fe2+ Fe + Cu2+ = Fe2+ + Cu
二、铁的化合物
1、铁的氧化物
FeO Fe2O3Fe3O4
铁的化合价+2+3+2、+3
颜色、状态黑色粉末红棕色粉末黑色晶体
俗名铁红磁性氧化铁
水溶性不溶于水不溶于水不溶于水
氧化物类别碱性氧化物碱性氧化物
与非氧化性酸反应FeO+2H + =Fe2+ +H2O Fe2O3+6H + =2Fe3+ +3H2O Fe3O4+8H+ =2Fe3+ +
Fe2++4H2O
与还原剂反应(H2、CO、Al等)FeO+CO Fe+CO2Fe2O3+3CO
2Fe+3CO2
3Fe3O4+8Al
9Fe+4Al2O3
用途用作红色油漆和涂料;
赤铁矿是炼铁原料
2、铁的氢氧化物
(1)Fe(OH)2的制备
Fe(OH)2易被氧化,在制备时应注意:⑴ FeS O4晶体中不能有 Fe3+;⑵配制后的FeSO4溶液中要
加入少量铁粉;⑶配制溶液的蒸馏水以及所用NaOH溶液均须煮沸以除去其中溶解的氧气;
实验:FeSO4溶液中加NaOH.
①现象:生成白色沉淀,后又迅速转变为灰绿色,最后生成红褐色
③为了防止滴加NaOH时带入空气,可将吸收NaOH的长滴管伸入FeSO4溶液液面下,再挤出NaOH溶液.
④为了防止Fe2+被氧化,还可以向盛有FeSO4溶液的试管中加入少量煤油或其它密度比水小但不溶于水的有机物以隔绝空气.
化学方程式: FeSO4 + 2NaOH = Fe(OH)2↓+Na2SO4 Fe2++ 2OH -= Fe(OH)2↓(白色)
4Fe(OH)2 + O2 + 2H2O = 4Fe(OH)3(红褐色)
(白色→灰绿色→红褐色)
(2)Fe(OH)3胶体的制备
向加热沸腾的蒸馏水中加入FeCI3溶液,待出现红褐色时,停止加热,便可得到 Fe(OH)3胶体。
制备时要注意:⑴不可长时间加热,因为加热会使胶体凝聚;⑵不能用自来水,因为自来水中的电
解质也可使胶体凝聚。
3.铁的两种氢氧化物的比较
化学式Fe(OH)2Fe(OH)3
色、态白色固体红褐色固体
溶解性难溶于水难溶于水
热稳定性分解产物复杂2Fe(OH)3 Fe2O3 +3H2O
四.铁盐和亚铁盐
(1)Fe3+、Fe2+的检验:
○1.Fe3+的检验: +盐溶液中滴加KSCN溶液。
现象是溶液变红色,反应方程式:FeCl3+3KSCN=
Fe(SCN)3+3KCl Fe 3++3SCN -= Fe(SCN)3(红色)
2.向Fe3+盐溶液中滴加NaOH溶液,现象是产生红褐色沉淀,反应方程式:FeCl3+3NaOH= Fe(OH)3↓+3NaCl Fe 3++ 3OH -= Fe(OH)3↓(红褐色)
○2.Fe2+的检验: ①向Fe2+盐溶液中滴加KSCN溶液,再滴加氯水(硝酸、H2O2等)。
现象是先无现象,加氯水后溶液呈红色,反应方程式:2FeCl2+Cl2=2FeCl3②向Fe2+盐溶液中滴加NaOH溶液,现象是产生白色沉淀迅速转变为灰绿色,最后变成红褐色沉淀,反应方程式:FeCl2+2NaOH= Fe(OH)2↓+2NaCl
4Fe(OH)2+O2+2H2O=4Fe(OH)3(红褐色)
(2)Fe3+的氧化性、Fe2+的还原性
①Fe3+的氧化性:
向FeCl3溶液中加入铁粉,现象是溶液由棕黄色变为浅绿色
对应离子方程式:2Fe3+(棕黄色)+Fe=3Fe2+(浅绿色)
Fe3+还可以与HI、H2S 2Fe 3++ 2I- =2Fe 2+ + I2 2Fe 3++ H2S =2Fe 2++2H + + S↓
②Fe2+的还原性:Fe2+在较强的氧化剂的作用下会被氧化为Fe3+
向FeCl2溶液中通入氯气,现象是溶液由浅绿色变为棕黄色
对应离子方程式:2Fe2++Cl2= 2Fe3++2Cl-
除杂: FeCl3(FeCl2) 滴加氯水 FeCl2 (FeCl3) 加入铁粉
(3).亚铁盐、铁盐溶液的保存
○1FeCI2、FeSO4等亚铁盐溶液保存时,要加入少量铁屑(防止 Fe2+被氧化)和滴入少量相应的
酸溶液 ( 抑制 Fe2+水解) 。
另外要注意,保存 Fe(NO3)2溶液时,只要加铁屑防止氧化即可,不能
加HNO3来防止水解。
○2FeCl3、Fe2(SO4)3等铁盐溶液保存时,要加少量相应的酸溶液(抑制Fe3+水解)。
(4).Fe3+盐的水解
Fe3+为典型的弱碱阳离子,通常情况下,在水溶液中只有少部分发生水解。
但在一定条件(如加
热,遇AlO2-、CO32-、CIO-等)下,水解程度会增大,甚至会发生彻底的双水解。
如:Fe3+ +3AlO2-+6H2O == Fe(OH)3↓+3AI(OH)3↓
2Fe3+ +3CO32-+3H2O == 2Fe(OH)3↓+3CO2↑
Fe3+ +3ClO-+3H2O == Fe(OH)3↓+3HCIO
另外,加热并蒸干FeCI3的水溶液,由于 FeCl3+3H2O Fe(OH)3+3HCl为一吸热反应,且 HCl 易挥发,加热会使平衡不断向右移动,FeCl3最终变成 Fe(OH)3,再灼烧,2Fe(OH)3Fe2O3+3H2O,最后留下的物质为 Fe2O3。
而加热并蒸干 Fe2(SO4)3的水溶液,由于Fe2(SO4)3水解产生的 H2S04难挥发,加热不会使平衡不断右移,只能使水份减少,酸度增强,最后仍留下Fe2(SO4)
铜的知识点整理
一.铜:
1)物理性质:颜色:红色(紫红色)金属
2).化学性质:价态:+1(不稳定) +2(稳定)
1.与某些非金属单质反应:
(1)与氧气反应:2Cu + O22CuO
(2)与硫反应:2Cu + S Cu2S (黑色物质)
(3)与氯气反应:Cu + Cl2 CuCl2 ( 棕黄色的烟)
2、与酸反应:(非氧化性酸不反应)
Cu + 2H2SO4(浓)CuSO4+SO2↑+2H2O
Cu + 4HNO3(浓) = Cu(NO3)2 + 2 NO2↑ + 2H2O
3Cu + 8HNO3(稀) = 3Cu(NO3)2 + 2 NO ↑ + 4H2O
3、与某些盐反应:
2FeCl3 + Cu = 2FeCl2 + CuCl2(印刷电路板)
二铜的氧化物:
CuO(黑色),Cu2O(红色)
(1). 与酸反应:
Cu2O + H2SO4 = CuSO4 + Cu + H2O
(2). 与还原性物质(如H2、CO、C等)反应:
CuO + co = Cu + CO2
三. 铜的氢氧化物及其反应
Cu(OH)2: 蓝色物质,不溶性弱碱,
1. 受热分解(是难溶碱的共性)
Cu(OH)2 CuO + H2O
2.弱氧化性:与新制氢氧化铜悬浊液反应
配制新制的Cu(OH)2悬浊液:
2ml 10%NaOH + 2%CuSO44~8滴蓝色絮状沉淀乙醛、加热红色沉淀Cu2O CH3CHO+2Cu(OH)2△ CH3COOH+Cu2O↓+2H2O (检验醛基)
四. 铜盐及其反应
(1). 碱式碳酸铜(铜绿)受热分解。