子宫内膜癌NCCN指南解读
- 格式:ppt
- 大小:1.01 MB
- 文档页数:19



2020年国际权威子宫内膜癌诊治指南解读(最全版)子宫内膜癌作为常见的女性生殖道恶性肿瘤,其发病率及死亡率近年来呈升高趋势。
据报道,2018年全球预计新发子宫内膜癌病例数为382069例,新增死亡例数为89929例[1]。
美国作为子宫内膜癌高发病率地区,2018年预计新发病例为63230例,新增死亡例数为11350例[2]。
在子宫内膜癌的诊治中,高危、复发及转移性子宫内膜癌一直是诊治的难点及重点。
目前,国际权威子宫内膜癌指南有3个:美国国家综合癌症网络(National Comprehensive Cancer Network,NCCN)子宫肿瘤临床实践指南[3]、国际妇产科联盟(Federation International of Gynecologyand Obstetrics,FIGO)子宫内膜癌诊治指南[4]及欧洲肿瘤内科学会(European Society for MedicalOncology,ESMO)子宫内膜癌临床实践指南[5~7],本文综合分析这三大国际权威指南的异同,解读三大指南的临床诊治要点。
1 诊断及筛查对于怀疑子宫肿瘤患者,应常规行血常规、肝肾功检查、生化检查、内膜活检及影像学检查,晚期患者可检查血CA125水平以监测病情及随访。
子宫内膜癌活检病理报告需包含肿瘤的组织类型及分化程度,同时完善胸腹部影像学检查以评估病情程度,决定后续治疗方式。
按照《第4版WHO女性生殖器官肿瘤组织学分类》[8],子宫内膜癌分为以下组织学类型:子宫内膜样腺癌、黏液性癌、浆液性癌、透明细胞癌、未分化癌、去分化癌、神经内分泌肿瘤及混合性癌。
其中子宫内膜样腺癌按肿瘤细胞分化程度分为高、中及低分化(G1、G2和G3),按照二分类法,G1和G2属于1型内膜癌,为雌激素依赖型,预后良好,而G3及其他非子宫内膜样腺癌类型的肿瘤均属于2型内膜癌,为非雌激素依赖型,预后较差。
子宫内膜癌在普通人群的筛查意义不大,出现绝经后出血或不规则阴道流血等症状后,阴道超声是首选的检查方法。


子宫内膜癌诊断与治疗指南一、本文概述《子宫内膜癌诊断与治疗指南》旨在为医疗专业人士提供关于子宫内膜癌的最新诊断与治疗策略的全面指南。
子宫内膜癌是一种常见的妇科恶性肿瘤,其早期诊断和恰当治疗对于提高患者生存率和生活质量具有重要意义。
本指南将结合最新的临床研究和医学进展,对子宫内膜癌的流行病学、病理生理学、临床表现、诊断方法、治疗策略以及预后评估等方面进行详细阐述。
本指南还将强调多学科协作在子宫内膜癌诊疗中的重要性,以推动子宫内膜癌的个体化、精准化治疗。
通过本指南的学习和应用,期望医疗专业人士能够提升对子宫内膜癌的诊疗水平,为患者提供更为优质的医疗服务。
二、子宫内膜癌的诊断子宫内膜癌的诊断通常涉及临床评估、实验室检查、影像学检查以及组织病理学检查等多个方面。
临床评估:医生会对患者进行详细的病史询问和体格检查,包括月经史、生育史、家族史等,以及观察是否存在异常阴道出血、腹部肿块、疼痛等症状。
实验室检查:血液检查可能包括全血计数、肝肾功能、肿瘤标志物等,以帮助评估患者的整体状况。
子宫内膜活检是诊断子宫内膜癌的关键步骤,可以通过刮宫术或宫腔镜检查获取子宫内膜组织样本。
影像学检查:超声检查是最常用的影像学检查方法,可以帮助确定肿瘤的大小、位置和浸润深度。
其他可能的影像学检查包括CT扫描、MRI和PET-CT等,这些检查可以提供更详细的肿瘤信息和评估疾病的分期。
组织病理学检查:这是确诊子宫内膜癌的金标准。
通过显微镜检查子宫内膜组织样本,病理学家可以观察到细胞的异常增生和恶性转化的证据。
免疫组化染色等技术还可以帮助进一步了解肿瘤的分子特征和预后。
子宫内膜癌的诊断需要综合临床评估、实验室检查、影像学检查和组织病理学检查等多个方面的信息。
正确的诊断是制定有效治疗方案的关键。
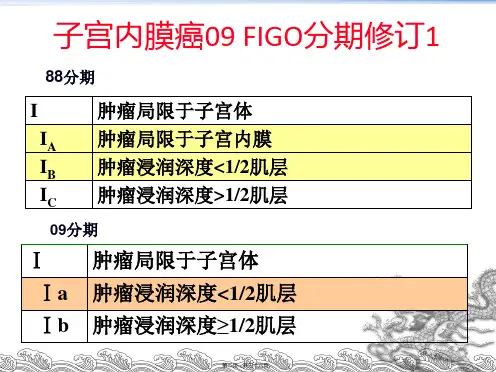
三、子宫内膜癌的分期与评估子宫内膜癌的分期是评估病情严重程度、制定治疗方案以及预测预后的重要依据。
根据国际妇产科联盟(FIGO)的分期系统,子宫内膜癌分为四期,即Ⅰ期、Ⅱ期、Ⅲ期和Ⅳ期。



子宫内膜癌癌症基因组图谱分子分型临床价值2024在妇科三大恶性肿瘤中,子宫内膜癌(endometrialcarcinoma,EC)由于被临床医生普遍认为是恶性程度较低,预后较好的肿瘤,故关注度不如子宫颈癌和卵巢癌。
其实,子宫内膜癌在临床诊治中经常有"出乎意料"的情况。
传统组织学分型和分级存在重复性低、对应性差、未考虑肿瘤异质性,对临床指导性差,越来越不能满足临床诊治的需求。
随着基因检测技术的发展,以及对肿瘤分子特征研究的深入,临床医生逐渐认识到,每种肿瘤的分子特性是恶性肿瘤精准诊治及预后的重要指标物。
2013年子宫内膜癌癌症基因组图谱(TCGA)分子分型的提出,以及2020年美国国立综合癌症网络(NCCN)指南第1版推荐了TCGA分子分型,推动了子宫内膜癌分子分型的临床应用。
国内相关的临床指南及专家共识也建议,在子宫内膜癌的病理报告、风险评估、诊疗流程中加入TCGA分子特征。
同时,分子分型还存在很多误区,临床实践中还存在诸多未厘清的问题。
因此,子宫内膜癌TCGA分子分型在临床应用中面临:机遇,挑战与突破。
1、子宫内膜癌TCGA分子分型在临床应用中面临的机遇1.1子宫内膜癌传统分型及病理学的局限性1983年Bohkman将流行病学、病理和临床特征联系起来,提出子宫内膜癌的两型分类模式,I型雌激素依赖型和II型非雌激素依赖型,二元分类成为过去30多年区分子宫内膜癌的重要框架。
但在实践中发现,根据子宫内膜癌组织形态学和免疫组化进行的I型和II型分类,患者预后与病理分型并不完全一致,给临床治疗带来很大困扰,比如:20%左右的肿瘤难以归纳到工型或者H型,另有约10%的肿瘤形态上是典型的子宫内膜样癌,但其生物学行为则是非子宫内膜样癌;透明细胞癌虽然在传统上被认为是口型子宫内膜癌,但是某些病例却表现出良好的预后和极低的复发率,而且,相当比例的透明细胞癌并无TP53的突变[1]β因此,二元分类法及组织病理学越来越显示出其局限性。

2022 NCCN子宫颈癌临床实践指南第一版解读(完整版)文章没有格式错误,但是有一些段落没有明显的信息或者重复了已经提到的内容,因此删除了这些段落。
同时,对每段话进行了小幅度的改写。
2022年NCCN子宫颈癌临床实践指南第一版解读子宫颈癌是全球女性第4大常见癌症,对女性健康构成了严重威胁。
为了更好地指导临床实践,美国国立综合癌症网络(NCCN)于2021年10月26日公布了“2022NCCN子宫颈癌临床实践指南(第1版)”。
该指南讨论的范围包括子宫颈鳞癌、腺鳞癌、腺癌以及小细胞神经内分泌癌。
主要更新新版指南主要更新了以下内容:1.持续性或复发转移子宫颈癌的监测方法为针对可疑部位进行影像学检查或选择性活检。
在此基础上新增:可采用有效的或经XXX(XXX)批准的基因组分析(CGP),如转移部位的组织活检难以获取可考虑血浆ctDNA检测进行CGP。
2.子宫颈神经内分泌癌组织形态学上类似于肺神经内分泌癌。
子宫颈小细胞神经内分泌癌免疫组化通常表现为染色粒素、CD56、突触素呈阳性。
3.影像学检查原则进行了较大修改:FIGOⅠB1~ⅠB3期不保留生育功能的患者首选盆腔增强MRI评估局部病灶;首选颈部/胸部/腹部/骨盆/腹股沟PET-CT或胸部/腹部/骨盆CT或PET-MRI评估全身情况。
保留生育功能患者首选盆腔MRI评估局部病灶和肿瘤与子宫颈内口的距离;MRI有禁忌者可行经超声检查进行评估。
全子宫切除术后意外发现的子宫颈癌患者,建议行颈部/胸部/腹部/骨盆/腹股沟PET-CT或胸部/腹部/骨盆CT评估转移性疾病和盆腔MRI评估盆腔残留病灶。
Ⅱ~ⅣA期患者亦首选盆腔增强MRI评估局部病灶。
小细胞神经内分泌癌首选颈部/胸部/腹部/骨盆/腹股沟PET-CT+脑部MRI进行评估。
4.复发转移性子宫颈癌(鳞状细胞癌、腺癌或腺鳞癌)一线联合治疗更新:PD- L1阳性患者首选帕博利珠单抗+顺铂/紫杉醇±贝伐珠单抗或帕博利珠单抗+卡铂/紫杉醇±贝伐珠单抗方案(1类证据);二线治疗药物新增纳武单抗用于PD-L1阳性患者(2A类证据);其他药物新增Tisotumab vedotin-tftv (抗体药物偶联物)(2A类推荐)。
