铜冶炼基础知识
- 格式:doc
- 大小:239.50 KB
- 文档页数:7

铜火法冶金原理基础知识全解1.铜矿的种类铜矿主要分为硫化铜矿和氧化铜矿两大类。
硫化铜矿包括黄铜矿、黄铜铁矿、黄铁矿等,氧化铜矿包括赤铁矿、绿矾石等。
不同的铜矿含有不同的铜含量和矿石结构,会影响到冶炼的方法和工艺流程的选择。
2.铜的提取方法铜的提取主要有火法冶金和湿法冶金两种方法。
火法冶金是指利用高温将铜矿石还原成金属铜的过程,而湿法冶金是指通过水溶液处理将铜离子沉积成金属铜的过程。
3.铜的火法冶金方法熔炼是将铜矿石与一定数量的焙烧助剂一起加入炉中,在高温下进行还原反应,将矿石中的铜鼓出来。
熔炼过程中,会采用不同的炉型,如隧道炉、转炉等,具体选择根据矿石种类和产量来决定。
焙烧是在熔炼之前将铜矿石进行预处理,使其中的硫化物转化为氧化物,提高熔炼效果。
焙烧会生成二氧化硫气体,需要进行捕集和处理,以减少环境污染。
浸出是将焙烧后的矿石进行浸出,从中提取出铜。
浸出过程可以采用硫酸浸出法或氨浸出法,具体选择取决于矿石和工艺条件。
4.铜的提纯方法通过火法冶炼得到的铜中还存在一些杂质,需要进行进一步的提纯。
铜的提纯主要有电解法和火法法两种。
电解法是将铜放入电解槽中,通过电解的方式将其中的杂质分离出来,得到纯净的铜。
电解法可以用于提纯高纯度铜,但成本较高。
火法法是指将铜通过高温蒸发和凝结的方式进行提纯。
火法法包括铸造法、蒸馏法和氧化冶炼法等。
不同的火法方法可以去除不同的杂质,从而得到高纯度的铜。
5.铜矿资源的循环利用铜矿资源是有限的,为了实现可持续发展,需要进行铜矿资源的循环利用。
目前,已经有一些技术用于回收和利用废铜,如冶金渣的综合利用和废电线的回收等。
总结:铜火法冶金是利用火法冶炼技术从铜矿中提取铜金属的过程。
它包括熔炼、焙烧和浸出三个步骤,以及提纯的方法。
铜矿资源的循环利用也是一个重要的课题。
通过这些基础知识的学习,我们能更好地了解铜火法冶金的原理和应用。

第一章铜冶金1.1铜冶金的一般知识1、铜的性质①.物理性质:符号Cu,ⅠB元素,原子序数29,原子量子63.57,熔点1083℃,沸点2310℃,密度8.89g/cm3(20℃),铜是一种紫红色、柔软、具有展性的金属,易于锻造和压延,是电和热的良导体,仅次于银居第二位。
铜②.化学性质:具有两个价电子,可形成一价和二价铜的化合物,在干燥空气中不起变化,在潮湿的CO2空气中,表面氧化成一薄层碱式碳酸铜(铜绿),铜绿有毒,不宜做餐具,它可保护铜不再被腐蚀。
铜在空气中加热,可与氧作用,依次生成Cu2O和CuO,颜色也逐渐从紫红色变成黄铜色,最后变为黑色。
铜不能溶于盐酸和没有溶解氧的硫酸中,能溶于硝酸和有氧化剂存在的硫酸及氨水中,铜也能与氧、硫、卤素等元素直接化合。
2、铜的主要化合物的性质①氧化铜(CuO):黑色无光泽,呈黑铜矿的矿物形态存在,不稳定加热时易分解为Cu2O,易被H2、C、CO、CxHy、硫化物及较负电性的金属如Zn、Fe、Ni等还原。
氧化铜不溶于水,但溶于FeCl2、FeCl3、Fe2(SO4)3、NH4OH及(NH4)2CO3中,且易与各种稀酸起作用。
②氧化亚铜(Cu2O):紫红色,呈赤铜矿的矿物形态存在,Cu2O只在1060℃时才稳定存在,低于这个温度会氧化成CuO。
Cu2O易被H2、C、CO、CxHy及较负电性的金属如Zn、Fe或对氧亲和力强的元素等还原成金属。
Cu2O不溶于水,能溶于HCl、H2SO4、FeCl2、FeCl3、Fe2(SO4)3、NH4OH等溶剂之中。
③铜的铁酸盐:即铁酸铜(CuO²Fe2O3)和铁酸亚铜(Cu2O²Fe2O3),铜的铁酸盐不易溶解于水、氨水及一般溶剂,但易被强碱性氧化物如FeO、CaO等及硫化物所分解,也易于被SO2还原,属于易还原的化合物。
④铜的碳酸盐:呈孔雀石CuCO3²Cu(OH)2和蓝铜矿2CuCO3²Cu(OH)2的矿物形态存在,两种化合物在高温下不稳定,分解为CuO、CO2和H2O,与各类熔剂发生类似于铜的氧化物与各种熔剂所发生的反应。

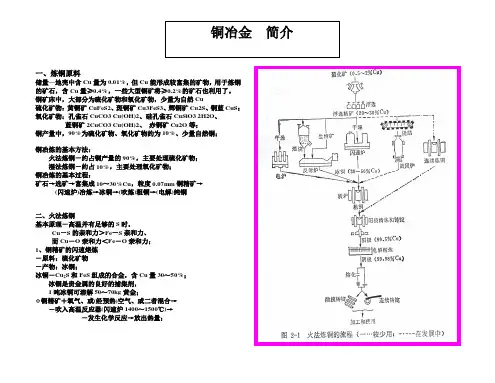
储量—地壳中含Cu量为0.01%,但Cu能形成较富集的矿物,用于炼铜的矿石,含Cu量≥0.4%,一些大型铜矿将≥0.2%的矿石也利用了。
铜矿床中,大部分为硫化矿物和氧化矿物,少量为自然Cu硫化矿物:黄铜矿CuFeS2、斑铜矿Cu3FeS3、辉铜矿Cu2S、铜蓝CuS;氧化矿物:孔雀石CuCO3 Cu(OH)2、硅孔雀石CuSiO3 2H2O、蓝铜矿2CuCO3 Cu(OH)2、赤铜矿Cu2O等;铜产量中,90%为硫化矿物、氧化矿物约为10%、少量自然铜;铜冶炼的基本方法:火法炼铜-约占铜产量的90%,主要处理硫化矿物;湿法炼铜-约占10%,主要处理氧化矿物;铜冶炼的基本过程:矿石→选矿→富集成10~30%Cu,粒度0.07mm铜精矿→(闪速炉)冶炼→冰铜→(吹炼)粗铜→(电解)纯铜二、火法炼铜基本原理-高温并有足够的S时,Cu-S的亲和力>Fe-S亲和力、而Cu-O亲和力<Fe-O亲和力;1、铜精矿的闪速熔炼-原料:硫化矿物-产物:冰铜;冰铜-Cu2S和FeS组成的合金,含Cu量30~50%;冰铜是贵金属的良好的捕集剂,1吨冰铜可溶解50~70kg黄金;铜精矿+氧气、或(经预热)空气、或二者混合→-吹入高温反应器(闪速炉1400~1500℃)→-发生化学反应→放出热量;分解反应:FeS2=FeS+1/2S2Fe n S n+1=nFeS+1/2S22CuFeS2=Cu2S+2FeS+1/2S22CuS=Cu2S+1/2S2氧化反应:FeS+3/2O2=FeO+SO23FeS+5O2=Fe3O4+3SO2Cu2O+FeS=Cu2S+FeO造渣反应:2FeO+SiO2=2FeO SiO2氧气熔炼时:氧化反应放出的热量,足够熔炼之用,不需补充燃料;空气(预热)熔炼时:需要补充燃料;2、冰铜的吹炼:原料:Cu2S+FeS,含Cu量30~50%原理:在1200~1250℃时第一周期:利用氧气(或空气中)~液态FeS→FeO+SiO2→熔渣2FeS+3O2+SiO2=2FeO SiO2+2SO2――造渣期剩下的Cu2S-叫做白冰铜;第二周期:Cu2S氧化→Cu2O+Cu2S→粗铜,贵金属富集在粗铜中;造渣后期,进行如下反应,2Cu2S+3O2=2Cu2O+2SO2Cu2S+2Cu2O=6Cu+SO2均为放热反应,不需补充燃料;3、铜的电解精炼阳极-火法熔炼的铜;在硫酸铜+硫酸电解液,通入直流电,阴极-电解铜,阳极反应:Cu-2e=Cu2+标准电极电位=0.34VMe-2e=Me2+标准电极电位<0.34V标准极电位比Cu低的(<0.34V)的金属,失去电子,变为离子,进入溶液,定期抽出一部分进行净化;标准极电位比Cu高的(>0.34V)的金属(多为贵金属),则不溶解,沉淀于电解槽的底部,成为阳极泥;阴极反应:Cu2++2e=Cu 标准电极电位=0.34VMe2++2e=Me 标准电极电位>0.34V只有电位高的金属离子能够优先进行还原,但它在阳极时不溶解,所以,只有Cu离子还原,这是阴极的主要反应;技术指标:电耗230~260kwh/吨铜;直接回收率85%;电解总回收率99.9%硫酸消耗4~5kg/吨铜;二、湿法炼铜-是利用低品位矿石、尾矿的有效途径;利用溶液浸出矿石中的Cu,使Cu进入溶液,从溶液中回收Cu;1、硫酸浸出:氧化状态的铜+1~5%硫酸=反应CuO+H2SO4=CuSO4+H2OCuCO3 Cu(OH)2+2H2SO4=2CuSO4+CO2+3H2O(CuCO3)2 Cu(OH)2+3H2SO4=3CuSO4+2CO2+4H2OCuSiO3 2H2O+H2SO4=CuSO4+SiO2+3H2O可在常温下进行;2、氨浸出:氨溶液在有CO2存在时,能够溶解所有的Cu氧化物和自然Cu;CuO+2NH4OH+(NH4)2CO3=Cu(NH3)4CO3+3H2OCu(NH3)4CO3+Cu= Cu2(NH3)4CO3可在常温下进行,但不能浸出硫化矿物;3、高价硫酸铁浸出:可处理Cu的硫化矿物;Cu2S+2Fe2(SO4)3=2CuSO4+4FeSO4+SCuS+Fe2(SO4)3=CuSO4+2FeSO4+S此反应在低温时进行速度很慢,加热到35℃以上才能正常进行;生产中,不单纯使用高价硫酸铁作为溶剂,常用硫酸+高价硫酸铁;因为:Fe2(SO4)3+H2O=Fe2(OH)2(SO4)+H2SO4此反应是可逆的,浸出时加入硫酸,可转变为高价硫酸铁;4、细菌浸出黄铜矿CuFeS2的浸出速度非常慢,利用细菌可以加速浸出,常用:氧化硫杆菌、氧化铁硫杆菌在硫酸和氧在细菌的作用下:CuFeS2+4O2=CuSO4+FeSO4细菌使Fe++转变为Fe3+离子:2FeSO4+2H2SO4+1/2O2=Fe2(SO4)3+H2O 高价硫酸铁溶解硫化矿物CuFeS2+2Fe2(SO4)3+3O2+2H2O=5FeSO4+CuSO4+2H2SO4细菌实际上起着催化作用,例如:黄铜矿浸出时,没有细菌,一年的浸出率不到20%, 在细菌参与时,20天就可以达到20%,一年的浸出率60%以上;5、浸出方法就地浸出、废矿堆浸、矿石堆浸、搅拌槽浸出;6、铜的回收电积法:在阴极~阳极之间通人直流电压,总反应:CuSO4+H2O=Cu+H2SO4+1/2O2。



cu的冶炼方法铜(Cu)是一种常见的金属元素,具有良好的导电性和导热性,因此在工业和生活中广泛应用。
那么,如何将铜从其矿石中提取出来呢?这就需要通过冶炼方法来实现。
冶炼铜的方法有很多种,其中最常用的是火法冶炼和电解法冶炼。
火法冶炼是一种传统的冶炼方法,主要用于低纯度的铜矿石。
这种方法的基本步骤是先将铜矿石破碎成合适的颗粒大小,然后经过浮选和磁选等物理方法将铜矿石中的杂质分离出来。
接下来,将分离后的铜矿石与石灰石、煤等配料一起放入冶炼炉中,加热至高温,使铜矿石中的铜矿物还原成氧化铜(Cu2O),再经过反应生成纯铜。
最后,通过冷却、凝固和分离等步骤,得到纯铜。
电解法冶炼是一种现代化的冶炼方法,主要用于高纯度的铜矿石。
这种方法的基本原理是利用电解的原理,将铜矿石中的铜离子通过电流的作用还原成纯铜。
具体操作时,首先将铜矿石破碎成合适的颗粒大小,然后与硫酸等配料一起放入电解槽中。
接下来,通过向电解槽中通入电流,使铜离子在阴极上还原成纯铜,同时在阳极上生成氧气。
最后,将电解槽中的铜板取出,经过清洗和加工等步骤,得到纯铜。
除了火法冶炼和电解法冶炼,还有其他一些冶炼方法,如溶剂萃取法、熔融盐电解法等。
这些方法在特定的情况下具有一定的优势和应用价值。
需要注意的是,在进行铜的冶炼过程中,还需要考虑到环境保护和资源利用的问题。
冶炼过程中会产生大量的废气、废水和固体废弃物,其中含有有害物质和有用物质。
因此,在冶炼过程中需要采取相应的环保措施,减少对环境的污染,并尽可能地回收和利用有用物质。
总的来说,冶炼铜的方法有很多种,每种方法都有其适用的场合和特点。
火法冶炼和电解法冶炼是最常用的方法,它们在工业生产中得到广泛应用。
随着科技的不断发展,冶炼技术也在不断创新和改进,以提高冶炼效率和资源利用率。
希望通过不断的研究和发展,能够找到更加高效、环保和经济的铜冶炼方法,为社会的可持续发展做出贡献。

铜的化工知识点总结一、铜的性质1. 物理性质铜的原子序数为29,原子量为63.55,属于过渡金属元素。
铜的密度为8.96克/立方厘米,熔点为1083摄氏度,沸点为2595摄氏度。
铜的导电性和导热性都很强,是一种重要的导电材料。
2. 化学性质铜在常温下不容易被氧化,但在高温、潮湿的环境下容易形成氧化铜。
铜能够形成不同的氧化态,其中最常见的是+1和+2价态。
铜与酸、碱、氧化剂等也能发生化学反应,广泛应用于化工生产中。
二、铜的制备1. 精炼铜的精炼方法主要包括火法、电解法和湿法等。
其中火法包括化铜和熔铜,电解法包括铜电解和氧化铜电解,湿法包括浮选法和浸出法等。
精炼方法的选择取决于铜矿石的品位和成分。
2. 合成除了从铜矿石中提取铜外,还可以通过化学合成方法来制备铜。
例如,将氧化铜和纯碱在高温下反应就能得到铜粉。
此外,还可以通过还原反应或电化学方法得到铜。
三、铜的应用1. 电子工业由于铜的良好导电性和导热性,广泛用于电子元器件、电缆、通讯设备等领域。
铜箔、铜线、铜箔板等产品在电子工业中得到广泛应用。
2. 建筑工业铜的抗腐蚀性和良好的可塑性使其成为一种理想的建筑材料,在建筑工业中用于制作屋顶、立面、管道等产品。
3. 化学工业铜在化学工业中被用作催化剂、还原剂、螯合剂等。
氨基乙醇胺、铜基催化剂、氧化铜等产品在化工生产中得到广泛应用。
4. 食品工业铜也被用作食品工业中的添加剂。
例如,用铜制成的锅具能有效杀灭细菌,保证食品安全。
5. 医药工业铜被用作医疗器械、药品原料等。
铜离子能抑制细菌生长,起到消毒杀菌的作用。
综上所述,铜是一种非常重要的化工原材料,具有良好的物理性质和化学性质,广泛应用于电子工业、建筑工业、化学工业、食品工业、医药工业等领域。
对铜的性质、制备和应用有一定的了解,有助于更好地利用铜资源,推动化工领域的发展。

铜冶炼原理铜是一种重要的金属材料,广泛应用于工业生产和日常生活中。
铜冶炼是将含铜矿石经过一系列的物理和化学处理,从中提取出纯铜的过程。
铜冶炼的原理主要包括矿石选矿、矿石破碎、矿石浮选、熔炼和精炼等步骤。
首先,矿石选矿是铜冶炼的第一步。
矿石选矿是指从矿石中分离出有用的矿物的过程。
在铜冶炼中,常见的铜矿石有黄铜矿、辉铜矿、赤铜矿等。
通过对矿石的物理性质和化学性质进行分析,选择合适的选矿方法,将有用的矿石与其他杂质分离开来。
接下来是矿石破碎的过程。
矿石破碎是将选矿后的矿石进行粉碎,使其达到一定的粒度要求。
通常采用颚式破碎机、圆锥破碎机等设备进行破碎,将大块矿石破碎成适合浮选处理的颗粒。
然后是矿石浮选。
矿石浮选是利用物理和化学方法将有用的矿物从杂质中分离出来的过程。
在铜冶炼中,常用的浮选剂有黄药、黑药等,通过调节浮选剂的种类和用量,控制气泡的大小和数量,使有用的矿物与杂质分离,从而得到含铜的浮选精矿。
接着是熔炼的步骤。
熔炼是将浮选精矿进行加热,使其熔化并分离出铜的过程。
通常采用的熔炼方法有火法熔炼和电炉熔炼。
在熔炼过程中,通过控制温度和添加熔剂,将含铜的浮选精矿中的铜提取出来,得到粗铜。
最后是精炼的过程。
精炼是将粗铜进行进一步的提纯,去除其中的杂质,得到纯净的铜的过程。
常见的精炼方法有火法精炼、电解精炼等。
通过控制温度、氧化性和还原性条件,将粗铜中的杂质如铅、锌等去除,得到高纯度的铜。
总的来说,铜冶炼的原理是通过矿石选矿、矿石破碎、矿石浮选、熔炼和精炼等步骤,将含铜的矿石提炼出纯铜。
这一过程涉及到物理、化学和冶金等多个领域的知识,是一个复杂的工程。
通过不断的技术创新和改进,铜冶炼技术得到了不断的提高,为铜资源的有效利用和保护环境作出了重要贡献。

铜的火法精炼一、概述1.铜的性质物理性质:铜是一种玫瑰红色、柔软、具有展性的金属,易于锻造和压延。
在导电和导热方面,铜仅次于银而居第二位,如果把银的导电率和导热率作为100%,则铜的导电和导热率分别为93%和73.2%,在元素周期表中,铜属于第一族,原子序数29,具具有两个价电子,形成一价和二价铜的化合物铜的主要物理性质如下:原子量63.57熔点:1083℃沸点:2310℃比重:20℃时8.89熔点时8.221100℃7.961200℃7.3125℃时的比热容386KJ/KG.K熔化潜热:205.2/kj kg-1铜的电阻率1.75 ×10-8(Ω m)标准电位:+0.34伏特液体铜能溶解某些气体,这些气体在铜凝固时又从铜中逸出,形成气孔。
化学性质铜在干燥的空气中不起变化,但在含有CO2的潮湿空气中,铜的表面会生成一薄层碱性碳酸铜(铜绿),这种薄膜保护铜不再被腐蚀,其反应如下3Cu+O2+H2O+ CO2=2 Cu CO2. Cu(OH)2铜在空气中加热到165℃即开始与氧作用生成铜氧化物,当温度超过350℃时铜的颜色从玫瑰红变成黄铜色最后变为黑色,黑色层为氧化铜,中间层为氧化亚铜,内层为金属铜。
铜的电位次序位于氢的下面,属正电性元素,不能从酸中置换出氢,因此,不能溶解于盐酸和没有溶解氧气的硫酸中,只有在具有氧化作用的酸中铜才能溶解,例如,铜能溶于硝酸和有氧化剂存在的硫酸中。
铜能溶于氨水。
铜的主要化合物及其性质氧化铜(CuO):为黑色无光泽物质,在自然界中以黑铜矿的矿物形态存在,其分子量为79.75,。
氧化铜是不稳定的化合物,加热时以下式离解:4C U O=2C U2O+O2当温度高于1060℃时,氧化铜完全转化为氧化亚铜,这是因为在这个温度下氧化铜的离解压力高于空气中样的分压。
氧化铜易被H2、C、CO、C X H Y等还原为金属,在冶炼过程中也被其它硫化物和负电性金属如锌、铁等还原。

化学高考知识点湿法炼铜湿法炼铜是一种重要的冶金过程,被广泛应用于铜的提取和精炼过程中。
它通过将铜矿石与化学试剂进行反应,从而将铜从其他杂质中分离出来。
本文将深入探讨湿法炼铜的相关知识点。
第一部分:湿法炼铜基础知识湿法炼铜是一种将铜矿石转化为纯铜的过程。
该过程主要包括矿石破碎、矿石浸出、溶液净化和电积四个主要阶段。
1. 矿石破碎在湿法炼铜的第一步中,需要将原始的铜矿石进行粉碎。
这样可以增加矿石的表面积,使其更容易与化学试剂反应。
通常使用球磨机或破碎机等设备进行粉碎。
2. 矿石浸出浸出是湿法炼铜的核心步骤之一。
在这一阶段,粉碎后的矿石与含有化学试剂的溶液接触,试剂将与铜矿石中的铜发生反应。
最常用的浸出试剂是硫酸,其会与矿石中的铜形成溶液。
3. 溶液净化在浸出过程中,溶液中除了铜以外还会存在大量的杂质。
为了提取纯铜,需要对溶液进行净化。
常用的净化方法包括电解、置换、沉淀和萃取等。
这些方法可以将溶液中的杂质与铜分离,并获得纯净的溶液。
4. 电积电积是湿法炼铜的最后一步,也是最关键的一步。
在这一过程中,从净化后的溶液中提取出的铜以电流的形式通过一个电解槽沉积到铜板上。
经过多次电积,铜的纯度逐渐提高,最终得到高纯度的纯铜。
第二部分:湿法炼铜的优势与应用湿法炼铜相较于其他提取铜的方法有着一些明显的优势,因此在实际应用中被广泛采用。
1. 适用性广泛湿法炼铜方法适用于多种不同类型的铜矿石,包括高铜矿、黄铜矿和含铜硫化物等。
这使得湿法炼铜能够处理各种不同品位和不同类型的矿石。
2. 高效提取湿法炼铜过程中使用的化学试剂可以快速将铜从矿石中提取出来,并通过净化步骤获得高纯度的铜。
相比之下,其他方法可能需要更多的步骤和时间才能达到相同的效果。
3. 环保可持续湿法炼铜方法对环境影响较小,因为它使用的化学试剂相对较少,并能够将废弃物处理得比较彻底。
此外,湿法炼铜还可以回收利用废水和废气等排放物,减少资源浪费和环境负荷。
4. 应用广泛湿法炼铜的纯铜产品在工业应用中有着广泛的用途。
铜冶炼基础知识冶金概论讲义1 冶金基本知识1.1 冶金的概念及冶金方法分类冶金就是从矿石或二次金属资源中提取金属或金属化合物,用各种加工方法制成具有一定性能的金属材料的过程和工艺。
冶金的技术主要包括火法冶金、湿法冶金以及电冶金,根据冶炼金属的不同,冶金工业又了可以分黑色冶金工业和有色冶金工业,黑色冶金主要指包括生铁、钢和铁合金(如铬铁、锰铁等)的生产,有色冶金指后者包括其余所有各种金属的生产。
1.2 火法冶金火法冶金是在高温条件下进行的冶金过程。
矿石或精矿中的部分或全部矿物在高温下经过一系列物理化学变化,生成另一种形态的化合物或单质,分别富集在气体、液体或固体产物中,达到所要捉取的金属与脉石及其它杂质分离的目的。
实现火法冶金过程所需热能,通常是依靠燃料燃烧来供给,也有依靠过程中的化学反应来供给的,比如,硫化矿的氧化焙烧和熔炼就无需由燃料供热;金属热还原过程也是自热进行的。
火法治金过程没有水溶液参加,所以又称为干法冶金。
火法冶金是提取金属的主要方法之一,其生产成本一般低于湿法治金。
火法冶金包括:干燥、焙解、焙烧、熔炼,精炼,蒸馏等过程。
1.3 湿法冶金湿法冶金是在溶液中进行的冶金过程。
湿法冶金温度不高,一般低于100℃,现代湿法冶金中的高温高压过程,温度也不过473K左右,极个别情况温度可达573K。
湿法冶金包括:浸出、净化、制备金属等过程。
(1)浸出用适当的溶剂处理矿石或精矿,使要提取的金属成某种离子(阳离子或络阴离子)形态进入溶液,而脉石及其它杂质则不溶解,这样的过程叫浸出。
浸出后经沉清和过滤,得到含金属(离子)的浸出液和由脉石矿物绢成的不溶残渣(浸出渣)。
对某些难浸出的矿石或精矿,在浸出前常常需要进行预备处理,使被提取的金属转变为易于浸出的某种化合物或盐类。
例如,转变为可溶性的硫酸盐而进行的硫酸化焙烧等,都是常用的预备处理方法。
(2)净化在浸出过程中,常常有部分金属或非金属杂质与被提取金属一道进入溶液,从溶液中除去这些杂质的过程叫做净化。
冶金概论讲义1 冶金基本知识1.1 冶金的概念及冶金方法分类冶金就是从矿石或二次金属资源中提取金属或金属化合物,用各种加工方法制成具有一定性能的金属材料的过程和工艺。
冶金的技术主要包括火法冶金、湿法冶金以及电冶金,根据冶炼金属的不同,冶金工业又了可以分黑色冶金工业和有色冶金工业,黑色冶金主要指包括生铁、钢和铁合金(如铬铁、锰铁等)的生产,有色冶金指后者包括其余所有各种金属的生产。
1.2 火法冶金火法冶金是在高温条件下进行的冶金过程。
矿石或精矿中的部分或全部矿物在高温下经过一系列物理化学变化,生成另一种形态的化合物或单质,分别富集在气体、液体或固体产物中,达到所要捉取的金属与脉石及其它杂质分离的目的。
实现火法冶金过程所需热能,通常是依靠燃料燃烧来供给,也有依靠过程中的化学反应来供给的,比如,硫化矿的氧化焙烧和熔炼就无需由燃料供热;金属热还原过程也是自热进行的。
火法治金过程没有水溶液参加,所以又称为干法冶金。
火法冶金是提取金属的主要方法之一,其生产成本一般低于湿法治金。
火法冶金包括:干燥、焙解、焙烧、熔炼,精炼,蒸馏等过程。
1.3 湿法冶金湿法冶金是在溶液中进行的冶金过程。
湿法冶金温度不高,一般低于100℃,现代湿法冶金中的高温高压过程,温度也不过473K左右,极个别情况温度可达573K。
湿法冶金包括:浸出、净化、制备金属等过程。
(1)浸出用适当的溶剂处理矿石或精矿,使要提取的金属成某种离子(阳离子或络阴离子)形态进入溶液,而脉石及其它杂质则不溶解,这样的过程叫浸出。
浸出后经沉清和过滤,得到含金属(离子)的浸出液和由脉石矿物绢成的不溶残渣(浸出渣)。
对某些难浸出的矿石或精矿,在浸出前常常需要进行预备处理,使被提取的金属转变为易于浸出的某种化合物或盐类。
例如,转变为可溶性的硫酸盐而进行的硫酸化焙烧等,都是常用的预备处理方法。
(2)净化在浸出过程中,常常有部分金属或非金属杂质与被提取金属一道进入溶液,从溶液中除去这些杂质的过程叫做净化。
(3)制备金属用置换、还原、电积等方法从净化液中将金属提取出来的过程。
1.3 电冶金电冶金是利用电能提取金属的方法。
根据利用电能效应的不同,电冶金又分为电热冶金和电化冶金。
(1)电热冶金是利用电能转变为热能进行冶炼的方法。
在电热冶金的过程中,按其物理化学变化的实质来说,与火法冶金过程差别不大,两者的主要区别只是冶炼时热能来源不同。
(2)电化冶金(电解和电积)是利用电化学反应,使金属从含金属盐类的溶液或熔体中析出。
前者称为溶液电解,如锕的电解精炼和锌的电积,可列入湿法冶金一类;后者称为熔盐电解,不仅利用电能的化学效应,而且也利用电能转变为热能,借以加热金属盐类使之成为熔体,故也可列入火法冶金一类。
从矿石或精矿中提取金属的生产工艺流程,常常是既有火法过程,又有湿法过程,即使是以火法为主的工艺流程,比如,硫化铜精矿的火法冶炼,最后还须要有湿法的电解精炼过程;而在湿法炼锌中,硫化锌精矿还需要用高温氧化焙烧对原料进行炼前处理。
2 铜冶金2.1铜的性质及用途2.1.1 物理性质铜的熔点1083℃,沸点2310℃;常温密度8.89g/cm3;标准电位+0.34V;具有良好的导电性和导热性,仅次于银。
铜与其他金属的互溶性好,很易与锌、镍、锡生成合金。
液态铜能溶解H2、O2、SO2、CO2、CO和水蒸气等,浇铸时要注意除气,否则会形成气孔。
2.1.2 化学性质在干燥空气中不氧化,在温度高于185℃时开始氧化,温度低于350℃时生成红色氧化亚铜(Cu2O),高于350℃时生成黑色氧化铜(CuO)。
长期放置在含CO2的潮湿空气中,铜表面会逐渐生成一层绿色的碱式碳酸铜[CuCO3·Cu(OH)2](铜绿)。
铜能形成一价化合物和二价化合物,前者在高温下稳定,后者则相反。
2.1.3 铜的用途其应用范围仅次于钢铁和铝,居第三位。
①电器工业,占55%;②机械制造,轴承、活塞、阀门、高压设备等;③国防工业;④建筑、热工、冷却装置、民用设备等。
2.2 铜的生产方法2.2.1 火法炼铜火法炼铜是当今生产铜的主要方法,占铜产量的80%~90%,主要是处理硫化矿。
工艺过程主要包括四个主要步骤:造锍熔炼、铜锍吹炼、粗铜火法精炼和阳极铜电解精炼。
造锍熔炼传统熔炼设备有反射炉、电炉和密闭鼓风炉等;强化熔炼设备有闪速炉、诺兰达炉、艾萨炉、白银炉等。
火法炼铜的优点是适应性强,能耗低,生产效率高,金属回收率高。
2.2.2 湿法炼铜湿法炼铜点铜生产量的10%~20%,主要用来处理氧化矿。
工艺过程主要包括四个步骤:浸出、萃取、反萃取、金属制备(电积或置换)。
氧化矿可以直接进行浸出,低品位氧化矿采用堆浸,富矿采用曹浸。
硫化矿在一般情况下需要先焙烧后再浸出,也可在高压下直接浸出。
2.3 造锍熔炼2.3.1 造锍熔炼的基本原理硫化铜精矿含铜一般为10%~30%,除脉石外,常伴生有大量铁的硫化物,其量超过主金属铜,所以用火法由精矿直接炼出粗金属,在技术上存在困难,在冶炼时金属回收率和金属产品质量也不容易达到要求。
因此采用造锍熔炼—铜锍吹炼的工艺来处理硫化铜精矿。
这种工艺的原理是,利用铜对硫的亲和力大于铁和一般杂质金额,而铁对氧的亲和力大于铜的特性,在高温及控制氧化气氛条件下,使铁等杂质金属逐步氧化后进入炉渣或烟尘而补除去,而金属铜则富集在各种中间物中,并逐步得到提纯。
2.3.2 造锍熔炼的方法造锍熔炼以往多在鼓风炉、反射炉、电炉等传统冶金炉内进行,这些方法熔炼强度低,能耗高,硫回收率低,生产成本高,环境污染严重,正逐步被强化铜锍熔炼工艺代替。
强化铜锍熔炼工艺已在工业上广泛推广采用,归纳起来有两大类:一类悬浮熔炼,如奥托昆普闪速熔炼,INCO氧气闪速熔炼和KHD公司的连续顶吹漩涡熔炼法等;另一类是熔池熔炼,如诺兰达熔炼法,三菱法,瓦纽柯夫法,艾萨法和我国的白银法等。
这些方法的共同特点是运用富氧技术,强化熔炼过程,充分利用炉料氧化反应热的能量,在自热或接近自热熔炼的条件下进行熔炼,产出高浓度SO2烟气,可有效地回收、制造硫酸和其他硫产品,环境友好,节能和经济效益好。
2.4 铜精矿的密闭鼓风炉熔炼鼓风炉熔炼是一种古老的炼铜方法,它是竖式炉子中依靠上升热气流加热炉料进行熔炼。
传统鼓风炉的炉顶是敞开的,炉气量大,所产烟气SO2浓度很低(约0.5%),难以回收,造成污染。
50年代中期,出现了直接处理铜精矿的密闭鼓风熔炼法,炉顶具有密封装置,铜精矿只需加水混捏的即可直接加入炉内,在烟气加热和料柱的压力作用下固结成块,使得熔炼顺利进行,炉气可用于制酸。
2.4.1 密闭鼓风熔炼的基本原理密闭鼓风炉的炉料由混捏铜精矿、熔剂和固体转炉渣。
块料的数量要求占炉料重的30%(或容积比50%)以上。
炉料经由加料斗加入,当炉料下降离开加料斗进入炉内时,炉料自然向两侧滚动。
由于偏析作用,细的精矿在炉子中心部分形成料柱,而料柱的两侧为块料所填充,选成炉内炉料分布不均匀状态。
由于炉内炉料分布的不均匀,造成了炉气的分布不均匀,即炉中间透气性差,炉气阻力大,而炉壁附近则相反,因此形成了鼓风炉炉气的周边行程。
由于这种中心料柱的存在和周边高温炉气的作用,使混捏精矿发生固结和烧结,为鼓风熔炼精矿创造了有利条件。
但由于炉料的偏析和炉气分布不均匀,从而破坏了炉气与炉料间、炉料相互间的良好接触,妨碍了多相反应的迅速进行,不利于硫化物的氧化和造渣反应。
这是密闭鼓风炉的床能率和冰铜品位低的根本原因。
由于炉料和炉气分布的不同,炉内的温度分布也不同,炉子两侧气流量大,气固接触好,反应强烈,温度较高。
而炉子中心部位则相反,温度较低。
尤其在炉子上部,这种温差更大。
2.5 铜精矿的电炉熔炼电炉熔炼是利用电能通过熔炼炉料产生的高温进行熔炼的过程,只能熔炼干燥过的生精矿或焙烧矿,20世纪初电炉在铜工业上开始应用。
其优点是:可利用炉气中的SO2,适合处理难熔物料,电能效率高。
其缺点是:不能利用精矿反应的热能,电能消耗大,费用高。
2.5.1 电炉熔炼的原理电炉熔炼的实质是将炉料加入熔池面上,由于炉气温度不高,故其表面不发生显著变化;炉料下部由于对流运动的渣流传热而熔化,不断下沉,同时发生与反射熔炼相同的各种物理化学变化,形成铜锍、炉渣和烟气。
2.6 铜锍的吹炼铜锍吹炼的任务是将铜锍吹炼成含铜98.5%~99.5%的粗铜。
吹炼的实质是在一定压力下将空气送到液体铜硫中,使铜锍中FeS氧化成FeO与加入的石英熔剂造渣,Cu2S则与氧化生成的Cu2O发生相互反应变成精铜。
吹炼过程所需热量全靠熔锍中的硫和铁的氧化和造渣反应所放出的热量供给,为自热过程。
吹炼过程的温度一般为1473~1523K。
吹炼是周期性的间歇作业,熔融铜锍分批装入转炉内,要经历由装料、吹炼、排渣等操作组成的几个循环,直至产生精铜才算完成一个完整的吹炼过程。
然后重新加入铜锍开始下炉吹炼。
吹炼过程严格分为两个周期。
第一周期(又称造渣周期),主要是FeS的氧化造渣,结果形成Cu2S熔体,称为白冰铜;第二周期(又称造铜期),主要是Cu2S的氧化成Cu2O,同时Cu2O在熔体中与未氧化的Cu2S作用生成金属铜(精铜),在这一周期,没有炉渣形成。
2.7 其他炼铜方法三菱法(Mitsubishi process) 将硫化铜精矿和熔剂喷入熔炼炉的熔体内,熔炼成冰铜和炉渣,而后流至贫化炉产出弃渣,冰铜再流至吹炼炉产出粗铜。
此法于1974年投入生产。
诺兰达法(Noranda process) 制粒的精矿和熔剂加到一座圆筒型回转炉内,熔炼成高品位冰铜。
所产炉渣含铜较高,须经浮选选出铜精矿返回炉内处理。
此法于1973年投入生产。
氧气顶吹旋转转炉法用以处理高品位铜精矿。
将铜精矿制成粒或压成块加入炉内,由顶部喷枪吹氧,燃料也由顶部喷入,产出粗铜和炉渣。
中国用此法处理高冰镍浮选所得铜精矿。
离析法用于处理难选的结合性氧化铜矿。
将含铜1~5%的矿石磨细,加热至750~800℃后,混以2~5%的煤粉和0.2~0.5%的食盐,矿石中的铜生成气态氯化亚铜(Cu3Cl3)并为氢还原成金属铜而附着于炭粒表面,经浮选得到含铜50%左右的铜精矿,然后熔炼成粗铜。
此法能耗高,很少采用。
2.7 铜的电解精炼铜的电解精炼是以火法精炼的铜为阳极,硫酸铜和硫酸水溶液为电解质,电铜为阴极,向电解槽直流电使阳极溶解,在阴极析出更纯的金属铜的过程。
根据电化学性质的不同,阳极中的杂质或者进入阳极泥或者保留在电解液中而被脱出。
2.8 湿法炼铜湿法炼铜是用溶剂浸出铜矿石或铜精矿使铜进入溶液,然后从经过净化处理后的含铜溶液中回收铜的方法。
此方法主要用于处理低品位铜矿石、氧化铜矿和一些复杂的铜矿石。
目前湿法炼铜在铜生产中所占比重不大,只占10%~20%,但从今后资源发展趋势看,随着矿石逐渐贫化,氧化矿、低品位难选矿石和多金属复杂铜矿的利用日益增多,湿法炼铜将成为处理这些原料的有效途径。