有机物分子式计算(成品)
- 格式:doc
- 大小:143.50 KB
- 文档页数:8


高中化学考点精讲有机物分子式和结构式的确定复习重点1.了解确定有机物实验式、分子式的方法,掌握有关有机物分子式确定的计算;2.有机物分子式、结构式的确定方法难点聚焦一、利用有机物燃烧反应的方程式进行计算有关化学方程式由上可知,相同碳原子数的烯烃(环烷烃)与一元饱和醇完全燃烧时,耗氧量相同(把:相同碳原子数的炔烃(二烯烃)与醛(酮)及饱和二元醇完全燃烧时,耗氧量相同(醛:饱和二元醇:);相同碳原子数的羧酸(酯)与三元醇完全燃烧,耗氧量相同(羧酸:→饱和三元醇:) 二、通过实验确定乙醇的结构式由于有机化合物中存在着同分异构现象,因此一个分子式可能代表两种或两种以上具有不同结构的物质。
在这种情况下,知道了某一物质的分子式,常常可利用该物质的特殊性质,通过定性或定量实验来确定其结构式。
例如:根据乙醇的分子式和各元素的化合价,乙醇分子可能有两种结构:为了确定乙醇究竟是哪一种结构,我们可以利用乙醇跟钠的反应,做下面这样一个实验。
实验装置如右下图所示。
在烧瓶里放入几小块钠,从漏斗中缓缓滴入一定物质的量的无水乙醇。
乙醇跟适量钠完全反应放出的H2把中间瓶子里的水压入量筒。
通过测量量筒中水的体积(应包括由广口瓶到量筒的导管内的水柱的体积),就可知反应生成的H2的体积。
讨论2 下面是上述实验的一组数据:根据上述实验所得数据,怎样推断乙醇的结构式是(1),还是(2)呢?由于0.100 mol C2H6O与适量Na完全反应可以生成1.12 L H2,则1.00 molC2H6O与Na反应能生成11.2 L H2,即0.5 mol H2,也就是1 mol H。
这就是说在1个C2H6O 分子中;只有1个H可以被Na所置换,这说明C2H6O分子里的6个H中,有1个与其他5个是不同的。
这一事实与(1)式不符,而与(2)式相符合。
因此,可以推断乙醇的结构式应为(2)式。
问题与思考1.确定有机物分子式一般有哪几种方法?2.运用“最简式法”确定有机物分子式,需哪些数据?3.如何运用“商余法”确定烃的分子式?问题与思考(提示)1、最简式法;直接法;燃烧通式法;商余法(适用于烃的分子式的求法等2、①有机物各元素的质量分数(或质量比)②标准状况下的有机物蒸气的密度(或相对密度)3、则为烯烃,环烷烃.②若余数=2,则为烷烃.③若余数=-2,则为炔烃.二烯烃④若余数=-6,则为苯的同系物.若分子式不合理,可减去一个C原子,加上12个H原子有机物分子式的确定典型例题例题精讲一、有机物分子式的确定【例1】实验测得某碳氢化合物A中,含碳80%、含氢20%,求该化合物的实验式。

有机物分子式的相关计算班级:姓名:号数:评价:方法一:最简式法1.某有机物组成中含碳54.5%%, 含氢9.1%,其余为氧又知其蒸汽在标况下的密度为3.94g/L,试求其分子式。
方法二:直接求法1.某有机物组成中含碳54.5%%, 含氢9.1%,其余为氧又知其蒸汽在标况下的密度为3.94g/L,试求其分子式。
小结:确定有机化合物的分子式的方法:[方法一]由物质中各原子(元素)的质量分数→各原子的个数比(实验式)→由相对分子质量和实验式→有机物分子式[方法二]1 mol物质中各原子(元素)的质量除以原子的摩尔质量→ 1 mol物质中的各种原子的物质的量→知道一个分子中各种原子的个数→有机物分子式2.燃烧某有机物A 1.50g,生成1.12L(标况)CO2和0.05mol H2O。
该有机物的蒸气对空气的相对密度是1.04,求该有机物的分子式。
方法三:燃烧通式法3.某有机物蒸汽对H2的相对密度为30,1.2g该有机物完全燃烧生成CO2(标况下)1.344L,H2O1.44g,求该有机物的分子式。
4.某气态烃10 mL与50 mL氧气在一定条件下作用,刚好消耗尽反应物,生成水蒸气40mL,一氧化碳和二氧化碳各20 mL(各气体体积均在同温、同压下测定) ,该烃的分子式为()A.C3H8B.C4H6C.C3H6D.C4H85. 将有机物完全燃烧,生成CO2和H2O,将12 g该有机物完全燃烧产物通过浓硫酸,浓硫酸增重14.4 g,再通过碱石灰,又增重26.4 g。
则该有机物的分子式为()A.C4H10B.C2H6OC.C3H8OD.C2H4O2方法四:讨论分析法6.两种气态烃组成的混合气体0.1 mol,完全燃烧得0.16 mol CO2和3.6 g水,下列说法正确的是()A.混合气体中一定有甲烷B.混合气体中一定有甲烷和乙烯C.混合气体中一定有乙烷D.混合气体中一定有乙炔7.两种气态烃以任意比例混合,在105℃时1 L 该混合烃与9 L氧气混合,充分燃烧后恢复到原状态,所得气体体积仍是10 L.下列各组混合烃中不符合条件的是A.CH4、C2H4B.CH4、C3H6C.C2H4、C3H4D.C2H2、C3H6方法五:巧用隐含条件(有机物质量分数上的隐含条件)8、甲醛(HCHO)和单烯烃的混合物含碳的质量分数为a,则其含氧的质量分数为( )方法六:耗氧量法(综合法)9、0.2 mol有机物A和0.4 mol O2在密闭容器中燃烧后的产物为CO2、CO和H2O(g)。

专题讲座(三) 有机物分子式及结构式的确定方法一、有机物分子式的确定1.最简式的确定。
(1)燃烧法。
则n (C)=m (CO 2)44 g·mol -1,n (H)=m (H 2O )18 g·mol -1×2,n (O)=m 有机物-n (C )×12 g·mol -1-n (H )×1 g·mol -116 g ·mol -1由它们的物质的量之比等于原子个数比可确定最简式。
(2)计算法。
根据有机物中C 和H 的质量分数来计算。
n (C)∶n (H)∶n (O)=w (C )12∶w (H )1∶1-w (C )-w (H )16。
2.相对分子质量的确定。
利用公式:a.M =m n ,b.ρ1ρ2=M 1M 2,c.M =ρ(标况)×22.4 L ·mol -1。
3.分子式的确定。
(1)由最简式和相对分子质量确定。
(2)根据计算确定1 mol 有机物中含有的各原子的数目。
(3)根据相对分子质量计算。
二、有机物结构式的确定1.根据价键规律确定:某些有机物根据价键规律只存在一种结构,则直接根据分子式确定其结构式。
例如C2H6,只能为CH3CH3。
2.通过定性实验确定。
实验→有机物表现的性质及相关结论→官能团→确定结构式。
如能使溴的四氯化碳溶液褪色的有机物分子中可能含有,不能使溴的四氯化碳溶液褪色却能使酸性高锰酸钾溶液褪色的可能是苯的同系物等。
3.通过定量实验确定。
(1)通过定量实验确定有机物的官能团,如乙醇结构式的确定;(2)通过定量实验确定官能团的数目,如1 mol某醇与足量钠反应可得到1 mol气体,则可说明该醇分子中含2个—OH。
4.根据实验测定的有机物的结构片段“组装”有机物。
实验测得的往往不是完整的有机物,这就需要我们根据有机物的结构规律,如价键规律、性质和量的规律等来对其进行“组装”和“拼凑”。

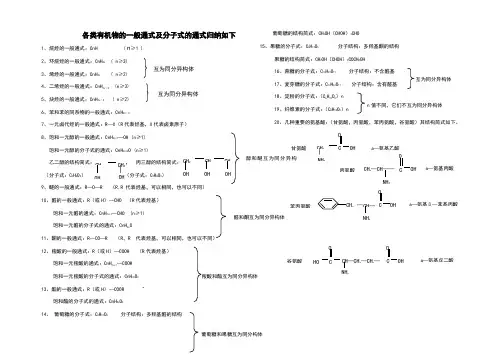
各类有机物的一般通式及分子式的通式归纳如下1、烷烃的一般通式:CnH ( ≥1 )2、环烷烃的一般通式:CnH 2n ( n ≥3)3、烯烃的一般通式:CnH 2n ( n≥2)4、二烯烃的一般通式:CnH 2n -2 (n ≥3)5、炔烃的一般通式:CnH 2n -2 ( n ≥2)6、苯和苯的同系物的一般通式:CnH 2n -67、一元卤代烃的一般通式:R —X (R 代表烃基,X 代表卤素原子) 8、饱和一元醇的一般通式:CnH 2n+1—OH (n ≥1) 饱和一元醇的分子式的通式:CnH 2n+2O (n ≥1)乙二醇的结构简式: , 丙三醇的结构简式: (分子式:C 2H 6O 2) (分子式:C 3H 8O 3)9、醚的一般通式:R —O —R (R,R 代表烃基,可以相同,也可以不同) 10、醛的一般通式:R (或H )—CHO (R 代表烃基)饱和一元醛的通式:CnH 2n+1—CHO (n ≥1) 饱和一元醛的分子式的通式:CnH 2n O11、酮的一般通式:R —CO —R (R ,R代表烃基,可以相同,也可以不同) 12、羧酸的一般通式:R (或H )—COOH (R代表烃基)饱和一元羧酸的通式:CnH 2n+1—COOH 饱和一元羧酸的分子式的通式:CnH 2n O 2 13、酯的一般通式:R (或H )—COOR饱和酯的分子式的通式:CnH 2n O 214、 葡萄糖的分子式:C 6H 12O 6 分子结构:多羟基醛的结构葡萄糖的结构简式:CH 2OH (CHOH )4CHO15、果糖的分子式:C 6H 12O 6 分子结构:多羟基酮的结构果糖的结构简式:CH 2OH (CHOH )3COCH 2OH16、蔗糖的分子式:C 12H 22O 11分子结构:不含醛基 17、麦芽糖的分子式:C 12H 22O 11 分子结构:含有醛基18、淀粉的分子式:(C 6H 10O 5)n 19、纤维素的分子式:(C 6H 10O 5)n20、几种重要的氨基酸:(甘氨酸,丙氨酸,苯丙氨酸,谷氨酸)其结构简式如下。

有机物分子式确定的计算方法有机物分子式的确定,即是确定有机物分子里所含元素的种类及各原子的数目。
有机物分子式的确定是有机物学习中,最为重要的知识点之一。
关于确定有机物分子式的计算题目,也是有机物计算题目当中的重要考题之一。
那么,如何确定有机物的分子式呢?总体来讲,先得确定有机物的组成元素,然后再确定各原子的数目从而确定有机物的分子式。
下面笔者重点介绍一下在确定有机物分子式的计算当中的一些具体计算方法。
1、确定元素的组成一般来说,有机物完全燃烧后,各元素对应的产物为c→co2,h→h2o。
若有机物完全燃烧后的产物只有co2和h2o,则其组成的元素可能为c、h或c、h、o。
欲判断该有机物是否含有氧元素,首先应求出产物中co2中的碳元素质量及h2o中的氢元素的质量,然后将这两种元素的质量相加,再和原有机物的质量进行比较,若相等,则原有机物中不含氧元素,若不相等则原有机物中必定含有氧元素。
2、确定分子式在确定有机物的组成元素之后,接下来根据题目条件来最终确定这几种元素构成的物质的分子式。
在确定分子式进行计算的时候,通常可以采用以下几种计算方法。
方法一、实验式法(即最简式法)根据有机物的分子式为最简式的整数倍,利用其相对分子质量及求得的最简式便可确定其分子式。
如烃的最简式求法为:例1:某含c、h、o三元素的有机物,其c、h、o的质量比为6:1:8,该有机物蒸汽的密度是相同条件下的h2密度的30倍,求该有机物的分子式。
【解析】该有机物中的原子个数比为故其实验式为ch2o,设其分子式为(ch2o)n,根据题意得:。
则该有机物的分子式为c2h4o2。
方法二、单位物质的量法根据题目中的已知条件,确定有机物的元素组成后,直接求出1mol该有机物中各元素原子的物质的量,即可推算出分子式。
若给出一定条件下该有机物气体的密度(或相对密度)及各元素的质量分数,则求解分子式的基本途径为:密度(或相对密度)→m→1mol有机物气体中各元素原子的物质的量→分子式。



有机物分子式求解方法浙江省玉环县玉城中学刘瑞东发表于《中学化学教学参考》2000年第5期求有机物分子式的途径有很多,笔者根据多年的教学就有机物分子式的求解总结出八种通用的方法。
一、“单位物质的量”法根据有机物的摩尔质量(或分子量)和有机物中各元素的质量分数(或质量之比),推算出1mol该有机物中各元素原子的物质的量,从而确定分子中的各原子个数来确定有机物的分子式。
例1.某化合物由碳、氢两种元素组成,其中含碳的质量分数为85.7%,在标准状况下11.2L此化合物气体的质量为14g,求此化合物的分子式。
(高中化学必修本第二册P65。
)解:此烃的摩尔质量为:Mr=14g÷(11.2L÷22.4L/mol)=28gmol1mol此烃中碳原子和氢原子的物质的量分别为:C:(1mol×28g/mol×85.7%)÷12g/mol=2molH:(1mol×28g/mol×14.3%)÷1g/mol=4mol∴1mol烃中含2molC和4molH。
即此烃的分子式为C2H4。
二、最简式法根据有机物各元素的质量分数求出分子组成中各元素的原子个数之比(最简式),然后结合该有机物的摩尔质量(或分子量)求有机物分子式。
例1另解:由前面求得此烃的分子量为28,C和H的个数之比为:(85.7%÷1)∶(14.3%÷1)=1∶2∴此烃的最简式为CH2,分子式为(CH2)n。
则有:12n+2n=28,解得:n=2即此烃的分子式为C2H4。
三、燃烧通式法根据有机物完全燃烧反应的通式以及依据反应物和生成物的质量、物质的量或体积关系求分子式。
如烃的分子式可设为C x H y,由于x和y是相对独立的,计算中数据运算简便。
根据烃的燃烧反应方程式。
借助通式C x H y进行计算,解出x,y最后得出烃的分子式。
例2.0.1mol某烃完全燃烧后,生成13.2gCO2和7.2gH2O,求该烃的分子式。
有机计算一、有机物分子式与结构式求法M =22.4ρ(标况) M =DM1 (同温、同压))M =m(总)/n(总) → 摩尔质量 → 相对分子质量 M =M1a1+M2a2+…根据化学方程式和元素守恒 → 分子式 →结构式碳氢氧元素的质量碳氢氧元素的质量比 → 原子个数比 → 实验式 碳氢氧元素的质量分数 燃烧产物的物质的量例1:有机物A 含碳54.5%、氢9.10%、氧36.4%(质量分数),在标准状况下,蒸气密度是1.96g •L-1,它易溶于水,其水溶液与新制的氢氧化铜混合,加热到沸腾,有红色沉淀生成。
有机物B 含碳60%、氢13.33%、氧26.67%(质量分数),蒸气密度是氢气的30倍,它能发生酯化反应。
则下列各组中,A 、B 的结构简式正确的是A .CH3CHO CH3CH2CH2OHB .CH3CH2CHO CH3COOHC .CH3CHO CH3COOHD .CH3CHO CH3CH(OH)CH3 答案:A 、D 分析:MA=1.96 g •L-1 × 22.4L •mol-1=44 g •mol-11molA 中 含C=(44g × 54.5%)/12 g •mol-1=2mol 含H=(44g × 9.10%)/1g •mol-1=4mol 含O=(44g × 36.4%)/16 g •mol-1=1mol ∴分子式为C2H4O MB=2 g •mol -1 × 30=60 g •mol-11molB 中 含C=(60g × 60%)/12 g •mol-1=3mol 含H=(60g × 13.33%)/1g •mol-1=8mol 含O=(60g × 26.67%)/16g •mol-1=1mol ∴分子式为C3H8O二、有机物燃烧的有关计算熟练掌握有机物燃烧通式的书写: 1、烃的燃烧: (1)烃燃烧的通式(2)各类烃燃烧的通式:(根据各类烃通式,具体写出)2、烃的含氧衍生物的燃烧:3、卤代烃的燃烧:一般生成二氧化碳、水和卤化氢。
有机化学有关计算Ⅰ、有机物分子式的求解方法有机物分子式求解方法较多,现归纳如下。
一、有机物分子式、结构式的确定中的计算【基本步骤】有机物分子式、结构式的确定步骤可按如下路线进行:【方法指导】其中涉及以下方法:基本方法、物质的量比法(又称摩尔比法)、燃烧规律法、商余法、平均分子式法、设“1”讨论法、分子组成通式法、等效转换法、官能团法、残基分析法、不饱和度法以及综合分析法等1.实验式的确定:实验式是表示化合物分子所含各元素的原子数目最简单整数比的式子(通过实验确定),实验式又叫最简式。
①若已知有机物分子中C、H等元素的质量或已知C 、H等元素的质量比或已知C、H等元素的质量分数,则N(C):N(H):N(O)==______②若有机物燃烧产生的二氧化碳和水的物质的量分别为n(CO2)和n(H2O),则N(C):N(H)==__________2.确定相对分子质量的方法:①M==m/n(M表示摩尔质量 m表示质量 n表示物质的量)②已知有机物蒸气在标准状况下的密度:Mr== 22.4* 密度(注意密度的单位)③已知有机物蒸气与某物质(相对分子质量为M’)在相同状况下的相对密度D:则Mr==M’* D (阿伏伽德罗定律的推论)④M== M(A)* X(A) + M(B)*X(B)……(M表示平均摩尔质量,M(A)、M(B)分别表示A、B物质的摩尔质量,X(A)、X(B)分别表示A B 物质的物质的量分数或体积分数)⑤根据化学方程式计算确定。
3.有机物分子式的确定:①直接法:密度(相对密度)→摩尔质量→1摩尔分子中各元素原子的物质的量→分子式②最简式法:最简式为CaHbOc,则分子式为(CaHbOc)n, n==Mr/(12a+b+16c)(Mr为相对分子质量).③余数法:a)用烃的相对分子质量除14,视商和余数。
M(CxHy)/M(CH2)==M/14==A……若余2,为烷烃;若除尽 ,为烯烃或环烷烃;若差2,为炔烃或二烯烃;若差为6,为苯或其同系物。
CH 3—CH 2—CH 2—CH 3有机物分子式的求算有机化学基础是高考考试内容中的五分之一,是高考的重点与难点,也是新课程下五个选修模块的五分之一,有机知识不可忽视。
而在有机部分中,有机物分子式的求算又是有机部分的重点,也是热点。
以下分列几种情况下的求算方法。
一、已知分子量求分子式例1:已知某有机物的分子量为58。
试根据下列条件回答:(1)若该有机物只由碳、氢元素组成, 则可能有的结构简式为 。
(2)若该有机物为含氧衍生物, 且分子中有一个—CH 3, 则可能结构简式为__________(3)若该有机物分子中无—CH 3、又无—OH, 但能发生银镜反应, 那么该物质的结构简式为 。
解析:若为烃类,用分子量除14法(商余法)来计算,整除为烯、余2为烷烃、少2为炔、少6为苯及其同系物;若为烃的衍生物,根据条件用分子量减去已知的基团的分子量,剩余部分再除于14求烃基部分,再跟据要求写其结构简式。
答案:(1) (2) (3)跟踪练习:相同状况下9升甲烷与6升某烯烃混合, 所得混合气的密度等于相同条件下氧气的密度, 求该烯烃的分子式、可能的结构简式?二、最简式法求分子式例2:某气态烃含碳、氢元素质量比为6∶1, 又知同温、同压下该气体密度为氢气密度的14倍, 求该烃的分子式。
解析:根据含碳、氢元素质量比,求出通式C n H 2n ,再由分子量求算。
答案为C 2H 4练习:某有机物组成中含碳54.5%, 含氢9.1%,其余为氧又知其蒸汽在标况下的密度为3.94g/L ,试求其分子式(答案:C 4H 8O 2)三、通式法求分子式例3:标准状况下10毫升某气态烷烃跟80毫升过量的氧气混合, 通入一个容积为90毫升的密闭容器中点火爆炸后, 恢复到原状态, 测得的压强为原来的55.56%。
求烷烃的分子式?解析:根据烷烃的燃烧同时来求算出C n H 2n +2中的n 值。
答案:C 5H 12四、用差量法求烃分子中的氢原子数例4:常温常压下一体积某气态烃在足量的氧气中充分燃烧后恢复到原来的温度和压强,体积缩小了2体积。
有机物分子式的确定一、有机物组成元素的判断——燃烧法有机物完全燃烧后,各元素对应产物为:C→CO2,H→H2O,Cl→HCl。
某有机物完全燃烧后若产物只有CO2和H2O,则其组成元素欲判定该有机物中是否含氧元素二、实验式(最简式)和分子式的区别与联系(1)最简式:表示化合物分子所含各元素的原子数目最简单整数比的式子。
不能确切表明分子中的个各原子的个数。
注意:①最简式是一种表示物质组成的化学用语;②无机物的最简式一般就是化学式;③有机物的元素组成简单,种类繁多,具有同一最简式的物质往往不止一种;④最简式相同的物质,所含各元素的质量分数是相同的,若相对分子质量不同,其分子式就不同。
例如,苯(C6H6)和乙炔(C2H2)的最简式相同,均为CH,故它们所含C、H元素的质量分数是相同的。
(2)分子式:表示化合物分子所含元素的原子种类及数目的式子。
注意:①分子式是表示物质组成的化学用语;②无机物的分子式一般就是化学式;③由于有机物中存在同分异构现象,故分子式相同的有机物,其代表的物质可能有多种;④分子式=(最简式)n。
,。
三、有机物相对分子质量的计算方法1、标准状况下,M=22.4ρ(单位:克/升)2、相对密度法:M=2D (D是氢气密度的倍数)M=29D (D是空气密度的倍数)四、确定分子式的方法——关键是计算M(1)、实验式法:由各元素的质量分数→求出实验式→相对分子质量→求分子式。
例1:某有机物含碳40%,氢6.67%,氧53.3%,如果0.2mol该有机物质量为6g,求它的分子式。
(2)、物质的量关系法——比值法求:1摩尔有机物中各元素的物质的量之比,就是分子式下标的比。
例2:某混合气体由两种气态烃组成。
取2.24升该混合气体完全燃烧后得到4.48升二氧化碳(在标况下)和3.6克水,则这两种气体可能是A、CH4、C3H8B、CH4、C3H4C、C2H4、C3H4D、C2H2、C2H6E、C2H4、C2H6例3:由两种气态烃组成的混合气体30ml,与过量氧气完全燃烧后,生成CO2 60ml,水蒸气45ml(相同条件下测得)。
求原混合气的成分及体积比。
(3)、化学方程式法——利用化学方程式求分子式。
(已知物质的类别)(4)、燃烧通式法——利用通式和相对分子质量求分子式。
(5)、通式法:如烷烃、烯烃等例4:标准状况下体积为1L的某气态单烯烃,其质量为1.875g,确定该烯烃的分子式。
(6)商余法:例5:某烃分子量为82,试判断它的分子式(7)M的估值法:例6:某有机化合物A的相对分子质量(分子量)大于110,小于150。
经分析得知,其中碳和氢的质量分数之和为52.24%,其余为氧。
请回答:(1)该化合物分子中含有几个氧原子,为什么?(2)该化合物的相对分子质量(分子量)是。
(3)该化合物的化学式(分子式)是。
(4)该化合物分子中最多含个羰基(—CO—)练习一:1、3.26g样品燃烧后,得到4.74gCO2和1.92gH2O,实验测得其相对分子质量为60,求该样品的实验式和分子式。
(1)、求各元素的质量分数(2)、求样品分子中各元素原子的数目(N)之比(3)、求分子式。
2、实验测得某烃A中含碳85.7%,含氢14.3%。
在标准状况下11.2L此化合物气体的质量为14g。
求此烃的分子式。
3、6.0g某饱和一元醇跟足量的金属钠反应,让生成的氢气通过5g灼热的氧化铜氧化铜固体的质量变成4.36g。
这时氢气的利用率是80%。
求该一元醇的分子。
4、有机物A是烃的含氧衍生物,在同温同压下,A蒸气与乙醇蒸气的相对密度是2。
1.38gA完全燃烧后,若将燃烧的产物通过碱石灰,碱石灰的质量会增加3.06g;若将燃烧产物通过浓硫酸,浓硫酸的质量会增加1.08g;取4.6gA与足量的金属钠反应,生成的气体在标准状况下的体积为1.68L;A不与纯碱反应。
通过计算确定A的分子式和结构简式。
【练习】1、某烃0.1mol,在氧气中完全燃烧,生成13.2g CO2、7.2gH2O,则该烃的分子式为。
2、已知某烃A含碳85.7%,含氢14.3%,该烃对氮气的相对密度为2,求该烃的分子式。
3、125℃时,1L某气态烃在9L氧气中充分燃烧反应后的混合气体体积仍为10L(相同条件下),则该烃可能是A. CH4B. C2H4C. C2H2D.C6H64、一种气态烷烃和气态烯烃组成的混合物共10g,混合气密度是相同状况下H2密度的12.5倍,该混合气体通过装有溴水的试剂瓶时,试剂瓶总质量增加了8.4g,组成该混合气体的可能是A. 乙烯和乙烷B. 乙烷和丙烯C. 甲烷和乙烯D. 丙稀和丙烷5、室温下,一气态烃与过量氧气混合完全燃烧,恢复到室温,使燃烧产物通过浓硫酸,体积比反应前减少50mL,再通过NaOH溶液,体积又减少了40mL,原烃的分子式是A. CH4B. C2H4C. C2H6D.C3H86、A、B两种烃通常状况下均为气态,它们在同状况下的密度之比为1∶3.5。
若A完全燃烧,生成CO2和H2O的物质的量之比为1∶2,试通过计算求出A、B的分子式。
7、使乙烷和丙烷的混合气体完全燃烧后,可得CO2 3.52 g,H2O 1.92 g,则该混合气体中乙烷和丙烷的物质的量之比为A.1∶2B.1∶1C.2∶3D.3∶48、两种气态烃的混合气共1mol,在空气中燃烧得到1.5molCO2和2molH2O。
关于该混合气的说法合理的是A.一定含甲烷,不含乙烷B.一定含乙烷,不含甲烷C.一定是甲烷和乙烯的混合物D.一定含甲烷,但不含乙烯9、25℃某气态烃与O2混合充入密闭容器中,点燃爆炸后又恢复至25℃,此时容器内压强为原来的一半,再经NaOH溶液处理,容器内几乎成为真空。
该烃的分子式可能为A. C2H4B. C2H2C. C3H6D. C3H810、某烃7.2g进行氯代反应完全转化为一氯化物时,放出的气体通入500mL0.2mol/L的烧碱溶液中,恰好完全反应,此烃不能使溴水或酸性高锰酸钾溶液褪色,试求该烃的分子式。
11、常温下某气态烷烃10mL与过量O285mL充分混合,点燃后生成液态水,在相同条件下测得气体体积变为70mL,求烃的分子式。
12、由两种气态烃组成的混合烃20mL,跟过量O2完全燃烧。
同温同压条件下当燃烧产物通过浓H2SO4后体积减少了30mL,然后通过碱石灰又减少40mL。
这种混合气的组成可能有几种?13、A、B都是芳香族化合物,1 mol A水解得到1 mol B和1 mol醋酸.A、B的分子量都不超过200,完全燃烧都只生成CO2和H2O.且B分子中碳和氢元素总的质量百分含量为65.2%(即质量分数为0.652).A溶液具有酸性,不能使FeCl3溶液显色.(1)A、B分子量之差为_______________.(2)1个B分子中应该有_______________个氧原子.(3)A的分子式是_______________.(4)B可能的三种结构简式是:_______________、_______________、_______________.《有机物分子式的确定》参考答案[例1] 3.26g样品燃烧后,得到4.74gCO2和1.92gH2O,实验测得其相对分子质量为60,求该样品的实验式和分子式。
解:(1)求各元素的质量分数样品CO2H2O3.26g4.74g 1.92g(2)求样品分子中各元素原子的数目(N)之比这个样品的实验式为CH2O。
(3)求分子式通过实验测得其相对分子质量为60,这个样品的分子式=(实验式)n。
故这个样品的分子式为C2H4O2。
答:这个样品的实验式为CH2O,分子式为C2H4O2。
[例2]实验测得某烃A中含碳85.7%,含氢14.3%。
在标准状况下11.2L此化合物气体的质量为14g。
求此烃的分子式。
解:(1)求该化合物的摩尔质量根据得(2)求1mol该物质中碳和氢原子的物质的量即1mol该化合物中含2molC原子和4molH原子,故分子式为C2H4。
[例3] 6.0g某饱和一元醇跟足量的金属钠反应,让生成的氢气通过5g灼热的氧化铜,氧化铜固体的质量变成4.36g。
这时氢气的利用率是80%。
求该一元醇的分子。
解:设与CuO反应的氢气的物质的量为x而这种一元醇反应后生成的氢气的物质的量为。
饱和一元醇的通式为,该一元醇的摩尔质量为M(A)。
该一元醇的相对分子质量是60。
根据这一元醇的通式,有下列等式:则饱和一元醇的分子式是C2H6O。
[例4]有机物A是烃的含氧衍生物,在同温同压下,A蒸气与乙醇蒸气的相对密度是2。
1.38gA完全燃烧后,若将燃烧的产物通过碱石灰,碱石灰的质量会增加3.06g;若将燃烧产物通过浓硫酸,浓硫酸的质量会增加1.08g;取4.6gA与足量的金属钠反应,生成的气体在标准状况下的体积为1.68L;A不与纯碱反应。
通过计算确定A的分子式和结构简式。
解:燃烧产物通过碱石灰时,CO2气体和水蒸气吸收,被吸收的质量为3.06g;若通过浓硫酸时,水蒸气被吸收,被吸收的质量为1.08g。
故CO2和水蒸气被吸收的物质的量分别为:列方程解之得x=3 y=8由题意知A 与金属钠反应,不与Na 2CO 3反应,可知A 含羟基不含羧基(—COOH )。
4.6gA 所含物质的量为4.6gA 中取代的H 的物质的量为 。
即1molA 取代H 的物质的量为3mol ,可见1个A 分子中含有3个羟基,故A 为丙三醇,结构简式为:【练习】⒈解析:烃.完全燃烧产物为CO 2、H 2O ,CO 2中的C 、H 2O 中的H 全部来自于烃。
13.2g CO 2物质的量为13.2g 0.3mol 44g /mol =,7.2gH 2O 物质的量为7.2g0.4mol 18g /mol=, 则0.1mol该烃中分子含C :0.3mol ,含H :0.4mol×2=0.8mol (CO 2~C 、H 2O ~2H ),所以1mol 该烃分子中含C3mol 、含H8mol 。
答案:C 3H 8。
⒉解析:85.7%14.3%n(C):n(H):1:2121==,即最简式为CH 2、化学式为2n (CH ),该烃的相对分子质量:M r (A)=M r (N 2)×2=28×2=56,r r 2M (A)56n 4M (CH )14===,故分子式为C 4H 8。
⒊解析:任意烃与一定量氧气充分燃烧的化学方程式:C x H y + (x + y 4 )O 2−−→−点燃xCO 2 + y 2H 2O 当温度高于100℃时,生成的水为气体。
若烃为气态烃,反应前后气体的体积不变,即反应消耗的烃和O 2与生成的二氧化碳和气态水的体积相等。
∴1 + (x + y 4 ) = x + y2y = 4就是说气态烃充分燃烧时,当烃分子中氢原子数等于4时(与碳原子数多少无关),反应前后气体的体积不变(生成物中水为气态)。