m(O) 1.5g (0.6g 0.1g) 0.8g
N(C) :
N(H) :
N (O)
0.6g 12g mol1
:
1
0.1g g mol1
:
1
6
0.8g g mo
l1
1: 2:1
M (A) 1.04 29 30
又因该有机物的相对分子质量 ∴实验式CH2O即为分子式。
第4页/共8页
[例] 2.3g 某有机物A完全燃烧后,生成 0.1molCO2和2.7gH2O,测得该化合物的蒸气 体与空气的相对分密度是1.6,求该化合物的 分子式
的比值 D.测定该试样的质量及试样完全燃烧后生成
CO2和H2O的质量
2、教材p21 “学与问”
第6页/共8页
亲爱的同学们:
第7页/共8页
谢谢您的观看!
第8页/共8页
N (C) : N (H) 82.8 : 17.2 2 : 5 12 1
[注意]:C2H5仅仅代表碳原子和氢原子的最简整数 比,是该烃的实验式,不是该烃的分子式.若设 该烃有n个C2H5,则n=58/29=2因此,该烃的分子 式为C4H10。
第3页/共8页
(2)根据气态有机物密度或相对密度求分子式
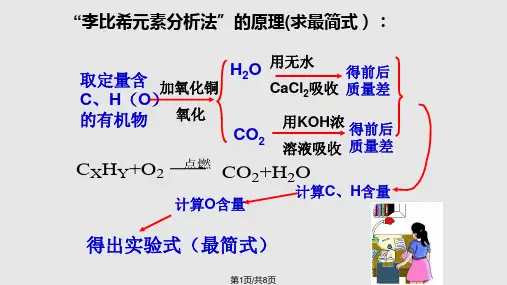
“李比希元素分析法”的原理(求最简式):
取C、定H量(含O)加氧化铜
H2O 用无水
得前后
CaCl2吸收 质量差
的有机物
氧化
CO2
用KOH浓 得前后 溶液吸收 质量差
CXHY+O2 点燃 CO2+H2O
计算C、H含量 计算O含量
得出实验式(最简式)
第1页/共8页
案例分析
某含C、H、O三种元素的未知物A,经燃烧分析实验测 定该未知物A中碳的质量分数为52.16%,氢的质量分数 13.14%,试求该未知物A的实验式。