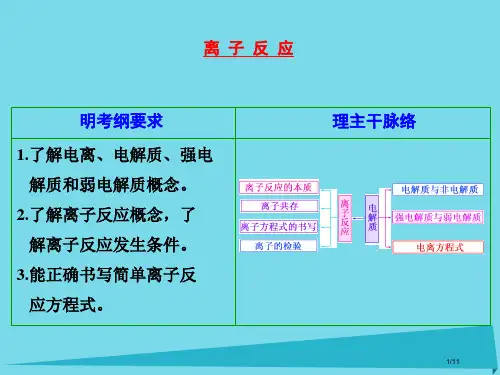
离子反应发生条件(公开课)
- 格式:ppt
- 大小:140.00 KB
- 文档页数:15





第二节离子反应的本质江夏一中姜辉【教学目的】1.使学生理解离子反应的本质和离子反应发生的条件。
2.使学生掌握离子反应方程式的书写和应用。
3.培养学生对所学知识进行归纳和小结的能力。
【教学重点】离子反应的本质,离子反应发生的条件。
【教学难点】离子反应发生的条件之———发生氧化还原反应,有关某些离子在溶液中不能大量共存的讨论。
【教学方法】复习讨论、归纳总结。
【教学过程】【引言】高一时我们对离子反应有了一些了解,今天我们将进一步学习离子反应的本质。
【投影】下列反应能否发生?如果能发生,写出反应现象及相应的离子方程式。
(由学生填写前三项)【讨论】上述反应物的离子浓度有什么变化?【归纳】如果反应物的某些离子能结合生成新物质,使溶液中的这些离子浓度减小,就会发生离子反应。
如果反应物的离子之间不能结合生成新物质,溶液中的这些离子浓度没有改变,离于反应就不能发生。
也就是说,离子反应的实质是反应物的某些离子浓度的减小。
【板书】一、离子反应的本质是反应物的某些离子浓度的减小。
【设疑】是不是反应物的所有离子浓度都降低呢?【分析】上述反应1中,Ba2+与到SO42-浓度因反应而降低,而Cu2+、Cl-浓度并没有因此而降低,所以说是某些反应物离子浓度降低,并不是所有反应物的离子浓度都降低。
【讨论】在什么条件下,可以使反应物的某些离子浓度减小呢?(引导学生从上述反应现象分析、归纳、补充)【归纳】由于反应物之间的离子互相结合,生成难溶于水的物质、易挥发的物质或难电离的物质,使反应物中的某些离子浓度大大减小。
也就是说,离子反应发生的条件之一,就是生成难溶、难电离、易挥发的物质。
【板书】二、离子反应发生的条件1.生成难溶的物质【设疑】常见的难溶物有哪些?【投影】常见的难溶物质(由学生归纳):①酸: H2SiO3( H4SiO4)②碱: Mg(OH)2、 Al(OH)3、Cu(OH)2、Fe(OH)3等③盐: BaSO4、BaCO3、CaCO3、AgCl等④金属单质: Fe、Ag、Cu等⑤非金属单质: S、Si等⑥氧化物: Ag2O、Al2O3等【讲述】当有关离子浓度足够大时,生成微溶物的反应也能发生,如硝酸银溶液与硫酸钠溶液混合时,当银离子、硫酸根离子浓度足够大时,也能生成硫酸银沉淀。




高中化学离子反应教案一、教学目标:1. 理解离子反应的概念和基本原理;2. 掌握离子反应的化学方程式的写法和平衡方法;3. 能够应用离子反应解释化学现象和推导化学方程式;4. 培养学生的实验设计和数据分析能力。
二、教学重点:1. 离子反应的概念和特点;2. 离子反应方程式的写法和平衡方法;3. 应用离子反应解释化学现象。
三、教学难点:1. 离子反应方程式的写法和平衡方法;2. 应用离子反应解释化学现象。
四、教学过程:1. 离子的概念和离子反应的特点(15分钟)a. 引导学生回顾离子的定义和离子的电荷;b. 解释离子反应的概念和离子反应相对于分子反应的特点。
2. 离子反应方程式的写法(30分钟)a. 介绍离子反应方程式的写法和平衡方法;b. 引导学生通过例题掌握离子反应方程式的写法;c. 帮助学生理解离子反应方程式的平衡方法。
3. 离子反应方程式的应用(40分钟)a. 教师引导学生通过实验数据解释化学现象;b. 帮助学生从实验现象中推导出离子反应方程式;c. 引导学生通过例题和习题巩固应用离子反应方程式解释化学现象的能力。
4. 实验设计和数据分析(35分钟)a. 学生进行相关实验,完成实验报告;b. 教师引导学生分析实验数据,并帮助学生总结实验结果;c. 学生通过实验和数据分析培养实验设计和数据分析能力。
五、教学资源:1. 教材:高中化学教材;2. 实验器材:根据实验需要准备相应的实验器材和化学试剂;3. 讲义和习题:准备相应的讲义、例题和习题。
六、教学评价:1. 针对学生对离子反应概念的理解程度进行课堂教学评价;2. 针对学生对离子反应方程式的写法和平衡方法的掌握情况进行课堂教学评价;3. 针对学生应用离子反应解释化学现象和推导化学方程式的能力进行实验报告的评价。
七、教学延伸:1. 帮助学生了解离子反应在日常生活和工业中的应用;2. 引导学生进一步研究离子反应的应用和相关领域的发展。
八、教学反思:本节课主要围绕离子反应的概念、方程式写法和应用展开教学。