无机化学 第十五章 氮族元素
- 格式:ppt
- 大小:2.98 MB
- 文档页数:141



高中化学知识点规律大全——氮族元素1.氮和磷[氮族元素]包括氮(7N)、磷、(15P)、砷(33As)、锑(51Sb)、铋(83Bi)五种元素.氮族元素位于元素周期表中第V A族,其代表元素为氮和磷.[氮族元素的原子结构](1)相似性:①最外层电子数均为5个;②主要化合价:氮有-3、+1、+2、+3、+4、+5价;磷和砷有-3、+3、+5价;锑、铋有+3、+5价.(2)递变规律:按氮、磷、砷、锑、铋的顺序,随着核电荷数的增加,电子层数增多,原子半径增大,失电子能力增强,得电子能力减弱,非金属性减弱,金属性增强.在氮族元素的单质中,氮、磷具有较明显的非金属性;砷虽然是非金属,但有一些金属性;锑、铋为金属.[氮族元素单质的物理性质]N2P As Sb Bi颜色无色白磷:白色或黄色红磷:红棕色灰砷:灰色银白色银白色或微显红色状态气体固体固体固体固体密度逐渐增大熔点、沸点先按N2、P、As的顺序逐渐升高,而后按Sb、Bi的顺序逐渐降低[氮气](1)氮元素在自然界中的存在形式:既有游离态又有化合态.空气中含N2 78%(体积分数)或75%(质量分数);化合态氮存在于多种无机物和有机物中,氮元素是构成蛋白质和核酸不可缺少的元素.(2)氮气的物理性质:纯净的氮气是无色气体,密度比空气略小.氮气在水中的溶解度很小.在常压下,经降温后,氮气变成无色液体,再变成雪花状固体.(3)氮气的分子结构:氮分子(N2)的电子式为,结构式为N≡N.由于N2分子中的N≡N键很牢固,所以通常情况下,氮气的化学性质稳定、不活泼.(4)氮气的化学性质:①N2与H2化合生成NH3N2 +3H22NH3说明该反应是一个可逆反应,是工业合成氨的原理.②N2与O2化合生成NO:N2 + O22NO说明在闪电或行驶的汽车引擎中会发生以上反应.(5)氮气的用途:①合成氨,制硝酸;②代替稀有气体作焊接金属时的保护气,以防止金属被空气氧化;⑧在灯泡中填充氮气以防止钨丝被氧化或挥发;④保存粮食、水果等食品,以防止腐烂;⑤医学上用液氮作冷冻剂,以便在冷冻麻醉下进行手术;⑥利用液氮制造低温环境,使某些超导材料获得超导性能.[NO、NO2性质的比较]氮的氧化物一氧化氮(NO) 二氧化氮(NO2)物理性质为无色、不溶于水、有毒的气体为红棕色、有刺激性气味、有毒的气体,易溶于水化学性质①极易被空气中的O2氧化:2NO + O2= 2NO2②NO中的氮为+2价,处于中间价态,既有氧化性又有还原性与H2O反应:3NO2 + H2O=2HNO3 + NO(工业制HNO3原理.在此反应中,NO2同时作氧化剂和还原剂)[自然界中硝酸盐的形成过程](1)电闪雷鸣时:N2+O 22NO(2) 2NO + O2= 2NO2(3)下雨时:3NO2 + H2O=2HNO3 + NO(4)生成的硝酸随雨水淋洒到土壤中,并与土壤中的矿物作用生成能被植物吸收的硝酸盐.[光化学烟雾]NO、NO2有毒,是大气的污染物.空气中的NO、NO2污染物主要来自于石油产品和煤燃烧的产物、汽车尾气以及制硝酸工厂的废气.NO2在紫外线照射下,发生一系列光化学反应,产生一种有毒的烟雾——光化学烟雾.因此,NO2是造成光化学烟雾的主要因素.光化学烟雾刺激呼吸器官,使人生病甚至死亡.[磷](1)磷元素在自然界中的存在形式:自然界中无游离态的磷.化合态的磷主要以磷酸盐的形式存在于矿石中.动物的骨骼、牙齿和神经组织,植物的果实和幼芽,生物的细胞里都含有磷.(2)单质磷的化学性质:①与O2反应:4P+5O 22P2O5②磷在C12中燃烧:2P+3C12(不足量) 2PCl32P+5Cl2(足量) 2PCl5[磷的同素异形体——白磷与红磷]磷的同素异形体白磷红磷说明物理性质颜色、状态无色蜡状固体红棕色粉末①白磷与红磷的结构不同是物理性质存在差别的原因②由两者物理性质的不同,证明了白磷与红磷是不同的单质密度(g·cm-3)1.822.34溶解性不溶于水,溶于CS2不溶于水,也不溶于CS2毒性剧毒无毒着火点40℃(白磷受到轻微的摩擦就会燃烧;常温时,白磷可被氧化而发光)240℃化学性质白磷、红磷在空气中燃烧,都生成白色的P2O5白磷与红磷燃烧都生成P2O5,证明它们都是由磷元素形成的单质相互转化白磷红磷证明白磷与红磷所含元素相同——互为同素异形体保存方法密封保存,少量白磷保存在水中密封保存,防止吸湿切削白磷应在水中进行用途制造高纯度磷酸;制造燃烧弹、烟幕弹制造高纯度磷酸;制农药、安全火柴[五氧化二磷、磷酸](1)五氧化二磷的性质:五氧化二磷是白色粉末状固体,极易吸水(因此可作酸性气体的干燥剂).P2O5是酸性氧化物,与水反应:P2O5+3H2O2H3PO4(2)磷酸的性质、用途:磷酸(H3PO4)是一种中等强度的三元酸,具有酸的通性.磷酸主要用于制造磷肥,也用于食品、纺织等工业.[氮、磷元素及其单质、化合物性质的比较]元素氮(N)磷(P)自然界中存在的形式游离态和化合态只有化合态单质与O2化合的情况N2+O22NO(易)4P+5O22P2O5(难)单质与H2化合的情况N2 +3H22NH32P(蒸汽) + 3H22PH3单质的化学活泼性及原因单质活泼性:N2<P原因:N2分子中N≡N键很牢固,故N2性质稳定、不活泼氢化物的稳定性 NH 3>PH 3 最高价氧化物对应水化物的酸性 HNO 3>H 3PO 4非金属性 N >P2.铵盐 [氨](1)氨的物理性质:①氨是无色、有刺激性气味的气体,比空气轻;②氨易液化.在常压下冷却或常温下加压,气态氨转化为无色的液态氨,同时放出大量热.液态氨气化时要吸收大量的热,使周围的温度急剧下降;③氨气极易溶于水.在常温、常压下,1体积水中能溶解约700体积的氨气(因此,氨气可进行喷泉实验);④氨对人的眼、鼻、喉等粘膜有刺激作用.若不慎接触过多的氨而出现病症,要及时吸入新鲜空气和水蒸气,并用大量水冲洗眼睛.(2)氨分子的结构:NH 3的电子式为,结构式为,氨分子的结构为三角锥形,N 原子位于锥顶,三个H 原子位于锥底,键角107°18′,是极性分子. (3)氨的化学性质:①跟水反应.氨气溶于水时(氨气的水溶液叫氨水),大部分的NH 3分子与H 2O 分子结合成NH 3·H 2O(叫一水合氨).NH 3·H 2O 为弱电解质,只能部分电离成NH 4+和OH -:NH 3 + H 2O NH 3·H 2O NH 4+ + OH -a .氨水的性质:氨水具有弱碱性,使无色酚酞试液变为浅红色,使红色石蕊试液变为蓝色.氨水的浓度越大,密度反而越小(是一种特殊情况).NH 3·H 2O 不稳定,故加热氨水时有氨气逸出:NH 4++ OH -NH 3↑+ H 2Ob .氨水的组成:氨水是混合物(液氨是纯净物),其中含有3种分子(NH 3、NH 3·H 2O 、H 2O)和3种离子(NH 4+和OH -、极少量的H +).c .氨水的保存方法:氨水对许多金属有腐蚀作用,所以不能用金属容器盛装氨水.通常把氨水盛装在玻璃容器、橡皮袋、陶瓷坛或内涂沥青的铁桶里.d .有关氨水浓度的计算:氨水虽然大部分以NH 3·H 2O 形式存在,但计算时仍以NH 3作溶质. ②跟氯化氢气体的反应:NH 3 + HCl = NH 4C1说明 a .当蘸有浓氨水的玻璃棒与蘸有浓盐酸的玻璃棒靠近时,产生大量白烟.这种白烟是氨水中挥发出来的NH 3与盐酸挥发出来的HCl 化合生成的NH 4C1晶体小颗粒.b .氨气与挥发性酸(浓盐酸、浓硝酸等)相遇,因反应生成微小的铵盐晶体而冒白烟,这是检验氨气的方法之—.c .氨气与不挥发性酸(如H 2SO 4、H 3PO 4等)反应时,无白烟生成.③跟氧气反应: 4NH 3 + 5O 2 4NO + 6H 2O说明 这一反应叫做氨的催化氧化(或叫接触氧化),是工业上制硝酸的反应原理之一. (4)氨气的用途:①是氮肥工业及制造硝酸、铵盐、纯碱的原料;②是有机合成工业如合成纤维、塑料、染料、尿素等的常用原料;③用作冰机中的致冷剂.[铵盐]铵盐是由铵离子(NH 4+)和酸根阴离子组成的化合物.铵盐都是白色晶体,都易溶于水. (1)铵盐的化学性质:①受热分解.固态铵盐受热都易分解.根据组成铵盐的酸根阴离子对应的酸的性质的不同,铵盐分解时有以下三种情况:a .组成铵盐的酸根阴离子对应的酸是非氧化性的挥发性酸时,则加热时酸与氨气同时挥发,冷却时又重新化合生成铵盐。

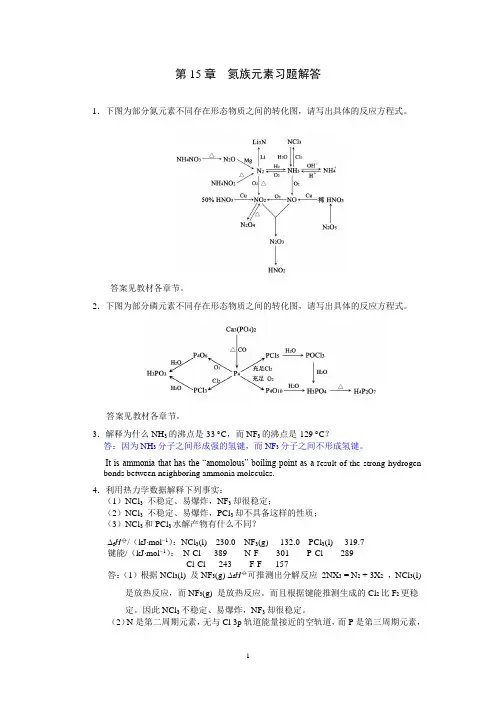
第15章氮族元素习题解答1.下图为部分氮元素不同存在形态物质之间的转化图,请写出具体的反应方程式。
答案见教材各章节。
2.下图为部分磷元素不同存在形态物质之间的转化图,请写出具体的反应方程式。
答案见教材各章节。
3.解释为什么NH3的沸点是-33 ︒C,而NF3的沸点是-129 ︒C?答:因为NH3分子之间形成强的氢键,而NF3分子之间不形成氢键。
It is ammonia that has the “anomolous” boiling point as a r esult of the strong hydrogen bonds between neighboring ammonia molecules.4.利用热力学数据解释下列事实:(1)NCl3不稳定、易爆炸,NF3却很稳定;(2)NCl3不稳定、易爆炸,PCl3却不具备这样的性质;(3)NCl3和PCl3水解产物有什么不同?∆f H/(kJ⋅mol-1):NCl3(l) 230.0 NF3(g) -132.0 PCl3(l) -319.7键能/(kJ⋅mol-1):N-Cl 389 N-F 301 P-Cl 289Cl-Cl 243 F-F 157答:(1)根据NCl3(l) 及NF3(g) ∆f H可推测出分解反应2NX3 = N2 + 3X2,NCl3(l) 是放热反应,而NF3(g) 是放热反应。
而且根据键能推测生成的Cl2比F2更稳定。
因此NCl3不稳定、易爆炸,NF3却很稳定。
(2)N是第二周期元素,无与Cl 3p轨道能量接近的空轨道,而P是第三周期元素,最低空轨道是3d轨道,与Cl的3p轨道能量接近,形成的PCl3中的P-Cl键除σ键以外,还有p-d 反馈π键,使P-Cl 键键级大于1,相对稳定。
所以NCl3不稳定、易爆炸,PCl3却不具备这样的性质。
(3)NCl3水解是亲电水解,产物是NH3和HOCl;PCl3水解是亲电加亲核水解,产物H3PO3和HCl。

第15课 氮族元素(建议2课时)[课程目标]1.认识氮族元素以及在周期表中的位置和原子结构特点2.掌握N 2的性质、了解氮的主要用途3.掌握NO 、NO 2的重要性质及其与环境的关系4.了解氨的物理性质,掌握氨的化学性质及氨的实验室制法5.了解铵盐的性质,掌握铵根离子的检验方法6.掌握硝酸的化学性质,了解硝酸的用途[要点精讲]一、氮族元素氮族元素包括N (氮)、P (磷)、As (砷)、Sb (锑)、Bi (铋)5种元素。
在元素周期表中位于ⅤA 族,最高正化合价为+5价,最高价氧化物的通式为R 2O 5 ,其对应水化物通式为HRO 3或H 3RO 4 。
最低负化合价为–3价,其氢化物通式为RH 3 。
氮族元素原子结构的异同点:相同点——最外层都是5个电子;不同点——电子层数逐渐增多,原子半径逐渐增大。
氮族元素化学性质上主要递变规律:从上到下,元素的非金属性逐渐减弱,金属性逐渐增强。
最高价氧化物的水化物的酸性逐渐减弱;气态氢化物(RH 3)的热稳定性逐渐减弱,还原性逐渐增强;二、氮气与氮的固定1、氮气的物理性质:无色、无味气体,难溶于水,难液化,空气中含78%(体积分数)的氮气。
沸点为–195.8℃,熔点为–209.9℃2、分子结构:N ;N ≡N ;氮氮叁键键能很高。
3、化学性质:常温稳定,高温活泼。
(1)还原性:N 2 + O 2 ==== 2NO(2)氧化性:N 2 + 3H 2 2NH 34、用途:合成氨、制硝酸、作保护气等。
5、氮的固定:使空气中游离态的氮转化为含氮化合物的方法叫做氮的固定。
氮的固定主要有自然固氮和人工固氮。
自然固氮的途径主要有两种:一种是通过闪电等产生含氮化合物的高能固氮(约占自然固氮的10%);另一种是生物固氮,即自然界中的一些微生物种群(如豆科植物的根瘤菌)将空气中的氮气通过生物化学过程转化为含氮化合物(约占自然固氮的90%)。
合成氨属于人工固氮,即工业固氮。
此外还发现某些金属有机化合物可以起到根瘤菌的作用,以此做催化剂实现了常温、常压固氮,即仿生固氮。


氮族元素,第V主族:元素符号核电荷数电子层结构原子半径pm 主要化合价氮N 7 2 5 70 -3、+1、+2、+3、+4、+5 磷P 15 2 8 5 110 -3、+3、+5砷As 33 2 8 18 5 121 -3、+3、+5锑Sb 51 2 8 18 18 5 141 +3、+5铋Bi 83 2 8 18 32 18 5 152 +3、+5【最外层电子排布、元素化合价共同点】∵最外层电子都有5个,∴最高价+5,最低价-3∴最高价氧化物R2O5,气态氢化物RH3【原子半径、金属性、非金属性的递变规律】∵原子半径随着电子层数的增加而增大,得电子能力减弱→非金属性减弱失电子能力增强→金属性增强氮、磷:较显著的非金属性砷:较弱的金属性和非金属性锑、铋:较显著的金属性氮族元素的非金属性比同周期的氧族和卤族元素弱氮气N2一、氮元素的存在:单质:氮气,占大气体积的78%,总质量的75%化合物:无机物(硝酸盐、铵盐、氮的氧化物)有机物(蛋白质、核酸)二、物理性质:无色、无味、气体标况下,密度=1.25g/L(比空气略小,但相近,只能用排水法收集)沸点:-195.8℃无色液体(液氮)难液化熔点:-209.86℃雪状固体难溶于水(1:0.02)三、氮分子的结构:分子式:N2电子式:结构式:用元素符号和短线来表示分子中原子结合的式子(一根短线表示一对共用电子,即共价键)氮分子的结构很稳定,破坏分子中的共价键需要很大的能量通常情况下,N 2的化学性质很不活泼,很难跟其他物质发生化学反应一定条件下(高温、放电),获得足够能量,能跟H 2、O 2、金属等反应四、化学性质:1、与H 2反应:N 2+ 3H 2 2NH 3 + Q (工业合成氨)【注】反应要加热,不一定是吸热反应2、与O 2反应:NO 2O N 22−−→−+放电 (无色、有毒、不溶于水)3、与金属反应:高温时,N 2能跟钾、钠、镁、钙、锶、钡等金属化合 -3232N Mg N Mg 3−−→−+高温 (式量100:CaCO 3、KHCO 3)氮化镁、灰色【镁在空气中燃烧】232N Mg N Mg 3−−→−+高温 (微量)MgO 2O Mg 22−−→−+点燃 (主要产物,因O 2比N 2活泼)C MgO 2CO Mg 22+−→−+△【氮化镁遇水】↑+↓−→−+32223NH 2OH Mg 3O H 6N Mg )((非氧化还原)五、用途1、 利亚N 2的稳定性(化学性质不活泼):代替稀有气体作焊接金属时的保护气充填灯泡,防止钨丝氧化,减慢钨丝的挥发 充氮包装,食品保鲜高温高压 催化剂2、 利用液氮的低温:深度冷冻物质提供超导材料的工作环境 保存待移植的活性器官 冷冻麻醉开刀3、 利用一定条件下的反应:合成氨、制硝酸、氮肥、炸药、塑料、药品、染料等六、氮的固定(固氮)【定义】把大气中游离态的氮转化为氮的化合物的过程1、生物固氮豆科植物根部的根瘤菌中存在固氮酶,能把空气中游离的氨变成氨(铵态氮肥)2、大气固氮——“雷电发庄稼”闪电时,大气中的氮转化为氮的氧化物,经降水生成极稀的硝酸(硝态氮肥)NO 2O N 22−−→−+放电 22NO 2O NO 2−→−+NO HNO 2O H NO 3322+−→−+3、工业固氮——“先合成氨,再生产各种化肥”N 2 + 3H 22NH 3固氮途径自然固氮 人工固氮 生物固氮 大气固氮 化学模拟生物固氮 工业固氮 高温高压 催化剂氨NH 3一、氨分子的结构:氮的气态氢化物 分子式:NH 3电子式:N HH H结构式:N HH H分子空间构型:三角锥形氮原子位于锥顶,3个氢原子位于锥底,键角107°18′,极性分子二、物理性质:1、无色、刺激性气味、气体2、比空气轻,标况下,密度=0.771g/L3、极易溶于水(1:700),形成氨水难溶 不易溶 能(可)溶 易溶 极易溶 H 2、CON 2<O 2CO 2 1:1Cl 2 1:2 H 2S 1:2.6SO 2 1:40HCl 1:500 NH 3 1:700【喷泉实验】视频现象:气体体积迅速减小,烧杯里的酚酞溶液由玻璃管喷入烧瓶,形成红色喷泉 结论:① 氨气极易溶于水 ② 氨水溶液呈碱性原理:气体能被胶头滴管中挤出的少量液体快速吸收,使烧瓶内气体压强远远低于外界大气压关键:① 烧瓶、预先吸液的滴管、长直玻璃管外部都要干燥 ② 气体要充满圆底烧瓶③ 装置气密性好,不漏气,止水夹要夹紧 烧瓶中气体 Cl 2 CO 2 H 2S NO 2+NO HCl 滴管中液体浓NaOH浓NaOH浓NaOH浓NaOHH 2O4、易液化,成无色液体,放出大量的热(常温冷却到-33.5℃、常温加压到700-800kPa ) (易液化的气体还有:Cl 2、SO 2、HF )液氨气化时要吸收大量热,能使周围温度剧降——制冷剂三、化学性质: 1、与水反应:NH 3 + H 2O NH 3·H 2O NH 4+ + OH -化学平衡 电离平衡【氨水中有6种微粒,3分3离】NH 3、H 2O 、NH 3·H 2ONH 4+、OH -、H +(极少量)【氨水与液氨的区别】液氨是纯净物,只有NH 3分子氨水是混合物,含6种微粒【氨水的性质】弱碱性:氨气本身不显碱性弱电解质溶液:电解质是NH 3·H 2O不稳定性:O H NH O H NH 2323+↑−→−⋅△刺激性气味:游离的氨分子挥发性:NH 3易挥发(浓氨水瓶口有白雾) 保存:密封、阴暗处密度小于纯水,越浓密度越小(28%,密度=0.91g/cm 3) 同酒精 计算氨水的浓度,以NH 3计算沉淀性:很好的沉淀剂,制取Al(OH)3、Fe(OH)3弱还原性:O H 8N Cl NH 6O H NH 8Cl 3224232++−→−⋅+ 离子方程式书写:① 反应物, 写化学式② 生成物:浓溶液+加热——NH 3↑+H 2O 稀溶液+不加热——化学式 2、与酸反应:视频Cl NH HCl NH 43−→−+ 白烟(挥发出的氨跟氯化氢化合生成的微小的氯化铵晶体)3433NO NH HNO NH −→−+ 硝铵 白烟424423S O NH S O H 2NH )(−→−+ 硫胺 无白烟 34223HCO NH O H CO NH −→−++ 碳铵 无白烟【注】NH 3与挥发性酸反应生成铵盐,有白烟 【氨跟强酸溶液反应的本质】++−→−+43NH H NH3、与氧气反应:(最低价,具有还原性)(Pt 、Cr 2O 3)Q O H 6NO 4O 5NH 4223++→+催化剂△ 氨的催化氧化(接触氧化),工业制硝酸的基础【现象】 ① 虽然停止加热,催化剂仍能保持红热② 圆底烧瓶内出现红棕色气体 22NO 2O NO 2−→−+ ③ 紫色石蕊溶液变红 NO HNO 2O H NO 3322+−→−+ ④ 烧瓶内有时会看到白色烟雾 3433NO NH HNO NH −→−+ ⑤ 圆底烧瓶内红棕色不明显 322HNO 4O H 2O 3NO 4−→−++4、与其他氧化剂反应:Cl NH 6N NH 8Cl 34232+−→−+ 氨气过量 ——工厂检验氯气 HCl 6N NH 2Cl 3232+−→−+ 氯气过量O H 3N Cu 3NH 2CuO 3223++−→−+△H 2O 2、KMnO 4 均可氧化NH 3四、制法1、自然界:动植物体内的蛋白质腐败产生2、工业制法: 原理: N 2 + 3H 2 2NH 3 【注】可逆反应,得到的产品是3者的混合物,利用NH 3易液化的特点将其分离后,N 2和H 2可循环使用N 2:蒸馏液态空气H 2:焦炭与高温水蒸气反应 22H CO O H C +−−→−+高温222H CO O H CO +−−→−+高温3、实验室制法:、1) 固态铵盐与固体强碱加热【原料】常用消石灰,不用烧碱:① 在加热条件下烧碱对玻璃的腐蚀作用更强,试管易碎裂 ② 烧碱价格昂贵【原理】 O H 2NH 2CaCl OH Ca Cl NH 223224+↑+−→−+△)( 强碱制弱碱【装置】固固加热,同O 2【干燥】碱石灰——干燥管、U 型管(不能用浓硫酸、无水氯化钙 CaCl 2·8NH 3)【收集】只能用向下排空气(集气试管口棉花作用:防止气体对流,有利于集满) 【检验】① 湿润的红色石蕊试纸,变蓝高温高压 催化剂② 把气体通入酚酞试液,试液变红氨气是中学化学唯一的碱性气体③ 蘸有浓盐酸的玻璃棒,白烟【验满】① 湿润的红色石蕊试纸放在集气瓶口,变蓝 ② 蘸有浓盐酸的玻璃棒接近瓶口,白烟 【尾气】用水浸湿的棉花团2)在生石灰(或固体烧碱)中加入浓氨水生石灰(或固体烧碱)遇到浓氨水放出大量热,使一水合氨分解。
