(完整版)有机答案汇总(1)(1)
- 格式:doc
- 大小:3.07 MB
- 文档页数:67

有机化学课后习题参考答案完整版⽬录第⼀章绪论 0第⼆章饱和烃 (1)第三章不饱和烃 (5)第四章环烃 (13)第五章旋光异构 (23)第六章卤代烃 (28)第七章波谱法在有机化学中的应⽤ (33)第⼋章醇酚醚 (43)第九章醛、酮、醌 (52)第⼗章羧酸及其衍⽣物 (63)第⼗⼀章取代酸 (71)第⼗⼆章含氮化合物 (78)第⼗三章含硫和含磷有机化合物 (86)第⼗四章碳⽔化合物 (89)第⼗五章氨基酸、多肽与蛋⽩质 (100)第⼗六章类脂化合物 (105)第⼗七章杂环化合物 (114)Fulin 湛师第⼀章绪论1.1扼要归纳典型的以离⼦键形成的化合物与以共价键形成的化合物的物理性质。
答案:1.2 NaCl 与KBr 各1mol 溶于⽔中所得的溶液与NaBr 及KCl 各1mol 溶于⽔中所得溶液是否相同?如将CH 4及CCl 4各1mol 混在⼀起,与CHCl 3及CH 3Cl 各1mol 的混合物是否相同?为什么?答案:NaCl 与KBr 各1mol 与NaBr 及KCl 各1mol 溶于⽔中所得溶液相同。
因为两者溶液中均为Na +,K +,Br -, Cl -离⼦各1mol 。
由于CH 4与CCl 4及CHCl 3与CH 3Cl 在⽔中是以分⼦状态存在,所以是两组不同的混合物。
1.3碳原⼦核外及氢原⼦核外各有⼏个电⼦?它们是怎样分布的?画出它们的轨道形状。
当四个氢原⼦与⼀个碳原⼦结合成甲烷(CH 4)时,碳原⼦核外有⼏个电⼦是⽤来与氢成键的?画出它们的轨道形状及甲烷分⼦的形状。
答案:C+624H CCH 4中C 中有4个电⼦与氢成键为SP 3杂化轨道,正四⾯体结构CH 4SP 3杂化2p y2p z2p x2sH1.4写出下列化合物的Lewis 电⼦式。
a.C 2H 4b.CH 3Clc.NH 3d.H 2Se.HNO 3f.HCHOg.H 3PO 4h.C 2H 6i.C 2H 2j.H 2SO 4 答案:a.C C H H H HCC HH HH 或b.H C H c.H N Hd.H S H e.H O NOf.OC H Hg.O P O O H H Hh.H C C HHH H HO P O O H HH或i.H C C Hj.O S O HH OS H H或1.5下列各化合物哪个有偶极矩?画出其⽅向。


第一章绪论(一)用简练的文字解释下列术语。
(1)有机化合物(2)键能(3)极性键(4)官能团(5)实验式(6)构造式(7)均裂(8)异裂(9)sp2杂化(10)诱导效应(11)氢键(12)Lewis酸【解答】(1)有机化合物—碳氢化合物及其衍生物。
(2)键能—形成共价键的过程中体系释放出的能量,或共价键断裂过程中体系所吸收的能量。
(3)极性键—由不相原子形成的键,由于成键原子的电负性不同,其吸引电子的能力不同,使电负性较强原子的一端电子云密度较大,具有部分负电荷,而另一端则电子云密度较小,具有部分正电荷,这种键具有极性,称为极性键。
云对称地分布在两个成键原子之间,这种键没有极性,称为极性键。
(4)官能团—分子中比较活泼而容易发生反应的原子或基团,它常常决定着化合物的主要性质,反映化合物的主要特征。
(5)实验式—表示组成物质的元素原子最简整数比的化学式。
(6)构造式—表示分子构造的化学式。
(7)均裂—成键的一对电子平均分给两个成键原子或基团,这种断裂称均裂。
(8)异裂—成键的一对电子完全为成键原子中的一个原子或基团所占有,形成正、负离子,这种断裂称异裂。
(9)sp2杂化—2s轨道和两个2p轨道杂化。
(10)诱导效应—由于分子内成键原子的电负性不同,而引起分子中电子云密度分布不平均,且这种影响沿分子链静电诱导地传递下去,这种分子内原子间相互影响的电子效应,称为诱导效应。
(11)氢键—当氢原子与电负性很强且原子半径较小的原子(如N,O,F等原子)相连时,电子云偏向电负性较大的原子,使氢原子变成近乎氢正离子状态,此时若与另一个电负性很强的原子相遇,则发生静电吸引作用,使氢原子在两个电负性很强的原子之间形成桥梁,这样形成的键,称为氢键。
(12)Lewis酸—能够接受未共用电子对的分子或离子。
(二)下列化合物的化学键如果都为共价键,而且外层价电子都达到稳定的电子层结构,同时原子之间可以共用一对以上的电子,试写出化合物可能的Lewis结构式。
药学专业有机化学综合练习题参考答案一.命名下列化合物,若为立体结构式需标明构型。
1.CH 3CH 2CHCH 2CHCH 3CH 3CH 32. (CH 3)2CHCH 2CHCHCH 2CH 32CH 3CH 33.CH 3CHCH 2CHCH 2CH 2CH 332CH 32,4-二甲基己烷2,5-二甲基-4-乙基庚烷 2-甲基-4-乙基庚烷4.CH 3CHCH 2CH 2CHCH 2CH 333CH 3 5.Cl2CH 36.BrCH 3CH 22,6-二甲基-3-乙基庚烷 (1R,3R)-1-乙基-3-氯环己烷顺-1-乙基-4-溴环己烷7.H 3CCH 38. 9.10.Br3,6-二甲基二环[3.2.2]壬烷 1,3,8-三甲基螺[]癸烷 5-氯螺[]辛烷 2-溴二环[4.3.0]壬烷C CCOOHCH 3H CH 3CH 2.CH 3CH 2CH 2CHCHC CCH 33CH 2CH 313. CH 3CH=CHC CH 14. CH=CH 2CH 3C CE-2-甲基-2-戊烯酸 4-甲基-5-乙基-2-辛炔 3-戊烯-1-炔1-戊烯-3-炔15.CHCH 2CHCH 3CH 2 16.C C2HH 3CHCH 3CH 32CH 3OH H .HSCH 2CH 2OH4-戊烯-2-醇(2R,4E)-4-己烯-2-醇 (S)-2-丁醇2-巯基乙醇19.SO 3HCH 320.OHOH21. OH22.OH223.SO 3H22-甲基苯磺酸 间苯二酚 2-萘酚 5-硝基-2-萘酚 5-硝基-2-萘磺酸24.CH 3CH 2OCH=CH 225.CH 3CHO26.CO 2HOH27.CH 3CH 2CCH 2CH(CH 3)2O乙基乙烯基醚 对甲基苯甲醛 3-羟基苯甲酸 5-甲基-3-己酮28.CH 3CH 2CHCH 2COCl329. HOH CO 2H 330.COOCH 2CH 33-甲基戊酰氯D-乳酸(R-2-羟基丙酸) 苯甲酸乙酯31. CH 3CH 22COOCH 3O32. HCON(CH 3)2 33.CH 3CH 2CONHCH 3 34.N(CH 3)23-戊酮酸甲酯 N,N-二甲基甲酰胺 N-甲基丙酰胺 N,N-二甲基苯胺35.NCOOH36. NN F. 37.OCHO38.NCH 339.COOHH H 2N2SHβ-吡啶甲酸 5-氟嘧啶 2-呋喃甲醛 3-甲基吡啶 L-半光氨酸二.根据名称写出其结构式1. 螺[]辛烷2. 2,7,7-三甲基二环[2.2.1]庚烷3. 双环[3.2.1]辛烷4. 2,3-二甲基,4-己二烯5. Z-3-甲基-2-氯-2-戊烯6. (Z)-3-乙基-2-己烯7. 1,6-二甲基环己烯8. 乙基9. 乙烯基CC Cl CH 3CH 3CH 2H 3CCH 3C CHCH 2CH 2CH 2CH 2CH 3CH 3CH 3CH 3CH 2-CH 2=CH10. 异丁基11.异戊基12.苄基 13. 苯基 14.烯丙基15. 叔丁醇 16. (2R,3R)-1,2,3-三氯丁烷 17. (2R,3R)-,2,3-二氯-1-丁醇 18. 反-2-甲基-2-丁烯醇19. 4,5-二甲基-2-乙基-1,3-己二醇 20. 甲异丙醚 21. 苯甲醚22. 3-戊烯醛23. 4-甲基-2-戊酮24. 苯乙酮25. 1-环己基-2-丁酮 26.2-甲基-1-苯基-1-丁酮27. R-乳酸 28. L-2-氨基丙酸 29. 丙二酸 30. 3-羟基戊二酸31. 顺-丁烯二酸酐32. 乙酸丙酸酐 33. 乙酸乙酯34. 3-甲基丁酸乙酯35. N-甲基苯甲酰胺36. 1,4-戊二胺37. N,N-二甲基苯胺 38. N-甲基-N-乙基环己胺 39. 溴化甲基三乙基铵40. 氢氧化三甲基异丙基铵 41. 2-呋喃甲醛 42. N-甲基-2-羟基咪唑 43. 5-乙基噻唑 44. 嘌呤三.写出下列反应的主要产物1. CH3CH CH2 + HBr CH3CHBrCH32.+ HBrCH3C CH23CH33CH3Br3.CH3+ HICH3CH2CHCH34.CH3+ HClCH3CH3CH2C3CH3Cl5+ HBrCH3Br6.+ HBrCH3Br7.CH2=CH-CH=CH2 + CH2=CH-CHOCHO8.O+O9.(CH 3)3CCH 2CH KMnO 4,H +3)3CCOOH10.CH33CH 3Cl11.C 2H 5+ Cl 2FeCl 3C 2H 5Cl+C 2H 5Cl12.CH 2CH 3NBSCHCH 313.CH 3NBSBrCH 2BrBr14.+ Br 2FeBr 3OOC OO Br +C OO Br15.+ Br 2NO 2CN3NO 2CN Br16.(CH 3)2CHCHCH 3Cl (CH3)2C CHCH 317.BrCH 3CH 2CHCH 3CH 3CH=CHCH 318.BrCH 3CH 2C CH 3CH 3CH 3CH=CCH 3319. CH3CH2CH2Br + NaOCH3 CH3CH2CH2OCH320.CH2Cl + (CH3)3CH2OC(CH3)321. (CH3)2CHCl + NaSH (CH3)2CHSH22.Br CH2NaOHBr CH2OH23.ClCH2CH CH2Cl HOCH2CH CH2Cl24.CH3CH2CHCH2C6H CH3CH2CH CHC6H5 25.CH2CH2OH+ SOCl2CH2CH2Cl 26.OH+ SOCl2Cl+ SO2 + HCl27.CH3CHCHCH3+CH3CH2CCH33+28.CH3C+3CH3CH2CH3C+3CH2CH329.CH3OCH3 + HI CH3OH + CH3I30.+ HClC6H5CH CH2O3C6H5CH CH231.+ HOCH3OCH3CH3CH3CH3CH3CHOCH3332.CH3CH2CHO稀NaOH低温CH3CH2CH CHCHO333.O+ CH 3CH 2MgBr2HO CH 2CH 334.3+CH 3CCH 3+ CH 3Mg ICH 33CH 3 35.O +(C 6H 5)3P=CH 2DMSOCH 236.+ HCHO(CH 3)3C CHO NaOH(浓)+ HCOO -(CH 3)3CCH 2OH37.CHO +H 2N-NHO 2N NO 2N-NHO 2NNO 2CH=38.CH 3CH 2CH 2CHO + HOCH 2CH 2干HClCH 3CH 2CH 2CHO O39.HOCH 3OCH 3COONa + 2CHI 3I 2 +NaOH40.C 6H 5COCH 2CH 2CH 3C 6H 5CH 2CH 2CH 2CH 341.CH 3CH 2CH 2COOH + Cl PCH 3CH 2CHCOOH42.CH 3CH 2CCH 2COOHOCH 3CH 2CCH 3 + CO 2O43.CH 3CH 2CHCH 2CH 3CH 2CH CHCOOH44.COOHOH(CH 3CO)2O+COOHOOCCH 345.COOHOH+ NaHCO 3COONa OH46. 180o CCOOHCOOHO OO47.NaOH+C Cl ONH C NO 48.COONa + CH 3CH 2Cl COOCH 2CH 349.OOO+ CH 3OH回流HOOCCH 2CH 2COOCH 350.2(1)NaOC H 2 CH 3CO 2C 2H 5CH 322CH 3O O51.Br CH 3(CH 2)4C NH 2OCH 3CH 2CH 2CH 2CH 2NH 252.CH 2CH 2CONH 2+ Br 2CH 2CH 2NH253.O + NH 3OCH 2CH 2CH 2CONH 254.CH 3NHCH 3CH 3N (CH 3CO)2OCH 3COCH 355.+ HN(CH 2CH 3)2CH 3SO 2Cl CH 3SO 2N(CH 2CH 3)256.NH 2+ NaNO 2+ HCl0~5℃N 2+Cl57.CH 3N +(CH 3)3OHCH 258.N H32-32N HNO 259.+N SO 3N SO 3-+60. OCHO + NaOH (浓)OCH 2OH +OCO 2-四、选择题1.下列结构中所有碳原子均在一条直线上的是 【 C 】 A .CH 2=CHCH 2Cl B .CH 3CH=CH 2 C .CH 2=C=CH 2 D . CH 2=CH-CH=CH 2 2.下列结构中,所有原子共平面的是:【 A 】A .CH CH 2B . CH 3C .CH 2OHD .OCH 33. 分子中所有碳原子均为sp 3杂化【 D 】A. C 6H 5CH=CH 2B. (CH 3)2C=CH 2C. HC ≡CCH=CH 2D. CH 3CHClCH 3 4.下列结构中,碳原子都是sp 2杂化的是:【 D 】 A .CH 2CH CH 3 B .CH 2C CH 2C .CH 2CH C CHD .CH 2CH CH 2+5. 分子中所有碳原子均为sp 2杂化 【 D 】A. HC ≡CCH=CH 2 C. (CH 3)2C=CH 2 D. CH 2=CHCH=CHCl 6. 具有最长碳碳键长的分子是【 A 】A.乙烷 B. 乙烯 C. 乙炔 D. 苯7.顺反异构与对映异构可共存的结构是【 B 】A.B.C.CH3CH3D.CH3CH=CHCH(CH3)28. 不存在顺反异构的化合物是【 C 】9. 存在对映异构的是【 B 】10. 存在 p-π共轭体系的分子是【 D 】A. 1,3-环己二烯B. 苯甲醛C. Cl-CH2CH=CH2D. Cl-CH=CH211. 立体异构不包括【 D 】A. 构象异构B. 对映异构C. 顺反异构D. 互变异构12. 具有芳香性的化合物是【 B 】13. 不具有芳香性的化合物是【 A 】14. 最稳定的正碳离子是【 A 】15.下列正碳离子最稳定的是CH3CH CHCHCH3【 C 】A .C 6H 5CH 2+B .(CH 3)3C +C .C 6H 5C +(CH 3)2D .CH 3+16. 最稳定的游离基是【 A 】17. 分子中同时含有1°, 2°, 3°和 4°碳原子的化合物是 【 B 】A. 2, 2, 3-三甲基丁烷B. 2, 2, 3-三甲基戊烷C. 2, 3, 4-三甲基戊烷D. 3, 3-二甲基戊烷18. 薄荷醇的构造式为OH,其可能的旋光异构体数目是【 D 】A. 2个B. 4个C. 6个D. 8个 19.吲哚的结构式是:【 C 】A .NHB .C .N HD .N20.既是叔胺又是芳香胺的是【 D 】A .叔丁胺B . N-甲基对甲苯胺C .3-甲基苯胺D .N,N-二甲基苯胺 21.以C 2-C 3分析正丁烷的优势构象是【 C 】 A .完全重叠式 B .部分重叠式 C .对位交叉式 D .邻位交叉式 .下列基团属于间位定位基的是:【 B 】 A .甲基 B .羧基 C .乙酰氨基 D .甲氧基 23.下列基团属邻.对位定位基的是:【 B 】 A .-CNB .-BrC .-COOHD .-NO 2 24. 属于邻对位定位基的是【 C 】A. -CHOB. -SO 3HC. -CH=CH 2D. -CN 25. 在亲电反应中能钝化苯环的基团是【 B 】 A. —OH B. —NO 2 C. —OCH 3 D. —NH 326.卤代烃的消除反应一般遵循:【 D 】A .马氏规则B .休克尔规则C .霍夫曼规D .查依采夫规则丁醇和S-2-丁醇性质不同的是: 【 D 】 A .水溶性B .熔点C .沸点D .比旋光度 28. 水溶性最小的化合物是【 C 】29. 熔点最高的化合物是【 D 】A. 2-甲基丙烷B. 戊烷C. 异戊烷D. 新戊烷30.下列化合物与金属钠反应放出氢气速度最快的是: 【 A 】 A .甲醇B .乙醇C .异丙醇D .叔丁醇31.能与氯化亚铜的氨溶液反应产生红色沉淀的是:【 B 】A .CH 3CH 2CH 2CHOB .CH 3CH 2C CH C .CH 3CH 2C CCH 3D .CH 3CH 2CH CH 232. 最易发生消去HX 反应的是【 C 】A. 2-甲基-3-溴丁烷B. 3-甲基-1-溴丁烷C. 2-甲基-2-溴丁烷D.1-溴丁烷 33.下列化合物不与FeCl 3显色的有【 D 】A .苯酚B .邻甲基苯酚C .2,4-戊二酮D .苯甲醚 34.下列化合物最难发生水解反应的是【 B 】 A .CH 3COOC 2H 5 B .CH 3CONH 2 C .CH 3COCl D .(CH 3CO)2O 35.下列化合物不能发生碘仿反应的有【 D 】 A .乙醇B .乙醛C .苯乙酮D .正丁醇 36.不能发生碘仿反应的是【 A 】37. 能发生碘仿反应的是 【 B 】 38.下列化合物不能与HCN 加成的是【 C 】 A .正壬醛 B .丁酮C .苯乙酮D .环己酮39.下列物质与氢氰酸能发生加成反应又能发生碘仿反应的是:【 C 】40. A .O HB .OCH 341.C .CH 3OD .CH 3CH 22CH 3O40. 下列化合物可发生Cannizzaro 反应的是:【 B 】 A .乙醛B .苯甲醛C .丙醛D .丙酮41.下列试剂中能发生Cannizzaro歧化反应的是【 B 】 A .甲醇 B .甲醛 C .甲酸D .甲胺42.能与丙酮反应的是:【 D 】A .托伦试剂B .斐林试剂C|.班乃德试剂D .格氏试剂 43. 最易与硝酸银作用生成白色沉淀的化合物是【 A 】44. 下列羧酸衍生物发生亲核取代反应速度最快的是 【 C 】 A .CH 3CONH 2B .(CH 3CO)2OC .CH 3COClD .CH 3COOC 2H 545.下列化合物中可发生克莱森酯缩合反应的是: 【 A 】 A .乙酸乙酯B .甲酸甲酯C .苯甲酸乙酯D .苯酚46. 最容易发生脱羧反应的是【 A 】 A .β-丁酮酸B .β-羟基丁酸C .α-羟基丁酸D .α-丁酮酸47.CH 3CH=CHCH 2CH=CHCH 3经酸性KMnO 4氧化后的产物是 【 A 】 A .CH 3COOH + HOOCCH 2COOHB .CO 2 + OHCCH 2CHOC .HCOOH + OHCCH 2CHOD .HCOOH + HOOCCH 2COOH 48.能发生缩二脲反应的是:【 D 】 A .丙氨酸B .乙酰苯胺C .尿素D .多肽49.. 能与重氮盐发生偶联反应的是【 B 】50. 室温下能与HNO 2 作用放出N 2 的是【 B 】 A. (CH 3)3N B. H 2NCONH 2 C. C 6H 5NHCH 3 D. HCON(CH 3)251.吡咯环碳上的硝化属于【 C 】 A .亲核取代B .亲核加成C .亲电取代D .亲电加成 52. 醛与醇加成生成半缩醛的反应属于 【 A 】A. 亲核加成B. 亲电加成C. 亲核取代D. 亲电取代 53.乙醛与乙醇在干燥HCl条件下的反应属于【 B 】 A .醇醛缩合反应B .亲核加成反应C .Cannizarro 反应D.Diels-Alder反应54. 在光照下,甲苯与氯气反应生成氯化苄,这一反应的机理是:【 D 】A.亲电加成B.亲核取代C.亲电取代D.自由基取代55.亚硫酸氢钠与醛反应生成结晶性沉淀的反应机理是:【 C 】A.亲核取代B.亲电取代 C.亲核加成D.亲电加成1反应特征的是56.下列叙述不属于SN【 C 】A.有重排产物生成B.产物外消旋化C.反应一步完成D.反应分步进行2 反应的是57. 最易发生 SN【 A 】A. 溴乙烷B. 溴苯C.溴乙烯D. 2-溴丁烷1 反应的是【 D 】58. 最易发生 SNA. 溴甲烷B. 溴乙烷C. 3-溴-2-甲基丁烷D. 2-溴-2-甲基丁烷2 反应特征的是59. 下列说法中,属于 SN【 B 】A. 有正碳离子中间体生成B. 中心碳的构型完全发生转化C. 得到外消旋化产物D. 反应活性 3°RX > 2°RX > 1°RX > CHX360. 反应 CH 2=CHCH 3 + HCl → CH 3CHClCH 3 属于【 C 】A. 亲核加成B. 亲电取代C. 亲电加成D. 自由基取代 61. 属于亲电试剂的是【 A 】A. HNO 3B. HCNC. NaHSO 3D. H 2N -NH 2 62. 属于亲核试剂的是【 B 】 A. Br 2B. NaHSO 3C. H 2SO 4D. HBr 63. 在亲电反应中能活化苯环的基团是【 C 】 A. —CO 2HB. —SO 3HC. —OCH 3D. —NO 2 64. 亲核取代反应活性最高的是【 A 】 A. CH 3COCl B. (CH 3CO)2O C. CH 3CO 2CH 3 D. CH 3CONH 2 65.亲电取代反应速度比苯快的是:【 A 】 A .吡咯B .吡啶C .硝基苯D .喹啉 66. 亲电取代反应活性最高的是【 B 】A. 苯B. 吡咯C. 吡啶D.嘧啶 67. 与甲醇发生酯化反应速率最大的是【 A 】A. 乙酸B. 丙酸C. 2-甲基丙酸D. 2,2-二甲基丙酸68. 与乙酸发生酯化反应的速率最大的是【 A 】 A. 甲醇B. 乙醇C. 丙醇D. 丁醇69.化合物:a 乙醇.b 乙酸.c 苯酚.d 碳酸,其酸性由强到弱排列是 【 B 】 A .abcdB .bdcaC .bcadD .bcda70. 酸性最强的是【 D 】A .苯酚B. 3-硝基苯酚C. 4-硝基苯酚D. 2,4-二硝基苯酚 71. 酸性最强的是【 B 】 72.下列化合物碱性最强的是【 A 】 A .二甲胺 B .NH 3 C .苯胺 D .吡咯73 碱性最强的是【 C 】A. CH 3CONH 2B. C 6H 5NH 2C. (CH 3)2NHD. NH 3 74. 碱性最弱的是【 A 】 75.可用作重金属解毒剂的是【 C 】 A .乙醚B .乙硫醇C .二巯基丙醇D .二氯亚砜76.下列试剂中能区别苯甲醛和苯乙酮的是 【 D 】 A .FeCl 3溶液 B .Grignard 试剂C .Fehling试剂D .Tollens 试剂77.能溶于NaOH 溶液,通入CO 2后又析出来的化合物是 【 B 】 A .环己醇B .苯酚C .苯胺D .苯甲酸78.下列试剂中,可把苯胺与N-甲基苯胺定性区别开来的是 【 B 】 A .5%HCl 水溶液B .先用C 6H 5SO 2Cl 再用NaOHC .AgNO 3 + NH 3·H 2OD .Cu 2Cl 2 + NH 3·H 2O 79. 区别甲苯与氯苯最好采用【 C 】A. Br 2/CCl 4B. AgNO 3C. KMnO 4D. 浓H 2SO 4五、判断题。
【最新整理,下载后即可编辑】1.(17分)“张-烯炔环异构反应”被《Name Reactions》收录。
该反应可高效构筑五元环化合物:(R、R‘、R“表示氢、烷基或芳基)合成五元环有机化合物J的路线如下:已知:(1)A属于炔烃,其结构简式是。
(2)B由碳、氢、氧三种元素组成,相对分子质量是30。
B 的结构简式是(3)C、D含有与B相同的官能团,C是芳香族化合物,E 中含有的官能团是(4)F与试剂a反应生成G的化学方程式是;试剂b是。
(5)M和N均为不饱和醇。
M的结构简式是(6)N为顺式结构,写出N和H生成I(顺式结构)的化学方程式:。
2.〔化学—选修5:有机化学基础〕(15分)席夫碱类化合物G在催化、药物、新材料等方面有广泛应用。
合成G的一种路线如下:已知以下信息:①②一摩尔B经上述反应可生居二摩尔C,且C不能发生银镜反应。
③D属于单取代芳烃,其相对分子质量为106。
④核磁共振氢谱显示F苯环上有两种化学环境的⑤回答下列问题:(1)由A生成B的化学方程式为,反应类型为(2)D的化学名称是,由D生成E的化学方程式为:(3)G的结构简式为(4)F的同分异构体中含有苯环的还有____种(不考虑立体异构)。
其中核磁共振氢谱中有4组峰,且面积比为6:2:2:1的是_______。
(写出其中的一种的结构简式)。
(5)由苯和化合物C经如下步骤可合成N-异丙基苯胺。
反应条件1所选择的试剂为____________;反应条件2所选择的试剂为________;I的结构简式为_____________。
3.[化学选修——5:有机化学基础](15分)立方烷()具有高度的对称性.高致密性.高张力能及高稳定性等特点,因此合成立方烷及其衍生物成为化学界关注的热点。
下面是立方烷衍生物I的一种合成路线:回答下列问题:C 的结构简式为 ,E 的结构简式为 。
③的反应类型为 ,⑤的反应类型为化合物A 可由环戊烷经三步反应合成:反应1的试剂与条件为 ;反应2的化学方程式为 ;反应3可用的试剂为 。

1.有机物分子结构如图,其分子肯定可以共平面的碳原子有()
A.6个B.7个C.8个D.9个
2.下列分子中所有原子不可能共平面的是()
A .
B .
C .
D .
3.已知的所有原子共平面,对于OHC-CH=CH-C≡C-CH2CH2OH在同一平面上的原子最多有几个()
A.12个B.11个 C.13个 D.10个
4.已知甲醛的所有原子共平面,对于OHC-CH=CH-C≡C-CH2CH3在同一平面上的原子最多有几个 ( )
A.9个B.11个 C.13个D.15个
下列对于苯乙烯的叙述中:①能使KMnO4酸性溶液褪色;②可发生加聚反应;
③可溶于水;④所有的原子可能共平面.其中正确的是()
A.①②③B.②③④C.①②④D.全部正确
某有机物的分子结构如下表示:CH3-C≡C-CH=CH- -CH3,该分子中最多可以有多少个原子共平面()
A.18 B.20C.22 D.24
下列分子种的碳原子不可能同在一个平面的是()
A .B.C .D .
在分子中,处于同一平面上的原子数最多可能是()
A.15个 B.16个C.17个 D.18个
下列分子中的碳原子不可能处在同一平面上的是()
A .
B .
C .
D .。

有机化学综合练习一答案1—5: ABBBA, 6—10 :D DB CC 11—14 : BDBD 15、 答案:(1)醛基 (酚)羟基 醚键 (2)(a )取代反应 (b )CHCOOH CH 2OH(3)CH 3O --CHO CH 3O --COOHCH 3O --COOCH 3解析:(1)由题给乙基香草醛的结构简式可知其结构中含有氧原子的官能团有醛基、(酚)羟基、醚基。
(酚)羟基、醚基。
(2)由题给提示②可知,与苯环直接相连的碳原子上有氢原子时,此碳原子可以被酸性高锰酸钾溶液氧化成羧基,再结合题给转化关系:A 生成苯甲酸可知A 中苯环上只有一个支链;由提示①和转化关系A→B ,可知A 中有“—“—CHCH 2OH”,A 是有机酸,则可知其结构中有羧基,结合其分子式可以确定A 的结构简式是:CHCOOHCH 2OH ,由转化关系A→C 和A 、C 分子的差别可知:A 生成C 的过程中,其碳碳键没有变化,只是—OH 被Br 代替,则A→C 的反应类型是取代反应。
的反应类型是取代反应。
(3)比较茴香醛(CH 3O --CHO )和D (CH 3O --COOCH 3)的结构差别可知:茴香醛中的醛基(—CHO )经过一系列反应后转化成了—COOCH 3,茴香醛可以被酸性高锰酸钾氧化成羧酸,羧酸继续与甲醇发生酯化反应即可得到D ,由题给示例可知茴香醛合成D 的反应流程图是:的反应流程图是: CH 3O --CHO CH 3O --COOHCH 3O --COOCH 3。
16、答案:、答案:(1)(2)是)是(3)H 3C -C =C -CH 3CH 3 CH 3H 3C -C —C -CH 3+2NaOH+2NaOH CH 3 CH 3Cl ClC 2H 5OH△H 2C==C —C==CH 2+2NaCl+2H 2OCH 3 CH 31,4—加成反应加成反应 取代反应取代反应解析:烃类化合物A 的相对分子质量为84,设其分子式为C x H y ,则x 的最大值为71284==x ,此时H 原子数y =0,显然不合理,所以x =6,y =12,即分子式C 6H 12,因分子中含有碳碳双键,且分子中只有一种类型的氢继12个氢原子完全相同,所以A 的结构简的结构简式为式为 ,根据双键的结构特点可知6个碳原子共平面。

目录第一章绪论 0第二章饱和烃 (1)第三章不饱和烃 (5)第四章环烃 (13)第五章旋光异构 (23)第六章卤代烃 (28)第七章波谱法在有机化学中的应用 (33)第八章醇酚醚 (43)第九章醛、酮、醌 (52)第十章羧酸及其衍生物 (63)第十一章取代酸 (71)第十二章含氮化合物 (77)第十三章含硫和含磷有机化合物 (85)第十四章碳水化合物 (88)第十五章氨基酸、多肽与蛋白质 (99)第十六章类脂化合物 (104)第十七章杂环化合物 (113)Fulin 湛师第一章 绪论1.1 扼要归纳典型的以离子键形成的化合物与以共价键形成的化合物的物理性质 答案:离子键化合物共价键化合物熔沸点 高低溶解度 溶于强极性溶剂溶于弱或非极性溶剂硬度高低1.2 NaCl 与 KBr 各 1mol 溶于水中所得的溶液与 NaBr 及 KCl 各 1mol 溶于水中所得溶液是否相同?如将CH 4及 CCl 4各 1mol 混在一起,与 CHCl 3及 CH 3Cl 各 1mol 的混合物是否相同?为什么? 答案:NaCl 与KBr 各1mol 与NaBr 及KCl 各1mol 溶于水中所得溶液相同。
因为两者溶液中均为 Na +,K +,Br -, Cl -离子各 1mol 。
由于 CH 4与 CCl 4 及 CHCl 3与 CH 3Cl 在水中是以分子状态存在,所以是两组不同的混合物。
1.3 碳原子核外及氢原子核外各有几个电子?它们是怎样分布的?画出它们的轨道形状。
当四个氢原子与CH 4)时,碳原子核外有几个电子是用来与氢成键的?画出它们的轨道形状及 甲烷分子的形状。
答案:答案:一个碳原子结合成甲烷 3为SP 3杂化轨道 ,正四面体1.4 写出下列化合物的 Lewis 电子式。
a.C 2H 4b.CH 3Clc.NHd.H 2Se.HNOf.HCHOg.H 3PO 4h.C 2 H 6i.C 2H 2j.H 2SO 4+62p2p HCH4 中C 中有 4个电子与氢成键CH 4Ha. H C C HHH H C C HHHb. HH C ClHe.OHONOf.OHCHg.OH O P O H 或OHc.H N HHOHOPOHOHd.h.HSHHHCHCi. HCCH j.O HOSOHO1.5 下列各化合物哪个有偶极矩?画出其方向。
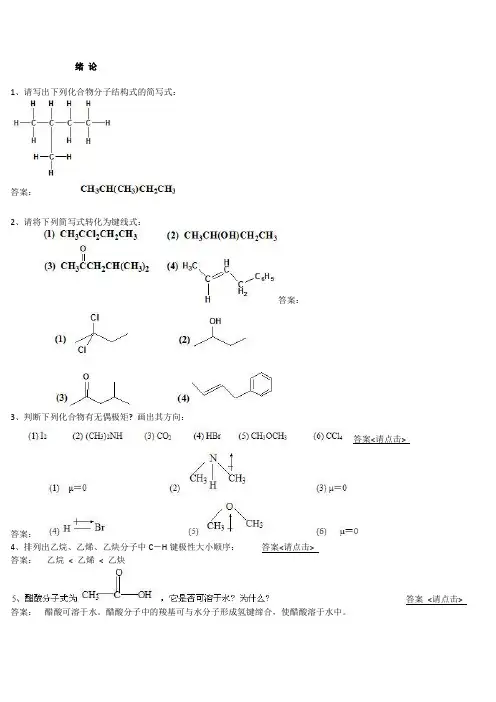
绪论1、请写出下列化合物分子结构式的简写式:答案:2、请将下列简写式转化为键线式:答案:3、判断下列化合物有无偶极矩? 画出其方向:答案<请点击>答案:4、排列出乙烷、乙烯、乙炔分子中C-H键极性大小顺序:答案<请点击>答案:乙烷< 乙烯< 乙炔答案<请点击> 答案:醋酸可溶于水。
醋酸分子中的羧基可与水分子形成氢键缔合,使醋酸溶于水中。
烷烃1、命名或写出下列化合物的结构式:答案:2、回答下列问题:(1)2,2-二甲基丁烷的一氯代主要产物是(2).一分子量为72的烷烃进行氯代时,只得一种氯代产物,其结构为(3).写出1,2-二溴乙烷Newman投影式的优势构象。
(4).将下面化合物按其沸点由高到低的顺序排列A、辛烷B、3-甲基庚烷C、2,3-二甲基戊烷D、2-甲基己烷(5). 下列自由基中最稳定的是A、B、C、D、答案<请点击>答案:3、用不同符号表示下列化合物中伯、仲、叔、季碳原子答案<请点击> 答案:4、某烷烃相对分子质量为72,氯化时(1)只得一种一氯化产物,(2)得三种一氯化产物,(3)得四种一氯化产物,分别写出这些烷烃的构造式。
答案<请点击> 答案:烯烃、炔烃及共轭二烯烃1、命名或写出下列化合物的结构式:答案:(1) 4-甲基-2-己炔(2) 4-异丙基环己烯(3) 1-丁烯-3-炔(4) 反-3,4-二甲基环丁烯2、选择题:(1)下列化合物中碳氢键解离能最小的是:(2)下列碳正离子中最稳定的是:(3)下列烯烃在和溴水发生加成反应时,反应速度最快的是:(4)下列烯烃最稳定的是(),最不稳定的是()A、2,3-二甲基-2-丁烯B、3-甲基-2-戊烯C、反-3-己烯D、顺-3-己烯(5)下列烯烃不具有顺、反异构体的是:(6)下列烯烃氢化热(KJ/mol)最低的是:答案:3、完成下列反应式:答案:4、用简单并有明显现象的化学方法鉴别下列各组化合物:正庚烷1,4-庚二烯1-庚炔答案<请点击> 答案:5、合成题:(1)以环己醇为原料合成:1,2,3-三溴环己烷(2)从异丙醇为原料合成:溴丙烷(3)由1-氯环戊烷为原料合成:顺-1,2-环戊二醇。
习题参考答案第九章 习题1.完成下列反应:(1)CHO (2)OOHOCH 3(3)H 2C ClOHCH 2MgCl(4)OCH 3(5)OCH 3OH(6)Me SNa3I(7)S O (8)S C 2H 5C 2H 5I2.用反应机理解释下列反应略4. 用指定的原料和必要的试剂合成:(1)(CH 3)3CClSOCl (CH 3)3COHMg Et 2O(CH 3)3TMO(2)CH 3COCH NaBH 4CH 33NaOEtCH 3CHCH ONaCH 3CH 2CH 2ITM(3)OHCH 3IOCH 3CH 3ClOCH 3CH 3AlCl AlCl ClO3TM(4)O2CH3CH2IO4TM(5)2CH3CH2ITM (6)NaOEt RCO3R'OH3PCCTM(7)Br2hvNaOEt RCO3R'O(8)O3Zn,H2O2TM(9)OH24RCO3R'OTM(10)H2C CH2Br2H2C CH2BrBr222224H2SO4,H2OOHBrROOR'BrH2PtBr MgEt2OMgBrOH H2PtTM第十章习题2.完成下列反应:(1)H 2SO 4PCCONa CH 3(2)OO OO CH 3(3)H 3CO H 3COH 3BrO O (4)OH O(5)C 3H 7COCl 34.由指定的原料和必要的有机或无机试剂合成下列化合物 (1)OH ClNaBH4OHClNaOEt 3TM(2)ClO 3OZn-Hg HClTM(3)OHNi,H 2OHPCCOHOOH OHOOMe PCC H 3O(4)CNH 3OOOHLiAlH 4PCCTM(5)AlCl 3OH TMO(6)OH 2PCCHO2NaOEtOH OHO LiAlH 4(7)ONaOHOHO HO KCN7试解释下列反应进行的机理。
(1)PhPhOPhPhOO MeOHPhPhOOHPhPhOOOMeOPhPhO(2)OH(3) OBrOK第十一章 习题3.完成下列反应:(1)D 2OH(2)H CPPh LiAlH 4Et 2O(3)O2Et ,O2H ,O(4)OO(5)OCNCOCl(6)LindlarHOOCOO4.由指定原料和必要的试剂合成下列化合物。
第一章绪论1-1 扼要解释下列术语.(1)有机化合物(2) 键能、键的离解能(3) 键长(4) 极性键(5) σ键(6)π键(7) 活性中间体(8) 亲电试剂(9) 亲核试剂(10)Lewis碱(11)溶剂化作用(12) 诱导效应(13)动力学控制反应(14) 热力学控制反应答:(1)有机化合物-碳氢化合物及其衍生物(2) 键能:由原子形成共价键所放出的能量,或共价键断裂成两个原子所吸收的能量称为键能。
键的离解能:共价键断裂成两个原子所吸收的能量称为键能。
以双原子分子AB为例,将1mol气态的AB拆开成气态的A和B原子所需的能量,叫做A—B键的离解能。
应注意的是,对于多原子分子,键能与键的离解能是不同的。
分子中多个同类型的键的离解能之平均值为键能E(kJ.mol-1)。
(3) 键长:形成共价键的两个原子核之间距离称为键长。
(4) 极性键: 两个不同原子组成的共价键,由于两原子的电负性不同, 成键电子云非对称地分布在两原子核周围,在电负性大的原子一端电子云密度较大,具有部分负电荷性质,另一端电子云密度较小具有部分正电荷性质,这种键具有极性,称为极性共价键。
(5) σ键:原子轨道沿着轨道的对称轴的方向互相交叠时产生σ分子轨道, 所形成的键叫σ键。
(6) π键:由原子轨道侧面交叠时而产生π分子轨道,所形成的键叫π键。
(7) 活性中间体:通常是指高活泼性的物质,在反应中只以一种”短寿命”的中间物种存在,很难分离出来,,如碳正离子, 碳负离子等。
(8) 亲电试剂:在反应过程中,如果试剂从有机化合物中与它反应的那个原子获得电子对并与之共有形成化学键,这种试剂叫亲电试剂。
(9) 亲核试剂:在反应过程中,如果试剂把电子对给予有机化合物与它反应的那个原子并与之共有形成化学键,这种试剂叫亲核试剂。
(10) Lewis碱:能提供电子对的物种称为Lewis碱。
(11)溶剂化作用:在溶液中,溶质被溶剂分子所包围的现象称为溶剂化作用。