乙烯烯烃二烯烃
- 格式:ppt
- 大小:929.50 KB
- 文档页数:23

第三节乙烯烯烃【知识讲解】一、乙烯的分子结构(与乙烷比较)乙烯乙烷分子式C2H4C2H6电子式结构式结构简式CH2=CH2CH3CH3C原子间键C=C(双键)C-C(单键)键角120°109°28'键长 1.33×10-10m 1.54×10-10m键能615KJ/mol(一个键易断)348KJ/mol 分子内各原子相对位置各原子均在同一平面不在一个平面加成反应不能能取代反应能较难二、乙烯的实验室制法1、试剂:乙醇(酒精)和浓硫酸按体积比1:3混合2、反应原理3、气体发生装置:的装置(与制Cl2相似)4、集气方法:排水集气法5、几个应该注意的问题① 浓硫酸的作用催化和脱水② 碎瓷片的作用防止液体剧烈跳动(防止煮沸)。
③ 反应温度应控制在170℃,若温度过低(140℃)将发生副反应,而生成乙醚;若温度过高,则乙醇易被浓H2SO4氧化。
为了控制温度,应将温度计的水银球插在液面下。
以准确测定反应液体的温度。
④ 反应后液体易变黑,且有刺激性气味气体产生。
这是由于浓硫酸的强氧化性将乙醇氧化生成C和CO2,且硫酸被还原成SO2所致。
其反应方程式可表示为:若要净化乙烯,可将其通过NaOH溶液除去SO2、CO2。
三、乙烯的性质通常情况下,乙烯是无色,稍有气味的气体,密度与空气相近,难溶于水。
乙烯化学性较活泼,易发生如下反应:1、加成反应:有机物分子里不饱和碳原子跟其它原子或原子团直接结合生成别的物质的反应。
① 与卤素加成:CH2=CH2+Br2→CH2Br-CH2Br(使溴水褪色,可用于检验乙烯或除去乙烯)② 与氢气加成:③ 与卤化氢HX加成:(可用于制氯乙烷)④ 与水加成:(可用于工业上制酒精)2、氧化反应① 燃烧:(火焰明亮有黑烟)② 可与强氧化剂反应:使酸性KMnO4溶液褪色(可用于检验乙烯)3、加聚反应:(可用于制聚乙烯塑料)加聚反应是指不饱和单体通过加成反应互相结合成高分子化合物的反应。





烯烃和二烯烃的化学性质Ⅰ 烯烃的化学性质烯烃主要化性示意图:一、加成反应1、催化加氢(亦即烯烃还原)R CH=CH R ’ + H 2 RCH 2CH 2R ’NiPt or意义:实验室制备纯烷烃;工业上粗汽油除杂;根据吸收氢气的量测定重键数目2、加卤素CH 2=CH 2 + Br 2 CH 2BrCH 2Br红棕无色应用:鉴别X 2反应活性:F 2>Cl 2>Br 2>I 2,常用Cl 2和Br 2 机理:极性条件下的分步的亲电加成①极性条件下Br 2发生极化Br -Br Br δ+——Br δ–②亲电进攻,形成中间体溴鎓离子Br CH 2CH 2+δ+CH 2CH 2δ+CH 2CH 2+Br –Br BrBr Br溴鎓离子③Br -背面进攻中间体得产物(反式加成,立体化学此处不需掌握,了解即可)Br CH 2CH 2+Br–BrCH 2CH 2Br3、加卤化氢CH 2=CH 2 + H Br3CH 2CH 2Br H历程:分步的亲电加成H + Br CH 2=CH 2 + H +HBr+ + Br -CH 3 —CH 2-+CH 3CH 2BrCH 3 —— CH 2+(碳正离子,有时会重排)HX 反应活性:HI>HBr>HCl**不对称烯烃与卤化氢加成产物符合马氏规律:氢加到含氢多的碳上。
**当有过氧化物存在、且只与HBr 加成时产物为反马氏:氢加到含氢少的碳上。
4、加水(直接水合)CH 3CH=CH 2 + H 2OH +CH 3CHCH 3OH(异丙醇)强酸催化,遵守马氏规律,产物为醇;副反应较多。
5、加浓硫酸(间接水合)CH 3CHCH 3 + H 2SO 4OSO 2OHCH 3CHCH 3OH 硫酸氢异丙酯异丙醇丙烯CH 3CH=CH 2相当于间接水合,遵守马氏规律,产物为醇(注意硫酸的结构表示:S OO OHHO )。
6、加次卤酸CH 3CH=CH 2 + X 2 + H 2O CH 3CHCH 2XOHδ-HO Xδ+产物卤代醇,遵守马氏规律(次卤酸极性:X —OH ,由于氧的电负性较大,所以X 带部分正电荷,OH 带部分负电荷)7、硼氢化反应甲硼烷以B —H 键与烯(炔)加成 有机硼化合物。

第三章烯烃和二烯烃第一节烯烃一、烯烃的同分异构现象烯烃的通式: CnH2n。
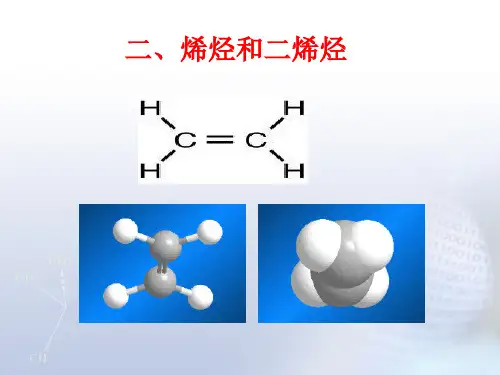
烯烃的官能团:C=C1.构造异构2.顺反异构(a)反-2-丁烯(b) 顺-2-丁烯二、烯烃的结构1.碳的sp2杂化及乙烯的结构碳原子的sp2杂化过程如下:每一个sp2杂化轨道含有1/3s成分和2/3p成分,其形状也是一头大,一头小的葫芦形。
三个sp2杂化轨道以平面三角形对称地排布在碳原子周围,它们的对称轴之间的夹角为120°,未参与杂化的2p轨道垂直于三个sp2杂化轨道组成的平面。
如图3-1所示。
(a)三个sp2杂化轨道(b) 三个sp2杂化轨道与一个p轨道图3-2碳原子的sp2杂化轨道乙烯分子形成时,两个碳原子各以一个sp2杂化轨道沿键轴方向重叠形成一个C—Cσ键,并以剩余的两个sp2杂化轨道分别与两个氢原子的1s轨道沿键轴方向重叠形成四个等同的C—Hσ键,五个σ键都在同一平面内,因此乙烯为平面构型。
此外,每个碳原子上还有一个未参与杂化的p轨道,两个碳原子的p轨道相互平行,于是侧面重叠成键。
这种成键原子的p轨道侧面重叠形成的共价键叫做π键。
乙烯分子中的σ键和π键如图3-2所示。
图3-2 乙烯分子的结构2.σ键和π键的比较σ键和π键的特点比较如下:其他烯烃的结构与乙烯相似,双键碳原子也是sp2杂化,与双键碳原子相连的各个原子在同一平面上,碳碳双键都是由一个σ键和一个π键组成的。
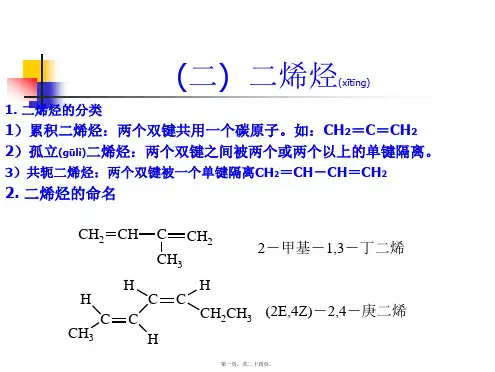
三、烯烃的命名1.构造异构体的命名烯烃分子去掉一个氢原子剩下的部分,叫做烯基;常见的烯基有:CH2=CH—CH3—CH=CH—CH2=CH—CH2—乙烯基丙烯基烯丙基(二)烯烃的命名(1)习惯命名法烯烃和二烯烃的个别化合物常采用习惯命名法命名。
例如:正丁烯异丁烯异戊二烯(2)系统命名法命名方法与烷烃基本相似,原则如下:①选择含有官能团的最长碳链作为母体,母体命名原则同直链烯化合物。
若有多条最长链可供选择时,选择原则与烷烃相同。
②靠近官能团一端编号,即使官能团的位次符合“最低系列”。


二烯烃的转化
二烯烃是一类具有两个双键的不饱和碳氢化合物,可以通过多种方法进行转化。
以下是一些常见的二烯烃转化反应:
1. 加成反应:二烯烃可以与其他化合物发生加成反应,形成新的化合物。
常见的加成反应包括:
- 氢化反应:二烯烃与氢气在合适的催化剂存在下反应,生成饱和烃。
- 水化反应:二烯烃与水反应,生成醇或醛。
- 卤素化反应:二烯烃与卤素反应,生成卤代烃。
- 硫化反应:二烯烃与硫化物反应,生成硫代烃。
2. 氧化反应:二烯烃可以与氧气或氧化剂反应,生成含氧化合物。
常见的氧化反应包括:
- 氧化反应:二烯烃与氧气反应,生成环氧化合物。
- 烯醇化反应:二烯烃与水和氧气反应,生成烯醇。
- 羟基化反应:二烯烃与羟胺或醇反应,生成烯醇。
3. 聚合反应:二烯烃可以进行聚合反应,将多个二烯烃分子连接在一起形成高分子化合物。
常见的聚合反应包括:
- 乙烯聚合:二烯烃乙烯与催化剂反应,生成聚乙烯。
- 丁二烯聚合:二烯烃丁二烯与催化剂反应,生成聚丁二烯。
二烯烃还可以通过其他反应进行转化,如重排反应、环化反应等,
具体转化方式取决于二烯烃的结构和反应条件。
烯烃知识点总结笔记一、烯烃的基本概念烯烃是一类含有碳碳双键结构的化合物,其中每个碳原子的四个化合价都得到了饱和。
烯烃可以按照双键的位置分为内烯烃和外烯烃两类。
在内烯烃中,双键结构位于分子的内部位置,而在外烯烃中,双键结构则位于分子的末端位置。
烯烃也可以按照双键的数量分为单烯烃、二烯烃和多烯烃等。
它们的通用结构式为CnH2n,其中n为烯烃分子中碳原子的个数。
二、烯烃的命名与结构1. 单烯烃单烯烃是指含有一个碳碳双键结构的烃类化合物,它的通用名称为“-ene”,例如乙烯、丙烯、丁烯等。
单烯烃的命名方法是根据碳原子数量及双键的位置进行命名,首先确定碳原子链的主链,并使双键的位置得到最佳编号,然后根据双键位置距离主链两端最近的碳原子的编号确定取代基的位置,并用多取代基使用逗号隔开,取代基按字母表次序进行排列。
2. 二烯烃二烯烃是指含有两个碳碳双键结构的烃类化合物,它的通用名称为“-diene”,例如丙二烯、戊二烯等。
二烯烃的命名方法和单烯烃相似,首先确定碳原子链的主链,并使双键的位置得到最佳编号,然后根据双键位置距离主链两端最近的碳原子的编号确定取代基的位置,并用多取代基使用逗号隔开,取代基按字母表次序进行排列。
3. 多烯烃多烯烃是指含有多个碳碳双键结构的烃类化合物,它的通用名称为“-diene”,例如戊二烯、己三烯等。
多烯烃的命名方法和单烯烃相似,首先确定碳原子链的主链,并使双键的位置得到最佳编号,然后根据双键位置距离主链两端最近的碳原子的编号确定取代基的位置,并用多取代基使用逗号隔开,取代基按字母表次序进行排列。
三、烯烃的物理性质1. 沸点和密度烯烃的沸点一般较低,它的分子量较小,分子间的作用力较弱,因此易于挥发和溶解。
烯烃的密度一般小于1,具有较好的浮于水的特性。
2. 反应活性烯烃中的双键具有较高的反应活性,它容易进行加成反应、氢化反应、氧化反应等。
双键的位置和数量决定了烯烃的反应性,通常含有多个双键的多烯烃比含有一个双键的单烯烃具有更高的反应活性。
第三节乙烯烯烃●教学目的:1、了解乙烯的物理性质和主要用途,掌握乙烯的化学性质和实验室制法。
2、使学生了解加成反应和聚合反应以及不饱和烃的概念。
3、使学生了解烯烃在组成、结构、主要化学性质上的共同点,以及物理性质随碳原子数的增加而变化的规律。
●教学重点:乙烯的化学性质。
●教学难点:乙烯的结构以及与化学性质的关系。
教学过程:[引入]何谓烷烃?其通式如何?它属于何类烃?(饱和链烃)与此相对应就应该有不饱和烃。
另外有机物之所以种类繁多,除了存在大量的同分异构现象,在有机物中碳原子除了可以形成C —C ,还可能形成或—C ≡C —,从而使得碳原子上的氢原子数少于饱和链烃里的氢原子数。
这样的烃叫做不饱和烃。
[板书]不饱和烃:烃分子里含有碳碳双键或碳碳三键,碳原子所结合的氢原子数少于饱和链烃里的氢原子数,这样的烃叫做不饱和烃。
[讲解] 根据烃分子中碳原子的连接方式不同,烃可以分为如下类别:饱和烃——烷烃链烃烯烃烃不饱和烃炔烃环烃[过渡]今天我们来学习最简单的烯烃——乙烯。
一、乙烯来源及用途 C C二、乙烯的分子组成和结构1、[设问]:(1)把乙烷C 2H 6中H 原子去掉两个就变成了乙烯C 2H 4,根据每个原子通过共用电子对达到饱和的原理,试推导C 2H 4中共价键是怎样组成的? 电子式:分子式:C 2H 4 最简式:CH 2 结构简式:CH 2=CH 2 结构式:(2)展示乙烯和乙烷的球棍模型,对比两者有何不同?2、[[设问](1)乙烯中C==C 双键可否认为是两个C —C 的加和?不能,因为C==C 键能小于C —C 单键键能的2倍,615<2×384=768 (2)通过键能大小来看,乙烯和乙烷哪个化学性质较活泼?C C H H H H乙烯为平面分子,键角为120°,“C==C”中有一个碳碳键等同于C—C,叫δ键,另一个碳碳键键能小于C—C,叫π键,π键稳定性较差。
因此乙烯的化学性质较为活泼,表现为“C==C”中有一个碳碳键易断裂........。