DNS法测定总糖和还原糖
- 格式:doc
- 大小:88.00 KB
- 文档页数:3

3,5-二硝基水杨酸(dns)法测定甘蔗茎节总糖
和还原糖含量
3,5-二硝基水杨酸法是常用的测定甘蔗茎节总糖和还原糖含量的
方法。
该方法操作简便、灵敏度高、重现性好。
具体步骤如下:
1. 样品制备:取适量甘蔗茎节,去除表皮和髓部,仅留下髓骨。
将髓骨切成小丁块,加入清水,煮沸5分钟,离火冷却后离心取上清,过滤掉杂质,即为样品。
2. 取样:取样品5mL,加入试管中。
3. 加试剂:加入2mL DNS试剂,混匀。
4. 加热:将试管放在沸水中加热10分钟。
5. 冷却:取出试管,放置至室温下冷却。
6. 吸光度测定:利用分光光度计测定样品的吸光度。
7. 计算含量:根据标准曲线计算出样品中总糖和还原糖的含量。
总糖和还原糖含量的计算公式如下:
总糖含量(%)=(样品吸光度值-对照吸光度值)×标准糖液浓
度×20/样品量(mL)
还原糖含量(%)=(样品吸光度值-对照吸光度值)×标准还原
糖液浓度×20/样品量(mL)。

DNS⽐⾊法测定还原糖和总糖还原糖和总糖的测定(3,5-⼆硝基⽔杨酸⽐⾊法)⼀、实验⽬的1、掌握还原糖和总糖测定的基本原理2、学习⽐⾊法测定还原糖的操作⽅法和分光光度计的使⽤⼆、实验原理还原糖的测定是糖定量测定的基本⽅法。
还原糖是指含有⾃由醛基或酮基的糖类。
单糖都是还原糖,双糖和多糖不⼀定是还原糖,例如乳糖和麦芽糖是还原糖,蔗糖和淀粉是⾮还原糖。
利⽤各种糖的溶解度不同,可将植物样品中的单糖、双糖和多糖分别提取出来。
对⾮还原性的双糖和多糖,可⽤酸⽔解法使其降解成还原性单糖进⾏测定,再分别求出样品中还原糖和总糖的含量(常以葡萄糖含量计)。
还原糖在碱性条件下加热可被氧化成糖酸及其它产物,⽽氧化剂3,5-⼆硝基⽔杨酸则被还原为棕红⾊的3-氨基-5-硝基⽔杨酸。
在⼀定范围内,还原糖的量与棕红⾊物质颜⾊的深浅成正⽐关系,利⽤分光光度计在540nm波长下测定光密度值,查对标准曲线并计算,便可求出样品中还原糖和总糖的含量。
由于多糖⽔解为单糖时,每断裂⼀个糖苷键需加⼊⼀分⼦⽔,所以在计算多糖含量时应乘以系数0.9。
三、实验材料和试剂1、实验材料⾯粉2、实验试剂①1mg/ml葡萄糖标准液准确称取80℃烘⾄恒重的分析纯葡萄糖100mg,置于⼩烧杯中,加少量蒸馏⽔溶解后,转移到100ml容量瓶中,⽤蒸馏⽔定容⾄100ml,混匀,4℃冰箱中保存备⽤。
②3,5-⼆硝基⽔杨酸(DNS)试剂将6.3g DNS和262ml 2M NaOH溶液,加到500ml含有185g酒⽯酸钾钠的热⽔溶液中,再加5g结晶酚和5g亚硫酸钠,搅拌溶解,冷却后加蒸馏⽔定容⾄1000ml,贮于棕⾊瓶中备⽤。
③碘-碘化钾溶液:称取5g碘和10g碘化钾,溶于100ml蒸馏⽔中。
④酚酞指⽰剂:称取0.1g酚酞,溶于250ml 70%⼄醇中。
⑤6M HCl和6M NaOH各100ml。
四、实验器材具塞璃玻刻度试管:20ml×11 ⼤离⼼管:50ml×2烧杯:100ml×1 三⾓瓶:100ml×1容量瓶:100ml×3 刻度吸管:1ml×1;2ml×2;10ml×1恒温⽔浴锅沸⽔浴离⼼机扭⼒天平分光光度计五、操作步骤1、制作葡萄糖标准曲线取7⽀具塞刻度试管编号,按表1分别加⼊浓度为1mg/ml的葡萄糖标准液、蒸馏⽔和DNS试剂,配成不同浓度的葡萄糖反应液。

D N S法测定总糖和还原糖 Prepared on 24 November 2020实验九总糖和还原糖的测定(二)──3,5-二硝基水杨酸法一、目的要求:掌握还原糖和总糖的测定原理,学习用比色法测定还原糖的方法。
二、实验原理:在NaOH和丙三醇存在下,3,5-二硝基水杨酸(DNS)与还原糖共热后被还原生成氨基化合物。
在过量的NaOH碱性溶液中此化合物呈桔红色,在540nm波长处有最大吸收,在一定的浓度范围内,还原糖的量与光吸收值呈线性关系,利用比色法可测定样品中的含糖量。
黄色桔红色三、试剂和器材1、试剂(1)1 mg/ml葡萄糖标准溶液:准确称取干燥恒重的葡萄糖100mg,加少量蒸馏水溶解后,以蒸馏水定容至100ml,即含葡萄糖为ml。
(2)3,5—二硝基水杨酸试剂:称取 g 3,5—二硝基水杨酸并量取262 ml 2mol/L NaOH加到酒石酸钾纳的热溶液中(182 g酒石酸钾纳溶于500 ml水中),再加5 g结晶酚和5 g亚硫酸氢钠溶于其中,搅拌溶解,冷却后定容到1000 ml贮于棕色瓶中。
(3)碘-碘化钾溶液:称取5g碘,10g碘化钾溶于100ml蒸馏水中。
(4)6N NaOH:称取120g NaOH溶于500ml蒸馏水中。
(5)% 酚酞指示剂。
(6)6 mol/L HCl溶液2、材料小麦淀粉或玉米淀粉。
3、器材分光光度计,天平,水浴锅,电炉,试管若干等。
四、操作方法1、葡萄糖标准曲线制作取8支15mm×180mm试管,按下表加入ml葡萄糖标准液和蒸馏水。
管号试剂0 1 2 3 4 5 6 7 8葡萄糖标准液(ml)0蒸馏水(ml)水杨酸溶液(ml)葡萄糖含量(mg)0将各管溶液混合均匀,在沸水中加热5 min,取出后立即用冷水冷却到室温,再向每管加入 ml蒸馏水,摇匀。
λ=540nm处测定吸光度以葡萄糖含量(mg)为横坐标,光吸收值为纵坐标,绘制标准曲线。
2、样品中还原糖的提取准确称取 0.5g小麦(淀)粉,放在100ml烧杯中,先以少量蒸馏水(约2 ml)调成糊状,然后加入40ml蒸馏水,混匀,于50℃恒温水浴中保温20min,不时搅拌,使还原糖浸出混。

D N S法测定总糖和还原糖Company Document number:WTUT-WT88Y-W8BBGB-BWYTT-19998实验九总糖和还原糖的测定(二)──3,5-二硝基水杨酸法一、目的要求:掌握还原糖和总糖的测定原理,学习用比色法测定还原糖的方法。
二、实验原理:在NaOH和丙三醇存在下,3,5-二硝基水杨酸(DNS)与还原糖共热后被还原生成氨基化合物。
在过量的NaOH碱性溶液中此化合物呈桔红色,在540nm波长处有最大吸收,在一定的浓度范围内,还原糖的量与光吸收值呈线性关系,利用比色法可测定样品中的含糖量。
黄色桔红色三、试剂和器材1、试剂(1)1 mg/ml葡萄糖标准溶液:准确称取干燥恒重的葡萄糖100mg,加少量蒸馏水溶解后,以蒸馏水定容至100ml,即含葡萄糖为ml。
(2)3,5—二硝基水杨酸试剂:称取 g 3,5—二硝基水杨酸并量取262 ml 2mol/L NaOH加到酒石酸钾纳的热溶液中(182 g酒石酸钾纳溶于500 ml水中),再加5 g结晶酚和5 g亚硫酸氢钠溶于其中,搅拌溶解,冷却后定容到1000 ml贮于棕色瓶中。
(3)碘-碘化钾溶液:称取5g碘,10g碘化钾溶于100ml蒸馏水中。
(4)6N NaOH:称取120g NaOH溶于500ml蒸馏水中。
(5)% 酚酞指示剂。
(6)6 mol/L HCl溶液2、材料小麦淀粉或玉米淀粉。
3、器材分光光度计,天平,水浴锅,电炉,试管若干等。
四、操作方法1、葡萄糖标准曲线制作取8支15mm×180mm试管,按下表加入ml葡萄糖标准液和蒸馏水。
管号试剂0 1 2 3 4 5 6 7 8葡萄糖标准液(ml)0蒸馏水(ml)水杨酸溶液(ml)葡萄糖含量(mg)0将各管溶液混合均匀,在沸水中加热5 min,取出后立即用冷水冷却到室温,再向每管加入 ml蒸馏水,摇匀。
λ=540nm处测定吸光度以葡萄糖含量(mg)为横坐标,光吸收值为纵坐标,绘制标准曲线。

──3,5-二硝基水杨酸法一、目的要求:掌握还原糖和总糖的测定原理,学习用比色法测定还原糖的方法。
二、实验原理:在NaOH和丙三醇存在下,3,5-二硝基水杨酸(DNS)与还原糖共热后被还原生成氨基化合物。
在过量的NaOH碱性溶液中此化合物呈桔红色,在540nm波长处有最大吸收,在一定的浓度范围内,还原糖的量与光吸收值呈线性关系,利用比色法可测定样品中的含糖量。
黄色桔红色三、试剂和器材1、试剂(1)1 mg/ml葡萄糖标准溶液:准确称取干燥恒重的葡萄糖100mg,加少量蒸馏水溶解后,以蒸馏水定容至100ml,即含葡萄糖为ml。
(2)3,5—二硝基水杨酸试剂:称取 g 3,5—二硝基水杨酸并量取262 ml 2mol/L NaOH加到酒石酸钾纳的热溶液中(182 g 酒石酸钾纳溶于500 ml水中),再加5 g结晶酚和5 g亚硫酸氢钠溶于其中,搅拌溶解,冷却后定容到1000 ml贮于棕色瓶中。
(3)碘-碘化钾溶液:称取5g碘,10g碘化钾溶于100ml蒸馏水中。
(4)6N NaOH:称取120g NaOH溶于500ml蒸馏水中。
(5)% 酚酞指示剂。
(6)6 mol/L HCl溶液2、材料小麦淀粉或玉米淀粉。
3、器材分光光度计,天平,水浴锅,电炉,试管若干等。
四、操作方法1、葡萄糖标准曲线制作取8支15mm×180mm试管,按下表加入ml葡萄糖标准液和蒸馏水。
管号试剂012345678葡萄糖标准液(ml)0蒸馏水(ml)水杨酸溶液(ml)葡萄糖含量(mg)0将各管溶液混合均匀,在沸水中加热5 min,取出后立即用冷水冷却到室温,再向每管加入 ml蒸馏水,摇匀。
λ=540nm处测定吸光度以葡萄糖含量(mg)为横坐标,光吸收值为纵坐标,绘制标准曲线。
2、样品中还原糖的提取准确称取 0.5g小麦(淀)粉,放在100ml烧杯中,先以少量蒸馏水(约2 ml)调成糊状,然后加入40ml 蒸馏水,混匀,于50℃恒温水浴中保温20min,不时搅拌,使还原糖浸出混。

DNS比色法测定还原糖及总糖实验报告实验目的:通过DNS比色法测定还原糖和总糖的含量。
实验原理:DNS比色法是一种常用的测定还原糖和总糖含量的方法。
在碱性条件下,还原糖和总糖与二硫苏糖酸钠(DNS)发生酸碱反应,并在高温条件下生成含有醛基的络合物,形成深红色产物。
产物的吸光度与还原糖或总糖的浓度成正比关系。
实验步骤:1.准备样品溶液:将待测样品加入蒸馏水中,使体积恒定为50mL。
2.取2mL样品溶液加入试管中,加入2mL硫酸溶液,并用1%甲基绿稀溶液滴定溶液颜色变黄为止。
3. 在水槽中加热样品溶液至90°C,加入2 mLDNS试剂稀溶液,迅速搅拌均匀,继续加热5 min。
4.将试管取出,立即置于冷水中冷却。
5. 测定吸光度:使用比色计测定试管中产物的吸光度,以440 nm为波长。
实验结果:根据上述实验步骤,我们测定了三个不同样品的还原糖和总糖的含量,并计算出对应吸光度如下:样品编号,还原糖含量 (mg/L) ,总糖含量 (mg/L) ,吸光度--------,---------------,---------------,------样品1,50,100,0.345样品2,75,150,0.540样品3,100,200,0.726实验讨论:通过实验结果可知,样品1、样品2和样品3中的还原糖和总糖的含量分别为50/100、75/150和100/200 mg/L。
通过计算吸光度与还原糖/总糖浓度的线性关系,可以进一步推断未知样品中还原糖和总糖的浓度。
实验结论:通过DNS比色法,我们成功测定了三个样品中还原糖和总糖的含量,并得到了吸光度与浓度的线性关系。
实验结果表明,该方法可以用于定量测定还原糖和总糖的浓度。

DNS比色法测还原糖标准曲线绘制及测定Tr21培养液中初始和最终还原糖及总糖含量实验报告1.研究背景木霉菌在发酵过程中,利用碳源导致发酵液中糖含量的变化,其中还原糖是一个主要的反映参数。
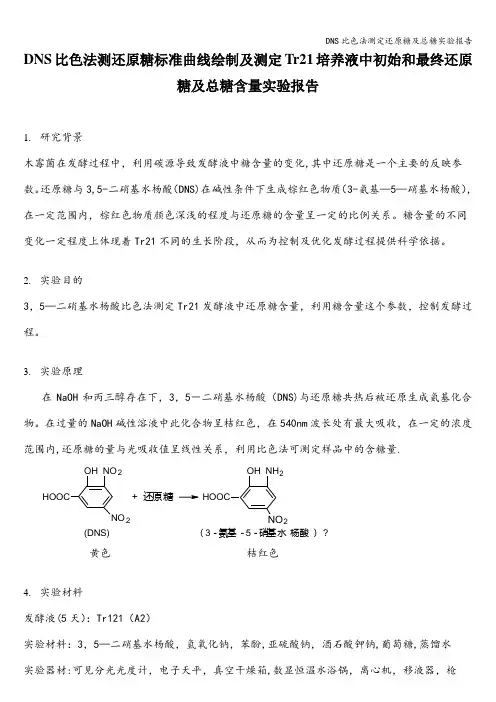
还原糖与3,5-二硝基水杨酸(DNS)在碱性条件下生成棕红色物质(3-氨基—5—硝基水杨酸),在一定范围内,棕红色物质颜色深浅的程度与还原糖的含量呈一定的比例关系。
糖含量的不同变化一定程度上体现着Tr21不同的生长阶段,从而为控制及优化发酵过程提供科学依据。
2.实验目的3,5—二硝基水杨酸比色法测定Tr21发酵液中还原糖含量,利用糖含量这个参数,控制发酵过程。
3.实验原理在NaOH和丙三醇存在下,3,5-二硝基水杨酸(DNS)与还原糖共热后被还原生成氨基化合物。
在过量的NaOH碱性溶液中此化合物呈桔红色,在540nm波长处有最大吸收,在一定的浓度范围内,还原糖的量与光吸收值呈线性关系,利用比色法可测定样品中的含糖量.黄色桔红色4.实验材料发酵液(5天):Tr121(A2)实验材料:3,5—二硝基水杨酸,氢氧化钠,苯酚,亚硫酸钠,酒石酸钾钠,葡萄糖,蒸馏水实验器材:可见分光光度计,电子天平,真空干燥箱,数显恒温水浴锅,离心机,移液器,枪头,500ML容量瓶,试管,500 ml 烧杯,1000ml量筒5.实验方法5.1试剂配制(1)1 mg/ml葡萄糖标准溶液:准确称取干燥恒重的葡萄糖100mg,加少量蒸馏水溶解后,以蒸馏水定容至100ml,即含葡萄糖为1.0mg/ml。
(2)3,5—二硝基水杨酸试剂:称取6。
3 g 3,5—二硝基水杨酸并量取262 ml 2mol/L NaOH加到酒石酸钾纳的热溶液中(182 g酒石酸钾纳溶于500 ml水中),再加5 g结晶酚和5 g亚硫酸氢钠溶于其中,搅拌溶解,冷却后定容到1000 ml贮于棕色瓶中。
(3)碘-碘化钾溶液:称取5g碘,10g碘化钾溶于100ml蒸馏水中。
(4)6N NaOH:称取120g NaOH溶于500ml蒸馏水中。

实验九总糖和还原糖的测定(二)──3,5-二硝基水杨酸法一、目的要求:掌握还原糖和总糖的测定原理,学习用比色法测定还原糖的方法。
二、实验原理:在NaOH和丙三醇存在下,3,5-二硝基水杨酸(DNS)与还原糖共热后被还原生成氨基化合物。
在过量的NaOH碱性溶液中此化合物呈桔红色,在540nm波长处有最大吸收,在一定的浓度范围内,还原糖的量与光吸收值呈线性关系,利用比色法可测定样品中的含糖量。
黄色桔红色三、试剂和器材1、试剂(1)1 mg/ml葡萄糖标准溶液:准确称取干燥恒重的葡萄糖100mg,加少量蒸馏水溶解后,以蒸馏水定容至100ml,即含葡萄糖为1.0mg/ml。
(2)3,5—二硝基水杨酸试剂:称取6.3 g 3,5—二硝基水杨酸并量取262 ml 2mol/L NaOH加到酒石酸钾纳的热溶液中(182 g 酒石酸钾纳溶于500 ml水中),再加5 g结晶酚和5 g亚硫酸氢钠溶于其中,搅拌溶解,冷却后定容到1000 ml贮于棕色瓶中。
2、材料小麦淀粉或玉米淀粉。
3、器材分光光度计,天平,水浴锅,电炉,试管若干等。
四、操作方法1、葡萄糖标准曲线制作取8支15mm×180mm试管,按下表加入1.0mg/ml葡萄糖标准液和蒸馏水。
管号试剂0 1 2 3 4 5 6 7 8葡萄糖标准液(ml)0 0.2 0.4 0.6 0.8 1.0 1.2 1.4 1.6蒸馏水(ml) 2.0 1.8 1.6 1.4 1.2 1.0 0.8 0.6 0.4水杨酸溶液(ml) 1.5 1.5 1.5 1.5 1.5 1.5 1.5 1.5 1.5葡萄糖含量(mg)0 0.2 0.4 0.6 0.8 1.0 1.2 1.4 1.6将各管溶液混合均匀,在沸水中加热5 min,取出后立即用冷水冷却到室温,再向每管加入21.5 ml蒸馏水,摇匀。
λ=540nm处测定吸光度以葡萄糖含量(mg)为横坐标,光吸收值为纵坐标,绘制标准曲线。
还原糖和总糖的测定(3,5-二硝基水杨酸比色法)一、实验目的1、掌握还原糖和总糖测定的基本原理2、学习比色法测定还原糖的操作方法和分光光度计的使用二、实验原理还原糖的测定是糖定量测定的基本方法。
还原糖是指含有自由醛基或酮基的糖类。
单糖都是还原糖,双糖和多糖不一定是还原糖,例如乳糖和麦芽糖是还原糖,蔗糖和淀粉是非还原糖。
利用各种糖的溶解度不同,可将植物样品中的单糖、双糖和多糖分别提取出来。
对非还原性的双糖和多糖,可用酸水解法使其降解成还原性单糖进行测定,再分别求出样品中还原糖和总糖的含量(常以葡萄糖含量计)。
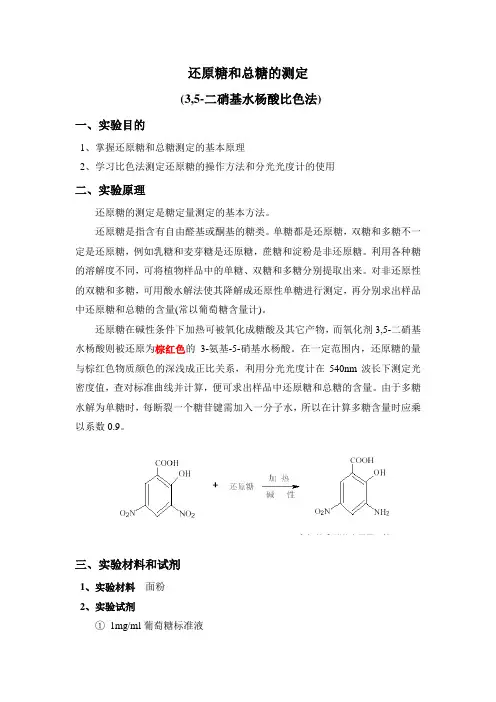
还原糖在碱性条件下加热可被氧化成糖酸及其它产物,而氧化剂3,5-二硝基水杨酸则被还原为棕红色的3-氨基-5-硝基水杨酸。
在一定范围内,还原糖的量与棕红色物质颜色的深浅成正比关系,利用分光光度计在540nm波长下测定光密度值,查对标准曲线并计算,便可求出样品中还原糖和总糖的含量。
由于多糖水解为单糖时,每断裂一个糖苷键需加入一分子水,所以在计算多糖含量时应乘以系数0.9。
三、实验材料和试剂1、实验材料面粉2、实验试剂①1mg/ml葡萄糖标准液准确称取80℃烘至恒重的分析纯葡萄糖100mg,置于小烧杯中,加少量蒸馏水溶解后,转移到100ml容量瓶中,用蒸馏水定容至100ml,混匀,4℃冰箱中保存备用。
②3,5-二硝基水杨酸(DNS)试剂将6.3g DNS和262ml 2M NaOH溶液,加到500ml含有185g酒石酸钾钠的热水溶液中,再加5g结晶酚和5g亚硫酸钠,搅拌溶解,冷却后加蒸馏水定容至1000ml,贮于棕色瓶中备用。
③碘-碘化钾溶液:称取5g碘和10g碘化钾,溶于100ml蒸馏水中。
④酚酞指示剂:称取0.1g酚酞,溶于250ml 70%乙醇中。
⑤6M HCl和6M NaOH各100ml。
四、实验器材具塞璃玻刻度试管:20ml×11 大离心管:50ml×2烧杯:100ml×1 三角瓶:100ml×1容量瓶:100ml×3 刻度吸管:1ml×1;2ml×2;10ml×1恒温水浴锅沸水浴离心机扭力天平分光光度计五、操作步骤1、制作葡萄糖标准曲线取7支具塞刻度试管编号,按表1分别加入浓度为1mg/ml的葡萄糖标准液、蒸馏水和DNS试剂,配成不同浓度的葡萄糖反应液。

实验九总糖和还原糖的测定(二)欧阳学文──3,5-二硝基水杨酸法一、目的要求:掌握还原糖和总糖的测定原理,学习用比色法测定还原糖的方法。
二、实验原理:在NaOH和丙三醇存在下,3,5-二硝基水杨酸(DNS)与还原糖共热后被还原生成氨基化合物。
在过量的NaOH 碱性溶液中此化合物呈桔红色,在540nm波长处有最大吸收,在一定的浓度范围内,还原糖的量与光吸收值呈线性关系,利用比色法可测定样品中的含糖量。
黄色桔红色三、试剂和器材1、试剂(1)1 mg/ml葡萄糖标准溶液:准确称取干燥恒重的葡萄糖100mg,加少量蒸馏水溶解后,以蒸馏水定容至100ml,即含葡萄糖为1.0mg/ml。
(2)3,5—二硝基水杨酸试剂:称取6.3 g 3,5—二硝基水杨酸并量取262 ml 2mol/L NaOH加到酒石酸钾纳的热溶液中(182 g酒石酸钾纳溶于500 ml水中),再加5 g结晶酚和5 g亚硫酸氢钠溶于其中,搅拌溶解,冷却后定容到1000 ml 贮于棕色瓶中。
(3)碘-碘化钾溶液:称取5g碘,10g碘化钾溶于100ml 蒸馏水中。
(4)6N NaOH:称取120g NaOH溶于500ml蒸馏水中。
(5)0.1% 酚酞指示剂。
(6)6 mol/L HCl溶液2、材料小麦淀粉或玉米淀粉。
3、器材分光光度计,天平,水浴锅,电炉,试管若干等。
四、操作方法1、葡萄糖标准曲线制作取8支15mm×180mm试管,按下表加入1.0mg/ml葡萄糖标准液和蒸馏水。
试剂管号012345678葡萄糖标准液00.20.40.60.8 1.0 1.2 1.4 1.6(ml)蒸馏水(ml) 2.0 1.8 1.6 1.4 1.2 1.00.80.60.4水杨酸溶液(ml) 1.5 1.5 1.5 1.5 1.5 1.5 1.5 1.5 1.5葡萄糖含量(mg) 00.20.40.60.8 1.0 1.2 1.4 1.6将各管溶液混合均匀,在沸水中加热5 min,取出后立即用冷水冷却到室温,再向每管加入21.5 ml蒸馏水,摇匀。
实验九总糖和还原糖的测定(二)──3,5-二硝基水杨酸法一、目的要求:掌握还原糖和总糖的测定原理,学习用比色法测定还原糖的方法。
二、实验原理:?在(1)(2)3,5182g酒石酸分光光度计,天平,水浴锅,电炉,试管若干等。
四、操作方法?1、葡萄糖标准曲线制作取8支15mm×180mm试管,按下表加入1.0mg/ml葡萄糖标准液和蒸馏水。
管号试剂0 1 2 3 4 5 6 7 8葡萄糖标准液(ml)0 0.2 0.4 0.6 0.8 1.0 1.2 1.4 1.6蒸馏水(ml) 2.0 1.8 1.6 1.4 1.2 1.0 0.8 0.6 0.4水杨酸溶液(ml) 1.5 1.5 1.5 1.5 1.5 1.5 1.5 1.5 1.5葡萄糖含量(mg)0 0.2 0.4 0.6 0.8 1.0 1.2 1.4 1.6将各管溶液混合均匀,在沸水中加热5min,取出后立即用冷水冷却到室温,再向每管加入21.5ml蒸馏水,摇匀。
λ=540nm处测定吸将各管溶液混合均匀,在沸水中加热5min,取出后立即用冷水冷却到室温,再向每管加入21.5ml蒸馏水,摇匀。
λ=540nm处测定吸光度样品溶液中还原糖和总糖测定后,取样品的光吸收值在标准曲线上查出相应的糖量。
五、结果处理按下式计算出样品中还原糖和总糖的百分含量:式中:C──还原糖或总糖提取液的浓度,mg/ml;V──还原糖或总糖提取液的总体积,ml;m──样品重量,g;1000──mg换算成g的系数。
思考题1.比色时为什么要设计空白管?2.比较费林试剂比色法与3,5-二硝基水杨酸比色法测定可溶性淀粉中还原糖和总糖的结果,这。
实验九总糖和还原糖的测定(二)之答禄夫天创作──3,5-二硝基水杨酸法一、目的要求:掌握还原糖和总糖的测定原理,学习用比色法测定还原糖的方法。
二、实验原理:在NaOH和丙三醇存在下,3,5-二硝基水杨酸(DNS)与还原糖共热后被还原生成氨基化合物。
在过量的NaOH碱性溶液中此化合物呈桔红色,在540nm 波长处有最大吸收,在一定的浓度范围内,还原糖的量与光吸收值呈线性关系,利用比色法可测定样品中的含糖量。
黄色桔红色三、试剂和器材1、试剂(1)1 mg/ml葡萄糖尺度溶液:准确称取干燥恒重的葡萄糖100mg,加少量蒸馏水溶解后,以蒸馏水定容至100ml,即含葡萄糖为1.0mg/ml。
(2)3,5—二硝基水杨酸试剂:称取6.3 g 3,5—二硝基水杨酸并量取262 ml 2mol/L NaOH加到酒石酸钾纳的热溶液中(182 g酒石酸钾纳溶于500 ml水中),再加5 g结晶酚和5 g亚硫酸氢钠溶于其中,搅拌溶解,冷却后定容到1000 ml贮于棕色瓶中。
(3)碘-碘化钾溶液:称取5g碘,10g碘化钾溶于100ml蒸馏水中。
(4)6N NaOH:称取120g NaOH溶于500ml蒸馏水中。
(5)0.1% 酚酞指示剂。
(6)6 mol/L HCl溶液2、资料小麦淀粉或玉米淀粉。
3、器材分光光度计,天平,水浴锅,电炉,试管若干等。
四、操纵方法1、葡萄糖尺度曲线制作取8支15mm×180mm试管,按下表加入1.0mg/ml葡萄糖尺度液和蒸馏水。
管号试剂0 1 2 3 4 5 6 7 8葡萄糖尺度液(ml)0蒸馏水(ml)水杨酸溶液(ml)葡萄糖含量(mg)0将各管溶液混合均匀,在沸水中加热5 min,取出后立即用冷水冷却到室温,再向每管加入21.5 ml蒸馏水,摇匀。
λ=540nm处测定吸光度以葡萄糖含量(mg)为横坐标,光吸收值为纵坐标,绘制尺度曲线。
2、样品中还原糖的提取准确称取小麦(淀)粉,放在100ml烧杯中,先以少量蒸馏水(约2 ml)调成糊状,然后加入40ml蒸馏水,混匀,于50℃恒温水浴中保温20min,不时搅拌,使还原糖浸出混。
D N S法测定总糖和还原糖(总4页)-CAL-FENGHAI.-(YICAI)-Company One1-CAL-本页仅作为文档封面,使用请直接删除实验九总糖和还原糖的测定(二)──3,5-二硝基水杨酸法一、目的要求:掌握还原糖和总糖的测定原理,学习用比色法测定还原糖的方法。
二、实验原理:在NaOH和丙三醇存在下,3,5-二硝基水杨酸(DNS)与还原糖共热后被还原生成氨基化合物。
在过量的NaOH碱性溶液中此化合物呈桔红色,在540nm波长处有最大吸收,在一定的浓度范围内,还原糖的量与光吸收值呈线性关系,利用比色法可测定样品中的含糖量。
黄色桔红色三、试剂和器材1、试剂(1)1 mg/ml葡萄糖标准溶液:准确称取干燥恒重的葡萄糖100mg,加少量蒸馏水溶解后,以蒸馏水定容至100ml,即含葡萄糖为1.0mg/ml。
(2)3,5—二硝基水杨酸试剂:称取6.3 g 3,5—二硝基水杨酸并量取262 ml 2mol/L NaOH加到酒石酸钾纳的热溶液中(182 g 酒石酸钾纳溶于500 ml水中),再加5 g结晶酚和5 g亚硫酸氢钠溶于其中,搅拌溶解,冷却后定容到1000 ml贮于棕色瓶中。
(3)碘-碘化钾溶液:称取5g碘,10g碘化钾溶于100ml蒸馏水中。
(4)6N NaOH:称取120g NaOH溶于500ml蒸馏水中。
(5)0.1% 酚酞指示剂。
(6)6 mol/L HCl溶液2、材料小麦淀粉或玉米淀粉。
3、器材分光光度计,天平,水浴锅,电炉,试管若干等。
四、操作方法1、葡萄糖标准曲线制作取8支15mm×180mm试管,按下表加入1.0mg/ml葡萄糖标准液和蒸馏水。
管号试剂0 1 2 3 4 5 6 7 80.6 0.8 1.0 1.2 1.4 1.6葡萄糖标准液(ml) 0 0.2 0.4蒸馏水(ml) 2.0 1.8 1.6 1.4 1.2 1.0 0.8 0.6 0.4水杨酸溶液(ml) 1.5 1.5 1.5 1.5 1.5 1.5 1.5 1.5 1.5葡萄糖含量(mg)0 0.2 0.4 0.6 0.8 1.0 1.2 1.4 1.6将各管溶液混合均匀,在沸水中加热5 min,取出后立即用冷水冷却到室温,再向每管加入21.5 ml蒸馏水,摇匀。
真验九总糖战还本糖的测定(二)之阳早格格创做──3,5-二硝基火杨酸法一、手段央供:掌握还本糖战总糖的测定本理,教习用比色法测定还本糖的要领.二、真验本理:正在NaOH战丙三醇存留下,3,5-二硝基火杨酸(DNS)与还本糖同热后被还本死成氨基化合物.正在过量的NaOH碱性溶液中此化合物呈桔黑色,正在540nm波少处有最大吸支,正在一定的浓度范畴内,还本糖的量与光吸支值呈线性闭系,利用比色法可测定样品中的含糖量.黄色桔黑色三、试剂战器材1、试剂(1)1 mg/ml葡萄糖尺度溶液:准确称与搞燥恒沉的葡萄糖100mg,加少量蒸馏火溶解后,以蒸馏火定容至100ml,即含葡萄糖为1.0mg/ml.(2)3,5—二硝基火杨酸试剂:称与6.3 g 3,5—二硝基火杨酸并量与262 ml 2mol/L NaOH加到酒石酸钾纳的热溶液中(182 g酒石酸钾纳溶于500 ml火中),再加5 g结晶酚战5 g亚硫酸氢钠溶于其中,搅拌溶解,热却后定容到1000 ml贮于棕色瓶中.(3)碘-碘化钾溶液:称与5g碘,10g碘化钾溶于100ml蒸馏火中.(4)6N NaOH:称与120g NaOH溶于500ml蒸馏火中.(5)0.1% 酚酞指示剂.(6)6 mol/L HCl溶液2、资料小麦淀粉或者玉米淀粉.3、器材分光光度计,天仄,火浴锅,电炉,试管若搞等.四、支配要领1、葡萄糖尺度直线创造与8支15mm×180mm试管,按下表加进1.0mg/ml葡萄糖尺度液战蒸馏火.管号试剂0 1 2 3 4 5 6 7 8葡萄糖尺度液(ml)0蒸馏火(ml)火杨酸溶液(ml)葡萄糖含量(mg)0将各管溶液混同匀称,正在沸火中加热5 min,与出后坐时用热火热却到室温,再背每管加进21.5 ml蒸馏火,摇匀.λ=540nm处测定吸光度以葡萄糖含量(mg)为横坐标,光吸支值为纵坐标,画造尺度直线. 2、样品中还本糖的提与准确称与小麦(淀)粉,搁正在100ml烧杯中,先以少量蒸馏火(约2 ml)调成糊状,而后加进40ml蒸馏火,混匀,于50℃恒温火浴中保温20min,没有时搅拌,使还本糖浸出混.过滤,将滤液局部支集正在50ml的容量瓶中,用蒸馏火定容至刻度,即为还本糖提与液.3、样品总糖的火解及提与准确称与小麦(淀)粉,搁正在锥形瓶中,加进6mol/L HCl 10ml,蒸馏火15ml,正在沸火浴中加热,与出1~2滴置于黑瓷板上,加1滴I-KI溶液查看火解是可真足.如已火解真足,则没有浮现蓝色.火解毕,热却至室温后加进1滴酚酞指示剂,以6N NaOH溶液中战至溶液呈微黑色,并定容到100ml,过滤与滤液10ml于100ml容量瓶中,定容至刻度,混匀,即为密释1000倍的总糖火解液,用于总糖测定.4、样品中含糖量的测定试剂空黑还本糖总糖样品溶液(ml)0蒸馏火(ml)火杨酸(ml)将各管溶液混同匀称,正在沸火中加热5 min,与出后坐时用热火热却到室温,再背每管加进21.5 ml蒸馏火,摇匀.λ=540nm处测定吸光度样品溶液中还本糖战总糖测定后,与样品的光吸支值正在尺度直线上查出相映的糖量.五、截止处理按下式估计出样品中还本糖战总糖的百分含量:式中:C──还本糖或者总糖提与液的浓度,mg/ml;V──还本糖或者总糖提与液的总体积,ml;m──样品沉量,g;1000──mg换算成g的系数.思索题1. 比色时为什么要安排空黑管?2. 比较费林试剂比色法与3,5-二硝基火杨酸比色法测定可溶性淀粉中还本糖战总糖的截止,那二种要领各有何便宜?。
还原糖和总糖的测定(3,5-二硝基水杨酸比色法)一、实验目的1、掌握还原糖和总糖测定的基本原理2、学习比色法测定还原糖的操作方法和分光光度计的使用二、实验原理还原糖的测定是糖定量测定的基本方法。
还原糖是指含有自由醛基或酮基的糖类。
单糖都是还原糖,双糖和多糖不一定是还原糖,例如乳糖和麦芽糖是还原糖,蔗糖和淀粉是非还原糖。
利用各种糖的溶解度不同,可将植物样品中的单糖、双糖和多糖分别提取出来。
对非还原性的双糖和多糖,可用酸水解法使其降解成还原性单糖进行测定,再分别求出样品中还原糖和总糖的含量(常以葡萄糖含量计)。
还原糖在碱性条件下加热可被氧化成糖酸及其它产物,而氧化剂3,5-二硝基水杨酸则被还原为棕红色的3-氨基-5-硝基水杨酸。
在一定范围内,还原糖的量与棕红色物质颜色的深浅成正比关系,利用分光光度计在540nm波长下测定光密度值,查对标准曲线并计算,便可求出样品中还原糖和总糖的含量。
由于多糖水解为单糖时,每断裂一个糖苷键需加入一分子水,所以在计算多糖含量时应乘以系数0.9。
三、实验材料和试剂1、实验材料面粉2、实验试剂①1mg/ml葡萄糖标准液准确称取80℃烘至恒重的分析纯葡萄糖100mg,置于小烧杯中,加少量蒸馏水溶解后,转移到100ml容量瓶中,用蒸馏水定容至100ml,混匀,4℃冰箱中保存备用。
②3,5-二硝基水杨酸(DNS)试剂将6.3g DNS和262ml 2M NaOH溶液,加到500ml含有185g酒石酸钾钠的热水溶液中,再加5g结晶酚和5g亚硫酸钠,搅拌溶解,冷却后加蒸馏水定容至1000ml,贮于棕色瓶中备用。
③碘-碘化钾溶液:称取5g碘和10g碘化钾,溶于100ml蒸馏水中。
④酚酞指示剂:称取0.1g酚酞,溶于250ml 70%乙醇中。
⑤6M HCl和6M NaOH各100ml。
四、实验器材具塞璃玻刻度试管:20ml×11 大离心管:50ml×2烧杯:100ml×1 三角瓶:100ml×1容量瓶:100ml×3 刻度吸管:1ml×1;2ml×2;10ml×1恒温水浴锅沸水浴离心机扭力天平分光光度计五、操作步骤1、制作葡萄糖标准曲线取7支具塞刻度试管编号,按表1分别加入浓度为1mg/ml的葡萄糖标准液、蒸馏水和DNS试剂,配成不同浓度的葡萄糖反应液。
实验九总糖和复原糖的测定(二)之五兆芳芳创作──3,5-二硝基水杨酸法一、目的要求:掌握复原糖和总糖的测定原理,学习用比色法测定复原糖的办法.二、实验原理:在NaOH和丙三醇存在下,3,5-二硝基水杨酸(DNS)与复原糖共热后被复原生成氨基化合物.在过量的NaOH碱性溶液中此化合物呈桔白色,在540nm波长处有最大吸收,在一定的浓度规模内,复原糖的量与光吸收值呈线性关系,利用比色法可测定样品中的含糖量.黄色桔白色三、试剂和器材1、试剂(1)1 mg/ml葡萄糖尺度溶液:准确称取枯燥恒重的葡萄糖100mg,加少量蒸馏水溶解后,以蒸馏水定容至100ml,即含葡萄糖为1.0mg/ml.(2)3,5—二硝基水杨酸试剂:称取 6.3 g 3,5—二硝基水杨酸并量取262 ml 2mol/L NaOH加到酒石酸钾纳的热溶液中(182 g酒石酸钾纳溶于500 ml水中),再加5 g结晶酚和5 g亚硫酸氢钠溶于其中,搅拌溶解,冷却后定容到1000 ml贮于棕色瓶中.(3)碘-碘化钾溶液:称取5g碘,10g碘化钾溶于100ml蒸馏水中.(4)6N NaOH:称取120g NaOH溶于500ml蒸馏水中.(5)0.1% 酚酞指示剂.(6)6 mol/L HCl溶液2、资料小麦淀粉或玉米淀粉.3、器材分光光度计,天平,水浴锅,电炉,试管若干等.四、操纵办法1、葡萄糖尺度曲线制作取8支15mm×180mm试管,按下表参加1.0mg/ml葡萄糖尺度液和蒸馏水.管号试剂0 1 2 3 4 5 6 7 8葡萄糖尺度液(ml)0蒸馏水(ml)水杨酸溶液(ml)葡萄糖含量(mg)0将各管溶液混杂均匀,在滚水中加热5 min,取出后立即用冷水冷却到室温,再向每管参加21.5 ml蒸馏水,摇匀.λ=540nm处测定吸光度以葡萄糖含量(mg)为横坐标,光吸收值为纵坐标,绘制尺度曲线. 2、样品中复原糖的提取准确称取小麦(淀)粉,放在100ml烧杯中,先以少量蒸馏水(约2 ml)调成糊状,然后参加40ml蒸馏水,混匀,于50℃恒温水浴中保温20min,不时搅拌,使复原糖浸出混.过滤,将滤液全部收集在50ml的容量瓶中,用蒸馏水定容至刻度,即为复原糖提取液.3、样品总糖的水解及提取准确称取小麦(淀)粉,放在锥形瓶中,参加6mol/L HCl 10ml,蒸馏水15ml,在滚水浴中加热,取出1~2滴置于白瓷板上,加1滴I-KI 溶液查抄水解是否完全.如已水解完全,则不呈现蓝色.水解毕,冷却至室温后参加1滴酚酞指示剂,以6N NaOH溶液中和至溶液呈微白色,并定容到100ml,过滤取滤液10ml于100ml容量瓶中,定容至刻度,混匀,即为稀释1000倍的总糖水解液,用于总糖测定.4、样品中含糖量的测定试剂空白复原糖总糖样品溶液(ml)0蒸馏水(ml)水杨酸(ml)将各管溶液混杂均匀,在滚水中加热5 min,取出后立即用冷水冷却到室温,再向每管参加21.5 ml蒸馏水,摇匀.λ=540nm处测定吸光度样品溶液中复原糖和总糖测定后,取样品的光吸收值在尺度曲线上查出相应的糖量.五、结果处理按下式计较出样品中复原糖和总糖的百分含量:式中:C──复原糖或总糖提取液的浓度,mg/ml;V──复原糖或总糖提取液的总体积,ml;m──样品重量,g;1000──mg换算成g的系数.思考题1. 比色时为什么要设计空白管?2. 比较费林试剂比色法与3,5-二硝基水杨酸比色法测定可溶性淀粉中复原糖和总糖的结果,这两种办法各有何优点?。
实验九总糖和还原糖的测定(二)
──3,5-二硝基水杨酸法
一、目的要求:
掌握还原糖和总糖的测定原理,学习用比色法测定还原糖的方法。
二、实验原理:
在NaOH和丙三醇存在下,3,5-二硝基水杨酸(DNS)与还原糖共热后被还原生成氨基化合物。
在过量的NaOH碱性溶液中此化合物呈桔红色,在540nm波长处有最大吸收,在一定的浓度范围内,还原糖的量与光吸收值呈线性关系,利用比色法可测定样品中的含糖量。
黄色桔红色
三、试剂和器材
1、试剂
(1)1 mg/ml葡萄糖标准溶液:准确称取干燥恒重的葡萄糖100mg,加少量蒸馏水溶解后,以蒸馏水定容至100ml,即含葡萄糖为1.0mg/ml。
(2)3,5—二硝基水杨酸试剂:称取6.3 g 3,5—二硝基水杨酸并量取262 ml 2mol/L NaOH加到酒石酸钾纳的热溶液中(182 g 酒石酸钾纳溶于500 ml水中),再加5 g结晶酚和5 g亚硫酸氢钠溶于其中,搅拌溶解,冷却后定容到1000 ml贮于棕色瓶中。
(3)碘-碘化钾溶液:称取5g碘,10g碘化钾溶于100ml蒸馏水中。
(4)6N NaOH:称取120g NaOH溶于500ml蒸馏水中。
(5)0.1% 酚酞指示剂。
(6)6 mol/L HCl溶液
2、材料
小麦淀粉或玉米淀粉。
3、器材
分光光度计,天平,水浴锅,电炉,试管若干等。
四、操作方法
1、葡萄糖标准曲线制作
取8支15mm×180mm试管,按下表加入1.0mg/ml葡萄糖标准液和蒸馏水。
管号
试剂
0 1 2 3 4 5 6 7 8
葡萄糖标准液(ml)0 0.2 0.4 0.6 0.8 1.0 1.2 1.4 1.6
蒸馏水(ml) 2.0 1.8 1.6 1.4 1.2 1.0 0.8 0.6 0.4
水杨酸溶液(ml) 1.5 1.5 1.5 1.5 1.5 1.5 1.5 1.5 1.5
葡萄糖含量(mg)0 0.2 0.4 0.6 0.8 1.0 1.2 1.4 1.6
将各管溶液混合均匀,在沸水中加热5 min,取出后立即用冷水冷却到室温,
再向每管加入21.5 ml蒸馏水,摇匀。
λ=540nm处测定吸
光度
以葡萄糖含量(mg)为横坐标,光吸收值为纵坐标,绘制标准曲线。
2、样品中还原糖的提取
准确称取0.5g小麦(淀)粉,放在100ml烧杯中,先以少量蒸馏水(约2 ml)调成糊状,然后加入40ml 蒸馏水,混匀,于50℃恒温水浴中保温20min,不时搅拌,使还原糖浸出混。
过滤,将滤液全部收集在50ml 的容量瓶中,用蒸馏水定容至刻度,即为还原糖提取液。
3、样品总糖的水解及提取
准确称取0.5g小麦(淀)粉,放在锥形瓶中,加入6mol/L HCl 10ml,蒸馏水15ml,在沸水浴中加热0.5h,取出1~2滴置于白瓷板上,加1滴I-KI溶液检查水解是否完全。
如已水解完全,则不呈现蓝色。
水解毕,冷却至室温后加入1滴酚酞指示剂,以6N NaOH溶液中和至溶液呈微红色,并定容到100ml,过滤取滤液10ml 于100ml容量瓶中,定容至刻度,混匀,即为稀释1000倍的总糖水解液,用于总糖测定。
4、样品中含糖量的测定
试剂空白还原糖总糖样品溶液(ml)0 1.0 1.0
蒸馏水(ml) 2.0 1.0 1.0
水杨酸(ml) 1.50 1.50 1.50 将各管溶液混合均匀,在沸水中加热5 min,取出后立即用冷水冷却到室温,再向每管加入21.5 ml蒸馏水,摇匀。
λ=540nm处测定吸光度
样品溶液中还原糖和总糖
测定后,取样品的光吸收值在标准曲线上查出相应的糖量。
五、结果处理
按下式计算出样品中还原糖和总糖的百分含量:
式中:C──还原糖或总糖提取液的浓度,mg/ml;
V──还原糖或总糖提取液的总体积,ml;
m──样品重量,g;
1000──mg换算成g的系数。
思考题
1. 比色时为什么要设计空白管?
2. 比较费林试剂比色法与3,5-二硝基水杨酸比色法测定可溶性淀粉中还原糖和总糖的结果,这两种方法各有何优点?。