溶解度曲线及溶解度表
- 格式:docx
- 大小:14.68 KB
- 文档页数:3





三种溶液溶解度曲线
溶解度曲线是描述在不同温度下溶质在溶剂中溶解度随着温度变化的曲线。
一般来说,溶解度曲线可以分为三种类型,正常溶解度曲线、异常溶解度曲线和饱和溶解度曲线。
1. 正常溶解度曲线:
正常溶解度曲线是指溶解度随着温度的升高而增加的曲线。
这是最常见的类型,其中随着温度升高,溶质在溶剂中的溶解度也随之增加。
典型的例子是氯化钠在水中的溶解度曲线,随着温度的升高,氯化钠的溶解度也会增加。
2. 异常溶解度曲线:
异常溶解度曲线是指溶解度随着温度的升高而减小的曲线。
这种情况通常发生在某些化合物在溶剂中的溶解度在特定温度范围内随温度的升高而减小,然后再随温度的升高而增加。
这种情况通常涉及到一些非常规的化学现象,例如溶解热或者晶体结构的变化。
3. 饱和溶解度曲线:
饱和溶解度曲线是指在一定压力下,溶解度随着温度的变化而变化的曲线。
在这种情况下,压力是一个关键的因素,因为在一定压力下,溶解度随着温度的变化而变化。
典型的例子是二氧化碳在水中的溶解度曲线,随着温度的升高,二氧化碳的溶解度会减小。
总的来说,溶解度曲线是描述溶质在溶剂中溶解度随着温度变化的曲线,在不同的情况下会呈现出不同的特点,包括正常溶解度曲线、异常溶解度曲线和饱和溶解度曲线。
这些曲线的研究对于理解溶解过程和控制溶解度具有重要意义。


溶解度曲线与图像分析一、溶解度曲线【三变量: 、 、 】1.注意温度变量①a 物质溶解度大于c 物质溶解度。
( ) ②b 物质为易溶性物质。
( ) ③c 是氢氧化钙的溶解度曲线。
( ) ④a 、c 饱和溶液溶质质量分数相等。
( )⑤t 1-t 2℃之间a 饱和溶液浓度大于c 饱和溶液浓度。
( )2.注意饱和变量①t 1℃时,100ga 、c 两物质的溶液中,含a 、c 的质量相等。
( ) ②t 2℃时,b 溶液溶质质量分数大于c 溶液溶质质量分数。
( ) ③t 2℃时a 溶液的溶质质量分数比t 1℃时大。
( ) ④t 1℃时可以得到质量分数为16%的c 溶液。
( ) ⑤t 2℃时M 点所对应三种溶液的溶质质量分数:a >b >c 。
( )⑥t 2℃时将等质量的a 、b 两种物质的溶液分别降温至t ℃,析出晶体的质量a 一定大于b 。
3.注意等质量①t ℃时a 、b 饱和溶液中含有的a 、b 质量相等。
( )②t 2℃时,将a 、b 两物质的饱和溶液分别降温至t ℃析出晶体的质量a 大于b 。
( ) ③t 1℃,将a 、c 两种物质的饱和溶液分别恒温蒸发等质量的水,析出晶体的质量a=c 。
( ) ④a 、b 两物质的饱和溶液,温度从t 1℃升高到t 2℃时,所得溶液的溶质质量分数a >b 。
4.计算①t 1℃时将20g c 物质加入50g 水中能形成60g 溶液。
( ) ②t 1℃时a 物质的饱和溶液溶质质量分数为20%。
( )③t 2℃时75g a 的饱和溶液加入一定量的水,降温到t 1℃可得到125g16%的a 饱和溶液。
④t 2℃时,将60g a 物质放入100g 水中,所得溶液中溶质与溶液质量之比为1:3。
( ) ⑤将100g 溶质质量分数为10%的a 溶液从t 2℃降温到t 1℃其质量分数仍为10%。
( ) 5.其他①t 1℃时a 、c 物质的溶解度都为20。
( ) ②降温可以使C 的不饱和溶液变为饱和。

二、溶解度1.固体物质的溶解度:在一定温度下,某固体物质在100 g溶剂里达到饱和状态时所溶解的质量。
2.溶解度四要素:一定温度、100 g溶剂、饱和状态、溶质质量。
3.影响因素:影响溶解性大小的因素主要是溶质、溶剂的本性,其次是温度(固体溶质)或温度和压强(气体溶质)等。
固体物质的溶解度一般随温度的升高而增大,其中变化较大的如硝酸钾、变化不大的如氯化钠,但氢氧化钙等少数物质比较特殊,溶解度随温度的升高反而减小。
4.溶解度曲线:(1)表示:物质的溶解度随温度变化的曲线。
(2)意义:①表示同一种物质在不同温度时的溶解度;②可以比较同一温度时,不同物质的溶解度的大小;③表示物质的溶解度受温度变化影响的大小等。
5.气体的溶解度(1)定义:在压强为101 kPa和一定温度时,气体溶解在1体积水里达到饱和状态时的气体体积。
(2)五要素:101 kPa、一定温度、1体积水、饱和状态、气体体积。
(3)影响因素:温度、压强.升高温度,气体溶解度减小;降低温度,气体溶解度增大.增大压强,气体溶解度增大;减小压强,气体溶解度减小。
【例题2】对照溶解度概念分析“36 g食盐溶解在100 g水中,所以食盐的溶解度为36 g”这句话应怎样改正。
【解析】溶解度概念包括四要素:“一定的温度”“100 g溶剂”“饱和状态”“溶质的质量”。
题中错误之处在于:一没有指明在什么温度下,因为物质的溶解度随温度的改变而改变。
二没有指明是否达到饱和状态,所以不正确。
【答案】在20 ℃时,36 g NaCl溶解在100 g水中恰好达到饱和状态,所以20 ℃时NaCl的溶解度为36 g。
【例题3】甲、乙物质的溶解度均随温度的升高而增大。
在10 ℃时,在20 g水中最多能溶解3 g甲物质;在30 ℃时,将23 g乙物质的饱和溶液蒸干得到3 g乙物质。
则20 ℃时甲、乙两种物质的溶解度的关系是()A.甲=乙 B.甲<乙C.甲>乙 D.无法确定【解析】比较不同物质的溶解度大小,一定要在相同温度下进行。


溶解度与溶解度曲线一、溶解度1.定义在一定温度下,某固体物质在100g溶剂(通常为水)中,达到饱和状态时所溶解的质量,叫做该物质在该温度下的溶解度。
2.四要素①在一定温度下②100g水③达到饱和状态④单位:g二、溶解度曲线⑴溶解度曲线中的信息①溶解度曲线上的点:该温度下该物质的溶解度,饱和溶液②溶解度曲线上方的点:该温度下的饱和溶液③溶解度曲线下方的点:该温度下的不饱和溶液④溶解度曲线上交点的含义:该温度下甲乙两种物质的溶解度相同,其饱和溶液中溶质质量分数相同。
⑵饱和溶液与不饱和溶液的转化(针对溶解度随温度升高而增大的物质)⑶饱和溶液改变条件后,溶液的变化情况真题回顾【例1】(2011山东淄博)右图是某物质的溶解度曲线,60℃时,取100g水配制成该物质的饱和溶液,当温度降低至30℃时所得溶液的质量为( )A.130g B.140g C.160g D.180g【例2】(2011四川泸州)下列有关饱和溶液的说法中,正确的是( )A.饱和溶液的溶质质量分数一定比不饱和溶液的大B.饱和溶液降温析出晶体后的溶液一定是不饱和溶液C.任何饱和溶液升温后都会变成不饱和溶液D.一定温度下,向氯化钠饱和溶液中加入水后会变成不饱和溶液【例3】(2011江苏盐城市)右图为A、B、C三种固体物质(不含结晶水)的溶解度曲线。
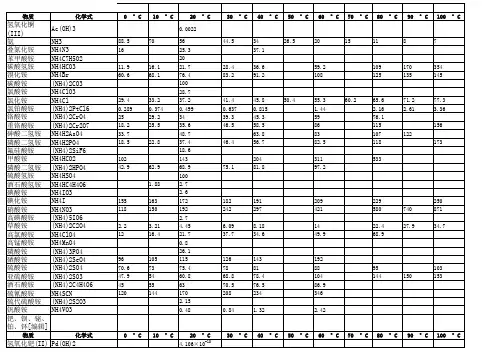
下列说法错误的是( ) A.t1℃时,三种物质中B的溶解度最大B.t2℃时,取三种物质各a g分别放入100g水中充分溶解,只有C物质能形成饱和溶液C.将等质量的三种物质的饱和溶液分别由t2℃降温到t1℃,A溶液中析出的晶体质量最大D.可用增加溶剂的方法使接近饱和的B溶液变为饱和溶液【例4】(2011北京选摘)根据下表回答问题。
①60℃时,向两个分别盛有50gNaCl和NH4Cl的烧杯中,各加入100g的水,充分溶解后,为饱和溶液的是________溶液。
②采用一种操作方法,将上述烧杯中的剩余固体全部溶解,变为不饱和溶液。
溶解度曲线及溶解度表
摘要:
一、溶解度曲线的概念和作用
1.溶解度曲线的定义
2.溶解度曲线的重要性
3.溶解度曲线在实际应用中的价值
二、溶解度曲线的类型和特点
1.固体的溶解度曲线
2.液体的溶解度曲线
3.气体的溶解度曲线
4.各类溶解度曲线的特点和区别
三、溶解度表的定义和用途
1.溶解度表的定义
2.溶解度表的重要性
3.溶解度表在实际应用中的价值
四、如何理解和使用溶解度曲线和溶解度表
1.了解溶解度曲线的形状和趋势
2.掌握溶解度表的数据和信息
3.将溶解度曲线和溶解度表应用于实际问题
正文:
溶解度曲线和溶解度表是化学领域中非常重要的概念,它们对于理解物质
的溶解性和在溶液中的行为具有重要作用。
溶解度曲线是一种图形表示方法,展示了在不同温度下,物质在溶剂中的溶解度变化情况。
而溶解度表则是一种数据表格,列出了在不同温度下,物质在溶剂中的溶解度数据。
一、溶解度曲线的概念和作用
溶解度曲线,也称为溶解度图,是一种将温度作为横坐标,溶解度作为纵坐标的曲线图。
通过溶解度曲线,我们可以了解物质在不同温度下的溶解度变化规律,以及溶解度与温度的关系。
溶解度曲线对于研究物质的溶解性和在溶液中的行为具有重要意义,有助于我们更好地理解化学反应和物质的性质。
二、溶解度曲线的类型和特点
根据溶质和溶剂的性质,溶解度曲线可以分为固体的溶解度曲线、液体的溶解度曲线和气体的溶解度曲线。
固体的溶解度曲线通常呈现出随着温度升高而上升的趋势,而液体的溶解度曲线则通常呈现出随着温度升高而下降的趋势。
气体的溶解度曲线则受到温度和压力的影响,一般情况下,随着温度的升高,气体的溶解度会降低。
三、溶解度表的定义和用途
溶解度表是一种数据表格,列出了在不同温度下,物质在溶剂中的溶解度数据。
溶解度表可以帮助我们快速查找和获取物质在不同温度下的溶解度信息,为实际问题提供数据支持。
溶解度表对于研究和分析物质的溶解性和在溶液中的行为具有重要作用,广泛应用于化学、地质、环境等领域。
四、如何理解和使用溶解度曲线和溶解度表
要理解和使用溶解度曲线和溶解度表,首先需要了解溶解度曲线的形状和趋势,以及溶解度表的数据和信息。
在此基础上,我们可以将溶解度曲线和溶
解度表应用于实际问题,例如分析物质的溶解度与温度的关系,预测化学反应在不同温度下的进行情况等。