汪小兰《有机化学》第四版_习题答案_高等教育出版社
- 格式:doc
- 大小:3.25 MB
- 文档页数:56

目录第一章绪论.......................................................................................................................................第二章饱和烃...................................................................................................................................第三章不饱和烃...............................................................................................................................第四章环烃.......................................................................................................................................第五章旋光异构...............................................................................................................................第六章卤代烃...................................................................................................................................第七章波谱法在有机化学中的应用...............................................................................................第八章醇酚醚...................................................................................................................................第九章醛、酮、醌...........................................................................................................................第十章羧酸及其衍生物...................................................................................................................第十一章取代酸...............................................................................................................................第十二章含氮化合物.......................................................................................................................第十三章含硫和含磷有机化合物...................................................................................................第十四章碳水化合物.......................................................................................................................第十五章氨基酸、多肽与蛋白质...................................................................................................第十六章类脂化合物.......................................................................................................................第十七章杂环化合物....................................................................................................................... Fulin 湛师第一章绪论1.1扼要归纳典型的以离子键形成的化合物与以共价键形成的化合物的物理性质。

目录之马矢奏春创作第一章绪论0第二章饱和烃1第三章不饱和烃5第四章环烃13第五章旋光异构21第六章卤代烃26第七章波谱法在有机化学中的应用31第八章醇酚醚41第九章醛、酮、醌50第十章羧酸及其衍生物61第十一章代替酸68第十二章含氮化合物74第十三章含硫和含磷有机化合物82第十四章碳水化合物85第十五章氨基酸、多肽与蛋白质96第十六章类脂化合物101第十七章杂环化合物109Fulin 湛师第一章 绪论1.1简明归纳范例的以离子键形成的化合物与以共价键形成的化合物的物理性质. 答案:1.2 NaCl 相同?如将CH4及CCl4各1mol 混在一路,与CHCl3及CH3Cl 各1mol 的混淆物是否相同?为什么? 答案:NaCl 与KBr 各1mol 与NaBr 及KCl 各1mol 溶于水中所得溶液相同.因为两者溶液中均为Na+,K+,Br -, Cl -离子各1mol.因为CH4与CCl4及CHCl3与CH3Cl 在水中是以分子状态消掉,所所以两组不合的混淆物.1.3碳原子核外及氢原子核外各有几个电子?它们是若何分布的?画出它们的轨道外形.当四个氢原子与一个碳原子结合成甲烷(CH4)时,碳原子核外有几个电子是用来与氢成键的?画出它们的轨道外形及甲烷分子的外形. 答案:C+624HCCH 4中C 中有4个电子与氢成键为SP 3杂化轨道,正四面体结构CH 4SP 3杂化2p y2p z2p x2sH1.4写出下列化合物的Lewis 电子式.a.C2H4b.CH3Clc.NH3d.H2Se.HNO3f.HCHOg.H3PO4h.C2H6 i.C2H2 j.H2SO4答案:a.C C H H H HCC HH HH 或 b.H C H H c.H N H Hd.H S H e.H O NOf.OC H Hg.O P OO O H H Hh.H C C HHH H HO P O O H HH或i.H C C Hj.O S O HH OOH H或1.5下列各化合物哪个有偶极矩?画出其标的目的.a.I2b.CH2Cl2c.HBrd.CHCl3e.CH3OHf.CH3OCH3 答案:b.ClClc.HBrd.HCe.H 3COHH 3COCH 3f.1.6 按照S 与O 的电负性不同,H2O 与H2S 比拟,哪个有较强的偶极-偶极传染感动力或氢键? 答案:电负性O>S,H2O 与H2S 比拟,H2O 有较强的偶极传染感动及氢键. 1.7 下列分子中那些可以形成氢键?a.H2b. CH3CH3c. SiH4d. CH3NH2e. CH3CH2OHf. CH3OCH3 答案:d.CH3NH2e.CH3CH2OH1.8 醋酸分子式为CH3COOH,它是否能溶于水?为什么?答案:能溶于水,因为含有C=O 和OH 两种极性基团,按照相似相容道理,可以溶于极性水.第二章饱和烃2.1 卷心菜叶概略的蜡质中含有29个碳的直链烷烃,写出其分子式.答案:C29H602.2 用系统命名法(假如可能的话,同时用通俗命名法)命名下列化合物,并指出(c)和(d)中各碳原子的级数.a.CH 3(CH 2)3CH(CH 2)3CH 3C(CH 3)2CH 2CH(CH 3)2 b.C H H C HH CH HH C H HC H H CHHH c.CH 322CH 3)2CH 23d.CH 3CH 2CH CH 2CH 3CHCH CH 2CH 2CH 3CH 3CH 3e.C CH 3H 3C CH 3Hf.(CH 3)4Cg.CH 3CHCH 2CH 3C 2H 5h.(CH 3)2CHCH 2CH 2CH(C 2H 5)21。

汪小兰《有机化学》第四版习题答案高等教育出版社汪小兰《有机化学》第四版-习题答案-高等教育出版社第一章为绪论1.1扼要归纳典型的以离子键形成的化合物与以共价键形成的化合物的物理性质。
答案:熔沸点溶解度硬度1.2离子键合化合物在强极性溶剂中高度可溶,高共价键合化合物在弱或非极性溶剂中较难溶解,通过在水中溶解1mol NaCl和KBr获得的溶液与通过在水中溶解1mol NaBr和KCl获得的溶液相同吗?如果1mol CH4和CCl4混合在一起,它们是否与1mol CHCl3和CH3Cl相同?为什么?答案:nacl与kbr各1mol与nabr及kcl各1mol溶于水中所得溶液相同。
因为两者--溶液中均为na+,k+,br,cl离子各1mol。
由于CH4和CCl4以及CHCl3和CH3Cl在水中以分子状态存在,因此它们是两种不同的混合物。
1.3碳原子核外及氢原子核外各有几个电子?它们是怎样分布的?画出它们的轨道形状。
当四个氢原子与一个碳原子结合形成甲烷(CH4)时,碳核外有多少电子被用来与氢结合?画出它们的轨道形状和甲烷分子的形状。
答复:c+624h+11ycyxx2pyzyx2pz1s2s2p2p2pyzxz2s2pxzhch4中c中有4个电子与氢成键为sp3杂化轨道,正四面体结构hch4sp3杂化chhh1.4写出下列化合物的路易斯电子式。
a.c2h2b.ch3clc.nh3d.h2se.hno3f.hchog.h3po4h.c2h6i.c2h2j.h2so4答复:a.hcchhhoo或hchf.chhb.hhcclhohopoh或ohc.hnhhd.hshe.honohchg.ohopohohhhh.hcchhhi、 hcchj。
Ohosoho还是Ohosoho1.5下列各化合物哪个有偶极矩?画出其方向。
a、 i2b。
ch2cl2c。
哈佛商学院。
chcl3e。
ch3ohf。
CH3OCH3答案:lclclh3che.ohf.h3coch31.6根据S和O之间的电负性差异,哪个比H 2O具有更强的偶极力或氢键?答复:电负性o>s,h2o与h2s相比,h2o有较强的偶极作用及氢键。

(汪小兰)有机化学第四版课后答案完全版第一章绪论1.1 扼要归纳典型的以离子键形成的化合物与以共价键形成的化合物的物理性质。
答案:1.2NaCl与KBr各1mol溶于水中所得的溶液与NaBr及KCl各1mol溶于水中所得溶液是否相同?如将CH4 及CCl4各1mol混在一起,与CHCl3及CH3Cl各1mol的混合物是否相同?为什么?答案:NaCl与KBr各1mol与NaBr及KCl 各1mol溶于水中所得溶液相同。
因为两者溶液中均为Na+ , K+ , Br-, Cl-离子各1mol。
由于CH4 与CCl4及CHCl3与CH3Cl 在水中是以分子状态存在,所以是两组不同的混合物。
i.H C C Hj.O S O HH OH H或1.5 下列各化合物哪个有偶极矩?画出其方向。
a. I 2b. CH 2Cl 2c. HBrd.CHCl 3 e. CH 3OH f. CH 3OCH 3 答案:b.ClClc.HBrd.He.H 3COHH 3COCH 3f.1.6 根据S 与O 的电负性差别,H 2O 与H 2S 相比,哪个有较强的偶极-偶极作用力或氢键? 答案:电负性 O > S , H 2O 与H 2S 相比,H 2O 有较强的偶极作用及氢键。
第二章 饱和脂肪烃2.2用系统命名法(如果可能的话,同时用普通命名法)命名下列化合物,并指出(c)和(d) 中各碳原子的级数。
a.CH 3(CH 2)3CH(CH 2)3CH 3C(CH 3)22CH(CH 3)2 b.C H C H CH H C H HC H CHHc.CH 322CH 3)2CH 23d.CH 3CH 2CHCH 2CH 3CHCH 2CH 2CH 3CH 3CH 3e.C CH 3H 3C 3Hf.(CH 3)4Cg.CH 3CHCH 2CH 32H 5h.(CH 3)2CHCH 2CH 2CH(C 2H 5)21。
答案:a. 2,4,4-三甲基-5-正丁基壬烷 5-butyl-2,4,4-trimethylnonane b. 正己 烷 hexane c. 3,3-二乙基戊烷 3,3-diethylpentane d. 3-甲基-5-异丙基辛烷 5-isopropyl -3-methyloctane e. 2-甲基丙烷(异丁烷)2-methylpropane (iso-butane) f. 2,2-二甲基丙烷(新戊烷) 2,2-dimethylpropane (neopentane) g. 3-甲基戊烷 3-methylpentane h. 2-甲基-5-乙基庚烷 5-ethyl -2-methylheptane2.3 下列各结构式共代表几种化合物?用系统命名法命名。

目录第一章绪论 (1)第二章饱和烃 (2)第三章不饱和烃 (6)第四章环烃 (14)第五章旋光异构 (23)第六章卤代烃 (28)第七章波谱法在有机化学中的应用 (33)第八章醇酚醚 (43)第九章醛、酮、醌 (52)第十章羧酸及其衍生物 (63)第十一章取代酸 (71)第十二章含氮化合物 (77)第十三章含硫和含磷有机化合物 (85)第十四章碳水化合物 (88)第十五章氨基酸、多肽与蛋白质 (99)第十六章类脂化合物 (104)第十七章杂环化合物 (113)Fulin 湛师第一章 绪论1.1扼要归纳典型的以离子键形成的化合物与以共价键形成的化合物的物理性质。
答案:1.2 NaCl 与KBr 各1mol 溶于水中所得的溶液与NaBr 及KCl 各1mol 溶于水中所得溶液是否相同?如将CH 4及CCl 4各1mol 混在一起,与CHCl 3及CH 3Cl 各1mol 的混合物是否相同?为什么? 答案:NaCl 与KBr 各1mol 与NaBr 及KCl 各1mol 溶于水中所得溶液相同。
因为两者溶液中均为Na +,K +,Br -, Cl -离子各1mol 。
由于CH 4与CCl 4及CHCl 3与CH 3Cl 在水中是以分子状态存在,所以是两组不同的混合物。
1.3碳原子核外及氢原子核外各有几个电子?它们是怎样分布的?画出它们的轨道形状。
当四个氢原子与一个碳原子结合成甲烷(CH 4)时,碳原子核外有几个电子是用来与氢成键的?画出它们的轨道形状及甲烷分子的形状。
答案:C+624H CCH 4中C 中有4个电子与氢成键为SP 3杂化轨道,正四面体结构CH 4SP 3杂化2p y2p z2p x2sH1.4写出下列化合物的Lewis 电子式。
a.C 2H 4b.CH 3Clc.NH 3d.H 2Se.HNO 3f.HCHOg.H 3PO 4h.C 2H 6i.C 2H 2j.H 2SO 4 答案:a.C C H H HHCC HH HH或 b.H C H c.H N Hd.H S He.H O NO f.O C H Hg.O POO H H Hh.H C C HHH H HO P O O H HH或i.H C C Hj.O S O HH OH H或1.5下列各化合物哪个有偶极矩?画出其方向。

绪论令狐采学1.1 扼要归纳典型的以离子键形成的化合物与以共价键形成的化合物的物理性质。
答案:1.2NaCl与KBr各1mol溶于水中所得的溶液与NaBr及KCl各1mol溶于水中所得溶液是否相同?如将CH4 及CCl4各1mol混在一起,与CHCl3及CH3Cl各1mol的混合物是否相同?为什么?答案:NaCl与KBr各1mol与NaBr及KCl各1mol溶于水中所得溶液相同。
因为两者溶液中均为Na+ , K+ , Br-, Cl -离子各1mol。
由于CH4 与CCl4及CHCl3与CH3Cl在水中是以分子状态存在,所以是两组不同的混合物。
1.3 碳原子核外及氢原子核外各有几个电子?它们是怎样分布的?画出它们的轨道形状。
当四个氢原子与一个碳原子结合成甲烷(CH4)时,碳原子核外有几个电子是用来与氢成键的?画出它们的轨道形状及甲烷分子的形状。
答案:1.4写出下列化合物的Lewis电子式。
a. C2H4b. CH3Clc. NH3d. H2Se. HNO3f. HCHOg. H3PO4 h. C2H6i. C2H2 j. H2SO4答案:1.5 下列各化合物哪个有偶极矩?画出其方向。
a. I2b. CH2Cl2c. HBrd. CHCl3e. CH3OHf. CH3OCH3答案:1.6根据S与O的电负性差别,H2O与H2S相比,哪个有较强的偶极-偶极作用力或氢键?答案:电负性O > S , H2O与H2S相比,H2O有较强的偶极作用及氢键。
1.7下列分子中那些可以形成氢键?答案:d. CH3NH2e. CH3CH2OH1.8醋酸分子式为CH3COOH,它是否能溶于水?为什么?答案:能溶于水,因为含有C=O和OH两种极性基团,根据相似相容原理,可以溶于极性水。
第二章饱和烃卷心菜叶表面的蜡质中含有29个碳的直链烷烃,写出其分子式。
C29H602.2 用系统命名法(如果可能的话,同时用普通命名法)命名下列化合物,并指出(c)和(d) 中各碳原子的级数。
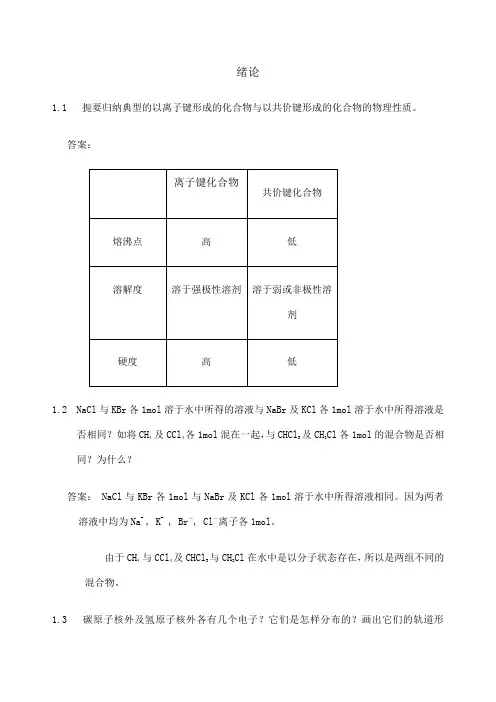
绪论1.1 扼要归纳典型的以离子键形成的化合物与以共价键形成的化合物的物理性质。
答案:1.2NaCl与KBr各1mol溶于水中所得的溶液与NaBr及KCl各1mol溶于水中所得溶液是否相同?如将CH4 及CCl4各1mol混在一起,与CHCl3及CH3Cl各1mol的混合物是否相同?为什么?答案: NaCl与KBr各1mol与NaBr及KCl各1mol溶于水中所得溶液相同。
因为两者溶液中均为Na+ , K+ , Br-, Cl-离子各1mol。
由于CH4 与CCl4及CHCl3与CH3Cl在水中是以分子状态存在,所以是两组不同的混合物。
1.3 碳原子核外及氢原子核外各有几个电子?它们是怎样分布的?画出它们的轨道形状。
当四个氢原子与一个碳原子结合成甲烷(CH4)时,碳原子核外有几个电子是用来与氢成键的?画出它们的轨道形状及甲烷分子的形状。
答案:1.4 写出下列化合物的Lewis电子式。
a. C2H4b. CH3Cl c. NH3d. H2S e. HNO3f. HCHOg. H3PO4h. C2H6i. C2H2j. H2SO4答案:1.5 下列各化合物哪个有偶极矩?画出其方向。
a. I2 b. CH2Cl2c. HBrd. CHCl3e. CH3OH f. CH3OCH3答案:1.6根据S与O的电负性差别,H2O与H2S相比,哪个有较强的偶极-偶极作用力或氢键?答案:电负性 O > S , H2O与H2S相比,H2O有较强的偶极作用及氢键。
1.7下列分子中那些可以形成氢键?答案:d. CH3NH2e. CH3CH2OH1.8 醋酸分子式为CH 3COOH ,它是否能溶于水?为什么?答案:能溶于水,因为含有C=O 和OH 两种极性基团,根据相似相容原理,可以溶于极性水。
第二章 饱和烃2.1 卷心菜叶表面的蜡质中含有29个碳的直链烷烃,写出其分子式。
C 29H 602.2 用系统命名法(如果可能的话,同时用普通命名法)命名下列化合物,并指出(c)和(d) 中各碳原子的级数。

目录第一章绪论 (1)第二章饱和烃 (2)第三章不饱和烃 (6)第四章环烃 (14)第五章旋光异构 (23)第六章卤代烃 (28)第七章波谱法在有机化学中的应用 (33)第八章醇酚醚 (43)第九章醛、酮、醌 (52)第十章羧酸及其衍生物 (63)第十一章取代酸 (71)第十二章含氮化合物 (77)第十三章含硫和含磷有机化合物 (85)第十四章碳水化合物 (88)第十五章氨基酸、多肽与蛋白质 (99)第十六章类脂化合物 (104)第十七章杂环化合物 (113)Fulin 湛师第一章 绪论1.1扼要归纳典型的以离子键形成的化合物与以共价键形成的化合物的物理性质。
答案:1.2 NaCl 与KBr 各1mol 溶于水中所得的溶液与NaBr 及KCl 各1mol 溶于水中所得溶液是否相同?如将CH 4及CCl 4各1mol 混在一起,与CHCl 3及CH 3Cl 各1mol 的混合物是否相同?为什么? 答案:NaCl 与KBr 各1mol 与NaBr 及KCl 各1mol 溶于水中所得溶液相同。
因为两者溶液中均为Na +,K +,Br -, Cl -离子各1mol 。
由于CH 4与CCl 4及CHCl 3与CH 3Cl 在水中是以分子状态存在,所以是两组不同的混合物。
1.3碳原子核外及氢原子核外各有几个电子?它们是怎样分布的?画出它们的轨道形状。
当四个氢原子与一个碳原子结合成甲烷(CH 4)时,碳原子核外有几个电子是用来与氢成键的?画出它们的轨道形状及甲烷分子的形状。
答案:C+624H CCH 4中C 中有4个电子与氢成键为SP 3杂化轨道,正四面体结构CH 4SP 3杂化2p y2p z2p x2sH1.4写出下列化合物的Lewis 电子式。
a.C 2H 4b.CH 3Clc.NH 3d.H 2Se.HNO 3f.HCHOg.H 3PO 4h.C 2H 6i.C 2H 2j.H 2SO 4 答案:a.C C H HCC HH HH或 b.H C H c.H N Hd.H S H e.H O NOf.O C H Hg.O P O O H H Hh.H C C HHH H HO P O O H HH或i.H C C Hj.O S O HH OS H H或1.5下列各化合物哪个有偶极矩?画出其方向。


目录之阿布丰王创作Fulin 湛师第一章绪论扼要归纳典型的以离子键形成的化合物与以共价键形成的化合物的物理性质。
答案:1.2 NaClCH4及CCl4各1mol混在一起,与CHCl3及CH3Cl各1mol的混合物是否相同?为什么?答案:NaCl与KBr各1mol与NaBr及KCl各1mol溶于水中所得溶液相同。
因为两者溶液中均为Na+,K+,Br-, Cl-离子各1mol。
由于CH4与CCl4及CHCl3与CH3Cl在水中是以分子状态存在,所以是两组分歧的混合物。
1.3碳原子核外及氢原子核外各有几个电子?它们是怎样分布的?画出它们的轨道形状。
当四个氢原子与一个碳原子结合成甲烷(CH4)时,碳原子核外有几个电子是用来与氢成键的?画出它们的轨道形状及甲烷分子的形状。
2H433 23 3PO4 2H6 2H2 2SO422Cl2333OCH31.6 22答案:电负性O>S,H 2O 与H 2S 相比,H 2O 有较强的偶极作用及氢键。
1.7 下列分子中那些可以形成氢键?a.H 2b. CH 3CH 3c. SiH 4d. CH 3NH 2e. CH 3CH 2OHf. CH 3OCH 3 答案:3NH 23CH 2OH1.8 醋酸分子式为CH 3COOH ,它是否能溶于水?为什么?答案:能溶于水,因为含有C=O 和OH 两种极性基团,根据相似相容原理,可以溶于极性水。
第二章饱和烃2.1 卷心菜叶概况的蜡质中含有29个碳的直链烷烃,写出其分子式。
答案:C 29H 602.2 用系统命名法(如果可能的话,同时用普通命名法)命名下列化合物,并指出(c)和(d)中各碳原子的a. 2,4,4-三甲基-5-正丁基壬烷 5-butyl -2,4,4-trimethylnonane b. 正己烷 hexane c.3,3-二乙基戊烷 3,3-diethylpentane-甲基-5-异丙基辛烷 5-isopropyl -3-methyloctane e.2-甲基丙烷(异丁烷) 2-methylpropane(iso-butane)f.2,2-二甲基丙烷(新戊烷) 2,2-dimethylpropane(neopentane)-甲基戊烷3-methylpentane h.2-甲基-5-乙基庚烷5-ethyl -2-methylheptane答案:a=b=d=e 为2,3,5-三甲基己烷 c=f 为2,3,4,5-四甲基己烷2.4 写出下列各化合物的结构式,假如某个名称违反系统命名原则,予以更正。

目录第一章绪论 (1)第二章饱和烃 (2)第三章不饱和烃 (6)第四章环烃 (14)第五章旋光异构 (23)第六章卤代烃 (28)第七章波谱法在有机化学中的应用 (33)第八章醇酚醚 (43)第九章醛、酮、醌 (52)第十章羧酸及其衍生物 (63)第十一章取代酸 (71)第十二章含氮化合物 (77)第十三章含硫和含磷有机化合物 (85)第十四章碳水化合物 (88)第十五章氨基酸、多肽与蛋白质 (99)第十六章类脂化合物 (104)第十七章杂环化合物 (113)Fulin 湛师第一章 绪论1.1扼要归纳典型的以离子键形成的化合物与以共价键形成的化合物的物理性质。
答案:1.2 NaCl 与KBr 各1mol 溶于水中所得的溶液与NaBr 及KCl 各1mol 溶于水中所得溶液是否相同?如将CH 4及CCl 4各1mol 混在一起,与CHCl 3及CH 3Cl 各1mol 的混合物是否相同?为什么? 答案:NaCl 与KBr 各1mol 与NaBr 及KCl 各1mol 溶于水中所得溶液相同。
因为两者溶液中均为Na +,K +,Br -, Cl -离子各1mol 。
由于CH 4与CCl 4及CHCl 3与CH 3Cl 在水中是以分子状态存在,所以是两组不同的混合物。
1.3碳原子核外及氢原子核外各有几个电子?它们是怎样分布的?画出它们的轨道形状。
当四个氢原子与一个碳原子结合成甲烷(CH 4)时,碳原子核外有几个电子是用来与氢成键的?画出它们的轨道形状及甲烷分子的形状。
答案:C+624H CCH 4中C 中有4个电子与氢成键为SP 3杂化轨道,正四面体结构CH 4SP 3杂化2p y2p z2p x2sH1.4写出下列化合物的Lewis 电子式。
a.C 2H 4b.CH 3Clc.NH 3d.H 2Se.HNO 3f.HCHOg.H 3PO 4h.C 2H 6i.C 2H 2j.H 2SO 4 答案:a.C C H H HHCC HH HH或 b.H C H c.H N Hd.H S He.H O NO f.O C H Hg.O POO H H Hh.H C C HHH H HO P O O H HH或i.H C C Hj.O S O HH OH H或1.5下列各化合物哪个有偶极矩?画出其方向。
绪论1.1 扼要归纳典型的以离子键形成的化合物与以共价键形成的化合物的物理性质。
1.2NaCl与KBr各1mol溶于水中所得的溶液与NaBr及KCl各1mol溶于水中所得溶液是否相同?如将CH4及CCl4各1mol混在一起,与CHCl3及CH3Cl各1mol的混合物是否相同?为什么?答案:NaCl与KBr各1mol与NaBr及KCl各1mol溶于水中所得溶液相同。
因为两者溶液中均为Na+ , K+ , Br-, Cl-离子各1mol。
由于CH4 与CCl4及CHCl3与CH3Cl在水中是以分子状态存在,所以是两组不同的混合物。
1.3 碳原子核外及氢原子核外各有几个电子?它们是怎样分布的?画出它们的轨道形状。
当四个氢原子与一个碳原子结合成甲烷(CH4)时,碳原子核外有几个电子是用来与氢成键的?画出它们的轨道形状及甲烷分子的形状。
答案:1.4 写出下列化合物的Lewis电子式。
a. C2H4b. CH3Clc. NH3d. H2Se. HNO3f. HCHOg. H3PO4h. C2H6i. C2H2 j. H2SO4答案:1.5 下列各化合物哪个有偶极矩?画出其方向。
a. I2b. CH2Cl2c. HBrd. CHCl3e. CH3OHf. CH3OCH3答案:1.6根据S与O的电负性差别,H2O与H2S相比,哪个有较强的偶极-偶极作用力或氢键?答案:电负性O > S , H2O与H2S相比,H2O有较强的偶极作用及氢键。
1.7下列分子中那些可以形成氢键?答案:d. CH3NH2e. CH3CH2OH1.8醋酸分子式为CH3COOH,它是否能溶于水?为什么?答案:能溶于水,因为含有C=O和OH两种极性基团,根据相似相容原理,可以溶于极性水。
第二章饱和烃2.1卷心菜叶表面的蜡质中含有29个碳的直链烷烃,写出其分子式。
C29H602.2用系统命名法(如果可能的话,同时用普通命名法)命名下列化合物,并指出(c)和(d) 中各碳原子的级数。
构思新颖,品质一流,适合各个领域,谢谢采纳目录第一章绪论 (1)第二章饱和烃 (2)第三章不饱和烃 (6)第四章环烃 (14)第五章旋光异构 (23)第六章卤代烃 (28)第七章波谱法在有机化学中的应用 (33)第八章醇酚醚 (43)第九章醛、酮、醌 (52)第十章羧酸及其衍生物 (63)第十一章取代酸 (71)第十二章含氮化合物 (78)第十三章含硫和含磷有机化合物 (86)第十四章碳水化合物 (89)第十五章氨基酸、多肽与蛋白质 (100)第十六章类脂化合物 (105)第十七章杂环化合物 (114)Fulin 湛师第一章 绪论1.1扼要归纳典型的以离子键形成的化合物与以共价键形成的化合物的物理性质。
答案:1.2 NaCl 与KBr 各1mol 溶于水中所得的溶液与NaBr 及KCl 各1mol 溶于水中所得溶液是否相同?如将CH 4及CCl 4各1mol 混在一起,与CHCl 3及CH 3Cl 各1mol 的混合物是否相同?为什么? 答案:NaCl 与KBr 各1mol 与NaBr 及KCl 各1mol 溶于水中所得溶液相同。
因为两者溶液中均为Na +,K +,Br -, Cl -离子各1mol 。
C+624H CCH 4中C 中有4个电子与氢成键为SP 3杂化轨道,正四面体结构CH 4SP 3杂化2p y2p z2p x2sH1.4写出下列化合物的Lewis 电子式。
a.C 2H 4b.CH 3Clc.NH 3d.H 2Se.HNO 3f.HCHOg.H 3PO 4h.C 2H 6i.C 2H 2j.H 2SO 4 答案:a.C C H H HHCC HH HH或 b.H C H c.H N Hd.H S He.H O NO f.O C H Hg.OPO O H H Hh.H C C HHH H HO P O O H HH或i.H C C Hj.O S O HH OH H或1.5下列各化合物哪个有偶极矩?画出其方向。
目录之老阳三干创作第一章绪论0第二章饱和烃1第三章不饱和烃5第四章环烃13第五章旋光异构21第六章卤代烃26第七章波谱法在有机化学中的应用31第八章醇酚醚41第九章醛、酮、醌50第十章羧酸及其衍生物61第十一章取代酸68第十二章含氮化合物74第十三章含硫和含磷有机化合物82第十四章碳水化合物85第十五章氨基酸、多肽与蛋白质96第十六章类脂化合物101第十七章杂环化合物109Fulin 湛师第一章 绪论1.1扼要归纳典型的以离子键形成的化合物与以共价键形成的化合物的物理性质。
答案:1.2 NaCl 相同?如将CH4及CCl4各1mol 混在一起,与CHCl3及CH3Cl 各1mol 的混合物是否相同?为什么? 答案:NaCl 与KBr 各1mol 与NaBr 及KCl 各1mol 溶于水中所得溶液相同。
因为两者溶液中均为Na+,K+,Br -, Cl -离子各1mol 。
由于CH4与CCl4及CHCl3与CH3Cl 在水中是以分子状态存在,所以是两组分歧的混合物。
1.3碳原子核外及氢原子核外各有几个电子?它们是怎样分布的?画出它们的轨道形状。
当四个氢原子与一个碳原子结合成甲烷(CH4)时,碳原子核外有几个电子是用来与氢成键的?画出它们的轨道形状及甲烷分子的形状。
答案:C+624HCCH 4中C 中有4个电子与氢成键为SP 3杂化轨道,正四面体结构CH 4SP 3杂化2p y2p z2p x2sH1.4写出下列化合物的Lewis 电子式。
a.C2H4b.CH3Clc.NH3d.H2Se.HNO3f.HCHOg.H3PO4h.C2H6 i.C2H2 j.H2SO4答案:a.C C H H H HCC HH HH 或 b.H C H H c.H N H Hd.H S H e.H O NOf.OC H Hg.O P OO O H H Hh.H C C HHH H HO P O O H HH或i.H C C Hj.O S O HH OOH H或1.5下列各化合物哪个有偶极矩?画出其方向。
绪论之袁州冬雪创作1.1 扼要归纳典型的以离子键形成的化合物与以共价键形成的化合物的物感性质.答案:1.2NaCl与KBr各1mol溶于水中所得的溶液与NaBr及KCl各1mol溶于水中所得溶液是否相同?如将CH4 及CCl4各1mol混在一起,与CHCl3及CH3Cl各1mol的混合物是否相同?为什么?答案: NaCl与KBr各1mol与NaBr及KCl各1mol溶于水中所得溶液相同.因为二者溶液中均为Na+ , K+ , Br -, Cl-离子各1mol.由于CH4 与CCl4及CHCl3与CH3Cl在水中是以分子状态存在,所以是两组分歧的混合物.1.3 碳原子核外及氢原子核外各有几个电子?它们是怎样分布的?画出它们的轨道形状.当四个氢原子与一个碳原子连系成甲烷(CH4)时,碳原子核外有几个电子是用来与氢成键的?画出它们的轨道形状及甲烷分子的形状.答案:1.4写出下列化合物的Lewis电子式.a. C2H4b. CH3Clc. NH3d. H2Se. HNO3f. HCHOg. H3PO4 h. C2H6i. C2H2 j. H2SO4答案:1.5 下列各化合物哪个有偶极矩?画出其方向.a. I2b. CH2Cl2c. HBrd. CHCl3e. CH3OHf. CH3OCH3答案:1.6根据S与O的电负性不同,H2O与H2S相比,哪个有较强的偶极-偶极作用力或氢键?答案:电负性 O > S , H2O与H2S相比,H2O有较强的偶极作用及氢键.1.7下列分子中那些可以形成氢键?答案:d. CH3NH2e. CH3CH2OH1.8醋酸分子式为CH3COOH,它是否能溶于水?为什么?答案:能溶于水,因为含有C=O和OH两种极性基团,根据相似相容原理,可以溶于极性水.第二章饱和烃2.1卷心菜叶概况的蜡质中含有29个碳的直链烷烃,写出其分子式.C29H602.2 用系统定名法(如果可以的话,同时用普通定名法)定名下列化合物,并指出(c)和(d) 中各碳原子的级数.a.CH 3(CH 2)3CH(CH 2)3CH 3C(CH 3)2CH 2CH(CH 3)2b.C H H C H H C H H H C H H C H H C H H Hc.CH 322CH 3)2CH 23d.CH 3CH 2CH CH 2CH 3CH CH CH 2CH 2CH 3CH 3CH 3 e.C CH 3H 3C CH 3Hf.(CH 3)4Cg.CH 3CHCH 2CH 3C 2H 5h.(CH 3)2CHCH 2CH 2CH(C 2H 5)21。
目录第一章绪论.......................................................................................................................................第二章饱和烃...................................................................................................................................第三章不饱和烃...............................................................................................................................第四章环烃.......................................................................................................................................第五章旋光异构...............................................................................................................................第六章卤代烃...................................................................................................................................第七章波谱法在有机化学中的应用...............................................................................................第八章醇酚醚...................................................................................................................................第九章醛、酮、醌...........................................................................................................................第十章羧酸及其衍生物...................................................................................................................第十一章取代酸...............................................................................................................................第十二章含氮化合物.......................................................................................................................第十三章含硫和含磷有机化合物...................................................................................................第十四章碳水化合物.......................................................................................................................第十五章氨基酸、多肽与蛋白质...................................................................................................第十六章类脂化合物.......................................................................................................................第十七章杂环化合物....................................................................................................................... Fulin 湛师第一章绪论1.1扼要归纳典型的以离子键形成的化合物与以共价键形成的化合物的物理性质。