β-葡萄糖苷酶测定试剂盒使用说明
- 格式:pdf
- 大小:95.82 KB
- 文档页数:4

葡萄糖苷酶(NAG)测定的标准操作程序【应用范围】体外检测血清和尿液中NAG活性浓度。
【适用仪器】Olympus AU-27全自动生化分析仪。
【程序改变】严格遵循仪器、试剂说明书及校准品使用说明。
【方法学原理】NAG催化PNP - NAG水解,生成产物对硝基苯酚(PNP),经一定时间后终止反应,并使PNP显色,在规定波长下检测PNP引起的吸光度高值,推算样品中的NAG活性。
在尿NAG测定的同时,测定尿肌酐(Cr )浓度,计算出NAG活性(U/L)与Cr浓度(mmol/L )的比值,借以消除尿液浓缩和稀释浓度对结果的影响。
【试剂】1.成份:低物液每升内含:对硝基苯-0-D氨基葡萄糖苷9.8克、18 -冠5醚50ml、叠氮钠1克;缓冲液每升内含:PH4.6柠檬酸-柠檬酸三钠1mmol/L、叠氮钠1克;终止液每升内含:氢氧化钠4.0克。
2.校准品:Electrollyte CAL 1、Electrollyte CAL 2.3.质控品:Randox Assayed Multiseral Level 2 and Level 3.【标本收集与准备】1.血清或血浆标本根据实验室标准采集程序采集标本,适用标本为血清或肝素抗凝血浆(肝素钠抗凝结果高0.5mmol/l),不可从正在静脉滴注手臂上采血,上机标本不能有凝块,样品采集后2天内离心标本,分离血清,血清或血浆标本室温保存4天,冷藏7天,冷冻保存6个月。
血清或血浆钠结果高于线性不建议稀释。
2.尿液标本定时或随机尿标本,不可加防腐剂,根据实验室标准采集程序采集标本,室温保存24小时,冷藏7天,冷冻保存6个月。
尿钠高于线性可用双蒸水对倍稀释。
【操作步骤】1. 仪器测定参数设置2. 试剂准备:将准备好的试剂置仪器试剂盘中(8C )。
3. 校准校准物的准备:将校准物从冰箱取出,冻干校准物按说明书加入蒸馏水复溶,轻轻颠倒混匀3次,不可用力震摇,室温放置30分钟至完全溶解;液体校准物从冰箱取出,室温放置15分钟以平衡至室温。

葡萄糖测定试剂盒(葡萄糖氧化酶法)
适用范围:本试剂用于体外定量测定人血清中的葡萄糖含量。
1.1型号规格
产品组成
2.1 外观
2.1.1 试剂为淡粉红色透明液体,无混浊,无未溶解物。
2.1.2 校准品为无色透明液体,无混浊,无未溶解物。
2.1.3 标签内容清晰,字迹牢固不易脱落。
2.2 试剂装量
液体试剂的净含量不少于标示值。
2.3 试剂空白吸光度
A≤0.15(光径1.0cm,500nm±20nm波长)。
2.4 分析灵敏度
测定1mmol/L 被测物,吸光度变化在0.05~0.08范围内。
2.5 线性区间
2.5.1 [0.1,28]mmol/L([1.8,500] mmol/L)。
在规定的线性范围内,测定值与样本浓度值的相关系数(r)应不低于0.990。
2.5.2[0.1,1]mmol/L范围内,线性绝对偏差应不超过±0.1mmol/L;(1,28]mmol/L范围内,线性相对偏差应不超过±10%。
2.6 精密度
2.6.1 重复性
变异系数CV≤5.0%。
2.6.2 批间差
批间相对极差≤6.0%。
2.7 准确度
相对偏差在±10%范围内(测试国家标准物质GBW(E)090544/GBW(E)090545 /GBW(E)090546)。
2.8 稳定性
原装试剂2℃~8℃保存,有效期12个月,有效期满后2个月内测定结果应符合2.1、2.3、2.4、2.5、2.6.1、和2.7要求。

N-乙酰-β-D-氨基葡萄糖苷酶(NAG)测定试剂盒(MPT法)适用范围:本产品用于体外定量测定人尿液中N-乙酰-β-D-氨基葡萄糖苷酶的含量。
1.1 规格试剂1(R1):2×45mL、试剂2(R2): 2×15mL;校准品(选配):1×2mL;质控品(选配):1×2mL。
1.2 组成试剂盒由试剂、质控品(选配)和校准品(选配)组成。
试剂1(R1):柠檬酸缓冲液(PH=4.5),200mmol/L。
试剂2(R2):6-甲基-2吡啶-N-乙酰-1-硫代-β-D-氨基葡萄糖苷,6mg/dl。
校准品:冻干品,含NAG:(100~200)IU/L、磷酸盐缓冲液:50mM、乳糖:5%、酶稳定剂:1%。
质控品:冻干品,含NAG:(5~25)IU/L、磷酸盐缓冲液:50mM、乳糖:5%、酶稳定剂:1%。
2.1 外观液体双试剂:R1:无色澄清液体;R2:无色或淡黄色液体。
校准品:冻干品,溶解后为无色液体。
质控品:冻干品,溶解后呈黄色匀质液体。
2.2 装量:不得低于标示体积。
2.3 溯源性:根据GB/T 21415及有关规定提供校准品的来源、赋值过程及测量不确定度等内容,该校准品溯源至Inner standard。
<1.5ABS ( 1cm;340nm;37℃)。
2.4 空白吸光度: A(空白)2.5 灵敏度:浓度为100IU/L时,吸光度变化△A/min>0.01 ABS。
2.6 线性:测定结果在(0,200]IU/L范围内r≥0.996;测定结果(5,200] IU/L 时相对偏差应≤15%,测定结果(0,5] IU/L时绝对偏差应<0.75 IU/L。
2.7 精密度:用(5~12)IU/L和(15~25)IU/L的样本各重复检测10次,其变异系数CV<5%。
2.8 批间差:取三个批号试剂,分别测定浓度接近正常值上限的样本,每个批号测3次,不同批号之间测定结果的相对极差应<10%。

乙酰-β-D-氨基葡萄糖苷酶测定试剂盒(CNP-NAG底物法)产品技术要求senmeixikemaN-乙酰-β-D-氨基葡萄糖苷酶测定试剂盒(CNP-NAG底物法)O-适用范围:用于体外定量测定人血清或尿液中N-乙酰-β-D-氨基葡萄糖苷酶的活性。
1.1规格a)试剂1:1×50ml,试剂2:1×10ml;b)试剂1:4×60ml,试剂2:1×48ml;c)试剂1:1×60ml,试剂2:1×12ml;d)试剂1:1×70ml,试剂2:1×14ml;e)试剂1:1×40ml,试剂2:1×8ml;f)试剂1:1×80ml,试剂2:1×16ml;g)试剂1:1×25ml,试剂2:1×5ml。
1.2 组成试剂主要组分见表1:2.1 净含量应不低于试剂瓶标示装量。
2.2 外观试剂1:无色或淡黄色透明溶液,试剂2:淡黄色透明溶液。
2.3 试剂空白2.3.1 试剂空白吸光度在405nm处测定试剂空白吸光度,应不超过1.2。
2.3.2 试剂空白吸光度变化率试剂空白吸光度变化率△A/min应不超过0.1。
2.4 分析灵敏度测试380U/L的被测物时,吸光度变化率(ΔA/min)应不低于0.005。
2.5 准确度回收率应在85%~115%范围内。
2.6 重复性变异系数(CV)应不超过5%。
2.7 线性2.7.1在[2,400]U/L范围内,线性回归的相关系数不低于0.990;2.7.2测试浓度(60,400]U/L的样品,相对偏差应不超过±15%;测试浓度[2,60]U/L的样品,绝对偏差应不超过±9U/L。
2.8 批间差相对极差应小于10%。
2.9 稳定性取在2℃~8℃条件下贮存达到18个月后的试剂进行检测,应符合本技术要求2.2、2.3、2.4、2.5、2.6、2.7之规定。

N-乙酰-β-D-氨基葡萄糖苷酶测定试剂盒(MPT底物法)适用范围:本试剂用于体外定量测定人血清或尿液中的N-乙酰-β-D-氨基葡萄糖苷酶含量。
1.1规格液体双剂型试剂1(R1):60mL×2,试剂2(R2):20mL×2;试剂1(R1):60mL×1,试剂2(R2):20mL×1;试剂1(R1):45mL×2,试剂2(R2):15mL×2;试剂1(R1):30mL×2,试剂2(R2):10mL×2;选配校准品:1mL×1;选配质控品(2个水平):1mL×2。
1.2规格划分说明根据净含量划分规格。
1.3主要组成成分试剂盒由试剂1(R1)液体、试剂2(R2)液体、校准品液体(选配)和质控品液体(选配)组成。
1.3.1 试剂1(R1)液体:柠檬酸缓冲液 0.1mmol/L1.3.2试剂2(R2)液体:MPT-NAG 50mmol/L1.3.3 校准品液体:人血清:10U/L~80U/L(每批定值)1.3.4质控品液体:人血清定值范围:水平1:10U/L~50U/L;水平2:50U/L~150U/L。
(每批定值)2.1 外观试剂盒中各组件的外观应满足:a)试剂1(R1)应为无色透明溶液,无杂质、无絮状物,外包装完整无破损;b)试剂2(R2)应为无色透明溶液,无杂质、无絮状物,外包装完整无破损;c)校准品应为无色至浅黄色透明溶液,无杂质、无絮状物,外包装完整无破损。
d)质控品应为无色至浅黄色透明溶液,无杂质、无絮状物,外包装完整无破损。
2.2 试剂空白吸光度和试剂空白吸光度变化率在波长340nm处(320~360nm)(光径1cm),试剂空白吸光度(A)应≤0.4000。
试剂空白吸光度变化率(△A/min)应≤0.0200。
2.3准确度测定N-乙酰-β-D-氨基葡萄糖苷酶纯品,回收率应在80%~120%范围内。

N-乙酰-β-D-氨基葡萄糖苷酶(NAG)测定试剂盒(MPT底物法)适用范围:用于体外定量测定人体尿液中N-乙酰-β-D-氨基葡萄糖苷酶的活性。
1.1试剂盒包装规格试剂1:1×15ml,试剂2:1×5ml;试剂1:2×54ml,试剂2:2×18ml;试剂1:3×39ml,试剂2:3×13ml;试剂1:4×54ml,试剂2:4×18ml;试剂1:2×300ml,试剂2:1×200ml;试剂1:2×30ml,试剂2:2×10ml。
校准品(选配,冻干品):1×1ml;1×2ml。
质控品(选配,冻干品):1×1ml;1×2ml。
1.2试剂盒主要组成成分2.1 外观试剂1:无色澄清液体;试剂2:无色或淡黄色液体。
校准品:冻干品,溶解后为无色至黄色液体。
质控品:冻干品,溶解后为无色至黄色液体。
2.2 净含量液体试剂的净含量不得低于标示体积。
2.3试剂空白2.3.1试剂空白吸光度在37℃、340nm波长、1cm光径条件下,试剂空白吸光度应不大于1.5。
2.3.2试剂空白吸光度变化率在37℃、340 nm波长、1cm光径条件下,试剂空白吸光度变化率(△A/min)应不大于0.05。
2.4 分析灵敏度测定活性为100U/L样本时,吸光度变化率(ΔA/min)应不小于0.01。
2.5 线性范围在(0,200)U/L线性范围内,线性相关系数r应不小于0.996。
在(20,200)U/L范围内的线性相对偏差应不大于±15%;在(0,20] U/L范围内的线性绝对偏差应不大于±3U/L。
2.6 重复性重复测试两份高低浓度的样本,所得结果的变异系数(CV%)应不大于5%。
2.7 批间差不同批号试剂测试同一份样本,测定结果的批间相对极差应不大于10%。

N-乙酰-β-D-氨基葡萄糖苷酶测定标准操作程序1.摘要N-乙酰-β-D-氨基葡萄糖苷酶检测主要用于肾脏疾病、肝硬化和慢性活动性肝炎的诊断。
2.适用范围程序适用于日立7600自动生化分析仪检测尿液中NAG的浓度。
3.职责使用日立7600自动生化分析仪进行测定NAG浓度的工作人员要严格按照本SOP程序进行,室负责人监督管理;本SOP的改动,可由任一使用本SOP的工作人员提出,并报经生化室负责人、科主任签字批准生效。
4.检测方法上海科华生物工程股份有限公司生产的N-乙酰-β-D-氨基葡萄糖苷酶(NAG)试剂盒采用的是速率法。
5.原理26N---O---β−+−→−DN NAG-H-氨基葡萄糖苷乙酰硫代吡啶甲基巯基吡啶氨基葡萄糖-甲基-乙酰62--2--N-乙酰-β-D-氨基葡萄糖苷酶(NAG)催化底物6-甲基-2-硫代吡啶-N-乙酰-β-D-氨基葡萄糖苷(MPT-NAG)水解产生6-甲基-2-巯基吡啶(MPT)和N-乙酰-氨基葡萄糖,MPT在340nm附近有吸收峰,所以,可以通过监测340nm附近的吸光度变化值计算样本中的N-乙酰-β-D-氨基葡萄糖苷酶活力。
6.仪器日立7600自动生化分析仪7.试剂7.1试剂来源:上海科华生物工程股份有限公司提供7.2试剂瓶内主要成分:柠檬酸缓冲液、Tris6-甲基-2-硫代吡啶-N-乙酰-β-D-氨基葡萄糖苷、防腐剂7.3试剂稳定性:试剂避光保存于2-8℃,若无污染,可稳定至失效期,本试剂有效期为12个月。
试剂不可冰冻。
7.4试剂准备:试剂为即用式。
8.标准品和质量控制8.1校准程序:使用上海科华公司提供的K校准因子对自动分析仪进行校准。
按照公司标准品使用要求,并以9g/L氯化钠溶液或去离子水为空白,经校准测定,仪器自动对标准品响应量通过合适的数学模型绘制校准曲线。
8.2质控品:上海科华公司提供的生化质控血清做为室内质控品。
每日在测定前做一次质控。
该质控品为干粉包装,在2-8℃冰箱可稳定到失效期,使用前用5ml去离子水复溶,待质控物充分溶解(大约30分钟)后使用。

葡萄糖测定试剂盒使用说明书(OX法)GLUCOSE MENSURATION REAGENT KIT OPERATION INSTRUCTION[用途]本试剂用于体外定量测定人血清、血浆或尿液中葡萄糖的浓度。
葡萄糖的准确测定对于诊断和处理高糖血症和低糖血症是十分重要的。
葡萄糖浓度的升高可由糖尿病、葡萄糖摄入过量、柯兴氏综合症和脑血管意外等引起。
葡萄糖浓度的降低则可由胰岛瘤、胰岛素过量、先天性碳水化合物代谢障碍或厌食等引起。
通常在查找这些病症的起因时,还将各种耐量试验和刺激试验与葡萄糖测定一同进行。
[方法原理]采用葡萄糖氧化酶(Glucose oxidase,GOD)偶联Trinder反应。
葡萄糖氧化酶催化葡萄糖的氧化产生葡萄糖酸和过氧化氢,后者与4-氨基安替比林和对羟基苯甲酸经过氧化物酶的作用(Trinder反应)形成红色的醌亚胺化合物,从而引起500nm处吸光度的上升,此种变化与样本中的葡萄糖浓度成正比。
双光束分析时,空白波长可设于660-700nm。
[产品规格]规格1(R1:4×60ml,R2:1×60ml),包装总量:300ml规格2(R1:2×80ml,R2:2×20ml),包装总量:200ml规格3(R1:4×20ml,R2:1×20ml),包装总量:100ml规格4(R1:4×1000ml,R2:1×1000ml),包装总量:5000ml[试剂成份]试剂1 对羟基苯甲酸盐25mmol/L 磷酸盐缓冲液100mmol/L试剂2 葡萄糖氧化酶>1KU/ml 过氧化物酶>1.5KU/L4-氨基安替比林0.3mmol/L 磷酸盐缓冲液100mmol/L[试剂制备]底物启动方式(双试剂模式)试剂1和试剂2均为液体制品,可直接使用。
样本启动方式(单试剂模式)将试剂1和试剂2以4:1的比例混匀。
[试剂稳定性和贮存]在2-8℃避光条件下未开封的试剂,可稳定12个月。
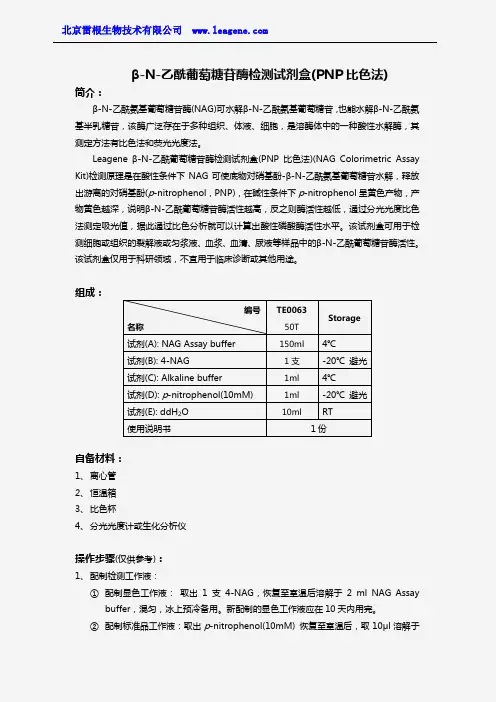
β-N-乙酰葡萄糖苷酶检测试剂盒(PNP 比色法)简介:β-N-乙酰氨基葡萄糖苷酶(NAG)可水解β-N-乙酰氨基葡萄糖苷,也能水解β-N-乙酰氨基半乳糖苷,该酶广泛存在于多种组织、体液、细胞,是溶酶体中的一种酸性水解酶,其测定方法有比色法和荧光光度法。
Leagene β-N-乙酰葡萄糖苷酶检测试剂盒(PNP 比色法)(NAG Colorimetric Assay Kit)检测原理是在酸性条件下NAG 可使底物对硝基酚-β-N-乙酰氨基葡萄糖苷水解,释放出游离的对硝基酚(p -nitrophenol ,PNP),在碱性条件下p -nitrophenol 呈黄色产物,产物黄色越深,说明β-N-乙酰葡萄糖苷酶活性越高,反之则酶活性越低,通过分光光度比色法测定吸光值,据此通过比色分析就可以计算出酸性磷酸酶活性水平。
该试剂盒可用于检测细胞或组织的裂解液或匀浆液、血浆、血清、尿液等样品中的β-N-乙酰葡萄糖苷酶活性。
该试剂盒仅用于科研领域,不宜用于临床诊断或其他用途。
组成:自备材料:1、 离心管2、 恒温箱3、 比色杯4、 分光光度计或生化分析仪操作步骤(仅供参考):1、 配制检测工作液:① 配制显色工作液: 取出1支4-NAG ,恢复至室温后溶解于2 ml NAG Assaybuffer ,混匀,冰上预冷备用。
新配制的显色工作液应在10天内用完。
② 配制标准品工作液:取出p -nitrophenol(10mM) 恢复至室温后,取10μl 溶解于编号 名称TE0063 50T Storage试剂(A): NAG Assay buffer 150ml 4℃ 试剂(B): 4-NAG 1支 -20℃ 避光 试剂(C): Alkaline buffer 1ml 4℃ 试剂(D): p -nitrophenol(10mM) 1ml -20℃ 避光 试剂(E): ddH 2O 10mlRT 使用说明书1份ACP Assay buffer,使p-nitrophenol达到3mM。

N-乙酰-β-D-氨基葡萄糖苷酶(NAG)测定试剂盒(MPT法)适用范围:该产品用于体外定量测定人尿液中N-乙酰-β-D-氨基葡萄糖苷酶的活性。
1.1 产品规格1.2 组成成分1.2.1 试剂组成试剂1:柠檬酸缓冲液(PH=4.5),200mmol/L试剂2:6-甲基-2吡啶-N-乙酰-1-硫代-β-D-氨基葡萄糖苷,6mg/dL。
1.2.2 校准品的组成冻干品,含NAG(30IU/L)、磷酸盐缓冲液(50mM)、乳糖(50g/L)。
定值范围为:20-50U/L。
1.2.3质控品的组成冻干品,含NAG(10IU/L)、磷酸盐缓冲液(50mM)、乳糖(50g/L)。
定值范围为:5-25U/L。
2.1 外观液体双试剂:试剂1:无色至淡黄色液体;试剂2:无色至淡黄色液体。
校准品:冻干品,溶解后为无色至淡黄色液体。
质控品:冻干品,溶解后呈黄色匀质液体。
2.2 装量不得低于标示体积。
2.3 空白吸光度空白吸光度应≤1.02.4 空白吸光度变化率空白吸光度变化率应≤0.05。
2.5 灵敏度浓度为100IU/L时,吸光度变化(△A/min)应≥0.01 。
2.6 线性:在(0,200.0]IU/L线性范围内,线性相关系数r 应≥0.990;在(0,50]IU/L范围内绝对偏差不超过5IU/L;在(50,200]U/L范围内的相对偏差不超过±10%。
2.7 精密度:变异系数CV应≤5%。
2.8 批间差:不同批号之间测定结果的相对极差应≤10%。
2.9 准确度回收试验:回收率在90%-110%之间。
2.10 质控品赋值有效性测定值在质控靶值范围内。
2.11瓶间重复性(均一性)校准品、质控品瓶间重复性CV≤5%。
2.12校准品溯源性根据GB/T21415-2008《体外诊断医疗器械生物样品中量的测量校准品控制物质赋值的计量学溯源性》及有关规定提供 N-乙酰-β-D-氨基葡萄糖苷酶校准品的来源、赋值过程以及测量不确定度等内容。
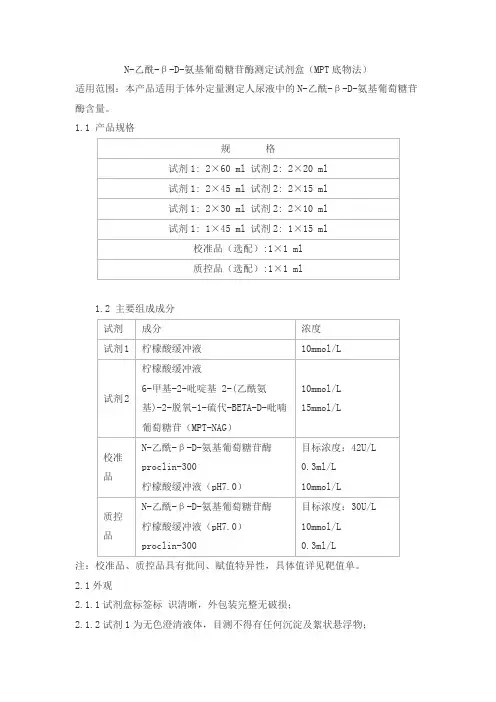
N-乙酰-β-D-氨基葡萄糖苷酶测定试剂盒(MPT底物法)适用范围:本产品适用于体外定量测定人尿液中的N-乙酰-β-D-氨基葡萄糖苷酶含量。
1.1 产品规格1.2 主要组成成分注:校准品、质控品具有批间、赋值特异性,具体值详见靶值单。
2.1外观2.1.1试剂盒标签标识清晰,外包装完整无破损;2.1.2试剂1为无色澄清液体,目测不得有任何沉淀及絮状悬浮物;2.1.3试剂2为无色澄清液体,目测不得有任何沉淀及絮状悬浮物;2.1.4校准品:无色或浅黄色液体,目测不得有任何沉淀及絮状悬浮物;2.1.5质控品:无色或浅黄色液体,目测不得有任何沉淀及絮状悬浮物。
2.2净含量净含量不低于标示值。
2.3空白吸光度测定待检试剂主波长505nm、副波长700nm、37℃条件下:A≤0.4。
2.4线性范围(0.5,200)U/L范围内,相关系数r≥0.990;(0.5,30]U/L范围内,绝对偏差应不大于±4.5U/L;(30,200)U/L范围内,相对偏差应不大于±15.0%。
2.5分析灵敏度样本浓度为20U/L时,其吸光度变化△A≥0.0040。
2.6 精密度2.6.1批内重复性CV≤10.0%。
2.6.2 批间差相对偏差R≤10.0%。
2.7 准确度与已上市产品比对:(0.5,200)U/L范围内,相关系数r≥0.990;(0.5,30]U/L范围内,绝对偏差应不大于±4.5U/L;(30,200)U/L范围内,相对偏差应不大于±15.0%。
2.8 校准品2.8.1 均一性:CV≤5.0%;2.8.2 开瓶稳定性:开瓶后3天,相对偏差不超过±10.0%。
2.9 质控品2.9.1赋值有效性:测定值在质控靶值范围内;2.9.2均一性:CV≤5.0%;2.9.3开瓶稳定性:开瓶后3天,测定值在质控靶值范围内。
2.10稳定性未开封试剂2℃~8℃储存,可稳定12个月。
取到效期后2个月内产品进行检测,检测结果应满足2.3、2.4、2.5、2.6.1、2.7和2.9.1的要求。
小鼠N-乙酰-β-D-氨基葡萄糖苷酶 (NAG)酶联免疫吸附测定试剂盒使用说明书产品编号:E-EL-M0812(本试剂盒仅供体外研究使用、不用于临床诊断!)声明:尊敬的客户,感谢您选用本公司的产品。
本产品选用世界著名生产厂家的原料,采用专业ELISA kit生产技术制造。
适用于体外定量检测小鼠血清、血浆、组织匀浆或细胞培养上清液中天然和重组NAG浓度。
使用前请仔细阅读说明书并检查试剂组分!如有疑问,请及时了解伊莱瑞特生物科技XXX。
*: [96T/48T](打开包装后请及时检查所有物品是否齐全完整)检测原理:本试剂盒采用双抗体夹心ELISA法。
用抗小鼠NAG抗体包被于酶标板上,实验时标本或标准品中的NAG会与包被抗体结合,游离的成分被洗去。
依次加入生物素化的抗小鼠NAG抗体和辣根过氧化物酶标记的亲和素。
抗小鼠NAG抗体与结合在包被抗体上的小鼠NAG结合、生物素与亲和素特异性结合而形成免疫复合物,游离的成分被洗去。
加入显色底物(TMB),TMB在辣根过氧化物酶的催化下现蓝色,加终止液后变黄。
用酶标仪在450nm波长处测OD 值,NAG浓度与OD450值之间呈正比,通过绘制标准曲线求出标本中NAG的浓度。
标本收集:1.血清:全血标本于室温放置2小时或4℃过夜后于1000×g离心20分钟,取上清即可检测,收集血液的试管应为一次性的无热原,无内毒素试管。
2.血浆:抗凝剂推荐使用EDTA.Na2,标本采集后30分钟内于1000×g离心15分钟,取上清即可检测。
避免使用溶血,高血脂标本。
3.组织匀浆:用预冷的PBS (0.01M, pH=7.4)冲洗组织,以去除残留血液(匀浆中裂解的红细胞会影响测量结果),称重后将组织剪碎。
将剪碎的组织与对应体积的PBS(一般按1:9的重量体积比,比如1g的组织样本对应9mL的PBS,具体体积可根据实验需要适当调整,并做好记录。
推荐在PBS中加入蛋白酶抑制剂)加入玻璃匀浆器中,于冰上充分研磨。
N-乙酰-β-D氨基葡萄糖苷酶测定试剂盒(MNP-G1cNAc底物法)适用范围:本试剂盒用于体外定量测定人尿液中N-乙酰-氨基葡萄糖苷酶(NAG)的含量。
1.1包装规格序号规格序号规格1 试剂1:3×15ml;试剂2:1×15ml。
2 试剂1:2×45ml;试剂2:2×15ml。
3 试剂1:2×60ml;试剂2:2×20ml。
4 试剂1:3×500ml;试剂2:1×500ml。
5 试剂1:5×18ml;试剂2:5×6ml。
6 试剂1:3L;试剂2:1L。
1.2主要组成成分本试剂由试剂1(R1)和试剂2(R2)组成。
试剂1(R1):MNP-G1cNAc 7.6g/L试剂2(R2):柠檬酸缓冲液30mmol/L磷酸氢二钾 6.25g/L2.1 外观试剂盒外观应整洁,文字符号标识清晰;R1为无色至淡黄色液体,R2为无色至淡黄色液体。
液体试剂不得有沉淀和絮状物。
2.2 装量试剂瓶内液体装量应不少于标示值。
2.3 空白吸光度以生理盐水为样品,在37℃、505nm波长、1cm光径条件下,吸光度<0.5。
2.4 分析灵敏度浓度为50 U/L的样本,吸光度差值△A>0.1。
2.5 准确性回收试验,回收率在90%~110%范围内。
2.6 重复性用不同浓度的两个样本进行检测,各重复检测10次,其批内变异系数(CV)应不超过5%。
2.7 线性2.7.1在(2,200)U/L范围内,线性相关系数r应不低于0.990;2.7.2 在(2,20]U/L范围内绝对偏差不超过±2U/L;(20,200)U/L范围内相对偏差不超过±10%。
2.8 批间差用三个批号的试剂盒测定同一份样本,试剂盒批间相对极差应不超过6%。
2.9 稳定性试剂盒在2~8℃避光保存,可稳定14个月。
取到效期后的样品检测试剂空白吸光度、分析灵敏度、准确度、重复性、线性范围应分别符合2.3、2.4、2.5、2.6、2.7的要求。
N-乙酰-β-D-氨基葡萄糖苷酶测定试剂盒(MPT底物法)适用范围:本产品用于体外定量测定人血清或尿液中N-乙酰-β-D-氨基葡萄糖苷酶的活性。
1.1 规格具体产品规格见下表:1.2 组成成分试剂1:柠檬酸缓冲液 200mmol/L试剂2:MPT-NAG 6.34g/L2.1 外观2.1.1 外包装完整无破损;2.1.2 试剂1:无色澄清透明无杂质液体;2.1.3 试剂2:无色澄清透明无杂质液体。
2.2 净含量净含量不低于标示值。
2.3 试剂空白2.3.1 试剂空白吸光度在波长340nm、37℃条件下,试剂空白吸光度不大于0.5。
2.3.2 试剂空白吸光度变化率在波长340nm、37℃条件下,试剂空白吸光度变化率不大于0.01。
2.4 线性2.4.1 线性范围[10.0,200.0]U/L,相关系数r≥0.990。
2.4.2 线性偏差(30.0,200.0]U/L线性范围内,相对偏差不超过±10%;[10.0,30.0]U/L线性范围内,绝对偏差不超过±4.5U/L。
2.5 分析灵敏度检测浓度为40.0U/L的样本时,吸光度变化率不小于0.008。
2.6 重复性检测高、低浓度的血清样本或质控品,重复测试20次,CV≤10%。
2.7 批间差用三个不同批号的试剂测试(20.0±5.0)U/L的同一样本,重复测试3次,相对极差R≤10%。
2.8 准确度回收率在90%~110%范围内。
2.9 稳定性原包装试剂2~8℃避光储存,有效期12个月。
效期后1个月内产品符合2.3、2.4和2.8的要求。
http://www.solarbio.com
β-葡萄糖苷酶测定试剂盒使用说明
分光光度法50管/24样
货号:BC2560
产品简介:
β-GC(EC3.2.1.21)广泛存在于动物、植物、微生物和培养细胞中,催化β
-糖苷键水解,
具有多方面生理作用:在纤维素的糖化作用中,β-GC负责进一步水解纤维素二糖和纤维素
寡糖生成葡萄糖;β-GC水解萜烯类香气前驱体,使糖苷键合态变成游离态。从而产生香味;
β
-GC能够水解植物体内野黑樱苷,释放HCN,从而防止昆虫取食。
β-GC分解对-硝基苯-β
-D-吡喃葡萄糖苷生成对-硝基苯酚,后者在400nm有最大吸收峰,
通过测定吸光值升高速率来计算β-GC活性。
试验中所需的仪器和试剂:
可见分光光度计、台式离心机、水浴锅、可调式移液器、1ml玻璃比色皿、研钵、冰和蒸馏
水。
产品内容:
提取液:液体50ml×1瓶,4℃保存。
试剂一:粉剂×2瓶,-20℃保存;临用前每瓶加入10ml双蒸水,充分溶解备用;用不完的
试剂仍-20℃保存。
试剂二:液体25ml×1瓶,4℃保存。
试剂三:液体80ml×1瓶,4℃保存。
标准品:液体×1支,取1.5mlEP管加入1ml,5mol/ml的对硝基苯酚溶液。
操作步骤:
一、样品的前处理:
http://www.solarbio.com
1.细菌或培养细胞:
先收集细菌或细胞到离心管内,离心后弃上清;按照细菌或细胞数量(104个):提取液体
积(ml)为500~1000:1的比例(建议500万细菌或细胞加入1ml提取液),超声波破碎细
菌或细胞(冰浴,功率20%或200W,超声3s,间隔10s,重复30次);15000g4℃离心
10min,取上清,置冰上待测。
2.组织:
按照组织质量(g):提取液体积(ml)为1:5~10的比例(建议称取约0.1g组织,加入1ml
提取液),进行冰浴匀浆。15000g4℃离心10min,取上清,置冰上待测。
3、标准样品的准备:取100μL标准液,加入到400μL试剂三中,得到1mol/ml标准液,
十倍稀释到100nmol/ml,倍比稀释:50、25、12.5、6.25nmol/ml,稀释液用试剂二。100、
50、25、12.5、6.25nmol/ml做标准液。
二、测定步骤:
1.分光光度计预热30min以上,调节波长至400nm,蒸馏水调零。
2.加样表
试剂名称(μl)对照管测定管标准管
试剂一
400
试剂二
500500
样本
100100
迅速混匀,放入37℃准确水浴30min后,立即放入沸水浴中煮沸5min(盖紧,以防止
水分散失),流水冷却后充分混匀(以保证浓度不变)
试剂一
400
充分混匀,8000g,4℃,离心5min,取上清液
http://www.solarbio.com
β-GC活力单位的计算:
1、标准曲线建立:根据标准管的浓度(y)和吸光度(x),建立标准曲线。
2、根据标准曲线,将ΔA(x)带入公式计算样品产物浓度(nmol/ml)。
(1)按样本蛋白浓度计算:
单位的定义:每mg组织蛋白在每ml每小时产生1nmol对-硝基苯酚定义为一个酶活力单位。
β
-GC活力(U/mgprot)=(y×V反总)÷(V样×Cpr)÷T
=20×y÷Cpr
需要另外测定,建议使用本公司BCA蛋白质含量测定试剂盒。
(2)按样本鲜重计算:
单位的定义:每g组织在每ml每小时产生1nmol对-硝基苯酚定义为一个酶活力单位。
β
-GC活力(U/g鲜重)=(y×V反总)÷(W×V样÷V样总)÷T
=20×y÷W
(3)按细菌或细胞密度计算:
单位的定义:每1万个细菌或细胞在每ml每小时产生1nmol对-硝基苯酚定义为一个酶活力
单位。
β
-GC活力(U/104cell)=(y×V反总)÷(500×V样÷V样总)÷T
=0.04×y
上清液
500500
标准液
500
试剂三
100010001000
充分混匀,室温静置2min后,用对照管调零,400nm处测定吸光值A,计算ΔA=A测定
管-A对照管。每个测定管需设一个对照管。
http://www.solarbio.com
Cpr:样本蛋白质浓度,mg/ml;V反总:反应体系总体积,1ml;V样:加入反应体系中样本
体积,0.1ml;V样总:加入提取液体积,1ml;W:样品质量,g;500:细胞或细菌总数,
500万;T:反应时间,0.5h。