平衡练习题
- 格式:docx
- 大小:258.76 KB
- 文档页数:24

初二物理重力平衡的练习题一、选择题1. 下面哪个是正确的重力平衡定义?A. 物体在静止或匀速直线运动中,所受的合外力为零B. 物体在匀速直线运动中,所受的合外力等于零C. 物体在任意运动中,所受的合外力为零D. 物体在静止时,所受的合外力等于零2. 在重力平衡的情况下,哪个是正确的?A. 物体的质量一定为零B. 物体的质量一定是正值C. 物体的质量可为零或正值D. 物体的质量可为零或负值3. 以下哪个是正确的,当物体处于重力平衡时?A. 物体的重力等于物体所受的空气阻力B. 物体的重力等于物体所受的支持力C. 物体的重力等于物体所受的摩擦力D. 物体的重力等于物体所受的弹簧力4. 当物体在水平面上受到两个相等大小、相反方向的力时,物体的运动状态是:A. 静止B. 匀速直线运动C. 加速直线运动D. 自由落体运动5. 在以下哪种情况下物体可以保持静止?A. 物体所受合外力等于零B. 物体所受合外力小于零C. 物体所受合外力大于零D. 物体所受合外力为负值二、解答题1. 一架直升机垂直上升时,飞行员身体处于重力平衡状态。
请解释为什么飞行员能够保持静止。
2. 一个物体质量为25千克,放在水平地面上。
物体受到一个与水平方向的摩擦力大小为100牛的作用力和一个垂直向上的支持力。
请计算物体所受的重力大小。
3. 一个质量为10千克的物体放在斜坡上,斜坡的倾角为30°。
物体受到斜坡平行于斜面方向的摩擦力大小为30牛和垂直向上的支持力。
请计算物体所受的重力大小。
4. 一个质量为20千克的物体靠在墙上。
物体受到一个与墙面平行的摩擦力大小为50牛和垂直向上的支持力。
请计算物体所受的重力大小。
三、计算题1. 一个质量为5千克的物体悬挂在天花板上,通过一根绳子。
绳子的拉力为30牛。
请计算物体所受的重力大小。
2. 一个物体质量为50千克,放在水平地面上。
物体受到一个与水平方向的摩擦力大小为150牛的作用力和一个垂直向上的支持力。

化学平衡复习题一、判断题:1、H3PO4溶液中,c (PO43- ) = K(H3PO4 ) mol·L-1。
.................................................()2、催化剂只能改变反应的活能,不能改变反应的热效应。
........................................()3、由CaCO3和CaO 构成的封闭系统,在任何条件下都不能使反应CaCO3 (s) CaO (s) + CO2 (g) 达到平衡。
................................................................()3、MnS (s) + 2 HAc Mn2+ + 2 Ac- + H2 S 反应的标准平衡常数K= K( MnS )·[ K( HAc ) ]2 / [ K( H2S )·K( H2S ) ]。
............. ()4、密闭容器中,A、B、C 三种气体建立了如下平衡:A (g) + B (g) C (g),若保持温度不变,系统体积缩小至原体积的2时,则反应商Q与平衡常数的关系3是:Q = 1.5 K。
..........................................................................()5、根据同离子效应,沉淀剂加入越多,其离子沉淀越完全。
. ()6、在一定温度下,随着可逆反应2SO2 (g) + O2 (g) 2SO3 (g) 的进行,p (O2 )、p (SO2 ) 不断减少,p (SO3 ) 不断增大,所以标准平衡常数K不断增大。
.....................................()二.选择题:1、在一恒压容器中,某温度、100.0 kPa 条件下,将1.00 mol A 和2.00 mol B 混合,按下式反应:A (g) + 2B (g) C (g)。

平衡力练习题平衡力是我们生活中常常需要用到的一项能力。
无论是日常行走、进行体育运动,甚至是做一些精细动作,平衡力都起着重要的作用。
为了提高平衡能力,我们可以进行一些简单的练习。
以下是一些平衡力练习题,通过坚持练习,可以有效提升平衡力。
让我们开始吧!1. 单脚站立这是一个最基础的平衡练习。
找到一个平稳的地面,然后抬起一只脚,尽量保持另一只脚稳定的站立。
开始时可以用手扶墙或者椅子来保持平衡,随着练习的进行,逐渐减少对外部支撑的依赖。
每天练习5-10分钟,逐渐增加站立时间。
2. 单脚闭眼站立一旦你能够轻松进行单脚站立,可以尝试闭上眼睛进行练习。
闭上眼睛会使平衡感受更加敏感,挑战你的平衡能力。
通过闭眼练习,你可以训练大脑更好地感知身体的平衡状态,提高平衡力。
3. 平衡板训练平衡板是一种专门用于平衡训练的工具。
站在平衡板上,调整身体的重心,保持平衡。
一开始可以选择较宽的平衡板,随着能力提高,逐渐转向窄一些的平衡板。
你也可以尝试一些平衡板上的动作,如单脚站立、前后倾斜等,以增加进一步的挑战。
4. 摸高绷带找一条长约2米的绷带,将其垂直挂在墙上。
站在绷带的一端,并将绷带抓住。
尽量保持身体稳定,然后慢慢将手向上移动,直到触碰绷带的最高点。
慢慢地,你可以尝试站在较短的绷带上,或者尝试用脚触碰绷带。
5. 倒立练习倒立可以锻炼全身肌肉的平衡力。
你可以选择借助墙面进行倒立,或者使用瑜伽球等辅助工具。
切记,倒立练习需要逐渐增加时间和难度,避免突然进行剧烈的倒立动作。
6. 瑜伽平衡姿势瑜伽中有很多平衡姿势,如树式、鹿式、光明式等。
通过练习这些平衡姿势,可以全面提高身体的平衡能力。
你可以在瑜伽馆或者通过网络学习相应的动作。
这些平衡力练习题可以根据个人情况进行调整。
切记,练习过程中要保持适度,并根据自身能力逐渐增加难度。
坚持练习,你的平衡力将会得到显著提升。
加油吧!。

化学平衡状态练习题1. 在高温下,将一定量的二氧化碳气体注入具有无机碱性基质的封闭容器中。
当化学平衡达到稳定时,会生成什么产物?解释该反应的方程式。
2. 硝酸和氢氨溶液通过混合反应生成氨硝酸。
写出反应的方程式,并解释过程中发生的氧化还原反应。
3. 某种金属与非金属氧化物发生反应,形成相应的金属氧化物和非金属。
描述该反应的平衡状态并解释该过程中出现的氧化还原反应。
4. 乙醇和氧气发生反应生成乙醛和水。
写出该反应的方程,并说明氧化还原反应的进行。
5. 铜和硫酸发生反应生成铜硫酸,同时生成二氧化硫和水。
描述该反应的平衡状态并解释该过程中发生的氧化还原反应。
6. 氨水和盐酸反应生成氯化铵和水。
解释该反应的方程式,并描述该反应中发生的酸碱中和反应。
7. 氧化亚氮气体和水反应生成硝酸溶液。
写出反应的方程式,并解释该反应中发生的氧化还原反应。
8. 某种金属与醋酸反应生成乙酸盐和氢气。
描述该反应的平衡状态并说明该过程中发生的氧化还原反应。
9. 硝酸和氢气反应生成一种金属盐和水。
解释该反应的方程式,并说明该反应中发生的氧化还原反应。
10. 大气中的氮气和氢气反应生成氨。
描述该反应的平衡状态并解释该过程中发生的氧化还原反应。
化学平衡状态是指化学反应达到稳定时,反应物和生成物之间的浓度保持恒定的状态。
在平衡状态下,反应的前向和反向反应发生的速率相等。
对于上述练习题中的每一个反应,平衡状态下都存在氧化还原反应。
氧化还原反应是指电子的转移过程。
在反应中,一种物质失去电子被氧化,而另一种物质获得电子被还原。
氧化还原反应通常涉及到电子的转移和氧化态的变化。
在化学平衡状态中,反应进行了一段时间后,反应物和生成物的浓度达到稳定。
在达到平衡时,前向反应的速率等于反向反应的速率,这意味着反应物和生成物的浓度保持不变。
根据Le Chatelier 定理,当外界条件发生变化时,平衡状态会产生位移,以减少这种变化。
通过解题练习,我们可以更好地理解化学平衡状态和氧化还原反应。

主题一 第四节 物体的平衡一、单选题1.如图所示,两直梯下端放在水平地面上,上端靠在竖直墙壁上,相互平行,均处于静止状态。
梯子与墙壁之间均无摩擦力,下列说法正确的是( )A .梯子越长、越重,所受合力越大B .地面对梯子的作用力一定竖直向上C .地面对梯子的作用力可能沿梯子向上.D .地面对梯子的作用力与水平面的夹角大于梯子的倾角2.如图所示,一玻璃清洁工人坐在简易的小木板BC 上,通过楼顶的滑轮和轻绳OA 在竖直平面内缓慢下降。
工人两腿并拢伸直,腿与竖直玻璃墙的夹角53β︒=,在下降过程中β角保持不变。
玻璃墙对脚的作用力始终沿腿方向,小木板BC 保持水平且与玻璃墙垂直。
某时刻轻绳OA 与竖直玻璃墙的夹角37α=,连接小木板的两等长轻绳AB 、AC 的夹角120θ=,且与OA 在同一平面内。
已知工人及工具的总质量70m kg =,小木板的质量可忽略不计,g 取10m/s 2。
工人在稳定且未擦墙时,下列说法正确的是( )A .从该时刻起,工人在缓慢下移的过程中,绳OA 的弹力减小B .从该时刻起,工人在缓慢下移的过程中,脚对墙的作用力增大C .此时若工人不触碰轻绳,小木板受的压力大小为448ND .此时若工人不触碰轻绳,绳AB 的张力大小为700N3.拖把是由拖杆和拖把头构成的擦地工具。
某同学用该拖把在水平地板上拖地,当沿拖杆方向施加大小为F的水平推力时,拖把头在地板上做匀速直线运动;当沿拖杆方向施加大小仍为F,方向与竖直方向成θ= 60°角的拉力时,拖把头也恰好做匀速直线运动。
拖把头与水平地板间的动摩擦因数为()A.32B.23C.36D.334.如图所示上海世博会江苏城市案例馆中的穹形门窗。
在竖直放置的穹形光滑支架上,一根不可伸长的轻绳通过轻质滑轮悬挂一重物G。
现将轻绳的一端固定于支架上的A点,另一端从C点沿支架缓慢地向B点靠近(C点与A点等高)。
则绳中拉力大小变化的情况是()A.先变小后变大B.先不变后变大C.先不变后变小D.先变大后变小5.在如图所示的四幅图中,AB、BC均为轻质杆,各图中杆的A、C端都通过铰链与墙连接,两杆都在B处由铰链相连接,且系统均处于静止状态。

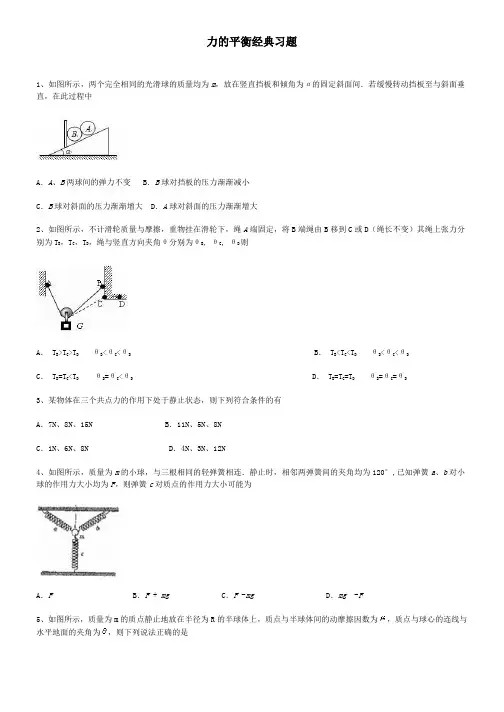
力的平衡经典习题1、如图所示,两个完全相同的光滑球的质量均为m,放在竖直挡板和倾角为α的固定斜面间.若缓慢转动挡板至与斜面垂直,在此过程中A.A、B两球间的弹力不变 B.B球对挡板的压力渐渐减小C.B球对斜面的压力渐渐增大 D.A球对斜面的压力渐渐增大2、如图所示,不计滑轮质量与摩擦,重物挂在滑轮下,绳A端固定,将B端绳由B移到C或D(绳长不变)其绳上张力分别为T B,T C,T D,绳与竖直方向夹角θ分别为θB, θC, θD则A. T B>T C>T D θB<θC<θD B. T B<T C<T D θB<θC<θDC. T B=T C<T DθB=θC<θD D. T B=T C=T D θB=θC=θD3、某物体在三个共点力的作用下处于静止状态,则下列符合条件的有A.7N、8N、15N B.11N、5N、8NC.1N、6N、8N D.4N、3N、12N4、如图所示,质量为m的小球,与三根相同的轻弹簧相连.静止时,相邻两弹簧间的夹角均为120°,已知弹簧a、b对小球的作用力大小均为F,则弹簧c对质点的作用力大小可能为A.F B.F + mg C.F -mg D.mg -F5、如图所示,质量为m的质点静止地放在半径为R的半球体上,质点与半球体间的动摩擦因数为,质点与球心的连线与水平地面的夹角为,则下列说法正确的是A.地面对半球体的摩擦力为零B.质点对半球体的压力大小为mg sinC.质点所受摩擦力大小为mg sinD.质点所受摩擦力大小为mg cos6、如图所示,一个质量为m=2.0 kg的物体,放在倾角为θ=30°的斜面上而静止,若用竖直向上的力F=5 N提物体,物体仍静止(g=10 m/s2),则下述正确的是A.斜面受的压力削减量等于5 N B.斜面受的压力削减量小于5 NC.地面受的压力削减量等于5 N D.地面受的压力削减量小于5 N7、半圆柱体P放在粗糙的水平地面上,其右端有固定放置的竖直挡板MN,在P和MN之间放有一个光滑匀称的小圆柱体Q,整个装置处于静止状态,右图所示是这个装置的纵截面图. 若用外力使MN保持竖直,缓慢地向右移动,在Q落到地面以前、发觉P始终保持静止. 在此过程中,下列说法中不正确的是A.MN对Q的弹力渐渐减小B.地面对P的摩擦力渐渐增大C.P、Q间的弹力先减小后增大 D.Q所受的合力渐渐增大8、如图所示,两个质量都是m的小球A、B用轻杆连接后斜放在墙上处于平衡状态.已知墙面光滑,水平地面粗糙.现将A球向上移动一小段距离.两球再次达到平衡,那么将移动后的平衡状态和原来的平衡状态比较,地面对B球的支持力N和轻杆上的压力F的变更状况是A.N不变,F变大B.N不变,F变小C.N变大,F变大 D.变大,F变小9、如图所示,A、B两物体通过两个质量不计的光滑滑轮悬挂起来,处于静止状态.现将绳子一端从P点缓慢移到Q点,系统仍旧平衡,以下说法正确的是A.夹角θ将变小 B.夹角θ将变大C.绳子张力将增大 D.物体B位置将变高10、如图所示,A、B两球完全相同,质量均为m,用两根等长的细线悬挂在O点,两球之间连着一根劲度系数为k的轻质弹簧,静止不动时,两根细线之间的夹角为。

二力平衡练习题一、选择题1. 当物体处于静止状态或匀速直线运动状态时,作用在物体上的两个力是:A. 作用力和反作用力B. 重力和支持力C. 摩擦力和拉力D. 平衡力2. 以下哪组力不是一对平衡力?A. 物体在水平面上受到的重力和支持力B. 物体在斜面上受到的重力和斜面的支持力C. 物体在斜面上受到的重力的下滑分力和摩擦力D. 物体在斜面上受到的重力的垂直分力和支持力3. 在二力平衡的条件下,以下哪个说法是错误的?A. 两个力作用在同一个物体上B. 两个力大小相等,方向相反C. 两个力作用在同一直线上D. 两个力可以不是同一性质的力4. 一个物体在水平面上受到两个力的作用,当这两个力的合力为零时,物体处于:A. 静止状态B. 匀速直线运动状态C. 加速运动状态D. 减速运动状态5. 以下哪个条件不是二力平衡的必要条件?A. 两个力作用在同一个物体上B. 两个力大小相等C. 两个力方向相同D. 两个力作用在同一直线上二、填空题6. 当物体受到两个力的作用,且这两个力的_______相等,_______相反,且作用在_______上时,物体处于平衡状态。
7. 一个物体在水平面上受到两个力的作用,如果这两个力的合力不为零,则物体将处于_______状态。
8. 在二力平衡的条件下,如果两个力的大小不相等,则物体将处于_______状态。
9. 一个物体在竖直方向上受到重力和拉力的作用,当这两个力满足二力平衡的条件时,物体将处于_______状态。
10. 当物体受到的两个力大小相等,方向相反,但作用在不同的物体上时,这两个力是_______。
三、判断题11. 物体在平衡状态下,受到的合力一定为零。
()12. 作用力和反作用力可以是平衡力。
()13. 物体在斜面上静止时,其受到的重力和斜面的支持力是一对平衡力。
()14. 一个物体在水平面上受到两个力的作用,如果这两个力的方向不在同一直线上,则这两个力一定不是平衡力。

化学平衡专项练习题1. 气态反应中的平衡常数(a)选择下列反应中的平衡常数的正确单位:i. 2NO(g) + O2(g) ⇌ 2NO2(g)ii. CO(g) + H2O(g) ⇌ CO2(g) + H2(g)(b)给出以下反应的平衡常数表达式:i. 2H2(g) + O2(g) ⇌ 2H2O(g)ii. N2(g) + 3H2(g) ⇌ 2NH3(g)2. 溶液中的平衡常数(a)给出以下酸碱反应的离子方程式:i. HCl(aq) + NaOH(aq) ⇌ NaCl(aq) + H2O(l)ii. H2SO4(aq) + 2NaOH(aq) ⇌ Na2SO4(aq) + 2H2O(l) (b)写出以下反应的平衡常数表达式:i. HCl(aq) + H2O(l) ⇌ H3O+(aq) + Cl-(aq)ii. H2SO4(aq) + H2O(l) ⇌ H3O+(aq) + HSO4-(aq)3. 应用平衡常数计算浓度和压力(a)根据以下反应的平衡常数,计算以下浓度:i. 2SO2(g) + O2(g) ⇌ 2SO3(g)ii. N2(g) + 3H2(g) ⇌ 2NH3(g)(b)根据以下反应的平衡常数,计算以下分压:i. PCl3(g) + Cl2(g) ⇌ PCl5(g)ii. H2(g) + Br2(g) ⇌ 2HBr(g)4. 平衡常数与反应方向(a)根据以下反应的平衡常数,判断反应的方向:i. 2CO(g) + O2(g) ⇌ 2CO2(g) (∆H=−563 kJ)ii. 2H2O(l) ⇌ 2H2(g) + O2(g) (∆H=+483 kJ)(b)根据以下反应的平衡常数和温度变化,判断反应的方向:i. 2SO3(g) ⇌ 2SO2(g) + O2(g) (ΔH<0,ΔS>0)ii. 3FeO(s) + CO(g) ⇌ 2Fe3O4(s) + CO2(g) (ΔH>0,ΔS>0)5. 影响平衡常数的因素(a)说明以下因素如何影响平衡常数:i. 温度变化ii. 压力变化(对气态反应)(b)举例说明温度和压力变化对平衡常数的影响。

物体的力的平衡和合力练习题1. 引言物体的力的平衡和合力是物理学中的基本概念,通过练习题的形式,我们可以深入理解这些概念并运用到实际问题中。
本文将介绍一些关于物体力的平衡和合力的练习题,帮助读者更好地掌握这些知识。
2. 物体的力的平衡练习题2.1 静止物体的平衡假设有一个质量为10kg的物块放在桌子上,请计算施加在物块上的重力和支持力的大小。
2.2 悬挂物体的平衡一根绳子的一端系着一个质量为5kg的物块,另一端悬挂在天花板上,请计算绳子对物块的拉力以及物块对绳子的拉力的大小。
2.3 物体在斜面上的平衡一个质量为8kg的物块放在倾斜角度为30°的斜面上,请计算斜面对物块的支持力的大小以及物块对斜面的摩擦力的大小。
3. 物体的合力练习题3.1 平行力的合力有两个力分别为10N和20N,方向相同,请计算它们的合力大小和方向。
3.2 垂直力的合力有两个力分别为15N和25N,方向垂直,请计算它们的合力大小和方向。
3.3 斜向力的合力有两个斜向力,大小分别为30N和40N,夹角为60°,请计算它们的合力大小和方向。
4. 综合练习题4.1 绳子拉扯物块的问题一根绳子分别和两个物块相连,物块A的质量为8kg,物块B 的质量为12kg,两个物块之间的距离为2m,请计算物块A受到的合力和物块B受到的合力。
4.2 受外力推拉的问题一个质量为20kg的物块受到一个水平方向的外力,外力大小为30N,请计算物块的加速度和所受合力的方向。
5. 结论通过以上练习题的解答,我们可以了解到物体的力的平衡和合力的相关概念和计算方法。
这些知识不仅在课堂中有着重要的应用,也能帮助我们更好地理解物体的运动和力的作用。
希望读者通过练习题的学习,能够对物体的力的平衡和合力有更深入的认识,提高物理学习的效果。

高中物理:力与物体的平衡练习(含答案)满分:100分时间:60分钟一、单项选择题(本题共8小题,每小题4分,共32分。
每小题只有一个选项符合题意。
) 1.(姜堰市模拟)如图所示,一只半径为R的半球形碗倒扣在水平桌面上处于静止状态,一质量为m的蚂蚁在离桌面高度45R时恰能停在碗上。
则蚂蚁受到的最大静摩擦力大小为()A.0.6 mg B.0.8 mg C.0.4 mg D.0.75 mg2.(长春质量监测)如图所示,小球a的质量为小球b质量的一半,分别与轻弹簧A、B和轻绳相连接并处于平衡状态。
轻弹簧A与竖直方向夹角为60°,轻弹簧A、B伸长量刚好相同,则下列说法中正确的是()A.轻弹簧A、B的劲度系数之比为3∶1B.轻弹簧A、B的劲度系数之比为2∶1C.轻绳上拉力与轻弹簧A上拉力大小之比为2∶1D.轻绳上拉力与轻弹簧B上拉力大小之比为1∶13.如图所示,由两种材料制成的半球面固定在水平地面上,右侧面是光滑的,左侧面是粗糙的,O点为球心,A、B是两个相同的小物块(可视为质点),小物块A静止在左侧面上,小物块B在图示水平力F作用下静止在右侧面上,A、B处在同一高度,AO、BO与竖直方向的夹角均为θ,则A、B对球面的压力大小之比为() A.sin2θ∶1 B.cos2θ∶1C.sin θ∶1 D.cos θ∶14.一串小灯笼(五只)彼此用轻绳连接,并悬挂在空中。
在稳定水平风力作用下发生倾斜,悬绳与竖直方向的夹角为30°,如图所示。
设每个灯笼的质量均为m。
则自上往下第一只灯笼对第二只灯笼的拉力大小为()A.23mg B.233mgC.833mgD .8 mg5.如图所示,两段等长细线串接着两个质量相等的小球a 、b ,悬挂于O 点。
现在两个小球上分别加上水平方向的外力,其中作用在b 球上的力大小为F 、作用在a 球上的力大小为2F ,则此装置平衡时的位置可能是图中( )6.如图所示,一轻杆水平放置,杆两端A 、B 系着不可伸长且光滑的柔软轻绳,绳上套着一小铁环。
平衡状态练习题平衡是我们生活中的重要概念,不仅仅应用于物理世界中,还涉及到心理、情感和人际关系等方面。
平衡状态的练习题可以帮助我们更好地理解平衡的本质,并提供实践机会来发展平衡的技能。
以下是一些平衡状态练习题,通过解答这些问题,我们可以更好地掌握平衡的要领。
1. 自我平衡:a. 你如何在日常生活中保持身心平衡?b. 你认为自我平衡对生活的重要性是什么?2. 心理平衡:a. 你如何处理挫折感和压力,以保持心理平衡?b. 你是否经历过心理失衡的时期?如何恢复平衡?3. 情感平衡:a. 平衡爱与被爱的关系是什么意思?b. 在人际关系中,如何保持情感平衡?4. 社交平衡:a. 你如何在工作和社交场合中保持平衡?b. 如何在人际关系中处理冲突,以维持平衡?5. 平衡与健康:a. 平衡饮食和锻炼对身体健康的作用是什么?b. 你如何在工作和休闲之间找到平衡,以保持健康的生活方式?6. 平衡与学习:a. 如何在学习和娱乐之间实现平衡?b. 你认为平衡对学习成就的影响是什么?7. 平衡与时间管理:a. 如何合理分配时间以实现工作与生活的平衡?b. 你有哪些有效的时间管理技巧来保持平衡?8. 平衡与目标设定:a. 平衡如何与目标设定和追求相结合?b. 你如何在追求目标的过程中保持平衡?9. 平衡与幸福:a. 你认为平衡对幸福的重要性是什么?b. 如何在追求自己的幸福同时保持平衡?以上是一些探索平衡状态的练习题,通过回答这些问题,你可以更好地理解平衡的概念,以及如何在日常生活中保持平衡。
平衡是一种艺术,需要我们不断地实践和调整,让生活变得更加美好和有意义。
希望这些练习题能够帮助你在平衡的道路上迈出更稳健的步伐。
初二物理平衡能力练习题在初二物理学习中,平衡是一个非常重要的概念。
学生们需要通过练习题来巩固和提高他们的平衡能力。
本文将为初二物理学生提供一些平衡能力练习题,旨在帮助他们更好地理解和掌握平衡的原理。
练习题一:平衡杆问题在一根质量均匀分布的平衡杆上,A、B两个物体分别位于杆的两侧。
A物体的质量为1kg,距离中心的距离为2m。
B物体的质量为2kg,距离中心的距离为1m。
求A、B两个物体分别处于平衡状态时所处的位置。
解析:根据平衡的条件,我们可以得到以下方程:A × a =B × b其中,A和B分别表示物体A和物体B的质量,a和b表示它们距离中心的距离。
代入已知量,可以得到:1 ×2 = 2 × b解得 b = 1所以,B物体位于杆中心的位置。
练习题二:吊挂物体问题在一个吊挂物体的系统中,有两个悬挂物体和一个吊轮。
悬挂物体A的质量为5kg,悬挂物体B的质量为10kg。
吊挂物体系统的质量为2kg。
已知悬挂物体A的左侧距离为3m,悬挂物体B的右侧距离为4m。
求吊轮所在位置的平衡条件。
解析:设吊轮所在位置的平衡条件为 x。
根据平衡的条件,我们可以得到以下方程:5 × 3 = 10 × 4 + 2 × (4 + x)解得 x = -21所以,吊轮所在位置的平衡条件为-21m。
练习题三:悬空物体问题在一个悬挂物体的系统中,有一个悬挂物体和一个吊挂系统。
悬挂物体的质量为8kg,吊挂系统的质量为2kg。
已知悬挂物体所受的合力为120N,吊挂系统的中心位于悬挂物体上方的2m处。
求吊挂系统的整体平衡条件。
解析:设吊挂系统的整体平衡条件为 x。
根据平衡的条件,我们可以得到以下方程:8 × x = 2 × 2解得 x = 0.5所以,吊挂系统的整体平衡条件为0.5m。
练习题四:垂直平衡问题在一个平面上,有一个质量为2kg的物体,通过一根轻杆与一个固定点相连。
三力平衡练习题三力平衡是指在物体上作用的三个力能够使物体保持静止或匀速直线运动的状态。
以下是一些关于三力平衡的练习题:1. 选择题A. 一个物体受到两个大小相等、方向相反的力作用,这两个力的合力大小为多少?a) 0b) 1c) 2d) 无法确定B. 已知一个物体受到三个力的作用,力F1=10N,力F2=20N,力F3=15N,这三个力能否使物体处于平衡状态?a) 能b) 不能2. 填空题- 当一个物体受到三个力的作用,且这三个力的大小分别为F1、F2和F3,若要使物体处于平衡状态,这三个力必须满足的条件是________。
3. 判断题- 一个物体受到三个力的作用,如果这三个力的合力为零,则物体一定处于平衡状态。
()4. 简答题- 描述三力平衡的条件,并解释为什么这些条件对于物体的平衡至关重要。
5. 计算题- 假设一个物体受到三个力的作用,力F1=30N,方向向右;力F2=40N,方向向左;力F3的大小和方向未知。
如果物体处于平衡状态,请计算力F3的大小和方向。
6. 应用题- 一个悬挂的吊灯受到三个力的作用:重力G、绳的拉力T1和墙壁对吊灯的支撑力T2。
如果吊灯处于静止状态,且重力G=50N,绳的拉力T1=30N,方向垂直向上,求墙壁对吊灯的支撑力T2的大小和方向。
7. 绘图题- 画出一个物体在三个力作用下的受力图,并标注这三个力的大小和方向。
假设物体处于平衡状态。
8. 实验设计题- 设计一个实验来验证三力平衡的条件。
描述实验的步骤、所需材料和预期结果。
9. 论述题- 论述在实际工程中如何应用三力平衡的原理来设计稳定的结构。
10. 案例分析题- 给出一个实际案例,例如桥梁的支撑结构,分析其如何利用三力平衡的原理来保持稳定。
请注意,这些练习题旨在帮助学生理解和掌握三力平衡的概念和应用。
在解答这些题目时,学生应该运用物理知识,特别是牛顿运动定律和力的合成与分解原理。
物体受力平衡分析练习题物体受力平衡分析是力学中的一个重要概念,用于研究物体在不同力的作用下是否处于平衡状态。
本文将提供一些物体受力平衡分析的练习题,帮助读者更好地理解和应用该概念。
练习题1:一个物体质量为50千克,静止在水平地面上。
求该物体所受的重力。
解析:根据牛顿第二定律,物体所受的重力等于物体的质量乘以重力加速度。
重力加速度的大小为9.8米/秒²。
重力 = 质量 ×重力加速度重力 = 50千克 × 9.8米/秒²重力 = 490牛顿练习题2:一个斜面上放置着一个物体,斜面的倾角为30°。
已知物体施加在斜面上的摩擦力为100牛顿,求物体所受的重力分力和垂直于斜面方向的力。
解析:首先,我们需要将物体的重力解析成斜面的两个分力:垂直于斜面方向的力和平行于斜面方向的力。
重力分解:物体在斜面上的重力分力分为垂直于斜面方向和平行于斜面方向。
重力垂直分力 = 重力 × sin(斜面角度)重力平行分力 = 重力 × cos(斜面角度)给定斜面角度为30°,重力则可进行分解:重力垂直分力 = 重力 × sin(30°)重力平行分力 = 重力 × cos(30°)已知重力平行分力为100牛顿,代入公式可得:重力 × cos(30°) = 100牛顿解得重力 = 100牛顿 / cos(30°)然后代入重力公式计算重力值。
垂直于斜面方向的力为重力垂直分力,由此可得物体所受的垂直于斜面方向的力为上述计算出的数值。
练习题3:一个物体静止在竖直墙面上,墙面的倾角为60°。
已知物体所受的重力分力为100牛顿,求物体所受的垂直于墙面方向的力和水平方向的力。
解析:同样地,我们需要将物体的重力分解为墙面方向的分力和垂直于墙面方向的分力。
重力分解:物体在墙面上的重力分力分为垂直于墙面方向和平行于墙面方向。
高中物理平衡问题练习题-CAL-FENGHAI-(2020YEAR-YICAI)_JINGBIAN平衡奥义种下希望就会收获1. 如图所示,两个完全相同的光滑球的质量均为m,放在竖直挡板和倾角为α的固定斜面间.若缓慢转动挡板至与斜面垂直,在此过程中()A.A、B两球间的弹力逐渐增大B.B球对挡板的压力逐渐减小C.B球对斜面的压力逐渐增大D.A球对斜面的压力逐渐增大2. 如图所示,质量为2m的物体A经一轻质弹簧与地面上的质量为3m的物体B相连,弹簧的劲度系数为k,一条不可伸长的轻绳绕过定滑轮,一端连物体A,另一端连一质量为m的物体C,物体A、B、C都处于静止状态.已知重力加速度为g,忽略一切摩擦.(1)求物体B对地面的压力;(2)把物体C的质量改为5m,这时C缓慢下降,经过一段时间系统达到新的平衡状态,这时B仍没离开地面,且C只受重力和绳的拉力作用,求此过程中物体A上升的高度.3. 如图所示,一根匀质绳质量为M,其两端固定在天花板上的A、B两点,在绳的中点悬挂一重物,质量为m,悬挂重物的绳PQ质量不计。
设、β分别为绳子端点和中点处绳子的切线方向与竖直方向的夹角,试求的大小。
4. 如图所示,倾角为θ的斜面体C置于水平面上,B置于斜面上,通过细绳跨过光滑的定滑轮与A相连接,连接B的一段细绳与斜面平行,A、B、C都处于静止状态.则()A.B受到C的摩擦力一定不为零B.C受到水平面的摩擦力一定为零C.水平面对C的摩擦力方向一定向左D.水平面对C的支持力与B、C的总重力大小相等5. 如图所示半圆柱体P固定在水平地面上,其右端有一固定放置的竖直挡板MN.在半圆柱体P和MN之间放有一个光滑均匀的小圆柱体Q,整个装置处于平衡状态.现使MN保持竖直并且缓慢地向右平移,在Q滑落到地面之前的此过程中,下列说法中正确的是()A.MN对Q的弹力逐渐减小 B.MN对Q 的弹力保持不变C.P对Q的作用力逐渐增大D.P对Q的作用力先增后减小6. 如图所示,质量为M、半径为R、内壁光滑的半球形容器静止放在粗糙水平地面上,O为球心。
多重平衡练习题一、背部平衡练习背部平衡对于保持身体的姿势和减少背部疼痛非常重要。
以下是一些多重平衡练习题,旨在帮助你加强背部肌肉并提高姿势:1. 桥式- 仰卧在地上,脚掌平放在地上,双手伸直放在身体两侧。
- 缩紧腹部肌肉,然后抬起臀部,使身体与地面平行。
- 尽量保持这个姿势,然后缓慢放下臀部回到初始位置。
- 重复10次。
2. 倒立姿势- 倚靠墙壁站立,双手平放在身体两侧。
- 缓慢向后倾斜身体,将双脚抬起并靠在墙上。
- 尽力保持平衡,并保持这个姿势30秒钟。
- 慢慢地回到站立姿势,然后放松几秒钟。
- 重复3至5次。
二、核心平衡练习核心肌群是身体稳定性的关键。
以下是一些多重平衡练习题,可帮助你加强核心肌肉并提高身体平衡:1. 木易杠杆- 双腿与肩同宽,双腿微微弯曲,双臂伸直向前伸展。
- 向前倾身,同时将右腿向后伸展,直到身体与右腿保持一条直线。
- 尽力保持平衡,然后慢慢地恢复初始姿势。
- 重复10次,然后换左腿重复相同动作。
2. 单腿平衡- 站立直立,保持腹部收紧。
- 将体重转移到右腿上,并将左腿抬起,使膝盖弯曲。
- 尽量保持平衡,然后缓慢地将左腿放下。
- 重复10次,然后换腿重复相同动作。
三、全身平衡练习全身平衡练习有助于提高身体的整体稳定性和协调性。
以下是一些多重平衡练习题,可锻炼全身肌肉并提高平衡能力:1. 步伐平衡- 站立直立,保持腹部收紧。
- 缓慢抬起右腿,弯曲膝盖。
- 尽量保持平衡,然后向前迈出一步。
- 缓慢地将右脚放下,与左脚并列。
- 重复10次,然后换腿重复相同动作。
2. 瑜伽平衡姿势- 站立直立,双手放在身体两侧。
- 缓慢将左脚抬起,弯曲膝盖并将左脚的脚底靠在右腿的内侧。
- 尽量保持平衡,然后将左手向上伸展,手指指向天花板。
- 尽量保持这个姿势,然后缓慢地回到初始姿势。
- 重复10次,然后换腿和手重复相同动作。
综上所述,这些多重平衡练习题旨在加强背部、核心和全身肌肉,提高平衡能力和姿势。
平衡练习题化学平衡常数【知识框架】一、建立完整的外部逻辑1、K值的计算2、K值的影响因素3、K值的综合运用二、梳理严谨的内部逻辑1、K值的计算(1)板块1-识记平衡常数定义和表达式(2)板块2-书写简单方程式K值的表达式(3)板块3-识记K值注意事项(4)板块4-书写复杂方程式K值的表达式(5)板块5-熟练运用三段式计算方法(6)板块6-掌握常见计算技巧2、K值的影响因素(1)板块1-识记K值的影响因素(2)板块2-判断外界条件对K值大小的影响(3)板块3-熟练运用三段式的计算方法3、K值的综合运用(1)板块1-反应速率(2)板块2-转化率(3)板块3-平衡移动(4)板块4-△H(5)板块5-图像【第一版块】K 值的计算【基础知识】1. 化学平衡常数(K )在一定温度下,当一个可逆反应达到平衡时,生成物浓度化学计量数次幂之积与反应物浓度化学计量数次幂之积的比值是一个常数。
这个常数就是该反应的化学平衡常数(简称平衡常数)mA(g)+nB(g) pC(g)+qD(g)注:某一化学反应的化学平衡常数(K )只与温度有关2. K 的表达式含义:①各物质的浓度一定是平衡..时的浓度,而不是其他时刻....的浓度。
②只写浓度可变的溶液相和气相,纯固态和纯液态物质不写入(一般可视为1)③化学平衡常数是指某一具体化学反应的平衡常数,当化学反应方程式的计量数增倍或减倍K = c p (C) c q (D)c m (A) c n (B)时,化学平衡常数也相应的发生变化。
④反应方程式相加(减),平衡常数相乘(除)板块1-识记平衡常数定义和表达式【经典例题】【例1】将固体NH4I 置于密闭容器中,在一定温度下发生下列反应:达到平衡时c(H2)=0.5mol·L-1,c(HI)=4mol·L-1,则此温度下反应①的平衡常数为()A、9B、16C、20D、25板块2-书写简单方程式K值的表达式【经典例题】【例1】PCl5的热分解反应为:PCl5(g)PCl3(g)+Cl2(g)(1) 写出反应的平衡常数表达式:(2) 已知某温度下,在容积为10.0 L的密闭容器中充入2.00 mol PCl5,达到平衡后,测得容器内PCl3的浓度为0.150 mol/L。
计算该温度下的平衡常数。
【例2】对于3Fe ( s) + 4H2O ( g) Fe3O4 ( s) c(Fe O c( Fe O ) ·+4H 2 (g),反应的化学平衡常数的表达式为( )板块3-识记K 值注意事项【经典例题】【例1】板块4-书写复杂方程式K 值的表达式【经典例题】【例1】碘钨灯比白炽灯使用寿命长。
灯管内封存的少量碘与使用过程中沉积在管壁上的钨可以发生反应:W (s )+I 2(g ) WI 2 (g ),ΔH <0(温度T 1<T 2)。
下列说法正确的是( )A 、灯管工作时,扩散到灯丝附近高温区的WI 2(g )会分解出W ,W 重新沉积到灯丝上B 、灯丝附近温度越高,WI 2(g )的转化率越低[ c ( H ) ]4[ c ( H O) ]4 D 、 A 、 C 、 C 、该反应的平D 、利用该反应【例2】高温下,某反应达平衡,平衡常数K=c(CO)·c(H 2O)c(CO 2 )·c(H 2)。
恒容时,温度升高,H 2 浓度减小。
下列说法正确的是( )A 、该反应的焓变为正值B 、恒温恒容下,增大压强,H 2浓度一定减小C 、升高温度,逆反应速率减小D 、该反应化学方程式为CO + H 2CO 2+ H 2板块5-熟练运用三段式计算方法【经典例题】【例1】板块6-掌握常见计算技巧【经典例题】【例1】【第二版块】K 值的计算【基础知识】1. K 值的应用①判断某可逆反应进行的限度K 值越大,表示反应进行得越完全,反应物转化率越大;K 值越小,表示反应进行得越不完全,反应物转化率越小。
②判断一个可逆反应是否达到平衡若用起始时各物质浓度化学计量数次幂之积的比值当Q=K 时,可逆反应达到平衡状态;当Q >K 时,可逆反应逆向进行;当Q <K 时,可逆反应正向进行。
③判断反应的热效应若升高温度,K 值增大,则正反应为吸热反应若升高温度,K 值减小,则正反应为放热反应④计算化学平衡与转化率(学习使用三步法)依据起始浓度(或平衡浓度)和平衡常数可以计算平衡浓度(或起始浓度),从而计算反应(用Q 表示Q= )与K 比较,{c (C)} p • {c (D)} q{c (A)} m • {c (B)} n的转化率。
【第三版块】K值的综合运用2、K值的影响因素板块1-识记K值的影响因素【经典例题】【例1】二氧化硫和氮的氧化物是常用的工业原料,但也是大气的主要污染物。
综合治理器污染是环境化学当前的重要研究内容之一。
硫酸生产中,SO2催化氧化成SO3:2SO2(g)+O2(g) 2SO3(g)。
某温度下,SO2的平衡转化率(α)与体系总压强(P)的关系如图1所示。
根据图示回答下列问题:(1)将2.0mol SO2和1.0molO2置于10L密闭容器中,反应达平衡后,体系总压强为0.10MPa。
该反应的平衡常数等于。
(2)平衡状态由A变到B时,平衡常数K(A) K(B)(填“>”、“<”或“=”)。
图板块2-判断外界条件对K值大小的影响【经典例题】【例1】已知可逆反应2NO(g) N2(g)+02(g)。
若在某温度下达到平衡时c(N2)=0.05mol·L-1,C(O2)=0.05mol·L-1,c(NO)=0.00055mol·L-1该反应的平衡常数为_____________。
保持温度不变,将容器体积缩小一半,则平衡常数为_________。
【例2】二氧化硫和氮的氧化物是常用的化工原料,但也是大气的主要污染物。
综合治理其污染是环境化学当前的重要研究内容之一。
(1)硫酸生产中,SO2催化氧化生成SO3:2SO2(g)+O2(g)催化剂2SO3(g)。
某温度下,△SO2的平衡转化率(α)与体系总压强(p)的关系如图所示。
根据图示回答下列问题:①将2.0 mol SO2和1.0 mol O2置于10 L 密闭容器中,反应达平衡后,体系总压强为0.10 MPa。
该反应的平衡常数等于____________。
②平衡状态由A变到B时,平衡常数K(A)_______K(B)(填“>”、“<”或“=”)。
(2)用CH4催化还原NO x可以消除氮氧化物的污染。
例如:CH4(g)+4NO2(g) = 4NO(g)+CO2(g)+2H2O(g);△H =-574 kJ/molCH4(g)+4NO(g) = 2N2(g)+CO2(g)+2H2O(g);△H =-1160 kJ/mol若用标准状况下4.48 L CH4还原NO2至N2,整个过程中转移的电子总数为_____________(阿伏加德罗常数的值用N A表示),放出的热量为_________kJ。
板块3-熟练运用三段式的计算方法【经典例题】3、K值的综合运用板块1-反应速率【经典例题】【例1】一定条件下,在体积为3L的密闭容器中,一氧化碳与氢气反应生成甲醇(催化剂为Cu2O/ZnO);CO(g)+2H2(g)CH3OH(g)。
根据题意完成下列各题:(1)反应达到平衡时,平衡常数表达式K= ,升高温度,K值(填“增大”、“减小”或“不变”)。
(2)在500℃,从反应开始到平衡,氢气的平均反应速率ν(H2)= 。
(3)在其他条件不变的情况下,对处于E点的体系体积压缩到原来的1/2,下列有关该体系的说法正确的是。
a.氢气的浓度减少b.正反应速率加快,逆反应速率也加快c.甲醇的物质的量增加n(H2)d.重新平衡时n(CH3OH)(4)据研究,反应过程中起催化作用的为Cu2O,反应体系中含少量CO2有利于维持催化剂Cu2O的量不变,原因是:(用化学方程式表示)。
【例2】某化学反应2A B+D在四中不同条件下进行,B、D起始浓度为0,反应物A的浓度(mol/L)随反应时间(min)的变化情况如下表:根据上述数据,完成下列填空:(1)在实验1,反应在10~20min 时间内平均速率为 mol/(L·min)。
(2)在实验2,A 的初始浓度c 2= mol/L ,反应经20min 就达到平衡,可推测实验2中还隐含的条件是 。
(3)设实验3的反应速率为v 3,实验1的反应速率为v 1,则v 3 v 1(填>、=、<),且c 31.0 mol/L(填>、=、<)(4)比较试验4和实验1,可推测该反应是 反应(选填吸热、放热),理由是板块2-转化率【经典例题】【例1】对于一般的可逆反应mA+nB pC+qD ,在一定温度下达平衡时反应物及生成物浓度满足下面关系:n m qp B A D C ][][][][••=K ,式中K 为常数,在密闭容器中给CO 和水蒸气的混合物加热到800℃时,有下列平衡:CO+H 20C02+H 2且K=1,若用2molCO 和10molH 20(气)相互混合并加热到800℃,达平衡时CO的转化率约为( )A.16.7%B.50%C.66.7%D.83%【例2】某温度下,H2(g)+CO2(g) H2O(g)+CO(g)的平衡常数9K 。
该温度下在甲、乙、丙4三个恒容密闭容器中,投入H2(g)和CO2(g),的是其起始浓度如右表所示。
下列判断不正确...( )A、平衡时,乙中CO2的转化率大于60%B、平衡时,甲中和丙中H2的转化率均是60%C、平衡时,丙中c(CO2)是甲中的2倍,是0.012mol/LD、反应开始时,丙中的反应速率最快,甲中的反应速率最慢板块3-平衡移动【经典例题】【例1】水煤气(主要成分:CO、H2 ) 是重要燃料和化工原料,可用水蒸气通过炽热的炭层制得:C (s) + H2O(g)CO (g) +H2(g);△H =+131.3kJ•mol-1(1)某温度下,四个容器中均进行着上述反应,各容器中炭足量,其它物质的物质的量浓度及正逆反应速率关系如下表所示。
请填写表中相应的空格。
容器编号c(H2O)/mol·L-1c(CO)/mol·L-1c(H2)/mol·L-1V正、V逆比较I 0.06 0.60 0.10V正=V逆II 0.06 0.50 0.40 ①?III 0.12 0.40 0.80V正<V逆IV 0.12 0.30 ②?V正=V逆压下,向其中加入1.0mol炭和1.0mol水蒸气(H216O),发生上述反应,达到平衡时,容器的体积变为原来的1.25 倍。
平衡时水蒸气的转化率为;向该容器中补充a mol 炭,水蒸气的转化率将(填“增大”、“减小”、“不变”),再补充a mol 水蒸气(H218O), 最终容器中C16O和C18O 的物质的量之比为。