高中化学选修三选修物质结构与性质第三章第章常见晶体结构晶胞分析归纳整理总结
- 格式:doc
- 大小:26.00 KB
- 文档页数:3

【人教版】高中化学选修3知识点总结:第三章晶体构造与特性
1. 晶体的基本概念
- 晶体是由原子、离子或分子以一定的方式排列形成的固体物质。
- 晶体的结构由晶格和基元组成。
晶格是由离子或原子排列所形成的三维重复结构,基元是晶格中最小的具有完整晶体结构的部分。
2. 晶体的分类
- 按照构成晶体的粒子种类可分为离子晶体、原子晶体和分子晶体。
- 按照晶体的组成方式可分为金属晶体、离子晶体、共价晶体和导电晶体等。
3. 晶体的结构与性质
- 晶体的结构决定了其性质。
晶体的结构可以通过X射线衍射实验来确定。
- 晶体的性质包括硬度、熔点、热胀冷缩性、电导率、光学性质等。
4. 离子晶体的结构与性质
- 离子晶体的结构是由正、负离子按一定比例排列形成的。
- 离子晶体具有高熔点、脆性、电解质导电性等特点。
5. 共价晶体的结构与性质
- 共价晶体是由原子通过共价键相互连接而成的。
- 共价晶体具有较高的熔点、硬度和脆性,不导电。
6. 金属晶体的结构与性质
- 金属晶体是由金属原子通过金属键相互连接而成的。
- 金属晶体具有良好的导电性、导热性和延展性。
7. 晶体缺陷
- 晶体缺陷是指晶体中原子或离子的位置发生偏离或缺失的现象。
- 晶体缺陷包括点缺陷、面缺陷和体缺陷。
以上是第三章晶体构造与特性的知识点总结,希望对你的学习有所帮助。
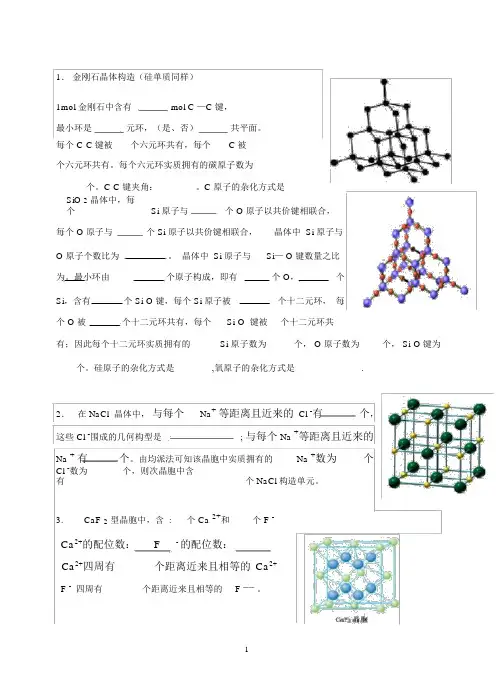
1.金刚石晶体构造(硅单质同样)1mol 金刚石中含有mol C —C 键,最小环是元环,(是、否)共平面。
每个 C-C 键被 ___个六元环共有,每个 C 被 _____个六元环共有。
每个六元环实质拥有的碳原子数为______个。
C-C 键夹角: _______。
C 原子的杂化方式是 ______SiO 2晶体中,每个Si 原子与个 O 原子以共价键相联合,每个 O 原子与个 Si 原子以共价键相联合,晶体中 Si 原子与O 原子个数比为。
晶体中 Si 原子与Si— O 键数量之比为。
最小环由个原子构成,即有个 O,个Si,含有个 Si-O 键,每个 Si 原子被个十二元环,每个 O 被个十二元环共有,每个Si-O 键被 __个十二元环共有;因此每个十二元环实质拥有的Si 原子数为 _____个, O 原子数为 ____个, Si-O 键为____个。
硅原子的杂化方式是 ______,氧原子的杂化方式是_________.2.在 NaCl 晶体中,与每个Na+等距离且近来的 Cl -有个,这些 Cl -围成的几何构型是; 与每个 Na +等距离且近来的Na +有个。
由均派法可知该晶胞中实质拥有的Na +数为____个Cl -数为 ______ 个,则次晶胞中含有_______个 NaCl 构造单元。
3.CaF 2型晶胞中,含 :___个 Ca 2+和 ____个 F -Ca2+的配位数:F- 的配位数:Ca2+四周有 ______个距离近来且相等的Ca2+F -四周有_______个距离近来且相等的 F ——。
14.如图为干冰晶胞(面心立方聚积),CO2分子在晶胞中的地点为;每个晶胞含二氧化碳分子的个数为;与每个二氧化碳分子等距离且最近的二氧化碳分子有个。
5.如图为石墨晶体构造表示图,每层内 C 原子以键与四周的个C原子联合,层间作使劲为;层内最小环有_____个 C 原子构成;每个 C 原子被个最小环所共用;每个最小环含有个C原子,个 C—C键;因此 C 原子数和 C-C 键数之比是 _________。

高中化学选修3知识点总结主要知识要点:1、原子结构2、元素周期表和元素周期律3、共价键4、分子的空间构型5、分子的性质6、晶体的结构和性质(一)原子结构1、能层和能级( 1)能层和能级的划分①在同一个原子中,离核越近能层能量越低。
②同一个能层的电子,能量也可能不同,还可以把它们分成能级s、p、d、f,能量由低到高依次为s、p、 d、 f。
③任一能层,能级数等于能层序数。
④ s、 p、 d、 f,, 可容纳的电子数依次是1、 3、 5、7,, 的两倍。
⑤能层不同能级相同,所容纳的最多电子数相同。
( 2)能层、能级、原子轨道之间的关系每能层所容纳的最多电子数是:2n2( n:能层的序数)。
主要知识要点:1、原子结构2、元素周期表和元素周期律3、共价键4、分子的空间构型5、分子的性质6、晶体的结构和性质(一)原子结构1、能层和能级( 1)能层和能级的划分①在同一个原子中,离核越近能层能量越低。
②同一个能层的电子,能量也可能不同,还可以把它们分成能级s、p、d、f,能量由低到高依次为s、p、 d、 f。
③任一能层,能级数等于能层序数。
④ s、 p、 d、 f,, 可容纳的电子数依次是1、 3、 5、7,, 的两倍。
⑤能层不同能级相同,所容纳的最多电子数相同。
( 2)能层、能级、原子轨道之间的关系每能层所容纳的最多电子数是:2n2( n:能层的序数)。
主要知识要点:1、原子结构2、元素周期表和元素周期律3、共价键4、分子的空间构型5、分子的性质6、晶体的结构和性质(一)原子结构1、能层和能级( 1)能层和能级的划分①在同一个原子中,离核越近能层能量越低。
②同一个能层的电子,能量也可能不同,还可以把它们分成能级s、p、d、f,能量由低到高依次为s、p、 d、 f。
③任一能层,能级数等于能层序数。
④ s、 p、 d、 f,, 可容纳的电子数依次是1、 3、 5、7,, 的两倍。
⑤能层不同能级相同,所容纳的最多电子数相同。

高中化学选修三晶胞的计算总结!新课标Ⅰ、Ⅱ、Ⅲ卷、海南等地的高考真题中有一道选作题为选修3·物质结构与性质内容,分值约为15分,其中最后一问一般考查晶胞的相关计算,这部分内容很难,很多同学对此不知如何下手,甚至放弃,但只要掌握技巧,此问题就能迎刃而解,今天小编为大家进行了总结。
1、要清楚几个基本的计算公式:2、能用均摊法计算出晶胞中每种原子的个数。
方法如下:(1)顶点上的原子,被8个晶体所共用,对每一个晶体只提供1/8(2)棱边上的原子,被4个晶体所共用,对每一个晶体只提供1/4(3)面心上的原子,被2个晶体所共用,对每一个晶体只提供1/2(4)体心上的原子,被1个晶体所共用,对每一个晶体只提供1栗子:如下图,是某晶体最小的结构单元,试写出其化学式。
根据均摊法,得出:化学式为xy3z。
3、得出晶胞中所含有的原子的个数。
4、根据题目要求,结合以上三点,计算所求的量如密度、空间利用率、晶胞参数等。
【好题演练】1(选自2016·新课标Ⅱ)某镍白铜合金的立方晶胞结构如图所示。
①晶胞中铜原子与镍原子的数量比为_____。
②若合金的密度为dg/cm3,晶胞参数a=________nm.答案【解析】铜失去的是全充满的3d10电子,镍失去的是4s1电子,所以ICu>INi。
(4)①根据均摊法计算,晶胞中铜原子个数为6×1/2=3,镍原子的个数为8×1/8=1,则铜和镍的数量比为3:1。
②根据上述分析,该晶胞的组成为Cu3Ni,若合金的密度为dg/cm3,根据p=m÷V,则晶胞参数a=nm。
【考点】晶胞的计算。
2(选自2016·新课标Ⅲ)砷化镓(GaAs)是优良的半导体材料,可用于制作微型激光器或太阳能电池的材料等。
回答问题:GaAs的熔点为1238℃,密度为ρg·cm-3,其晶胞结构如图所示。
该晶体的类型为________________,Ga与As以________键键合。


【人教版】高中化学选修3知识点总结:第三章晶体排列与特性
本文档总结了高中化学选修3课程中第三章晶体排列与特性的主要知识点。
一、晶体的定义和特点
- 晶体是具有规则的、有序的三维排列的固体结构。
- 晶体呈现出明显的平面、直线和点的等级性。
- 晶体有着明确的晶体结构和晶体缺陷。
二、晶体排列
- 晶体的排列方式主要有原子堆积和离子堆积两种。
- 原子堆积有3种典型的结构类型:简单立方堆积、面心立方堆积和密堆积。
- 离子堆积有3种典型的排列方式:简单立方堆积、体心立方堆积和面心立方堆积。
三、晶体的类型
- 晶体分为金属晶体、离子晶体、共价晶体和分子晶体四种类型。
- 金属晶体由金属原子组成,具有良好的导电性和热导性。
- 离子晶体由阳离子和阴离子组成,具有高熔点和良好的溶解性。
- 共价晶体由共价键连接的原子组成,具有高硬度和高熔点。
- 分子晶体由分子间的弱力相互作用连接的组成,具有低熔点和易溶性。
四、晶体的缺陷
- 晶体的缺陷分为点缺陷、线缺陷和面缺陷。
- 点缺陷包括空位、间隙原子和杂质原子等。
- 线缺陷包括位错和螺旋位错。
- 面缺陷包括阴极空位和阳极不完整等。
以上是高中化学选修3课程中第三章晶体排列与特性的知识点总结。
以上信息仅供参考,如有需要请自行查阅教材或参考其他可靠资料确认。



选修三物质结构与性质总结一.原子结构与性质.1、认识原子核外电子运动状态,了解电子云、电子层(能层)、原子轨道(能级)的含义.电子云:用小黑点的疏密来描述电子在原子核外空间出现的机会大小所得的图形叫电子云图.离核越近,电子出现的机会大,电子云密度越大;离核越远,电子出现的机会小,电子云密度越小.电子层(能层):根据电子的能量差异和主要运动区域的不同,核外电子分别处于不同的电子层.原子由里向外对应的电子层符号分别为K、L、M、N、O、P、Q.原子轨道(能级即亚层):处于同一电子层的原子核外电子,也可以在不同类型的原子轨道上运动,分别用s、p、d、f表示不同形状的轨道,s轨道呈球形、p轨道呈纺锤形,d轨道和f轨道较复杂.各轨道的伸展方向个数依次为1、3、5、7.2.(构造原理)了解多电子原子中核外电子分层排布遵循的原理,能用电子排布式表示1~36号元素原子核外电子的排布.(1).原子核外电子的运动特征可以用电子层、原子轨道(亚层)和自旋方向来进行描述.在含有多个核外电子的原子中,不存在运动状态完全相同的两个电子.(2).原子核外电子排布原理.①.能量最低原理:电子先占据能量低的轨道,再依次进入能量高的轨道.②.泡利不相容原理:每个轨道最多容纳两个自旋状态不同的电子.③.洪特规则:在能量相同的轨道上排布时,电子尽可能分占不同的轨道,且自旋状态相同.洪特规则的特例:在等价轨道的全充满(p6、d10、f14)、半充满(p3、d5、f7)、全空时(p0、d0、f0)的状态,具有较低的能量和较大的稳定性.如24Cr [Ar]3d54s1、29Cu [Ar]3d104s1.(3).掌握能级交错1-36号元素的核外电子排布式.ns<(n-2)f<(n-1)d<np3.元素电离能和元素电负性第一电离能:气态电中性基态原子失去1个电子,转化为气态基态正离子所需要的能量叫做第一电离能。
常用符号I1表示,单位为kJ/mol。


【人教版】高中化学选修3知识点总结:
第三章晶体构造与属性
晶体构造与属性是高中化学选修3课程中的重要内容。
本章主
要讲解了晶体的特点、晶体的拓扑结构、晶体的点阵和晶体的性质
等知识点。
1. 晶体的特点
- 晶体是由一定规律排列的原子、离子或分子组成的固体物质。
- 晶体具有规则的几何外形,有明确的晶面和晶点。
- 晶体中离子、原子或分子按照一定规律排列形成周期性结构,具有长程有序性。
2. 晶体的拓扑结构
- 晶体的拓扑结构是指晶体中原子、离子或分子之间的连接关
系和排列方式。
- 晶体可分为离子晶体、共价晶体和金属晶体等不同类型。
3. 晶体的点阵
- 晶体的点阵是晶体中最小的周期结构单元,在三维空间中重复排列形成整个晶体结构。
- 常见的晶体点阵有立方晶系、正交晶系、单斜晶系、正六角晶系等。
4. 晶体的性质
- 晶体的物理性质:晶体具有明确的熔点、硬度和透明度等特性。
- 晶体的光学性质:晶体对光具有不同的折射、吸收、散射和偏振等特性。
- 晶体的磁性性质:晶体中的离子或原子在外磁场作用下表现出不同的磁性行为。
以上是关于【人教版】高中化学选修3知识点总结中第三章晶体构造与属性的内容概述。
详细内容请参考教材或其他可靠资料。
高中化学-选修3第三章-晶体结构与性质-知识汇总work Information Technology Company.2020YEAR高中化学选修3第三章晶体结构与性质知识汇总高中化学选修三的第三章知识汇总,晶体结构这部分知识经常出现在推断题中【课标要求】1.了解化学键和分子间作用力的区别。
2.理解离子键的形成,能根据离子化合物的结构特征解释其物理性质。
3.了解原子晶体的特征,能描述金刚石、二氧化硅等原子晶体的结构与性质的关系。
4.理解金属键的含义,能用金属键理论解释金属的一些物理性质。
5.了解分子晶体与原子晶体、离子晶体、金属晶体的结构微粒、微粒间作用力的区别。
【要点精讲】一.晶体常识1.晶体与非晶体比较2.获得晶体的三条途径①熔融态物质凝固。
②气态物质冷却不经液态直接凝固(凝华)。
③溶质从溶液中析出。
3.晶胞晶胞是描述晶体结构的基本单元。
晶胞在晶体中的排列呈“无隙并置”。
4.晶胞中微粒数的计算方法——均摊法如某个粒子为n个晶胞所共有,则该粒子有1/n属于这个晶胞。
常见的晶胞为立方晶胞。
立方晶胞中微粒数的计算方法如下:注意:在使用“均摊法”计算晶胞中粒子个数时要注意晶胞的形状二.四种晶体的比较晶体熔、沸点高低的比较方法(1)不同类型晶体的熔、沸点高低一般规律:原子晶体>离子晶体>分子晶体。
金属晶体的熔、沸点差别很大,如钨、铂等熔、沸点很高,汞、铯等熔、沸点很低。
(2)原子晶体由共价键形成的原子晶体中,原子半径小的键长短,键能大,晶体的熔、沸点高。
如熔点:金刚石>碳化硅>硅(3)离子晶体一般地说,阴阳离子的电荷数越多,离子半径越小,则离子间的作用力就越强,相应的晶格能大,其晶体的熔、沸点就越高。
(4)分子晶体①分子间作用力越大,物质的熔、沸点越高;具有氢键的分子晶体熔、沸点反常的高。
②组成和结构相似的分子晶体,相对分子质量越大,熔、沸点越高。
③组成和结构不相似的物质(相对分子质量接近),分子的极性越大,其熔、沸点越高。
《晶体结构与性质》总结一、分子晶体:1.间以(,)相结合的晶体叫分子晶体(1)构成分子晶体的粒子是。
(2)粒子间的相互作用是。
(3)分子间作用力(范德华力<氢键)远化学键的作用;(4)分子晶体熔化破坏的是。
2.典型的分子晶体:(1)非金属氢化物:例(2)酸:例(3)部分非金属单质::例(4)部分非金属氧化物: 例(5)大多数有机物:例3.分子晶体结构:(1)只有范德华力,无分子间氢键的——分子密集堆积,如:C60、干冰、O2每个分子周围有个紧邻的分子,面心立方构型(2)有分子间氢键的——不具有分子密集堆积特征,如:HF 、冰、NH3冰中1个水分子周围有个水分子,1mol冰周围有mol氢键。
4.分子晶体熔沸点判断:的物质,越大,分子间作用力越大;分子量相等或相近,性分子的范德华力大,物质熔化和汽化时需要的能量就越多,物质的熔、沸点就越。
含有分子间氢键的,熔沸点较。
在烷烃的同分异构体中,一般来说,支链数越多,熔沸点越。
二、原子晶体:1.所有的相邻间都以相结合而形成空间立体网状结构的晶体。
(1)构成原子晶体的粒子是,(2)原子间以较强的相结合。
(3)整块晶体是一个三维的共价键网状结构,(4)原子晶体熔化破坏的是。
2.常见的原子晶体(1)某些非金属单质:硼(B)(2)某些非金属化合物:碳化硅(SiC)氮化硼(BN)(3)某些氧化物:Al2O3晶体3.原子晶体结构:金刚石晶体中:每个碳原子以与周围个碳原子结合,成为正四面体结构,碳以杂化轨道形成键。
向空间发展,彼此联结的立体网状结构,其中形成的最小环中含个碳原子。
每个碳原子被12个环共用。
1mol金刚石中含有的C-C共价键数mol。
在SiO2晶体中:①每个Si原子以个共价键结合个O原子;同时,每个O原子结合个Si原子。
SiO2晶体是由Si原子和O原子按的比例所组成的立体网状的晶体。
②最小的环是由个Si原子和个O原子组成的元环。
③1mol SiO2中含mol Si—O键。
【人教版】高中化学选修3知识点总结:第三章晶体形态与特征
本文档总结了高中化学选修3教材中第三章晶体形态与特征的知识点。
1. 晶体的概念和结构特点
- 晶体是由具有一定空间有序性的原子、离子或分子组成的凝聚态物质。
- 晶体的结构特点包括周期性、长程有序性和层状结构。
2. 晶体的晶体系和晶体面
- 晶体系根据对称性可分为三类:立方晶系、四方晶系和六角晶系。
- 晶体面是晶体表面的平坦部分。
3. 晶体的晶胞和晶格
- 晶胞是最小重复单元,包含了晶体的全部结构信息。
- 晶格是晶胞在空间中无限重复所形成的排列。
4. 晶体的晶体缺陷
- 晶体缺陷是指晶体中存在的结构异常或杂质。
- 晶体缺陷包括点缺陷、线缺陷和面缺陷。
5. 晶体的晶体学性质
- 晶体的晶体学性质包括透明性、折射性和散射性等。
- 不同晶体的晶体学性质有所差异。
以上是第三章晶体形态与特征的知识点总结,希望对您有帮助。
参考资料:
- 《高中化学选修3》人教版。
高三选修3晶胞知识点晶胞是晶体中最小重复单元,它的形状和结构对于晶体性质的理解具有重要的作用。
在高三选修3中学习晶胞的知识点对于理解晶体结构和材料科学具有重要意义。
本文将从三个方面介绍高三选修3中的晶胞知识点。
第一部分:晶胞的定义和分类晶胞是晶体中最小重复单元,由原子或分子组成。
根据晶体的对称性,我们可以将晶胞分为7个晶系和14个晶格。
1. 立方晶系:晶胞为立方体,边长相等,相互垂直。
2. 正交晶系:晶胞为长方体,边长相互垂直,但不相等。
3. 单斜晶系:晶胞为斜方体,边长不相等,存在一个直角。
4. 斜方晶系:晶胞为斜方体,边长不相等,所有角均不为直角。
5. 三斜晶系:晶胞为斜四面体,边长不相等,所有角均不为直角。
6. 菱面晶系:晶胞为菱形面体,边长不相等,存在4个相邻的直角。
7. 六方晶系:晶胞为六面体,边长不相等,存在6个角为直角。
以上是根据晶体对称性所确定的晶胞分类,不同晶胞的形状和结构决定了晶体的不同性质和应用。
第二部分:晶胞参数及其计算方法晶体的晶胞参数是描述晶体结构的重要参数,包括晶胞长度、晶胞角度等。
1. 晶胞长度:晶胞的长度由晶格常数确定,晶格常数是指晶体沿不同方向上的原子、离子或分子排列的周期性重复距离。
2. 晶胞角度:晶胞的角度也由晶格常数决定,不同晶体的晶胞角度不同。
计算晶胞参数的方法包括使用X射线衍射、粉末衍射和电子衍射等实验方法,以及分子动力学模拟和第一性原理计算等理论方法。
这些方法可以精确确定晶体的晶胞结构,为材料科学的研究提供重要的依据。
第三部分:晶胞的应用和意义晶胞的形状和结构对晶体的性质和应用具有重要的影响。
1. 晶胞的形状决定了晶体的外观和结构,不同晶体的晶胞形状各异。
2. 晶胞的结构决定了晶体的物理和化学性质,如硬度、电导率、光学性质等。
3. 晶胞的研究为材料科学和固体物理学等领域提供了重要的基础,促进了材料的开发和应用。
总结:本文介绍了高三选修3中的晶胞知识点,包括晶胞的定义和分类、晶胞参数及其计算方法,以及晶胞的应用和意义。
晶体结构与性质一、晶体的常识1.晶体与非晶体晶体与非晶体的本质差异自范性微观结构晶体有(能自发呈现多面体外形)原子在三维空间里呈周期性有序排列非晶体无(不能自发呈现多面体外形)原子排列相对无序晶体呈现自范性的条件:晶体生长的速率适当得到晶体的途径:熔融态物质凝固;凝华;溶质从溶液中析出特性:①自范性;②各向异性(强度、导热性、光学性质等)③固定的熔点;④能使X-射线产生衍射(区分晶体和非晶体最可靠的科学方法)2.晶胞--描述晶体结构的基本单元,即晶体中无限重复的部分一个晶胞平均占有的原子数=×晶胞顶角上的原子数+×晶胞棱上的原子+×晶胞面上的粒子数+1×晶胞体心内的原子数思考:下图依次是金属钠(Na)、金属锌(Zn)、碘(I2)、金刚石(C)晶胞的示意图,它们分别平均含几个原子?eg:1.晶体具有各向异性。
如蓝晶(Al2O3·SiO2)在不同方向上的硬度不同;又如石墨与层垂直方向上的电导率和与层平行方向上的电导率之比为1:1000。
晶体的各向异性主要表现在()①硬度②导热性③导电性④光学性质A.①③B.②④C.①②③D.①②③④2.下列关于晶体与非晶体的说法正确的是()A.晶体一定比非晶体的熔点高B.晶体一定是无色透明的固体C.非晶体无自范性而且排列无序D.固体SiO2一定是晶体3.下图是CO2分子晶体的晶胞结构示意图,其中有多少个原子?二、分子晶体与原子晶体1.分子晶体--分子间以分子间作用力(范德华力、氢键)相结合的晶体注意:a.构成分子晶体的粒子是分子b.分子晶体中,分子内的原子间以共价键结合,相邻分子间以分子间作用力结合①物理性质a.较低的熔、沸点b.较小的硬度c.一般都是绝缘体,熔融状态也不导电d.“相似相溶原理”:非极性分子一般能溶于非极性溶剂,极性分子一般能溶于极性溶剂②典型的分子晶体a.非金属氢化物:H2O、H2S、NH3、CH4、HX等b.酸:H2SO4、HNO3、H3PO4等c.部分非金属单质::X2、O2、H2、S8、P4、C60d.部分非金属氧化物:CO2、SO2、NO2、N2O4、P4O6、P4O10等f.大多数有机物:乙醇,冰醋酸,蔗糖等③结构特征a.只有范德华力--分子密堆积(每个分子周围有12个紧邻的分子)CO2晶体结构图b.有分子间氢键--分子的非密堆积以冰的结构为例,可说明氢键具有方向性④笼状化合物--天然气水合物2.原子晶体--相邻原子间以共价键相结合而形成空间立体网状结构的晶体注意:a.构成原子晶体的粒子是原子 b.原子间以较强的共价键相结合①物理性质a.熔点和沸点高b.硬度大c.一般不导电d.且难溶于一些常见的溶剂②常见的原子晶体a.某些非金属单质:金刚石(C)、晶体硅(Si)、晶体硼(B)、晶体锗(Ge)等b.某些非金属化合物:碳化硅(SiC)晶体、氮化硼(BN)晶体c.某些氧化物:二氧化硅( SiO2)晶体、Al2O3金刚石的晶体结构示意图二氧化硅的晶体结构示意图思考:1.怎样从原子结构角度理解金刚石、硅和锗的熔点和硬度依次下降2.“具有共价键的晶体叫做原子晶体”,这种说法对吗?eg:1.在解释下列物质性质的变化规律与物质结构间的因果关系时,与键能无关的变化规律是()A.HF、HCI、HBr、HI的热稳定性依次减弱B.金刚石、硅和锗的熔点和硬度依次下降C.F2、C12、Br2、I2的熔、沸点逐渐升高D.N2可用做保护气2.氮化硼是一种新合成的无机材料,它是一种超硬耐磨、耐高温、抗腐蚀的物质。
个六元环共有。
每个六元环实际拥有的碳原子数为
______个。
C-C键夹角:_______。
C原子的杂化方式是______
SiO2晶体中,每个Si原子与个O原子以共价键相结合,每个O原子与个Si 原子以共价键相结合,晶体中Si原子与O原子个数比为。
晶体中Si原子与Si—O键数目之比为。
最小环由个原子构成,即有个O,个Si,含有个Si-O键,每个Si原子被个十二元环,每个O被个十二元环共有,每个Si-O键被__个十二元环共有;所以每个十二元环实际拥有的Si原子数为_____个,O原子数为____个,Si-O键为____个。
硅原子的杂化方式是______,氧原子的杂化方式是_________.
知该晶胞中实际拥有的Na+数为____个
Cl-数为______个,则次晶胞中含有_______个NaCl结构单元。
3. CaF2型晶胞中,含:___个Ca2+和____个F-
Ca2+的配位数: F-的配位数:
Ca2+周围有______个距离最近且相等的Ca2+
F- 周围有_______个距离最近且相等的F——。
4.如图为干冰晶胞(面心立方堆积),CO2分子在晶胞中的位置为;每个晶胞含二氧化碳分子的个数为;与每个二氧化碳分子等距离且最近的二氧化
碳分子有个。
5.如图为石墨晶体结构示意图,
每层内C原子以键与周围的个C原子结合,层间作用力为;层内最小环有 _____个C原子组成;每个C原子被个最小环所共用;每个最小环含有个C原子,个C—C键;所以C原子数和C-C键数之比是_________。
C原子的杂化方式是__________.
6.冰晶体结构示意如图,冰晶体中位于中心的一个水分子
周围有______个位于四面体顶角方向的水分子,每个水分子通过
______条氢键与四面体顶点上的水分子相连。
每个氢键被_____个
水分子共有,所以平均每个水分子有______条氢键。
7.金属的简单立方堆积是_________层通过_________对
_________堆积方式形成的,晶胞如图所示:每个金属阳离子的
配位数是_____,代表物质是________________________。
8.金属的体心立方堆积是__________层通过
________对________堆积方式形成的,晶胞如图:
每个阳离子的配位数是__________.代表物质是
_____________________。
9.金属晶体的六方最密堆积是______层的第一层和第三层通过______对_________堆
积方式形成的,晶胞如图:每个阳离子的配位数是_________.代表物质是________________。
10.金属晶体的面心立方堆积是______层的第一层和第三层通过________对_________
堆积方式形成的,晶胞如图:每个阳离子的配位数是_________.代表物质是_____________________。
位于同一层原子可能是图中的那些球有什么规律吗。