高中有机化学-烯烃
- 格式:ppt
- 大小:706.00 KB
- 文档页数:73


有机烯烃知识点总结一、烯烃的基本结构烯烃是一类含有碳碳双键结构的有机分子,通式为CnH2n。
根据碳碳双键的位置,烯烃可分为1-烯烃与2-烯烃两类。
1-烯烃是指含有一个碳碳双键的有机物,通式为CnH2n;2-烯烃是指含有两个相邻碳原子之间含有一个碳碳双键的有机物,通式为CnH2n-2。
在烯烃中,碳碳双键的存在赋予了分子特殊的物理和化学性质。
二、烯烃的性质1. 物理性质烯烃是无色气体或液体,密度小于水,易挥发。
烯烃在常温下具有较高的活性,极易发生化学反应。
2. 化学性质烯烃具有一系列特殊的化学性质,包括加成反应、环加成反应等。
烯烃中碳碳双键的存在使其在化学反应中显示出与饱和碳氢化合物明显不同的性质,如易发生加成反应,参与环加成反应等。
三、烯烃的合成方法1. 裂解法裂解法是指将高级碳氢化合物(如石油烃、天然气)在高温下通过催化剂的作用,裂解为低级碳氢化合物的方法。
采用裂解法可以制备大量的烯烃。
2. 烷基化法烷基化法是通过将醇、酚或卤代烷和金属钠在干燥无水溶剂或干燥乙醚中反应制得的一种合成烯烃的方法。
该方法适用于制备不对称烯烃。
3. 水合物脱水法水合物脱水法是指将醇或醚经过脱水作用生成烯烃的方法。
该方法通常需要通过酸催化剂或热脱水来实现。
四、烯烃的反应特点1. 加成反应烯烃具有较高的反应活性,易于发生加成反应。
加成反应是指在不饱和化合物中的碳碳双键上发生一种原子或原子团的加成反应,生成饱和化合物的过程。
2. 环加成反应环加成反应是指在不饱和化合物中的碳碳双键上发生一种特定的分子结构的加成反应,生成环状化合物的过程。
3. 氧化反应烯烃中的碳碳双键易于发生氧化反应,生成醇、醛、酮等化合物。
4. 卤代反应烯烃中的碳碳双键易于发生卤代反应,生成卤代烃的过程。
五、烯烃的应用领域1. 有机合成烯烃在有机合成中具有广泛的应用价值,如制备醇、醛、酮、醚等化合物。
2. 材料科学烯烃可以作为高分子材料的单体,用于制备聚烯烃类高分子材料,如聚乙烯、聚丙烯等。


有机化学中的烯烃类化合物烯烃是有机化合物的一类,其分子中含有一个或多个碳碳双键。
烯烃分为单烯和多烯两种类型。
单烯指的是分子中只有一个碳碳双键,而多烯则指的是分子中存在两个或两个以上的碳碳双键。
烯烃类化合物在有机合成和工业生产中具有重要的应用。
为了更好地理解和利用烯烃类化合物,我们有必要了解其结构、性质和反应。
第一节:单烯烃的结构和性质单烯烃是由碳和氢组成的化合物,其基本结构为碳链上有一个碳碳双键。
根据双键的位置,单烯可以分为顺式和反式两种构型。
顺式烯烃指的是两个双键上的取代基位于同一侧,而反式烯烃则指的是取代基位于两侧。
这两种构型的烯烃在物理性质和化学性质上有所区别。
顺式烯烃通常比反式烯烃具有较低的熔点和沸点,这是因为两个双键上的取代基在空间构型上相互接近,使分子间的相互作用增强,从而增加了相对的稳定性。
而反式烯烃则相对较不稳定。
第二节:单烯烃的反应由于双键的存在,单烯烃可以进行多种不同的反应,其中一些是与饱和烃相似的,而另一些是由于双键的特殊化学性质而独有的。
1. 加成反应单烯烃可以与一些试剂发生加成反应,其中最常见的是氢气的加成反应。
在存在催化剂的条件下,双键上的碳原子可以与氢原子结合,生成饱和烃。
这种反应称为氢化反应。
例如,乙烯可以在催化剂存在下与氢气反应,生成乙烷,反应方程式为:C2H4 + H2 → C2H6。
2. 氧化反应单烯烃可以与氧气发生氧化反应,生成醇、酮等化合物。
最典型的是乙烯的燃烧反应,乙烯与氧气在高温条件下反应,生成二氧化碳和水。
例如,乙烯的燃烧反应方程式为:C2H4 + 3O2 → 2CO2 + 2H2O。
3. 加聚反应单烯烃中的双键可以进行加聚反应,生成高聚物。
通过调节反应条件和催化剂的选择,可以合成不同类型的高聚物,例如乙烯可以通过合适的催化剂合成聚乙烯。
例如,乙烯的加聚反应方程式为:nC2H4 → -(-CH2-CH2-)n-。
第三节:多烯烃的结构和性质多烯烃是含有两个或两个以上碳碳双键的烯烃。


有机物烯烃知识点总结高中一、烯烃的定义烯烃是一类含有碳-碳双键的有机物,其分子结构含有至少一个碳-碳双键的化合物。
烯烃是烃类化合物的一种,其主要特点是含有C=C的结构,通式为CnH2n。
二、烯烃的分类1.按碳-碳双键的数目分:单烯、二烯、三烯等2.按碳-碳双键位置分:顺式烯烃、反式烯烃3.按分子链结构分:直链烯烃、支链烯烃4.按环烷烃与烯烃的共轭结构分:环烯烃、线烯烃三、烯烃的性质1.化学性质(1)烯烃可以进行加成反应,如水、氢等的加成反应。
(2)烯烃的碳-碳双键中的碳原子上的键角较大,具有较大的活性。
(3)烯烃可以进行聚合反应,形成聚烯烃。
2.物理性质(1)烯烃的沸点通常较低,易挥发。
(2)烯烃的密度小,易溶于非极性溶剂。
四、烯烃的制备方法1.从原油中提取2.用催化剂、裂解剂等从石油和天然气中裂解制得。
五、烯烃的应用1.工业上用作燃料2.用作合成高分子材料的原料3.用于制备有机合成试剂六、常见烯烃1.乙烯(ethylene),是一种最简单的烯烃,通式为C2H4,是化工行业中重要的原料。
2.丙烯(propylene),通式为C3H6,是一种重要的烯烃,用途广泛,可用于合成丙烯酸、丙烯腈等有机物。
七、烯烃的环境影响和安全防护1.烯烃易燃、爆炸,应当远离火源存放。
2.在使用烯烃时要注意通风,避免吸入毒气。
八、烯烃在环保方面的意义1.烯烃作为供能的一种形式,对环境的影响相对较小。
2.烯烃是合成高分子材料的主要原料,制备塑料等产品。
九、烯烃的研究与发展趋势1.烯烃的合成技术不断改进,降低成本,提高产率。
2.烯烃在新型材料研究中的应用不断拓展,如制备新型聚合物材料等。
总的来说,烯烃是一类重要的有机物,具有丰富的化学性质和广泛的应用价值。
随着科学技术的不断发展,烯烃的研究和应用领域将不断扩展,为人类社会的发展进步做出更多的贡献。
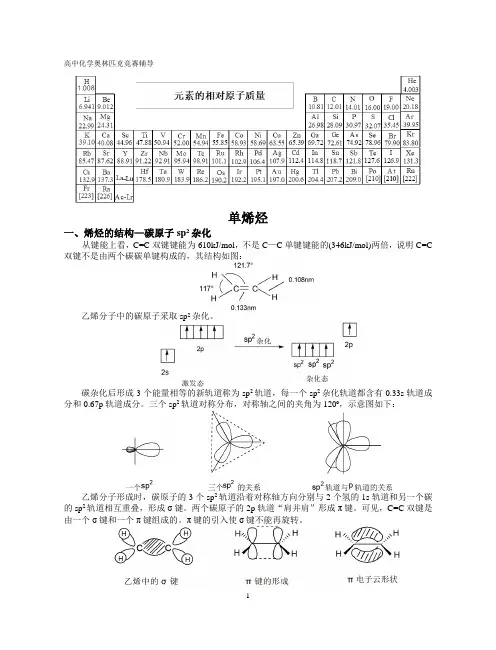
高中化学奥林匹克竞赛辅导单烯烃一、烯烃的结构—碳原子sp2杂化从键能上看,C=C双键键能为610kJ/mol,不是C—C单键键能的(346kJ/mol)两倍,说明C=C 双键不是由两个碳碳单键构成的,其结构如图:乙烯分子中的碳原子采取sp2杂化。
碳杂化后形成3个能量相等的新轨道称为sp2轨道,每一个sp2杂化轨道都含有0.33s轨道成分和0.67p轨道成分。
三个sp2轨道对称分布,对称轴之间的夹角为120º,示意图如下:乙烯分子形成时,碳原子的3个sp2轨道沿着对称轴方向分别与2个氢的1s轨道和另一个碳的sp2轨道相互重叠,形成σ键。
两个碳原子的2p轨道“肩并肩”形成π键。
可见,C=C双键是由一个σ键和一个π键组成的。
π键的引入使σ键不能再旋转。
碳碳双键中π键键能=碳碳双键键能—碳碳单键键能=615–348=267kJ/mol<348kJ/mol。
碳碳双键中π键的特点:①不如σ键牢固,π键键能(267kJ/mol)小于单键键能(348kJ/mol)。
②不能自由旋转(π键没有轨道轴的重叠)。
③电子云重叠少,不集中,易极化,发生反应。
二、烯烃的异构和命名1.烯烃的同分异构烯烃的同分异构包括碳链异构、C=C双键位置不同引起的位置异构和双键两侧的基团在空间的位置不同引起的顺反异构。
顺反异构:由于双键不能自由旋转,双键碳上所连接的四个原子或原子团是处在同一平面的,当双键的两个碳原子各连接两个不同的原子或原子团时,就能产生顺反异构体。
顺式烯烃是指两个双键碳原子的相同基团分布在C=C双键的同侧;反式烯烃是指两个双键碳原子的相同基团分布在C=C双键的异侧。
产生顺反异构体的必要条件:某个C=C双键碳原子上所连的两个基团要不同,两个C=C双键碳原子上所连的基团要有相同的。
顺反异构体的物理性质不同,因而分离它们并不很难。
2.烯烃的系统命名法(1)选主链:选择含C=C双键的最长碳链为主链,称为某烯。
(2)编号:从离C=C双键最近的主链碳原子一端开始依次编号。

有机化学基础知识点整理烯烃的结构与性质烯烃是有机化合物中一类重要的化合物,在有机化学中具有着重要的地位。
它们的分子结构中含有碳碳双键,因此在性质上与脂肪烃等饱和烃有着明显的区别。
本文将对烯烃的结构与性质进行整理,以帮助读者更好地理解有机化学中烯烃的基础知识。
一、结构特点烯烃的分子结构中含有碳碳双键,而双键的存在赋予了烯烃一系列的独特性质。
在烯烃中,碳原子通过双键连接,使得碳原子的杂化轨道从sp3杂化变为sp2杂化。
这种sp2杂化使得烯烃的结构变得扁平,具有较高的共轭能力。
另外,烯烃分子中的碳碳双键与单键之间存在π电子共轭,从而具有一系列重要的性质。
二、物理性质1. 烯烃的密度通常较小,且随着分子量的增大而增大;2. 烯烃的沸点较脂肪烃相对较低,且沸点随着碳链长度的增大而增大;3. 烯烃的溶解性较好,能够在非极性溶剂中溶解,但溶解度随着碳链长度的增大而减小。
三、化学性质1. 电子亲和性:由于双键的存在,烯烃具有较强的电子亲和性和容易发生加成反应的性质;2. 烯烃的加成反应:烯烃能够与许多物质发生加成反应,例如与卤素发生加成反应,生成二卤代烷烃;3. 烯烃的氧化反应:烯烃能够在氧气存在的条件下与氧气发生氧化反应,生成相应的醇或醛;4. 烯烃的聚合反应:烯烃具有聚合性,可以与自身发生聚合反应,形成高分子化合物。
四、常见的烯烃1. 乙烯:乙烯是最简单的烯烃,也是最重要的工业原料之一。
它是一种无色气体,在工业上广泛用于合成聚乙烯等高分子化合物;2. 丙烯:丙烯是一种常见的烯烃,具有重要的应用价值。
它可以用于制备丙烯酸、丙烯腈、丙烯酮等化学品,也可以用于合成高分子材料。
总结:烯烃作为有机化学中的重要研究对象,具有独特的结构与性质。
通过对烯烃结构特点、物理性质、化学性质以及常见种类的介绍,希望读者能够更好地掌握烯烃的基础知识,为进一步学习有机化学打下坚实的基础。
有关烯烃的更多应用以及不同衍生物的反应特性等内容,可以进一步探索和研究。

烯烃高中知识点总结一、基本概念1.1 烯烃的定义烯烃是一类含有碳碳双键的碳氢化合物,其通式为CnH2n。
烯烃是一类碳氢化合物中最简单的一类,一般来说,烯烃由一种碳碳双键构成,并且这种双键是由sp2杂化的碳原子形成的。
1.2 烯烃的命名烯烃的命名遵循着一定的规则,通常采用IUPAC命名法。
对于烯烃而言,其主链中双键所在的位置应该尽可能靠近最低的编号。
同时,在双键两侧的碳原子的序号应该尽可能小。
对于多个双键的烯烃而言,需要选择一个相对大编号和较少和定位双键的主链。
1.3 烯烃的分子结构烯烃分子结构中含有碳碳双键,这种双键是由两个sp2杂化的碳原子形成的。
由于碳碳双键中的π键的存在,烯烃的分子结构会影响其物理和化学性质。
二、结构特点2.1 碳碳双键的特点烯烃分子中的碳碳双键由两个sp2杂化的碳原子形成,因此,双键中存在着一个σ键和一个π键。
而π键是一种较弱的化学键,具有不饱和性,因此烯烃具有很高的活泼性和化学反应性。
2.2 碳碳双键的构型对于烯烃而言,碳碳双键的构型有两种可能性,即顺式构型和异式构型。
这两种构型主要是由于碳碳双键的空间构型不同造成的。
2.3 碳碳双键的立体化学由于碳碳双键具有不饱和性,因此烯烃在空间构型上有一定的限制。
一般来说,碳碳双键的平面结构是受到限制的,通常形成了平面三角形的结构。
三、性质3.1 化学性质烯烃是一类具有较高化学反应性的化合物,主要表现在其碳碳双键上。
烯烃的π键很容易发生加成反应、氧化反应等,因此烯烃具有较高的活泼性。
此外,烯烃还容易发生聚合反应,产生聚合物。
3.2 物理性质烯烃的物理性质与其分子构型和相互作用有关。
通常来说,烯烃具有较低的沸点、密度和相对较高的燃烧热。
而且烯烃在常温下通常是一种无色无味的气体或液体,但是由于其不饱和性,烯烃容易和空气中的氧气发生反应,因此需要储存和使用时需要特别小心。
3.3 活性烯烃由于其不饱和性,具有较高的活性。
烯烃通常很容易发生加成反应、氧化反应等。
有机烯烃知识点总结归纳一、烯烃的定义烯烃是一类含有碳碳双键的有机化合物。
其分子结构中含有一个或多个碳碳双键,而且分子中的C=C键为共轭双键。
由于共轭双键的存在,烯烃分子具有较高的反应活性,易发生加成反应、氧化反应等化学反应。
二、烯烃的结构与分类根据碳碳双键的位置和数量,烯烃可以分为链烯烃、环烯烃和共轭双烯烃三大类。
1. 链烯烃:分子中有一个碳碳双键,分子式为CnH2n。
2. 环烯烃:分子中含有一个碳碳双键,而且该双键与环状结构的其它碳原子相连。
3. 共轭双烯烃:分子中含有两个碳碳双键(通常是共轭排列),分子式为CnH2n-2。
三、烯烃的性质1. 物理性质:烯烃具有较低的沸点和熔点,大多数烯烃都是无色无味的液体,但也有部分是固体或气体。
2. 化学性质:烯烃具有较高的反应活性,易发生加成反应、氧化反应、裂解反应、聚合反应等化学反应。
由于C=C的存在,烯烃还可以发生环加成反应和立体选择性反应等特殊反应。
四、烯烃的合成烯烃的合成方法主要包括以下几种:1. 裂解:通过烃类、醇类、酮类等有机化合物的裂解反应制备烯烃。
2. 脱氢:通过脱氢反应制备烯烃,例如通过加热使醇类、烷烃等发生脱氢反应。
3. 氢化:通过氢化反应将炔烃转化为烯烃。
4. 烷基化:通过烷基化反应将烷基基团引入另一有机分子中,从而制备烯烃。
五、烯烃的应用1. 化工领域:烯烃广泛应用于柴油加氢裂化、烯烃烷基化、聚烯烃生产等化工生产工艺。
2. 医药领域:烯烃是一类重要的生物活性分子,许多药物的分子结构中含有烯烃基团,如β-胡萝卜素、维生素E等。
3. 农药领域:烯烃类农药具有广谱高效、毒性低、环境友好等特点,被广泛应用于农作物防治、病虫害防治等领域。
4. 香料领域:烯烃是许多香料的成分之一,具有独特的芳香味,被广泛应用于食品添加剂、香水等产品中。
5. 橡胶领域:烯烃是橡胶合成的主要原料之一,通过聚合反应可制备聚合物,并用于制备合成橡胶、塑料、纤维等产品。
高中烯烃知识点总结一、烯烃的结构特点烯烃分子中含有碳碳双键,这种双键结构赋予了烯烃独特的化学性质。
烯烃的双键结构使其具有较强的反应活性,易于发生加成反应和聚合反应。
由于烯烃分子中含有不饱和键,因此烯烃可以发生加成反应、氢化反应、卤代反应、酸碱反应等多种化学反应。
二、烯烃的制备方法1.裂解法:将高分子烃类化合物如石油、煤焦油等经加热裂解,在裂解产物中产生烯烃。
2.脱氢法:用氢化铝或氧化铬等催化剂将醇、醚等化合物进行脱氢反应,生成烯烃。
3.脱羧法:将羧酸类化合物在碱的作用下脱去羧基,生成烯烃。
4.添加剂法:将烷烃和醇类化合物在存在酸或碱催化剂的条件下进行脱氢反应,生成烯烃。
5.环化法:将环状化合物中的环裂开生成烯烃。
以上是常见的几种制备烯烃的方法,其中裂解法是目前工业上最常用的制备烯烃的方法。
三、烯烃的理化性质1. 烯烃的密度:烯烃的密度轻,比空气轻。
密度范围在0.65~0.75g/cm3。
2. 烯烃的沸点:烯烃的沸点通常较低,乙烯的沸点为-104℃,丙烯的沸点为-47℃。
3. 烯烃的燃烧性质:烯烃具有较高的燃烧热值,可以作为重要的燃料。
4. 烯烃的化学稳定性:烯烃具有良好的化学稳定性,但不饱和度较高,易于发生加成反应。
以上是烯烃的一些理化性质,这些性质对于烯烃的应用和研究具有重要意义。
四、烯烃的应用领域1. 燃料领域:烯烃是重要的燃料原料,可以用于制备乙烯、丙烯等烯烃类燃料。
目前,烯烃已经成为了工业生产中的重要燃料原料。
2. 化工领域:烯烃可以用于制备聚乙烯、聚丙烯等重要的聚合物,这些聚合物在塑料制品、合成纤维、涂料、胶粘剂等方面有着广泛的应用。
3. 医药领域:烯烃可以用于制备医药中的有机化合物,具有重要的生物活性,可用于制药工业。
4. 农药领域:烯烃可以用于制备各种农药原料,对农业生产有着重要的作用。
以上是烯烃在不同领域中的应用,可见烯烃在工业生产、生活和医药领域都有着广泛的应用前景。
五、烯烃的反应特点1. 加成反应:烯烃中的双键易于发生加成反应,如加氢、卤代反应等。