水密度和黏度随温度变化表
- 格式:pdf
- 大小:33.40 KB
- 文档页数:2
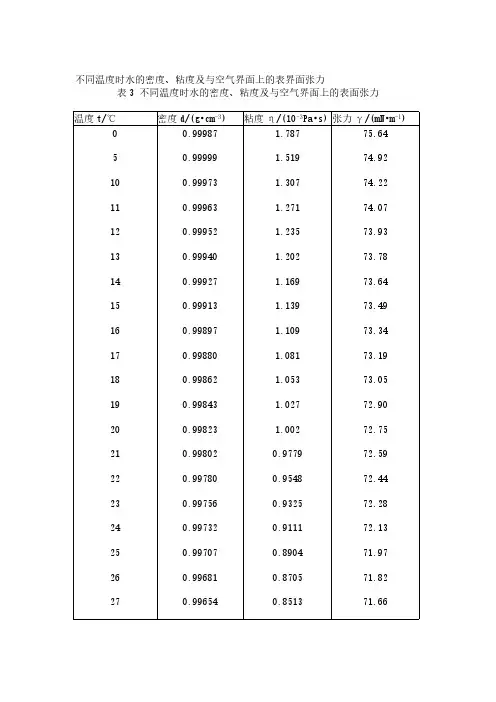
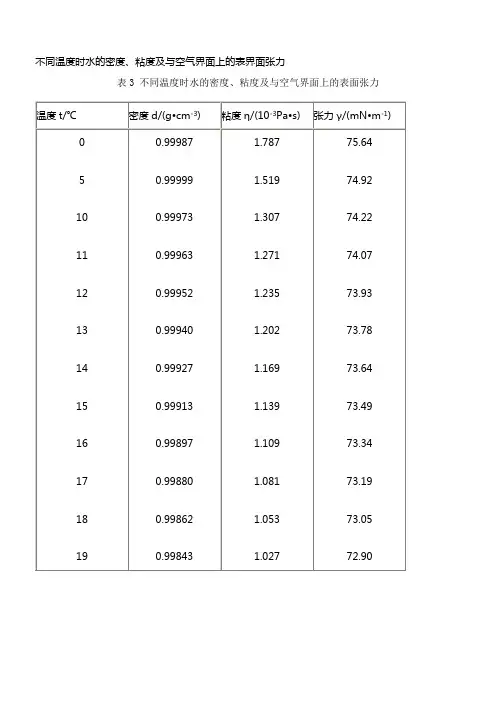
不同温度时水的密度、粘度及与空气界面上的表界面张力表3 不同温度时水的密度、粘度及与空气界面上的表面张力温度t/℃密度d/(g•cm-3)粘度η/(10-3Pa•s)张力γ/(mN•m-1)0 5 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 270.999870.999990.999730.999630.999520.999400.999270.999130.998970.998800.998620.998430.998230.998020.997800.997560.997320.997070.996810.996541.7871.5191.3071.2711.2351.2021.1691.1391.1091.0811.0531.0271.0020.97790.95480.93250.91110.89040.87050.851375.6474.9274.2274.0773.9373.7873.6473.4973.3473.1973.0572.9072.7572.5972.4472.2872.1371.9771.8271.662829304050600.996260.995970.995670.992240.988070.965340.83270.81480.79750.65290.54680.314771.5071.3571.1869.5667.9160.75在293K 下水的表面张力系数为72.75×10-3 N·m-1,乙醇为22.32×10-3N·m-1,正丁醇为24.6×10-3N·m-1,而水-正丁醇(4.1‰)的界面张力为34×10-3 N·m-1。
(1)定义或解释 ①促使液体表面收缩的力叫做表面张力[1]。
②液体表面相邻两部分之间,单位长度内互相牵引的力。

水的物理性质(温度-密度-粘度-饱和蒸汽压)水是生命之源,它在自然界中起着至关重要的作用。
为了深入理解和研究水的性质,我们需要了解水的物理性质。
本文将介绍水的温度、密度、粘度和饱和蒸汽压等方面的基本特性。
1. 温度温度是表示物体热量状态的物理量。
对于水来说,其特性是随着温度的变化而变化。
水的温度单位是摄氏度(℃)或开尔文(K),常温常压下的水温为20℃ 或 293.15 K。
水的温度与其物理性质密切相关。
随着温度的升高,水的密度会减小,粘度会降低,而饱和蒸汽压则会增加。
因此,在不同温度下,水的物理性质也会有所不同。
2. 密度密度是物质质量和体积的比值,通常用ρ表示。
水的密度在不同温度下会有所变化,这是因为温度会影响水分子的运动速度和分布,从而影响水的体积和密度。
在常温常压下,水的密度约为1 g/cm³。
随着温度的增加,水的密度逐渐降低,但这种变化不是线性的。
在4℃ 附近,水的密度取得最大值,约为 1.00 g/cm³,称为水的最密点。
当温度超过4℃ 时,水的密度逐渐降低,直到水的沸点时,密度约为 0.9584 g/cm³。
3. 粘度粘度是衡量流体内部摩擦阻力的物理量。
水是一种黏性较小的流体,但是其粘度也随着温度的变化而变化。
在不同温度下,水的粘度也会有所不同。
随着温度的升高,水分子的运动速度增加,分子间的距离加大,因此水的内部摩擦力减小,其粘度也会降低。
相反,当温度降低时,水的分子间距离缩小,内部摩擦力增强,其粘度也会增加。
4. 饱和蒸汽压饱和蒸汽压是指水蒸气在温度和压力的特定条件下与液态水达到相平衡时的压力。
这个值与温度有一定的关系。
随着温度的升高,水蒸气在相同的温度下可以容纳更多的水分子,因此饱和蒸汽压也会随之增大。
在100℃ 的沸点处,水的饱和蒸汽压为 1 atm(标准大气压),而在25℃ 的常温下,饱和蒸汽压约为 0.0313 atm。
总结水是一种重要的物质,在自然界中起着不可替代的作用。
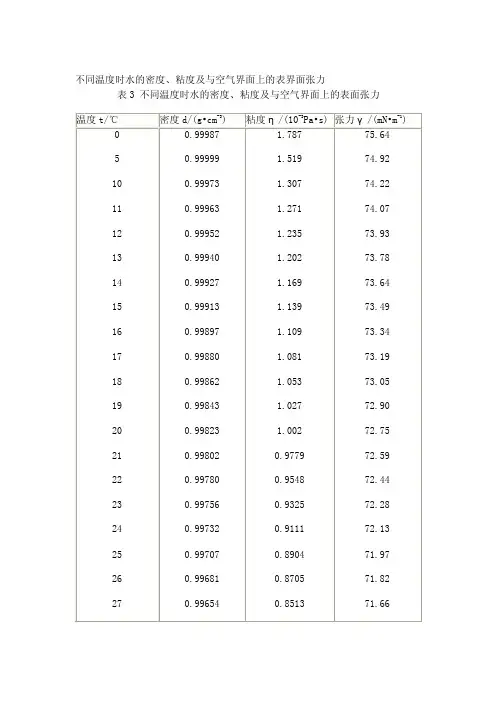
不同温度时水的密度、粘度及与空气界面上的表界面张力表3 不同温度时水的密度、粘度及与空气界面上的表面张力在293K下水的表面张力系数为72.75×10-3 N·m-1,乙醇为22.32×10-3 N·m-1,正丁醇为24.6×10-3N·m-1,而水-正丁醇(4.1‰)的界面张力为34×10-3 N·m-1。
(1)定义或解释①促使液体表面收缩的力叫做表面张力[1]。
②液体表面相邻两部分之间,单位长度内互相牵引的力。
(2)单位表面张力的单位在SI制中为牛顿/米(N/m),但仍常用达因/厘米(dyn/c m), 1dyn/cm = 1mN/m。
(3)说明①表面张力的方向和液面相切,并和两部分的分界线垂直,如果液面是平面,表面张力就在这个平面上。
如果液面是曲面,表面张力就在这个曲面的切面上。
②表面张力是分子力的一种表现。
它发生在液体和气体接触时的边界部分。
是由于表面层的液体分子处于特殊情况决定的。
液体内部的分子和分子间几乎是紧挨着的,分子间经常保持平衡距离,稍远一些就相吸,稍近一些就相斥,这就决定了液体分子不像气体分子那样可以无限扩散,而只能在平衡位置附近振动和旋转。
在液体表面附近的分子由于只显著受到液体内侧分子的作用,受力不均,使速度较大的分子很容易冲出液面,成为蒸汽,结果在液体表面层(跟气体接触的液体薄层)的分子分布比内部分子分布来得稀疏。
相对于液体内部分子的分布来说,它们处在特殊的情况中。
表面层分子间的斥力随它们彼此间的距离增大而减小,在这个特殊层中分子间的引力作用占优势。
因此,如果在液体表面上任意划一条分界线MN把液面分成a、b两部分。
F表示a部分表面层中的分子对b部分的吸引力,F6表示右部分表面层中的分子对a部分的吸引力,这两部分的力一定大小相等、方向相反。
这种表面层中任何两部分间的相互牵引力,促使了液体表面层具有收缩的趋势,由于表面张力的作用,液体表面总是趋向于尽可能缩小,因此空气中的小液滴往往呈圆球形状。