PCR实验室的基本设备与要求
- 格式:docx
- 大小:109.51 KB
- 文档页数:34

PCR检测实验室操作规范一、PCR 实验室的设置及管理1.目的:建立实验室的合理设置和科学管理,防止实验污染,保证检测结果的可靠性。
2.适用范围:本程序适用于分子诊断室的设置、工作流程和日常管理等。
3.负责人:4.细则:4.1流感实验室为急传所的专业实验室,从事临床标本的基因扩增检测及相关科研工作等。
4.2 本实验室采用实时荧光定量(定性)PCR 技术作为病毒基因诊断的主要手段,实验室分为三个区:试剂准备区(第一区)、标本处理区(第二区)、扩增分析区(第三区)。
每一工作区配备专用的设备、仪器、辅助设施、耗材、清洁用品、办公用品、专用工作服,并有明显的区分标识。
标本的接收则在检验科标本接收处进行。
4.3 各工作区专用的仪器设备、办公用品、工作服、实验耗材和清洁用具等,不可混用。
4.4 各工作区配置、功能和内务管理见各相关SOP 文件。
4.5 严格遵守从“试剂准备区→标本处理区→扩增分析区”的单一流向制度,不得逆向进入前一工作区。
4.6 非本实验室工作人员,未经许可不得入内;进修、实习或其他科室人员因科研活动需要,进入实验区域(试剂准备区、标本处理区、扩增分析区)需首先熟悉本程序的各项规定并严格遵守执行,在本实验室人员监督指导下进行。
4.7 实验完毕后做好清洁消毒工作。
二、PCR 实验室工作制度1.目的:保持良好的工作环境,以确保检测结果的可靠性,防止交叉污染,防止差错、事故及纠纷的发生。
2.适用范围:所有本实验室人员。
3.负责人:4.细则:4.1 本实验室进行临床基因扩增检测及相关实验工作,不得进行其它实验操作。
4.2 各区的用品不得混用。
4.3 在各区的实验操作过程中,操作者必须戴手套和帽子,严格按照操作规程。
4.4 试剂准备区只能进行试剂的贮存及配制等相关操作(见相关SOP 文件)。
4.5 标本处理区只能进行临床标本的保存,核酸提取、保存及其加入至扩增反应管和测定RNA 时cDNA 的合成(见相关SOP 文件)。

标准的PCR实验室简介1、主体结构:主体为彩钢板、铝合金型材。
室内所有阴角、阳角均采用铝合金50 内圆角铝,从而解决容易污染、积尘、不易清扫等问题。
结构牢固,线条简明,美观大方,密封性好。
2、标准的三区分隔和气压调节:将PCR过程分成试剂准备、标本制备和PCR扩增检测三个独立的实验区。
整个区域有一个整体缓冲走廊。
每个独立实验区设置有缓冲区,同时各区通过气压调节,使整个PCR实验过程中试剂和标本免受气溶胶的污染并降低扩增产物对人员和环境的污染。
可打开缓冲区Ⅰ,缓冲区Ⅱ和PCR 扩增区的排风扇往外排气,在实验区的外墙上和各扇门上都安装有风量可调的回风口,空气通过回风口向室内换气。
3、消毒:在三个实验区和三个缓冲区顶部以及传送窗内部安装有紫外灯,供消毒用。
在试剂准备区和标本制备区还设置移动紫外线灯,对实验桌进行局部消毒。
4、机械连锁不锈钢传递窗:试剂和标本通过机械连锁不锈钢(不建议使用电子连锁方式)传递窗传递,保证试剂和标本在传递过程中不受污染(人物分流)。
5、地面地面建议使用PVC卷材地面或自流坪地面,整体性好。
便于进行清扫,耐腐蚀。
没有条件的也可采用水磨石地面,或大块的瓷砖(至少800mm× 800mm)接缝需要小于2mm。
6、照明灯具要选用净化灯具,能达到便于清洗、不积尘的特点。
标准的PCR实验室在建设的过程中应注意:•规范的安装流程和全面的服务流程。
•严格按照规范科学设计的安装流程。
•安装前需要确定以下安装条件,如:电源电压,电源进线位置,电话网络线进线位置,进水水压,最小安装空间,地面平整度,通风孔、进水管和下水管的位置等,理想状态的空间尺寸和通风口尺寸。
1.1.1PCR 实验室基本要求2.1PCR 实验室依据所使用的方法可分为试剂准备、标本制备、扩增、产物分析等三或四个区域。
只是使用实时荧光PCR仪、HIV病毒载量测定仪的PCR实验室,有上述前面三个区域即可。
各区域应完全独立分隔,不应有任何的空气直通。

生物安全实验室PCR实验室的建设要求(一)主体结构主体为彩钢板或铝合金型材。
室内所有阴角、阳角均采用铝合金50度内圆弧角铝,从而解决容易污染、积尘、不易清扫等问题。
结构要求牢固,线条简明,美观大方,密封性好。
(二)分区与气流组织将PCR过程分成试剂准备、样本处理(核酸提取)、核酸扩增和产物分析四个独立的实验区,每个区域应严格分开、隔离。
整个PCR实验区域有一个整体缓冲走廊。
每个独立实验区与走廊间应设置缓冲区,同时各区通过气压调节,使整个PCR实验过程中试剂和标本免受气溶胶的污染并降低扩增产物对人员和实验环境的污染。
在缓冲区和PCR扩增区可安装排风扇往外排风,在实验区的外墙上和各扇门上都安装有风量可调的回风口,空气通过回风口向室内换气。
要注意防止实验环境对核酸制备区的影响,防止造成污染。
建议核酸提取工作在生物安全柜中进行,在样本处理区如涉及致病性病原微生物等感染性材料时,此区最好设计成负压,确保实验人员与环境安全。
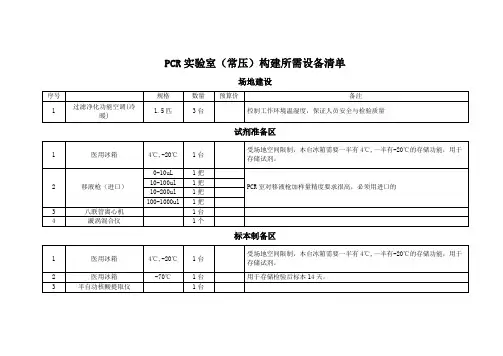
(三)各区仪器设备的配置要求工作区域仪器设备配置标准:1.试剂储存和准备区(1)2℃-8℃和-15℃冰箱;(2)混匀器;(3)微量加样器(覆盖1-1000ul);(4)移动式紫外线灯(近工作台面);(5)消耗品:一次性手套、一次性吸水纸、耐高压处理的离心管和加样器吸头(带滤芯);(6)专用工作服和工作鞋;(7)专用办公用品。
2.标本制备区(1)2℃~8℃冰箱、-20℃或-80℃冰箱;(2)高速台式冷冻离心机;(3)混匀器;(4)水浴箱或加热模块;(5)微量加样器(覆盖1~1000ul);(6)移动式紫外线灯(近工作台面);(7)超净工作台;(8)消耗品:一次性手套、一次性吸水纸、耐高压处理的离心管和加样器吸头(带滤芯);(9)专用工作服和工作鞋;(10)专用办公用品,如需处理大分子DNA,应具有超声波水浴仪。
3.扩增反应混合物配制和扩增区(1)核酸扩增仪(PCR仪);(2)微量加样器(覆盖1~1000ul);(3)移动式紫外线灯(近工作台面);(4)消耗品:一次性手套、一次性吸水纸、耐高压处理的离心管和加样器吸头(带滤芯);(5)专用工作服和工作鞋;(6)专用办公用品。
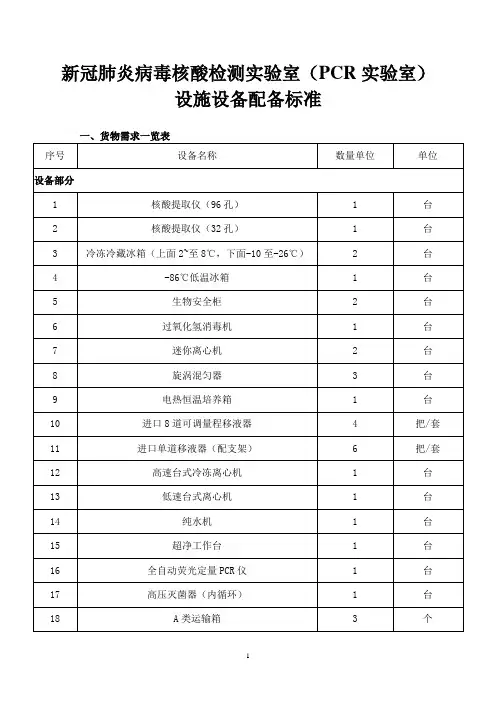
新冠肺炎病毒核酸检测实验室(PCR实验室)设施设备配备标准二、技术要求一、96孔核酸提取仪1、处理体积范围:20uL-1000uL2、样品通量范围:1-963、配套试剂磁珠回收效率:≥95%4、加热温度:裂解加热温度:室温-120℃;洗脱加热温度:室温-120℃5、磁棒结构:采用整体式磁棒,表面多层镀层处理,不易被样本和试剂粘附、污6、避免共振:磁棒架、磁套架均采用独立模块,避免仪器振动、共振。
7、自我清洁:具有内置可定时紫外消毒功能;8、污染控制:实验舱具备外排式HEPA过滤独立风路,其中的生物滤棉可吸附其中的核酸气溶胶;9、快速提取:操作时间短:通用模式30-50分钟/次;快提模式:小于18分钟/次,高纯度、高得率10、振荡混合:多模式多档速度可调11、试剂种类:磁珠法试剂12、操作界面:中文操作系统,可监控提取全过程13、内部程序:内建20组模式程序(可存储 >100组程序)14、二维码识别:可外接扫码枪,使用具有二维码试剂盒时扫码后即可运行,无需任何人工干预15、节约耗材:有单人份预装提取试剂用于随机少量样本提取,节约试剂耗材16、配套使用试剂:能提供1人份/板、8人份/板、16人份/板的核酸提取试剂能满足各种标本量的提取任务,减少试剂无谓的损耗17、产品资质要求取得国家批文(提供扫描件或影印件)18、生产企业资质通过高新技术企业认证和ISO13485认证(提供扫描件或影印件)二、32孔核酸提取仪1、样品通量: 1-322、配套试剂磁珠回收效率:≥95%3、磁棒结构:采用整体式磁棒,表面3层镀层处理,不易被样本和试剂粘附、污染。
整体式磁棒磁场均匀,吸附磁微粒效果极佳,吸附均匀;顶端吸附模式,吸附集中磁棒顶点,回收效果极佳(提供扫描件或影印件);4、高斯强度:采用军工级稀土磁原料,高斯强度高达4800-5000,永不磁性衰减,一般国产核酸提取仪高斯强度2500-3000。
保证磁吸效果(提供扫描件或影印件);5、磁棒模块、磁套模块结构:磁棒模块、磁套模块均采用独立丝杆结构,运动低噪声,低磨损,保证仪器长时间运行(提供扫描件或影印件);6、避免共振:磁棒架、磁套架均采用独立模块,避免仪器振动、共振。

PCR实验室要求PCR实验室是分子生物学研究中常见的实验室之一,其主要工作是进行聚合酶链反应(Polymerase Chain Reaction,简称PCR)实验。
PCR技术是一种通过体外复制DNA片段的方法,广泛应用于生物学研究、医学诊断、环境监测等领域。
首先,PCR实验室要求严格的实验室操作规范。
PCR实验室应具备良好的实验室卫生环境,包括地面、台面和设备的清洁度,以及对废弃物的正确处理。
实验人员必须穿戴适当的实验衣物,包括实验外套、手套和鞋套,以防止污染样品。
其次,PCR实验室要求高质量的实验材料和试剂。
PCR是一种高灵敏度的实验技术,对实验材料的纯净度要求较高。
因此,在PCR实验室中,应使用高质量的DNA模板、引物、酶和缓冲液等试剂。
实验人员应及时检测试剂的质量,并确保其适用于实验要求。
第三,PCR实验室要求严格的实验前准备工作。
在进行PCR实验之前,必须进行实验前准备工作,包括选择适当的引物序列、设定PCR反应条件和准备实验物品等。
对引物序列的选择要准确,并确保其与目标DNA片段的互补性,以避免非特异性扩增。
对PCR反应条件的设定要考虑到温度、时间和环境等因素,以确保PCR反应的可重复性和准确性。
第四,PCR实验室要求系统的实验记录和数据分析。
在进行PCR实验过程中,应及时记录实验条件、实验步骤及实验结果等。
实验人员应严格按照实验记录进行实验,并将实验数据进行整理和分析,以便后续的实验设计和数据比对。
最后,PCR实验室还应注重实验安全和质量管理。
实验人员应接受相关的实验安全培训,了解实验室内的潜在危险和应急处理方法,并定期检查和维护PCR设备的性能。
此外,PCR实验室还应建立健全的质量管理体系,包括质量控制标准和流程,以确保实验结果的准确性和可靠性。
综上所述,PCR实验室要求严格的实验室操作规范、高质量的实验材料和试剂、系统的实验记录和数据分析、实验安全和质量管理等要求。
只有严格遵守这些要求,才能保证PCR实验的可靠性和准确性,在分子生物学研究和实际应用中发挥其重要的作用。

PCR 实验室建设基本要求(中英对照)PCR 实验室依据所使用的方法可分为试剂准备、标本制备、扩增、产物分析等三或四个区域。
只是使用实时荧光PCR仪、HIV病毒载量测定仪的PCR实验室,有上述前面三个区域即可。
各区域应完全独立分隔,不应有任何的空气直通。
Based on the methods used by PCR lab, the PCR laboratory can be divided into three or four rooms or areas for (i) reagent preparation, (ii) sample preparation, (iii) amplification area, and (iv) product analysis area. If the PCR laboratory only uses real-time fluorescence PCR instruments and /or instruments for HIV virus load, the PCR lab may have only the first three rooms or areas (reagent preparation, sample preparation, amplification). The rooms or areas of the PCR lab should be independently separated, and there is no air flow through the separated rooms or areas.产物分析区或三个区域的最后一个区域(即扩增及产物分析区),空气流向应由室外向室内,可通过在室内设置通风橱、排风扇或其他排风系统达到空气流由室外向室内流动的要求。
For PCR product analysis area or last area of three areas (area for amplification and product analysis), direction of air flow shall be from outside to inside of the area by setting up fume hood, exhaust fan or other exhaust system in the area.PCR实验室各区域仪器设备配备通常如下:The equipment configuration for PCR labs are as follows:试剂准备区: Reagent preparation area仪器设备主要应有加样器、冰箱、天平、低速离心机、混匀器、可移动紫外灯等。

PCR实验室项目建设方案——SLD中检实验室技术一、PCR实验室项目:(一)PCR【基因扩增】技术在整个生命科学领域具有很高的地位,但是,如果缺乏对PCR技术完整深入的了解,以及相应的质量保证措施,就会导致检验结果有很大的主观性和随意性,常常出现假阳性和假阴性。
(二)根据基因扩增检验技术的特点和临床疾病诊断的需要,据SLD中检实验室技术所知,国家卫生部在2010年就下发了《医疗机构临床基因扩增检验实验室管理办法》(卫办医疗政发〔2010〕194号),对基因扩增检验实验室的设置、技术验收、人员培训、监督管理等作了全面的规定,要求从事临床基因扩增检验的技术人员必须经过上岗培训,持证上岗。
(三)临床基因扩增检验实验室是整个PCR实验的操作场所,它的设置是否合理直接影响到PCR实验结果的准确性,所以它必须按照国家卫生部颁布的《临床基因扩增检验实验室基本设置标准》进行设置。
二、PCR实验室系统:(一)标准PCR实验室是一种规格、大小、排列、布局、设置、工作规范、操作程序和管理制度等都确定,且经过多位专家和多家医院反复论证,并符合国家卫生部的《临床基因扩增检测实验室基本设置标准》要求的临床基因扩增检验实验室。
(二)PCR实验室采用全自动荧光定量PCR检测系统,主要设置三个工作区域,即:试剂准备区,标本制备区和PCR扩增区。
(三)PCR实验室示意图PCR实验室将三个工作区域按最理想的状态排列在一起,在三个工作区域前各设置一个缓冲区,如图1所示:图1标准PCR实验室布局图在三个缓冲区内设有挂衣架和整理盒,可供工作人员换工作服和工作鞋使用。
每间实验室和缓冲区顶部都安装有照明灯、紫外线灯和排风扇。
三、标准PCR实验室设计原则:(一)标准PCR实验室的工作区(1)试剂准备区设置有实验桌、柜子、冰箱、可移动紫外灯、与标本制备区连通的传递窗和椅子,在实验桌上可放置实验仪器设备(包括离心机、震荡器、移液器、离心管、废液缸和垃圾筒等)。

临床荧光PCR检测实验室仪器设备配置一览表(一)试剂存贮和准备区
1、2-8℃和-20℃冰箱
2、混匀器
3、微量加样器一套(覆盖0.2-1000μl)及移液器架
4、普通高速离心机
5、可移动紫外灯(近工作台面)
6、离心管架、废物缸
7、消耗品:一次性手套、离心管、加样吸头(带滤芯)、酒精棉球等
8、专用工作服和工作鞋
9、专用办公用品(如:记号笔、计算器、小镊子、纸、笔等)
10、专用垃圾桶
11、超净工作台(试剂分装,需待定是否必需)
(二)标本制备区
1、2-8℃、-20℃冰箱或-80℃冰箱
2、高速台式冷冻离心机
3、混匀器、普通高速离心机
4、恒温水浴或恒温金属浴
5、微量加样器(覆盖1-1000μl)及移液器架两套
6、可移动紫外灯(近工作台面)
7、生物安全柜
8、恒温水浴摇床
9、离心管架、废物缸和玻璃干燥器
10、消耗品:一次性手套、吸水纸、离心管、加样吸头(带滤芯)、酒精棉球等
11、专用工作服和工作鞋
12、专用办公用品(如:记号笔、小剪刀、小镊子、纸、笔等)
13、专用垃圾桶
(三)扩增反应混合物配制、扩增及扩增产物分析区
1、荧光PCR检测仪(如Lightcycler等)及电脑
2、可移动紫外灯(近工作台面)
3、消耗品:一次性手套、帽子、口罩等
6、专用工作服和工作鞋
7、专用办公用品(如:小镊子、纸、笔等)
8、专用垃圾桶。

PCR实验室的基本设备与要求临床基因扩增检验实验室管理暂行办法第一章总则第一条为规范临床基因扩增检验实验室管理;保证临床基因扩增检验质量;使临床诊断和治疗更为科学、合理;特制定本办法..第二条临床基因扩增检验技术指以临床诊断治疗为目的;以扩增检测DNA或RNA为方法的检测技术;如聚合酶链反应PCR、连接酶链反应LCR、转录依赖的放大系统TAS自主序列复制系统3SR和链替代扩增SDA等..第三条本办法适用于开展临床基因扩增检验的实验室..临床基因扩增检验实验室设立在二级以上医院..第四条临床基因扩增检验实验室必须使用经国家药品监督管理局批准的临床检验试剂开展临床基因扩增检验项目..第五条卫生部临床检验中心以下简称卫生部临检中心和省、自治区、直辖市临床检验中心以下简称省临检中心负责对所辖行政区域内临床基因扩增检验实验室的质量监督管理工作.. 第二章实验室设置和验收第六条拟设置临床基因扩增检验实验室的医疗机构按照《临床基因扩增检验实验室基本设置标准》见附件筹建实验室;筹建完成后;由法定代表人向卫生部临检中心提出技术验收申请..申请时需提交以下材料:一《医疗机构执业许可证》复印件;二可行性研究报告;1、拟设临床基因扩增检验实验室机构的所在地医疗卫生资源状况、本机构的基本情况、对临床基因扩增检验的需求以及临床基因扩增实验室运行的预测分析;2、拟设临床基因扩增检验实验室的设置平面图;3、拟设临床基因扩增检验实验室将开展的检验项目、实验设备条件和有关技术人员资料第七条卫生部临检中心和省临检中心共同组织相关专业的专家组以下简称专家组;按照《临床基因扩增检验实验室基本设置标准》对提出申请的临床基因扩增检验实验室进行技术验收..验收完成后;在20日内将验收报告寄送至申请机构..第八条经专家组技术验收合格的医疗机构将本办法第六条规定的材料及专家组验收报告送至省级行政部备案..在将符合规定的全部材料送达省级卫生行政部门后15日内未收到省级卫生行政部门不同意的意见;方可开展专家组技术验收合格的临床基因扩增检验项目..第九条未经专家组验收合格并报省级卫生行政部门备案的医疗机构不得擅自开展临床基因扩增检验项目..第三章实验室监督管理第十条临床基因检验实验室必须按照《临床基因扩增检验实验室工作规范》另发开展临床基因扩增检验工作..第十一条临床基因扩增检验实验室技术人员必须进行上岗培训..经培训合格者;由培训单位发给合格证书;并将培训合格人员名单报卫生部临检中心备案..获得培训合格证书者方可从事临床基因扩增检验工作..培训单位为卫生部临检中心;或由省级卫生行政部门指定并经卫生部临检中心认定的机构..培训时使用规定的统一教材..第十二条以科研为目的的基因扩增检验项目..不得向临床出具检验报告;不得向病人收取任何费用..第十三条临床基因扩增检验实验室必须按照《临床基因扩增实验室工作规范》开展室内质量控制;并参加卫生部临检中心组织的室内质量评价..第十四条卫生部临检中心按照本方法和《临床基因扩增实验室工作规范》协调、组织省临检中心对临床基因扩增检验实验室的检验质量进行监测..监测结果报省级卫生行政部门;同时抄送被监测的临床基因扩增检验实验室所在医疗机构..第十五条卫生部临检中心或省级临检中心受省级以上卫生行政部门委托可对临床基因扩增检验实验室进行现场检查;现场检查工作人员在履行职责时应出示证件..在进行现场检查时;检查人员有权调阅有关资料;被检查机构不得拒绝或隐瞒..第十六条卫生部临检中心对在室间质量评价中不合格的临床基因扩增检验实验室提出警告;对连续二次或三次中有二次发现临床基因扩增检验结果不合格的临床基因扩增检验实验室;卫生部临检中心报省级以上卫生行政部门由省级以上卫生行政部门责令其暂停有关临床基因扩增检验项目;限期整改..经专家组进行再次技术验收并合格;并报省级卫生行政部门核准后;方可重新开展临床基因扩增检验项目..第十七条对于未经卫生部临检中心组织的专家组技术验收合格并报省级卫生部门备案;擅自开展临床基因检验项目的医疗机构;由省级卫生行政部门依据《医疗机构管理条例》第四十七条和《医疗机构管理条例实施细则》第八十条予以处罚;并予以公告..公告所需费用由被公告机构支付..第十八条出现下列情况之一的临床基因扩增检验实验室;由省级卫生行政部门责令其停止开展临床基因扩增检验;并对其所在医疗机构予以公告..公告所需费用由被公告机构支付:一开展超出卫生部临检中心组织的技术验收合格并报省级卫生行政部门备案临床基因扩增检验项目的;二使用未经国家药品监督管理局批准的试剂开展临床基因扩增检验的;三在临床基因扩增检验中未开展室内质量控制的;四在临床基因扩增检验中未参加室间质量评价的;五在临床基因扩增检验中弄虚作假的;六以科研为目的的基因扩增检验项目向病人收取费用的;七使用未经培训合格的专业技术人员从事临床基因扩增检验的;第四章附则第十九条对采供血机构的基因扩增检验实验室开展基因扩增检验项目的管理;参照本办法执行..第二十条卫生部临检中心组织的专家组对申请开展临床基因扩增检验的实验室进行技术验收所需费用按国家有关规定执行..第二十一条本办法由卫生部负责解释..第二十二条本办法自发布之日起施行..附:临床基因扩增检验实验室基本设置标准根据《临床检验扩增检验实验室管理暂行办法》;制定本标准一、临床基因扩增检验实验室区域设置原则一临床基因扩增检验实验室区域设置原则1、试剂储存和准备区2、标本制备区3、扩增反应混合物配制和扩增区4、扩增产物分析区如使用全自动分析仪;区域可适当合并..二各工作区域必须有明确的标记;避免不同工作区域内的设备、物品混用..三进入各工作区域必须严格按照单一方向进行;即试剂储存和准备区—>标本制备区—>扩增反应混合物配制和扩增区—>扩增产物分析区..四不同的工作区域使用不同的工作服例如不同的颜色..工作人员离开各工作区域时;不得将工作服带出..二、工作区域仪器设备配置标准一试剂储存和准备区1、2-8C和-15C冰箱2、混匀器3、微量加样器覆盖1-1000ul4、移动紫外灯近工作台面5、消耗品:一次性手套、一次性吸水纸、耐高压处理的离心管和加样器吸头带滤心6、专用工作服和工作鞋7、专用办公用品二标本制备区1、2-8C冰箱、-20C或-80C冰箱2、高速台式冷冻离心机3、混允器4、水浴箱或加热模块5、微量加样器覆盖1-1000ul6、可移动紫外灯近工作台面7、超净工作台8、消耗品:一次性手套、一次性吸水纸、耐高压处理的离心管和加样器吸头带滤心9、专用工作服和工作鞋10、专用办公用品如需处理大分子DNA;应具有超声波水浴仪..三扩增反应混合物配制和扩增区1、核酸扩增仪2、微量加样器覆盖1-1000ul3、可移动紫外灯近工作台面4、消耗品:一次性手套、一次性吸水纸、耐高压处理的离心管和加样器吸头带滤心5、专用工作服和工作鞋6、专用办公用品四扩增产物分析区视检验方法不同而定..基本仪器设备如下:1、微量加样器覆盖1-1000ul2、可移动紫外灯近工作台面3、消耗品:一次性手套、一次性吸水纸、加样器吸头带滤心4、专用工作服和工作鞋5、专用办公用品临床基因扩增检验实验室工作规范为使基因扩增检验技术有效地应用于临床;更好地为疾病的预防、诊断和治疗服务;保证检验质量;特制定本规范..一、临床基因扩增检验实验室的规范化设置及其管理临床基因扩增检验实验室的规范化设置详见《临床基因扩增检验实验室管理暂行办法》卫医发200210号文附件《临床基因扩增检验实验室基本设置标准》..为避免污染;必须严格遵循《临床基因扩增检验实验室设置标准》设置临床基因扩增检验实验室..临床基因扩增检验实验室四个隔开的工作区域中每一区域都须有专用的仪器设备..各区域都必须有明确的标记;以避免设备物品如加样器或试剂等从其各自的区域内移出从而造成不同的工作区域间设备物品发生混淆..进入各个工作区域必须严格遵循单一方向顺序;即只能从试剂贮存和准备区、标本制备区、扩增反应混合物配制和扩增区简称扩增区至产物分析区;避免发生交叉污染..在不同的工作区域应使用不同颜色或有明显区别标志的工作服;以便于鉴别..此外;当工作者离开工作区时;不得将各区特定的工作服带出..清洁方法不当也是污染发生的一个主要原因;因此实验室的清洁应按试剂贮存和准备区至扩增产物分析区的方向进行..不同的实验区域应有其各自的清洁用具以防止交叉污染..一试剂贮存和准备区下述操作在该区进行:贮存试剂的制备、试剂的分装和主反应混合液的制备..贮存试剂和用于标本制备的材料应直接运送至试剂贮存和准备区;不能经过产物分析区..在打开含有反应混合液的离心管或试管前;应将其快速离心数秒..试剂原材料必须贮存在本区内;并在本区内制备成所需的贮存试剂..当贮存试剂溶液经检查可用后;应将其分装贮存备用;避免由于经常打开反应管吸液而造成污染..含反应混合液的离心管或试管在冰冻前都应快速离心数秒..大多数用于扩增的试剂都应冰冻贮存..为避免因单次反应取液而频繁的冻融主贮存试剂;应分装冰冻贮存试剂溶液..贮存试剂的分装体积根据通常在实验室内一次测定所需的扩增反应数来决定..主反应混合液的组成成份尤其是聚合酶的适用性和稳定性通过预试验来检查;评价结果必须有书面报告..对于"热启动"技术在第一个高温变性步骤后加入酶;聚合酶也可不包含在主反应混合液中..在整个本区的实验操作过程中;操作者必须戴手套;并经常更换..此外;操作中使用一次性帽子也是一个有效地防止污染的措施..严禁用嘴吸取液体;加样器和吸头等必须经高压处理..工作结束后必须立即对工作区进行清洁..本工作区的实验台表面应可耐受诸如次氯酸钠的化学物质的消毒清洁作用..实验台表面的紫外照射应方便有效..由于紫外照射的距离和能量对去污染的效果非常关键;因此可使用可移动紫外灯254nm波长;在工作完成后调至实验台上60~90cm内照射..由于扩增产物仅几百bp;对紫外线损伤不敏感;因此紫外照射扩增片段必须延长照射时间;最好是照射过夜..实验室及其设备的使用必须有日常记录..二标本制备区下述操作在该区进行:临床标本的保存;核酸RNA、DNA提取、贮存及其加入至扩增反应管和测定RNA时cDNA的合成..要正确使用加样器..由于在加样操作中可能会发生气溶胶所致的污染;所以应避免在本区内不必要的走动..可通过在本区内设立正压条件避免从邻近区进入本区的气溶胶污染..为避免样本间的交叉污染;加入待测核酸后;必须盖好含反应混合液的反应管..对具有潜在传染危险性的材料;必须有明确的样本处理和灭活程序..用过的加样器吸头必须放入专门的消毒例如含次氯酸钠溶液容器内..实验室桌椅表面每次工作后都要清洁;实验材料原始血标本、血清标本、提取中的标本与试剂的混合液等如出现外溅;则必须分别处理并作出记录..对实验台适当的紫外照射254nm波长;与工作台面近距离适合于灭活去污染..可移动紫外线管灯可用来确保工作后对实验台面的充分照射..样本处理对核酸扩增有很大影响;必须使用有效的核酸提取方法;可在开展临床标本检测前对提取方法进行评价..用于RNA扩增检测的样本制备好以后;应立即进行cDNA合成;因为cDNA链较RNA稳定;保存相对容易..为保证逆转录反应的需要;应在标本制备区设置一个以上的温育装置..cDNA合成的理想温度依所使用的酶而定;倾向于使用一步法:即使用在扩增反应缓冲液条件下具有逆转录活性的热稳定的DNA聚合酶进行逆转录;其较cDNA合成后再开盖以调节缓冲液或加入聚合酶进行扩增发生污染的可能性降低..待测RNA的cDNA拷贝须保存在标本制备区;不得在本区对样本进行PCR扩增..三扩增区下述工作在本区内进行:DNA或cDNA扩增..此外;已制备的DNA模板和合成的cDNA来自样本制备区的加入和主反应混合液来自试剂贮存和制备区制备成反应混合液等也可在本区内进行..在巢式PCR测定中;通常在第一轮扩增后必须打开反应管;因此巢式扩增有较高的污染危险性;第二次加样必须在本区内进行..不能从本区再进入任何"上游"区域;可降低本区的气压以避免气溶胶从本区漏出..为避免气溶胶所致的污染;应尽量减少在本区内的走动..如有加样则应在超净台内进行..打开预处理过的反应混合液时必须防止液体溅出;尤其是在巢式扩增步骤之间..一个简单的方法是在打开反应管前快速离心数秒..可使用体积较小的离心机;因其所占实验台面小;易于用一只手操作;适合于大多数超净台..防潮屏障如石蜡油或轻矿物油也具有防污染作用;但必须注意的是;矿物油本身也可能成为一种持续性的污染源..用过的加样器必须注意清洁消毒..完成操作及每天工作后都必须对实验室台面进行清洁和消毒;紫外照射方法与前面区域相同..如有溶液溅出;必须处理并作出记录..四扩增产物分析区下述操作在本区内进行:扩增片段的测定..核酸扩增后产物的分析方法多种多样;如膜上或微孔板上探针杂交方法同位素标记或非同位素标记、琼脂糖凝胶电泳、聚丙烯酰胺凝胶电泳、Southern转移、核酸测序方法等..目前国内的商品试剂盒绝大部分均采用非同位素标记的微孔板上探针杂交方法;即PCR-ELISA方法;也有膜上探针杂交方法..本区是最主要的扩增产物污染来源;因此必须注意避免通过本区的物品及工作服将扩增产物带出..在使用PCR-ELISA方法检测扩增产物时;必须使用洗板机洗板;废液必须收集至1mol/L HC1中;并且不能在实验室内倾倒;而应至远离PCR实验室的地方弃掉..用过的吸头也必须放至1mol/L HCl中浸泡后再放到垃圾袋中按程序处理;如焚烧..由于本区有可能会用到某些可致基因突变和有毒物质如溴化乙锭、丙烯酰胺、甲醛或同位素等;故应注意实验人员的安全防护..本区的清洁消毒和紫外照射方法同前面区域..本区如采用负压条件或减压情况下如安装排风扇可减少扩增产物从本区扩散至前面区域的可能性..二、临床基因扩增检验实验室质量保证临床基因扩增检验实验室质量保证涉及到整个基因扩增检验的所有阶段;即测定分析前的标本采集处理、测定中的核酸提取、扩增和产物分析以及测定后的结果报告等..一标本的采集常用于基因扩增检测的临床标本包括EDTA或枸橼酸钠抗凝全血或骨髓、血清或血浆、痰、脑脊液、尿及分泌物等..采血液等样本时;应使用一次性密闭容器;如真空采血管..当使用非密闭采样系统时;如尿、分泌物和骨髓的采样;必须注意防止来自采样者的皮屑或分泌物的污染..采样时必须戴一次性手套..玻璃器皿在使用前应高压处理;因为玻璃器皿常含有不易失活的RNA酶..最好是热灭菌;250℃烘烤4小时以上可使RNA酶永久性失活..全血和骨髓标本必须进行抗凝处理..EDTA和枸橼酸盐是首选的抗凝剂..不能使用肝素抗凝;因为肝素是Taq酶的强抑制剂;而且在其后的核酸提取步骤中很难去除..临床用于RNA如HCV RNA扩增检测的血标本建议进行抗凝处理;并尽快3小时以内分离血浆;以避免RNA的降解..如未作抗凝处理;则抽血后;必须在1小时内分离血清..二标本的稳定化处理用于DNA扩增检测的标本;采集后一般不需要特殊的稳定化处理;但标本应及时送至实验室..由于RNA易受RNA酶的降解;因此用于RNA测定的标本有时必须进行稳定化处理;如流行病学调查的现场采样..异硫氰酸胍盐Guanidine thiocyanate;GITC可使DNA酶和RNA酶立即失活;因此在采集标本时;可将标本材料如血清或血浆按1:4的比例加至含有5mol/L GITC的试管中;从而使血清浆中的RNA酶不可逆失活..经上述稳定化处理后;标本一般不需要冷藏即可邮寄..对于特定的检测项目;上述稳定化处理方法的效果究竟如何;要使用相应的逆转录PCR测定方法来评价..三标本的运送标本采集后必须尽快送至实验室..经过适当稳定化处理的标本可在常温下通过邮寄运送..如用于DNA扩增检测的EDTA抗凝全血标本及用于RNA扩增检测的经GITC稳定化处理的标本..通常在运送时;应采用不易破碎的容器装载标本..用于RNA检测的标本;如果未经稳定化处理;则必须速冻后;放在干冰中运送..四标本的贮存临床体液标本如血清/血浆等可于-70℃下长时间贮存..用于DNA测定的已纯化核酸样本可在10mmol/L Tris-1 mmol/L EDTA缓冲液pH 7.5-8.0中4℃保存..用于RNA测定的已纯化核酸样本应在缓冲液中-80℃或液氮中贮存..用乙醇沉淀的核酸样本贮存在-20℃即可..用GITC处理的RNA标本在室温可保存7天..五标本的处理核酸提取标本处理即核酸提取纯化是决定扩增检测成败的关键性步骤;在使用商品核酸提取试剂提取临床标本中的核酸模板前;应对其进行充分评价以验证其提取的有效性..通常;核酸制备质量不高是由于抑制物去除不完全所致;抑制物可能来源于标本本身如血红素及其前体或降解产物或核酸提取过程中残留的有机溶剂如酚、氯仿等;这些物质对其后的Taq酶扩增反应步骤具有强烈的抑制作用;从而影响靶核酸的扩增测定..当标本为痰时;则必须先进行液化处理;再提取核酸..需注意的是;液化时不能加热;液化时间不能过长..此外;当靶核酸为RNA 时;逆转录PCR测定失败的常见原因是标本在运送前未经充分的稳定化处理及核酸提取试剂的RNA酶的污染..对于前者;要核查测定分析前的步骤;如果发现有RNA降解的证据;实验室则应拒绝接受标本;要求重新采取标本;并对运送者给以详细的指导..对于后者;建议使用高质量的商品核酸提取试剂..六靶核酸的逆转录RT和扩增1、靶RNA的逆转录cDNA合成为逆转录PCR中的第一个酶反应步骤;所产生的cDNA为靶RNA的反向互补链;为后面扩增的模板..下述因素通常影响cDNA合成的效率:1逆转录效率的降低或完全缺乏..其可能的原因有逆转录酶质量不高、试剂降解变质或加样错误等;2用于逆转录的标本中存在逆转录或Taq酶的抑制物如酚、氯仿、血红素等;3RNA酶的存在导致RNA的降解..2、核酸的扩增有多种因素可引起核酸扩增检测的假阳性或假阴性结果;如扩增靶核酸中抑制剂存在、Taq 酶失活、退火温度不对、Mg++浓度不佳、患者标本或试剂受污染等..扩增仪孔中热传导的均一性极为重要;必须定期对扩增仪的温度控制和加热模块中热传导的一致性进行检查;以避免假阴性结果..七污染在实际工作中;常见有以下几种污染类型:扩增片段的污染产物污染;天然基因组DNA的污染、试剂污染贮存液或工作液以及标本间交叉污染如气溶胶从一个阳性标本扩散到原本阴性的标本..临床基因扩增检验实验室中污染的最主要来源是扩增产物的污染..由于一旦发生污染后;再围绕实验室来寻找污染源不仅耗时而且还很繁琐;所以防止污染重在预防..但如果发生了污染;实验就必须停止;直到发现了污染源为止;并且实验结果必须作废..1、测定分析前的污染源测定分析前实验材料的污染主要来自非病人标本来源的核酸..2、测定分析阶段的污染源通常;测定分析阶段的每一步都可能发生对样本的污染..反应混合液的任何成分及核酸的制备和反应建立阶段所涉及到的实验设备的任何部位都是可能的污染源..如受污染的试剂例如牛血清白蛋白;明胶或矿物油、商品酶制剂、消耗品如反应管;吸头和实验设备如加样器、离心机等..在前面三个工作区中;不当的实验操作会引起所使用的试剂、消耗品或实验设备的污染..而在产物分析区;当吸取扩增产物用于检测时;非常容易引起污染;因此必须制定标准操作程序SOP;并严格执行..3、污染的避免要避免污染;首先应是预防而不是排除污染;前面所述对工作区的严格划分的目的即是为了预防污染..为避免以前测定中所产生的扩增产物的污染;可设法将其破坏掉..如在扩增反应中用dUTP 取代部分dTTP;使得产生的特异扩增片段含有尿嘧啶;这样扩增前在反应混合液中加入尿嘧啶糖苷酶UNG;可破坏来自以前测定的扩增产物;从而避免其对以后要进行的扩增测定的污染..另外一种方法是持续的长波紫外灯照射;通过异补骨脂素光化学产生DNA加合物;由于DNA加合物对扩增没有反应但又不妨碍PCR后杂交过程;所以这种方法也能防止污染..上述防污染方法只在一定程度上有效;所以不能用其来替代严格的实验室设置和管理;尤其是这些方法不能防止外来非扩增的天然DNA的污染..4、去除污染的措施工作完后必须定期对实验室采取有效的去污染措施;结合各种不同的方法可达到最佳效果..去污染措施包括但不仅限下面几种:1用10%v/v次氯酸钠清洁表面;2试验后长时间的紫外照射实验操作台面和其他表面;3实验设备如加样器的高压消毒..八扩增产物的分析扩增产物的测定有各种方法;如电泳、限制性酶切、斑点印迹、探针杂交、测序、分光光度法定量等;但临床PCR检验项目基本上都使用探针杂交方法..杂交结果不充分的原因可能是基因探针不合适、标记方法不对、对探针的标记不够、杂交或洗涤方法不合适等..最常使用的基因探针有:DNA片段、合成的寡核苷酸和体外转录的反义RNA探针..探针的标记物常用的有生物素、地高辛、荧光素和同位素等..在扩增后的杂交检测中; 应该严格遵守商品试剂盒确定的杂交程序和杂交条件..温度太低。

验证PCR注意事项PCR(聚合酶链反应)是一种被广泛应用的基因检测技术,可以在短时间内扩增小片段DNA,使其数量快速增加。
然而,PCR技术操作繁琐,在实验过程中存在许多需要注意的事项,下面我将详细回答并讨论PCR技术的注意事项。
1. 实验室准备:在进行PCR实验前,要充分准备实验室所需的基本设备和试剂,如PCR仪、热循环程序控制器、离心机、PCR试剂盒等。
还需要保证空间干净整洁,避免交叉污染。
2. 基因组DNA提取:PCR反应的第一步是提取样本中的DNA,注意要选择适当的提取方法。
常用的方法有酚/氯仿法、磁珠法、硅胶膜法等,具体选择取决于样本类型和实验目的。
此外,提取过程中要避免样本的污染,严格遵守操作规程。
3. 靶标序列选择与设计:设计引物是PCR反应成功的关键。
引物应与目标DNA序列互补,长度在18-30碱基之间,GC含量约为50-60%。
引物间应该没有互补碱基片段,以避免引物二聚体的产生。
在设计引物时,可以利用一些在线工具进行引物评估,确保引物的特异性和稳定性。
4. 引物浓度的优化:引物浓度的优化对PCR反应的成功与否至关重要。
引物过多会导致引物二聚体或非特异性扩增,引物过少则可能导致不稳定的扩增。
一般来说,引物的最佳浓度为0.1-0.5μmol/L。
5. PCR反应体系的优化:PCR反应体系主要包括引物、DNA模板、dNTPs、聚合酶、缓冲液和Mg2+等。
体系中各个组分的浓度和比例需要优化,以确保PCR反应的成功。
一般来说,每个PCR反应管中最终反应体积为20-50μl,引物浓度为0.2-0.5μmol/L,模板DNA浓度为10-200ng。
6. 热循环程序设置的优化:PCR反应的关键步骤是反应体系的热循环程序。
温度和时间的设置需要根据引物和目标序列的特性进行优化。
常规的PCR热循环程序包括:变性(94-98C)、退火(50-68C)和扩增(72C)等步骤,反应周期数一般为25-40个。
荧光定量PCR实验室规范临床基因扩增检验实验室工作规范为使基因扩增检验技术有效地应用于临床,更好地为疾病的预防、诊断和治疗服务,保证检验质量,特制定本规范。
一、临床基因扩增检验实验室的规范化设置及其管理临床基因扩增检验实验室的规范化设置详见《临床基因扩增检验实验室管理暂行办法》(卫医发[2002]10号文)附件《临床基因扩增检验实验室基本设置标准》。
为避免污染,必须严格遵循《临床基因扩增检验实验室设置标准》设置临床基因扩增检验实验室。
临床基因扩增检验实验室四个隔开的工作区域中每一区域都须有专用的仪器设备。
各区域都必须有明确的标记,以避免设备物品如加样器或试剂等从其各自的区域内移出从而造成不同的工作区域间设备物品发生混淆。
进入各个工作区域必须严格遵循单一方向顺序,即只能从试剂贮存和准备区、标本制备区、扩增反应混合物配制和扩增区(简称扩增区)至产物分析区,避免发生交叉污染。
在不同的工作区域应使用不同颜色或有明显区别标志的工作服,以便于鉴别。
此外,当工作者离开工作区时,不得将各区特定的工作服带出。
清洁方法不当也是污染发生的一个主要原因,因此实验室的清洁应按试剂贮存和准备区至扩增产物分析区的方向进行。
不同的实验区域应有其各自的清洁用具以防止交叉污染。
(一)试剂贮存和准备区下述操作在该区进行:贮存试剂的制备、试剂的分装和主反应混合液的制备。
贮存试剂和用于标本制备的材料应直接运送至试剂贮存和准备区,不能经过产物分析区。
在打开含有反应混合液的离心管或试管前,应将其快速离心数秒。
试剂原材料必须贮存在本区内,并在本区内制备成所需的贮存试剂。
当贮存试剂溶液经检查可用后,应将其分装贮存备用,避免由于经常打开反应管吸液而造成污染。
含反应混合液的离心管或试管在冰冻前都应快速离心数秒。
大多数用于扩增的试剂都应冰冻贮存。
为避免因单次反应取液而频繁的冻融主贮存试剂,应分装冰冻贮存试剂溶液。
贮存试剂的分装体积根据通常在实验室内一次测定所需的扩增反应数来决定。
临床基因检测实验室建设的要求实验室硬件设备:1.基本设施:实验室应配备适用的实验台、实验室设备、检测设备、工作台和储存区域等。
必须符合国家安全标准和相关规定。
2.仪器设备:实验室应购置适用于临床基因检测的仪器设备,如PCR 仪、电泳仪、高通量测序平台等。
3.实验材料:实验室需要准备并储存一定数量和种类的试剂、标准质控品、样本处理试剂等,在满足质量需求的前提下,确保实验所需的材料的充足性。
质量管理体系:1.质量控制:实验室需要建立完善的质量控制计划,确保实验结果准确可靠。
包括设定质量控制标准、监测仪器性能、建立实验室内部质控体系等。
2.标准操作规范(SOP):实验室需要编制和实施临床基因检测相关的SOP文件,确保操作的规范和一致性。
安全防护措施:1.生物安全:实验室需要配备适当的生物安全柜,确保实验物品和人员安全,同时符合相关法规和标准。
应遵循包括基因实验室分类、操作限制、废物处理等在内的标准操作程序。
2.物理安全:实验室需要确保实验设备和试剂处于安全状态,并采取措施预防实验室设备的损失和破坏。
3.化学安全:实验室需要遵守危险化学品管理规范,标识和存放危险化学品,建立相应的安全操作规程,配备相应的个人防护用具。
实验室人员培训:1.资质要求:实验室人员需要具备相关背景,包括生物学、遗传学、分子生物学等相关专业知识,有一定的实验室经验和技能。
2.岗位职责和培训:实验室人员需要了解自己的岗位职责,并配备相关培训。
这可以涵盖实验室操作流程、实验室安全、质量控制和质量保证、SOP的执行等内容。
综上所述,临床基因检测实验室建设的要求非常严格。
合理配置实验室硬件设备,建立完善的质量管理体系和安全防护措施,以及培训合格的实验室人员,是确保临床基因检测实验室能够顺利运行和提供准确结果的重要要求。
卫健委关于pcr实验室的要求作为新型冠状病毒检测的有效手段,聚合酶链反应(PCR)实验室在疫情防控中扮演着重要的角色。
为了保证PCR实验室的有效性和可靠性,卫生健康委员会对PCR实验室设立和管理有一系列要求。
一、设立要求1. 环境:PCR实验室应设在符合卫生标准的洁净空间,并且保持良好的通风系统。
2. 动力:PCR实验室的设备应保证持续稳定的电力和实验所需的水、气及其他供应。
3. 设备:PCR实验室必须配备完备的实验设备和安全设备,同时需要保证设备的状况良好和运转稳定。
4. 物品储存:PCR实验室必须配备物品储存区域,并对存放的物品进行分类、储藏和管理。
二、管理要求1. 人员:PCR实验室人员必须具备相关专业背景,进行过相关培训并取得相关证书。
2. 物品使用:PCR实验室必须通过严格的操作规程来使用物品,避免混用,同时需要进行严格的检测和验证实验。
3. 清洁消毒:PCR实验室必须按照卫生健康委员会的要求进行定期的清洁、消毒和垃圾处理。
4. 安全管理:PCR实验室需要制定完备的应急预案和安全管理制度,并负责保障每个工作环节的安全和顺利进行。
三、实验要求1. 重要检测指标:PCR实验室应该对新型冠状病毒进行定期检测,确保检测结果的准确性。
2. 方式:PCR实验室的检测方式应该符合卫生健康委员会的标准要求,在操作过程中需要严格执行相应规程。
3. 样本获取:PCR实验室需要使用卫生健康委员会已经认可的样本采集方法,并严格把好样本环节。
4. 实验结果:PCR实验室会就实验结果进行清晰的记录和存档,进行有效的数据分析,以便有效指南疫情发展趋势。
通过以上要求的严格执行,可以保证PCR实验室的可靠性和有效性,为疫情抗击提供有效的支持和服务。
建议所有PCR实验室的管理者和工作者们严格遵守标准要求,提高自身的专业素养和责任意识,共同努力打赢疫情防控战役。
pcr实验室建设标准
PCR实验室是非常重要的实验室,要求实验室建设标准也非常严格。
首先,实验室的空间一定要宽敞明亮,空气流动自然,有足够的采光,确保环境无污染。
其次,室内温度和湿度使用标准,温度在15-25℃之间,湿度在30%-60%之间,变化不宜大于10%,以保证稳定的实验环境。
此外,实验室还需要安装必要的强制风机设备和安全措施,防止空调的漏风和安全事故的发生。
另外,实验室的基本设置也是十分重要的。
一般情况下,应当提供室内的石材镶边和换气口,并要求无尘、无污染,防止实验室引起噪音或空气污染。
除此之外,PCR实验室应具有必要的安全设备,包括门、窗及应急照明系统,以保障实验室安全。
总之,PCR实验室的建设标准严格,要求实验室空间明亮通风,温度、湿度处于稳定范围,安全设置完善,无尘无污染,以保证实验能有效高效地进行,并保障安全。
PCR实验室的基本设备与要求
Company number:【0089WT-8898YT-W8CCB-BUUT-202108】 PCR实验室的基本设备与要求 临床基因扩增检验实验室管理暂行办法 第一章 总 则第一条 为规范临床基因扩增检验实验室管理,保证临床基因扩增检验质量,使临床诊断和治疗更为科学、合理,特制定本办法。第二条 临床基因扩增检验技术指以临床诊断治疗为目的,以扩增检测DNA或RNA为方法的检测技术,如聚合酶链反应(PCR)、连接酶链反应(LCR)、转录依赖的放大系统(TAS)自主序列复制系统(3SR)和链替代扩增(SDA)等。第三条 本办法适用于开展临床基因扩增检验的实验室。临床基因扩增检验实验室设立在二级以上医院。第四条 临床基因扩增检验实验室必须使用经国家药品监督管理局批准的临床检验试剂开展临床基因扩增检验项目。第五条 卫生部临床检验中心(以下简称卫生部临检中心)和省、自治区、直辖市临床检验中心(以下简称省临检中心)负责对所辖行政区域内临床基因扩增检验实验室的质量监督管理工作。第二章 实验室设置和验收第六条 拟设置临床基因扩增检验实验室的医疗机构按照《临床基因扩增检验实验室基本设置标准》(见附件)筹建实验室;筹建完成后,由法定代表人向卫生部临检中心提出技术验收申请。申请时需提交以下材料:(一)《医疗机构执业许可证》复印件;(二)可行性研究报告;1、 拟设临床基因扩增检验实验室机构的所在地医疗卫生资源状况、本机构的基本情况、对临床基因扩增检验的需求以及临床基因扩增实验室运行的预测分析;2、 拟设临床基因扩增检验实验室的设置平面图;3、 拟设临床基因扩增检验实验室将开展的检验项目、实验设备条件和有关技术人员资料第七条 卫生部临检中心和省临检中心共同组织相关专业的专家组(以下简称专家组),按照《临床基因扩增检验实验室基本设置标准》对提出申请的临床基因扩增检验实验室进行技术验收。验收完成后,在20日内将验收报告寄送至申请机构。第八条 经专家组技术验收合格的医疗机构将本办法第六条规定的材料及专家组验收报告送至 省级行政部备案。在将符合规定的全部材料送达省级卫生行政部门后15日内未收到省级卫生行政部门不同意的意见,方可开展专家组技术验收合格的临床基因扩增检验项目。第九条 未经专家组验收合格并报省级卫生行政部门备案的医疗机构不得擅自开展临床基因扩增检验项目。第三章 实验室监督管理第十条 临床基因检验实验室必须按照《临床基因扩增检验实验室工作规范》(另发)开展临床基因扩增检验工作。第十一条 临床基因扩增检验实验室技术人员必须进行上岗培训。经培训合格者,由培训单位发给合格证书,并将培训合格人员名单报卫生部临检中心备案。获得培训合格证书者方可从事临床基因扩增检验工作。培训单位为卫生部临检中心,或由省级卫生行政部门指定并经卫生部临检中心认定的机构。培训时使用规定的统一教材。第十二条 以科研为目的的基因扩增检验项目。不得向临床出具检验报告,不得向病人收取任何费用。第十三条 临床基因扩增检验实验室必须按照《临床基因扩增实验室工作规范》开展室内质量控制,并参加卫生部临检中心组织的室内质量评价。第十四条 卫生部临检中心按照本方法和《临床基因扩增实验室工作规范》协调、组织省临检中心对临床基因扩增检验实验室的检验质量进行监测。监测结果报省级卫生行政部门,同时抄送被监测的临床基因扩增检验实验室所在医疗机构。第十五条 卫生部临检中心或省级临检中心受省级以上卫生行政部门委托可对临床基因扩增检验实验室进行现场检查,现场检查工作人员在履行职责时应出示证件。在进行现场检查时,检查人员有权调阅有关资料,被检查机构不得拒绝或隐瞒。第十六条 卫生部临检中心对在室间质量评价中不合格的临床基因扩增检验实验室提出警告,对连续二次或三次中有二次发现临床基因扩增检验结果不合格的临床基因扩增检验实验室,卫生部临检中心报省级以上卫生行政部门由省级以上卫生行政部门责令其暂停有关临床基因扩增检验项目,限期整改。经专家组进行再次技术验收并合格,并报省级卫生行政部门核准后,方可重新开展临床基因扩增检验项目。第十七条 对于未经 卫生部临检中心组织的专家组技术验收合格并报省级卫生部门备案,擅自开展临床基因检验项目的医疗机构,由省级卫生行政部门依据《医疗机构管理条例》第四十七条和《医疗机构管理条例实施细则》第八十条予以处罚,并予以公告。公告所需费用由被公告机构支付。第十八条 出现下列情况之一的临床基因扩增检验实验室,由省级卫生行政部门责令其停止开展临床基因扩增检验,并对其所在医疗机构予以公告。公告所需费用由被公告机构支付:(一) 开展超出卫生部临检中心组织的技术验收合格并报省级卫生行政部门备案 临床基因扩增检验项目的;(二) 使用未经国家药品监督管理局批准的试剂开展临床基因扩增检验的;(三) 在临床基因扩增检验中未开展室内质量控制的;(四) 在临床基因扩增检验中未参加室间质量评价的;(五) 在临床基因扩增检验中弄虚作假的;(六) 以科研为目的的基因扩增检验项目向病人收取费用的;(七) 使用未经培训合格的专业技术人员从事临床基因扩增检验的;第四章 附 则第十九条 对采供血机构的基因扩增检验实验室开展基因扩增检验项目的管理,参照本办法执行。第二十条 卫生部临检中心组织的专家组对申请开展临床基因扩增检验的实验室进行技术验收所需费用按国家有关规定执行。第二十一条 本办法由卫生部负责解释。第二十二条 本办法自发布之日起施行。附:临床基因扩增检验实验室基本设置标准根据《临床检验扩增检验实验室管理暂行办法》,制定本标准一、 临床基因扩增检验实验室区域设置原则(一) 临床基因扩增检验实验室区域设置原则1、 试剂储存和准备区2、 标本制备区3、 扩增反应混合物配制和扩增区4、 扩增产物分析区如使用全自动分析仪,区域可适当合并。(二) 各工作区域必须有明确的标记,避免不同工作区域内的设备、物品混用。(三) 进入各工作区域必须严格按照单一方向进行,即试剂储存和准备区 —>标本制备区—>扩增反应混合物配制和扩增区—>扩增产物分析区。(四) 不同的工作区域使用不同的工作服(例如不同的颜色)。工作人员离开各工作区域时,不得将工作服带 出。二、 工作区域仪器设备配置标准(一) 试剂储存和准备区1、2-8C和-15C冰箱2、混匀器3、微量加样器(覆盖1-1000ul)4、移动紫外灯(近工作台面)5、消耗品:一次性手套、一次性吸水纸、耐高压处理的离心管和加样器吸头(带滤心)6、专用工作服和工作鞋7、专用办公用品(二) 标本制备区1、2-8C冰箱、-20C或-80C冰箱2、高速台式冷冻离心机3、混允器4、水浴箱或加热模块5、微量加样器(覆盖1-1000ul)6、可移动紫外灯(近工作台面)7、超净工作台8、消耗品:一次性手套、一次性吸水纸、耐高压处理的离心管和加样器吸头(带滤心)9、专用工作服和工作鞋10、专用办公用品如需处理大分子DNA,应具有超声波水浴仪。(三) 扩增反应混合物配制和扩增区1、 核酸扩增仪2、 微量加样器(覆盖1-1000ul)3、 可移动紫外灯(近工作台面)4、 消耗品:一次性手套、一次性吸水纸、耐高压处理的离心管和加样器吸头(带滤心)5、 专用工作服和工作鞋6、 专用办公用品(四)扩增产物分析区视检验方法不同而定。基本仪器设备如下:1、 微量加样器(覆盖1-1000ul)2、 可移动紫外灯(近工作台面)3、 消耗品:一次性手套、一次性吸水纸、加样器吸头(带滤心)4、 专用工作服和工作鞋5、 专用办公用品 临床基因扩增检验实验室工作规范 为使基因扩增检验技术有效地应用于临床,更好地为疾病的预防、诊断和治疗服务,保证检验质量,特制定本规范。 一、临床基因扩增检验实验室的规范化设置及其管理 临床基因扩增检验实验室的规范化设置详见《临床基因扩增检验实验室管理暂行办法》(卫医发[2002]10号文)附件《临床基因扩增检验实验室基本设置标准》。为避免污染,必须严格遵循《临床基因扩增检验实验室设置标准》设置临床基因扩增检验实验室。 临床基因扩增检验实验室四个隔开的工作区域中每一区域都须有专用的仪器设备。各区域都必须有明确的标记,以避免设备物品如加样器或试剂等从其各自的区域内移出从而造成不同的工作区域间设备物品发生混淆。进入各个工作区域必须严格遵循单一方向顺序,即只能从试剂贮存和准备区、标本制备区、扩增反应混合物配制和扩增区(简称扩增区)至产物分析区,避免发生交叉污染。在不同的工作区域应使用不同颜色或有明显区别标志的工作服,以便于鉴别。此外,当工作者离开工作区时,不得将各区特定的工作服带出。 清洁方法不当也是污染发生的一个主要原因,因此实验室的清洁应按试剂贮存和准备区至扩增产物分析区的方向进行。不同的实验区域应有其各自的清洁用具以防止交叉污染。 (一)试剂贮存和准备区 下述操作在该区进行:贮存试剂的制备、试剂的分装和主反应混合液的制备。 贮存试剂和用于标本制备的材料应直接运送至试剂贮存和准备区,不能经过产物分析区。在打开含有反应混合液的离心管或试管前,应将其快速离心数秒。试剂原材料必须贮存在本区内,并在本区内制备成所需的贮存试剂。当贮存试剂溶液经检查可用后,应将其分装贮存备用,避免由于经常打开反应管吸液而造成污染。 含反应混合液的离心管或试管在冰冻前都应快速离心数秒。大多数用于扩增的试剂都应冰冻贮存。为避免因单次反应取液而频繁的冻融主贮存试剂,应分装冰冻贮存试剂溶液。贮存试剂的分装体积根据通常在实验室内一次测定所需的扩增反应数来决定。 主反应混合液的组成成份尤其是聚合酶的适用性和稳定性通过预试验来检查,评价结果必须有书面报告。对于"热启动"技术(在第一个高温变性步骤后加入酶),聚合酶也可不包含在主反应混合液中。