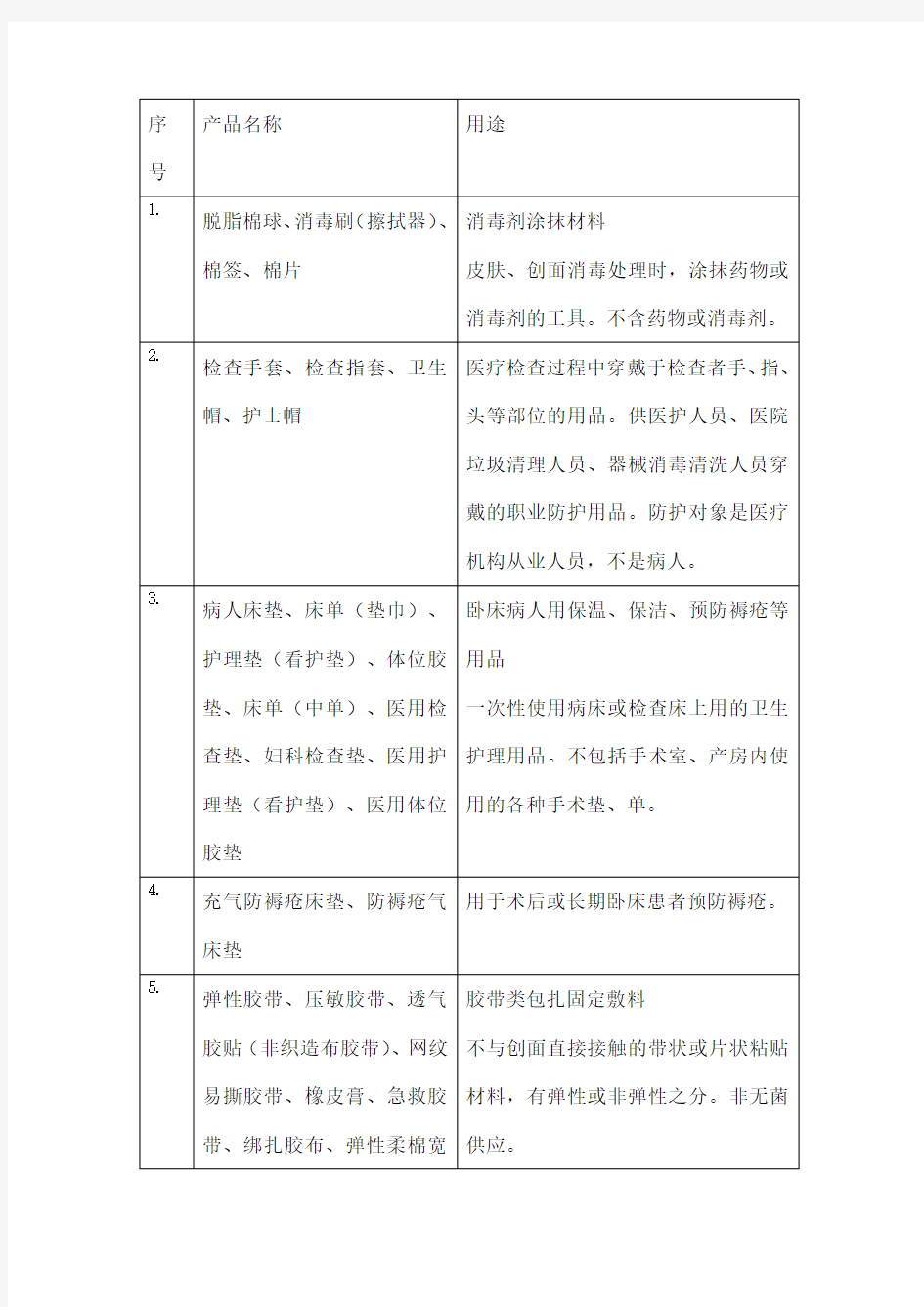
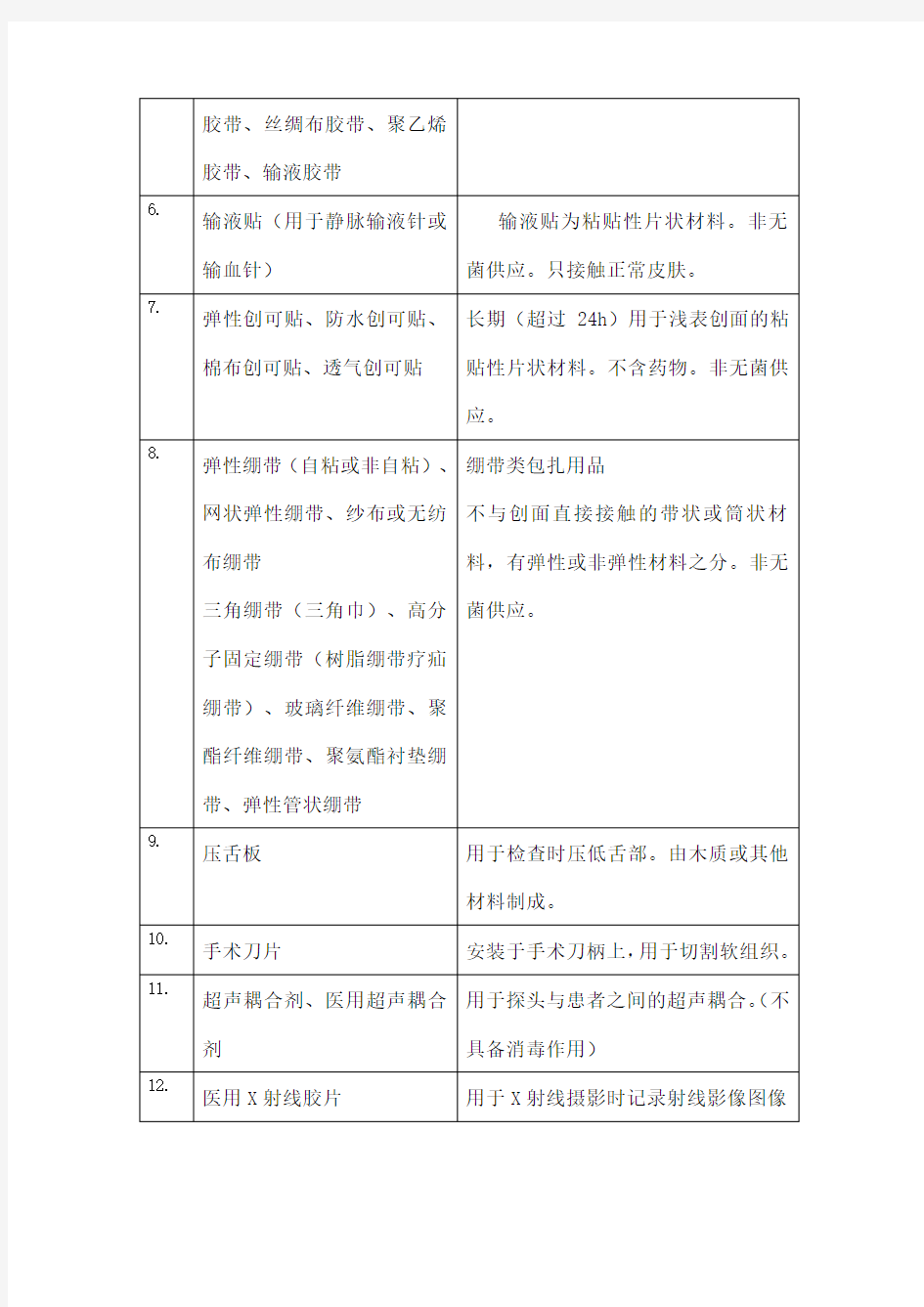
医疗器械公司简介范本医疗器械维修公司简介 医疗器械是指直接或者间接用于人体的仪器、设备、器具、体外诊断试剂及校准物、材料以及其他类似或者相关的物品。下面是小编整理的医疗器械公司简介范本,以供大家阅读。 医疗器械公司简介范本(一) 三瑞集团成立于1992年,2003年于新加坡主板上市,是中国第一家境外上市的医疗器械企业。集团总部位于广州、旗下骨干企业包括:广州三瑞医疗器械有限公司、香港耀滔有限公司、南京东大迪艾基因技术有限公司、广州丰宝泽德计算机科技有限公司、广州利菲达医疗设备有限公司和盟利(香港)有限公司等。 三瑞在广州和南京建有超过20000平方米的的研发、生产基地,22个用户服务中心遍布全国。骨干企业广州三瑞医疗器械有限公司具有现代化的技术研究和产品开发体系,已通过了ISO9001和ISO13485国际质量体系认证,是国家认定的高新技术企业和软件企业。目前,三瑞已为国内近8000家医疗机构(其中三甲医院600多家)和全球90多个国家和地区提供产品服务。 三瑞致力于妇女健康和优生优育事业,是著名的妇产科医疗器械专业制造商,为妇产科诊疗提供综合性解决方案,主要产品包括:围产监护和诊疗设备、宫颈病变诊疗器材、妇产科专用耗材等。同时三瑞凭借强大的技术支持能力与营销服务能力,不断引进国际先进的医疗技术和产品,目前是美国WALLACH妇科医疗产品、以色列TRIG的
分娩监护仪、美国MedGyn昆布条的独家代理。 医疗器械公司简介范本(二) 北京巴瑞医疗器械有限公司(Beijing Baron Medical Equipment Co., Ltd.)(简称巴瑞医疗)成立于2000年,落户于北京经济技术开发区,是人福医药(股票代码:600079)集团股份公司的控股子公司,是致力于体外诊断产品及生物试剂销售、生物医学转化、精准医疗检测、冷链物流配送为一体的科技型医疗服务企业。 巴瑞公司作为北京市场规模最大、检验诊断项目供应最齐全的医疗服务企业,奉行品德、责任、创新、远大的核心价值观,坚持与巨人同行的经营方针,坚持与合作伙伴保持长期、稳定、互惠、双赢的战略合作关系。同时,秉承以法为准、以德为先、以和为贵、以精为要、以远为行的经营原则,时刻以市场为导向,管理为基础,合作为途径,服务为核心。努力实现创新驱动、跨越发展、提质增效、及时高效地向国内医疗机构提供优质服务。 成立十五年,巴瑞已发展成为总部设在北京,覆盖京津冀多地的产业格局,市场网络覆盖区域超过500家医院,拥有高标准的市场、销售、客户服务、物流等体系,共有200多名员工,在新常态思路的引领下,巴瑞公司将抓住发展契机,勇于拼搏,锐意进取,不断深化与合作伙伴的价值合作、互利共赢、协同发展,打造医疗行业最受信赖的服务品牌,致力成为国内医疗领域卓越的服务商。 医疗器械公司简介范本(三) 南京华瑞医疗器械有限公司创建于1982年,前身为南京防腐设备
企业质量考核所需备案之各医疗器械标准 1.医用电气设备第一部分:安全通用要求-GB 9706.1-1995 2.医用电气设备第一部分:安全通用要求 1.并列标准:医用电气系统安全要求-GB 9706.15-1999 3.医用有机硅材料生物学评价试验方法-GB/T 16175-1996 4.医疗器械生物学评价第1部分:评价与试验-GB/T 16886.1-2001 5.编写和使用医用电气设备教材的导则-GB/Z 17994-1999 6.管理、医疗、护理人员安全使用医用电气设备导则-GB/T 17995-1999 7. 医疗保健产品灭菌生物指示物第1部分:通则-GB 18281.1-2000 8. 最终灭菌医疗器械的包装-GB/T 19633-2005 9. .医疗器械产品图样及设计文件的术语-YY/T 0047-91 10. 医疗器械产品工作图样的基本要求-YY/T 0048-91 1 1. 医疗器械产品图样及设计文件格式-YY/T 0049-91 12医疗器械产品图样及设计文件编号原则-YY/T 0050-91 13. 医疗器械产品图样及其主要设计文件的完整性-YY/T 0051-91 14. 医疗器械产品图样及设计文件的更改办法-YY/T 0052-91 15. 医疗仪器设备用产品铭牌-YY/T 0083-92 16. 质量体系医疗器械GB/T 19002-ISO 9002应用的专用要求-YY/T 0288-1996 17. 医疗器械风险管理对医疗器械的应用-YY/T 0316-2003 18. 医疗器械用于医疗器械标签、标记和提供信息的符号-YY 0466-2003 19. 医疗器械保障医疗器械安全和性能公认基本原则的标准选用指南-YY/T 0467-2003 20. 命名用于管理资料交流的医疗器械命名系统规范-YY/T 0468-2003
医疗器械标志、标签要求 医疗器械处黄荣建 二〇〇六年三月 一、范围 为医疗器械的安全和有效使用,给使 用者和其他人员规定了用于提供医疗器械 重要信息的标志、标识,主要由下列人员使 用。 ???? 医疗器械制造商 ???? 医疗器械使用者 ???? 负责医疗器械产品上市后监督的人员 ???? 主管部门、检测机构、认证机构等 二、依据 ???? 法律、法规 《医疗器械监督管理条例》 《医疗器械说明书、标签、包装标识》 ???? 国家标准、行业标准 通用标准 专用标准 产品标准 ???? 企业标准(注册产品标准) 标识、标签和使用说明书。 附录A安全要求中“外部标记”。(医用电气产 品) 通用标准 ?GB/T191-2000《包装储运图示标志》
?YY0466-2003《医疗器械用于医疗器械标签、标记和提供信息的符号》 ?YY/T0313-1998《医用高分子制品包装、标志、运输和贮存》?GB9706.1-1995《医用电气设备第一部分:安全通用要求》 ?YY91099-1999《医用X线设备标志、包装、运输和贮存》 专用标准 ?YY0089-1992《病人监护系统专用安全要求》 ?YY0319-2000《医用电气设备第二部分:医疗诊断用磁共振设备安全专用要求》 ?GB9706.X-XXXX《医用电气设备第X部分:XX设备安全专用要求》 ?YY0290.4-1997《人工晶体第4部分:标签和资料》 ?YY/T0486-2004《激光手术专用气管插管标志和提供信息的要求》 产品标准 ?GB8369-2005《一次性使用输血器》 ?GB10152《B型超声诊断设备》 ?YY0460-2003《超声洁牙设备》 医用高分子制品标志 ?单包装或初包装宜有下列标志: —产品名称、型号或规格; —制造厂名称、地址和商标; —生产批号或日期。 ?无菌产品的单包装或初包装还宜有下列标志:
GE GE在1998年收购了美国超声公司Diasonics, 结合自己产品开发了放射LOGIQ系列超声.1998年又收购了Vingmed公司,于是诞生了进入了心脏领域的VIVID系列超声产品。2001年从MEDISON手中收购了奥地利的超声巨头Kretz公司,凭借此公司在4D方面的优势,他们建立了妇科产科的VOLUSON系列超声。LOGIQ系列彩超产品是LOQIQ e, LOGIQ 3, LOGIQ 5, LOGIQ 7, LOGIQ 9.在不同国家和地区他们又丰富了中高端彩超产品系列。于2006年推出了LOGIQ P5, LOGIQ S6. 2008年又增加了LOGIQ P6,LOGIQ E9. 2009年金融危机时,针对中国4万亿的投资和乡村医疗计划,开发出了LOGIQ C3, LOGIQ C5低成本,低图像质量的投标产品。目前在亚太区域销售。VOLUSON系列便携彩超有VOLUSON e, VOLUSON i 台式妇科彩超VOLUSON 730(2007年)后来更新为VOLUSON E8. 中间增加了VOLUSON E6。VIVID心脏系列便携彩超有VIVID e, VIVID i, 台式VIVID S6,VIVID 7, VIVID E9。VIVID E9配有心脏4D成像探头。GE的手持式超声Vscan(手机大小)可以扫查心脏功能。在GE的黑白超逐渐停产之际,目前又推出了手持黑白Venue40。这个新的产品线体现了欧美市场的不景气。GE的特点就是市场营销非常优秀,对于低端产品的策略是解构主义加贴牌。 飞利浦Philips Philips当初是卖掉旗下一家公司,有了充足的资金而转投入医疗行业的。随着美国的两大超声企业ATL和HP公司分别被飞利浦收购,飞利浦拥有了放射和心脏两大彩超产品线。飞利浦放射超声有HD3, EnVisor(2002年),HD7,HD11,HD15。高端彩超iU22(全身),iE33(心脏)叱诧超声市场十年一直无人匹敌。其国外的代理商价格都是在20万美金左右。其HD3(2005年)基本在市场上已经销失。飞利浦与东软在2005年成立了一家各占51%与49%的股份的合资公司。飞利浦控制研发,东软负责生产。5年的合同已经到期,目前双方只是保持存在。EnVisor飞凡有美国生产和中国生产两款产品。中国的是由东软飞利浦生产。争力不是很强,目前不常见,国际上常见的是HD-7.东软目前自己在生产FLYING彩超。 西门子Siemens 在2001年西门子也通过兼并收购获得了美国超声巨头ACUSON公司。于是建立了全新的ACUSON系列超声产品:Cypress, X150, X300(2007年), CV70, X500. Sequoia,S2000, SC2000, P50, P10,Antares。西门子自己的SONOLINE系列超声G20(黑白),G40,G50,G60基本上已经消失。美中互利为其国内中高端彩超代理。蓝韵在国内代理西门子的X150(2007年)低端彩超。Acuson S2000 ABVS是女士乳腺全容积成像系统。是Acuson S2000彩超连接一个大线阵探头。大线阵探头设置在西门子著名的乳腺机下方。当乳房被卡位后,大线阵透过薄膜从下向上对乳腺进行扫描。Acuson SC2000是心脏超声,提供心脏定量分析。MEDISON在欧洲的品牌被别人注册,因此他们不得不使用产品型号SONOACE来参展。这次被三星收购后,MEDISON的品牌基本上就消失了。西门子一向最痛恨山寨版。这次自己却在X系列超声后列了个MEDASON。这是德国人很少见的幽默。
第一类医疗器械(包括体外诊断试剂)产品备案 一、办事项目: 第一类医疗器械(包括体外诊断试剂)产品备案 二、办事依据: 1、中华人民共和国国务院令第650号《医疗器械监督管理条例》 2、国家食品药品监督管理总局2014年第26号公告《关于第一类医疗器械备案有关事项的公告》 3、国家食品药品监督管理总局2014年第8号通告《关于发布第一类医疗器械产品目录的通告》 4、国家食品药品监督管理总局2014年第9号通告《关于发布医疗器械产品技术要求编写指导原则的通告》 5、国家食品药品监督管理总局2014年第25号公告《关于医疗器械生产经营备案有关事宜的公告》 6、国家食品药品监督管理总局《关于印发体外诊断试剂分类子目录的通知》(食药监械管〔2013〕242号) 7、国家食品药品监督管理总局2014年第23号公告《关于贯彻实施〈医疗器械监督管理条例〉有关事项的公告》 8、国家食品药品监督管理总局办公厅《关于实施第一类医疗器械备案有关事项的通知》(食药监办械管〔2014〕174号) 三、申请范围: l 本市第一类医疗器械备案人(持有企业营业执照和组织机构代码证),申请第一类医疗器械备案。 四、申请者资格/条件: l 申报备案的产品已经列入《第一类医疗器械产品目录》或属于《体外诊断试剂分类子目录》中第一类体外诊断试剂产品。 l 办理第一类医疗器械备案事务的人员应当受备案人委托,并具有相应的专业知识,熟悉相关法律、法规、规章和技术要求。 五、办理程序: 1、向备案人注册地所在区(县)的食品药品监督管理部门递交所有准备齐全的第一类医疗器械备案申报资料,内容包括: 1)第一类医疗器械备案表 2)安全风险分析报告; 3)产品技术要求, 4)产品检验报告 5)临床评价资料 6)生产制造信息 7)产品说明书及最小销售单元标签设计样稿 8)证明性文件 9)符合性声明
医疗器械公司介绍范文5篇Introduction of medical device company
医疗器械公司介绍范文5篇 小泰温馨提示:写作是运用语言文字符号以记述的方式反映事物、表达思想感情、传递知识信息、实现交流沟通的创造性脑力劳动过程。本文档根据写作活动要求展开说明,具有实践指导意义,便于学习和使用,本文下载后内容可随意修改调整修改及打印。 本文简要目录如下:【下载该文档后使用Word打开,按住键盘Ctrl键且鼠标单击目录内容即可跳转到对应篇章】 1、篇章1:医疗器械公司介绍范文 2、篇章2:医疗器械公司介绍范文 3、篇章3:医疗器械公司介绍范文 4、篇章4:医疗器械公司介绍范文 5、篇章5:医疗器械公司介绍范文 医疗器械是指直接或者间接用于人体的仪器、设备、器具、体外诊断试剂及校准物、材料以及其他类似或者相关的物品,下面是医疗器械公司介绍范文,欢迎参阅。 篇章1:医疗器械公司介绍范文 xxx有限公司成立于20xx年,成立十年多以来,携手国内外研究机构和高等学府,通过产学研的紧密结合,科曼集中
资源,在电生理监护、心电诊断、超声母婴监护、呼吸麻醉、婴儿保育、手术室设备等六大领域,深入研究,不断取得技术突破。拥有齐全、完整的监护产品线以及严格的质量管理控制体系. 科曼产品广泛应用于各级医疗机构、医用教育机构、医 学科研机构和社会服务保障机构。已初步形成心电图机系列、全院监护解决方案、手术室综合解决方案及NICU综合解决方案。 科曼研发制造出了全球第一款新生儿专用监护仪、心血 管专用监护仪。产品监测数据的准确性、填补了国内及世界专科专用方面的空白。 科曼采用标准导联(willson导联)测量心电向量,能达到麻醉机潮气量低至15ml,截止至今,国内发明专利103件,国际发明专利6件。 篇章2:医疗器械公司介绍范文【按住Ctrl键点此返回目录】山东xxx有限公司是一家专业生产手术无影灯、电动手 术床、医用吊塔、吊桥、空气消毒机、医用床、医用车,医用柜等护理、手术通用器械的公司。
大型医疗器械公司简介 医疗器械效用主要通过物理等方式获得,不是通过药理学、免疫学或者代谢的方式获得,或者虽然有这些方式参与但是只起辅助作用。下面是大型医疗器械公司简介范文,欢迎参阅。 大型医疗器械公司简介范文1 强生(中国)医疗器材有限公司成立于1994年,是强生公司在中国的独资企业,也是国内首家同时获得ISO9002质量体系和YY/T0288医疗器械应用专用标准两项权威认证的医疗器材公司。公司主要生产和销售强生先进的医疗器材和健康护理用品,同时,致力于将最新的医学技术和设备不断地介绍、引进到中国。位于闵行经济开发区的爱惜康缝线生产厂,是强生公司在全球最大的丝质医用缝合线生产厂。 公司共有员工1,000余名,总部设在上海,同时在北京、广州、武汉、南京、济南、杭州、重庆、成都、沈阳等城市均设有办事处,尽心为消费者提供最好的销售服务与研发环境,与中国医疗事业共同发展。位于北京和上海的两个"强生医疗学术中心"本着"探索人类科技,心系人类健康"的宗旨,以远程电视手术直播、电脑模拟手术、人体模拟操作系统、远程手术转播等设施为中国医护工作人员提供良好的专业培训机会,两个学术中心共同推动着中国医疗事业的进步,成为医护人员最可信赖的合作伙伴。 大型医疗器械公司简介范文2 上海懿城医疗器械有限公司[1] 国内总部坐落于云集了海内外众
多知名高新科技巨头的中国金融中心——上海。生产基地设在中国唯一的医疗器械高新技术产业中心(佛山市懿城医疗器械有限公司)——广东佛山。懿城集团是一家在生物科技、保健器材、医疗器械及康复设备等领域,集科研、开发、生产、销售于一体的现代化综合性高科技企业。 公司拥有一支国内、台湾及美国数位知名老专家及留德、留美归国硕士、博士等老中青专家所组成的研发队伍,科研力量十分雄厚。经过多国年的努力,结合了德国、美、台湾等国家和地区业已成熟的医械技术,精心研制出了新一代"懿城牌YC型系列心脑血管治疗仪"。大型医疗器械公司简介范文3 北京波姆医疗器械有限公司,简称BPM公司,它是集研发设计、生产制造、销售服务为一体的专业化企业,又是集红外电子医疗、康复理疗和诊断系列产品的专业化实体。BPM公司通过了ISO9000及ISO13485国际质量体系认证。 BPM红外偏振光疼痛治疗仪和红外光疗仪是公司的主打产品,它适应了国内医疗市场需求,正确地选择了目标市场定位和产品定位,拓宽了人文科技创新,开拓了产品的国有化升级、规范化和临床科学应用的新进展(即第二代红外偏振光治疗仪)。 公司产品是从人文理念和绿色治疗的新特点融入国内医疗领域,特别是基层社区和重点医院科室,如疼痛、中医针灸、骨伤、康复理疗等,为中老年常见病、多发病的疼痛治疗提供了有效的设备和可行的医疗方法,给广大患者带来福音,同时也给各基层社区和医疗单位
个人收集整理仅供参考学习 一、《医疗器械分类目录》核定的第一类医疗器械产品 6801 基础外科手术器械 编号代码名称6801-2 基础外科用刀 6801-3 基础外科用剪 6801-4 基础外科用钳 6801-5 基础外科用镊夹6801-6 基础外科用针、钩6801-7 基础外科其它器械 品名举例 手术刀柄和刀片、皮片刀、疣体剥离刀、柳叶刀、铲刀、剃毛刀、 皮屑刮刀、挑刀、锋刀、修脚刀、修甲刀、解剖刀 普通手术剪、组织剪、综合组织剪、拆线剪、石膏剪、解剖剪、 纱布绷带剪、教育用手术剪 普通止血钳、小血管止血钳、蚊式止血钳、组织钳、硬质合金镶 片持针钳、普通持针钳、创夹缝拆钳、皮肤轧钳、子弹钳、纱布 剥离钳、海绵钳、帕巾钳、皮管钳、器械钳 小血管镊、无损伤镊、组织镊、整形镊、持针镊、保健镊(简易 镊)、拔毛镊、帕巾镊、敷料镊、解剖镊、止血夹 动脉瘤针、探针、推毛针、植毛针、挑针、教学用直尖针、静脉 拉钩、创口钩、扁平拉钩、双头拉钩、皮肤拉钩、解剖钩 刀片夹持器、麻醉口罩、麻醉开口器、照明吸引器头、粉刺取出 器、黑头粉刺压出器、皮肤刮匙、皮肤套刮器、皮肤刮划测检器、 皮肤检查尺、皮肤组织钻孔器、开口器、卷棉子 6802 显微外科手术器械 编号代码名称品名举例 6802-1 显微外科用刀、凿显微喉刀 6802-2 显微外科用剪显微剪、显微枪形手术剪、显微组织剪 6802-3 显微外科用钳显微枪形麦粒钳、显微喉钳、显微持针钳 6802-4 显微外科用镊、夹显微镊、显微持针镊、显微止血夹 6802-5 显微外科用针、钩显微耳针、显微喉针、显微耳钩、显微喉钩 6802-6 显微外科用其他器械显微合拢器 6803 神经外科手术器械 编号代码名称品名举例 6803-2 神经外科脑内用钳银夹钳、 U 型夹钳、动脉瘤夹钳 6803-5 神经外科脑内用其他器械脑吸引器、后颅凹牵开器、手摇颅骨钻、脑打针锤、脑压板 6804 眼科手术器械 编号代码名称品名举例 6804-2 眼科手术用剪角膜剪、眼用手术剪、眼用组织剪 6804-3 眼科手术用钳晶体植入钳、环状组织钳 6804-4 眼科手术用镊、夹角膜镊、眼用镊、眼用结扎镊 6804-5 眼科手术用钩、针眼用钩针 6804-6 眼科手术用其他器械眼用板铲、眼用固定环、开睑器 6805 耳鼻喉科手术器械 编号代码名称品名举例 6805-1 耳鼻喉科用刀、凿耳鼓膜刀、鼻粘膜刀、扁桃体刀、酒渣鼻切割刀、鼻骨凿、乳突平(园)骨凿、上颌窦对孔凿、耳用骨凿 6805-2 耳鼻喉科用剪扁桃体剪、甲状腺剪、喉头剪、中耳剪、鼻剪 6805-3 耳鼻喉科用钳扁桃体止血钳、枪式间接喉钳、筛窦钳、耳钳、双关节鼻中隔咬
医疗器械公司简介范文 公司拥有一支国内、台湾及美国数位知名老专家及留德、留美归国硕士、博士等老中青专家所组成的研发队伍,科研力量十分雄厚。经过多国年的努力,结合了德国、美、台湾等国家和地区业已成熟 的医械技术,精心研制出了新一代“懿城牌YC型系列心脑血管治疗仪”。 BPM红外偏振光疼痛治疗仪和红外光疗仪是公司的主打产品,它 适应了国内医疗市场需求,正确地选择了目标市场定位和产品定位,拓宽了人文科技创新,开拓了产品的国有化升级、规范化和临床科 学应用的新进展(即第二代红外偏振光治疗仪)。 陕西省医疗器械公司成立于1982年,地址在西安市碑林区兴庆 路60号,是国有企业,原隶属于陕西省国资委,现隶属于西安市国 资委(西安市机电化工国有资产管理公司)管理。既是陕西省及西北 地区经营规模最大、品种最全的医疗器械商业企业,又是陕西省政 府指定的救灾医疗器械储备单位。也是陕西省食品药品监督管理局 唯一批准销售一、二、三类医疗器械的单位。 陕西省食品药品监督管理局唯一批准销售一、二、三类医疗器械的单位。 陕西省医疗器械公司和许多厂家、特别是国内外知名企业和大专院校及各级医院建立了长期的合作关系,并结成了良好的供销关系,形成了稳固的供销渠道。 公司代理了国内外许多名优产品。 徐州卫材厂耗材、山东威高集团系列耗材、鱼跃制氧机及家用保健器械等系列产品、上海华线高压灭菌器和X光机的全线产品、湖 北省荆州市医疗器械厂生产的自控中心供氧负压系统。 为方便客户,解除客户之忧,我公司设有售后服务部。
还和数十家供货单位签有售后服务及培训协议,以此保证质量,保证使用。 汉魏医疗立足于魏家屯镇医疗器械的行业基础,扎根文化沃土,整合优势资源,以传承为奠基之石,以创新为发展之源,以科技为制胜之本,力争为消费者提供更专业、更先进、更安全的医疗器械产品。 【公司简介】 广元市顺康医疗器械有限公司是一家各类医疗器械销售企业。公司座落于环境优美的风景区“雪梨之乡”,公司主要经营各类医疗设备、器械及医疗耗材销售服务。 【企业文化】 坚持“以人为本,尊重科学,注重产品质量,合法经营,共同发展”的理念,倡导“严谨、和谐、向上”的企业文化。 【工作时间】: 【薪资福利】 1、薪资结构(仅限于职员及以上): 基本工资+绩效工资+年终奖金+其他补贴 1)月度发放基本工资、绩效工资及其他补贴。 2)根据公司经营业绩及员工绩效表现发放年终奖金。 3)年度调薪。 2、福利及业余文化活动: 2)带薪年休假及法定节假日。 【培训与发展】:
YZB 医疗器械注册产品标准 YZB/苏(常)XXXX-200X 标准名称 标准英文名称(进口产品) 200X-XX-XX 发布200X-XX-XX 实施 X X X X (企业)发布
前言 XXX(产品名称)目前尚无国家标准和行业标准,根据《医疗器械标准管理办法》,特制定本标准,作为企业生产、监督的依据。 本标准的编写符合GB/T1.1-2000、GB/T1.2-2002和《医疗器械注册产品标准编写规范》的有关要求。 本标准的附录X是规范性附录; 本标准的附录X是资料性附录。 本标准由XXXXXXXXX(企业名称)提出。 本标准由XXXXXXXXX(企业名称)负责起草。 本标准主要起草人:XXX、XXX。 本标准首次发布时间:200X年X月。
XXXXXXXXX(标准名称) 1 范围 本标准规定了XXXXX的分类和标识、要求、试验方法、标志、使用说明书、包装、运输、储存的要求。 本标准适用于XXXXX(以下简称XXX)。该产品用于XXXXXXXXXXXXXXXXXXXXXXXX。 2 规范性引用文件 下列文件中的条款通过本标准的引用而成为本标准的条款。凡是注日期的引用文件,其随后所有的修改单(不包括勘误的内容)或修订版均不适用于本标准,然而,鼓励根据本标准达成协议的各方研究是否可使用这些文件的最新版本。凡是不注日期的引用文件,其最新版本适用于本标准。 GB XXXX-XXXX XXXXXXX YY XXXX-XXXX XXXXXXX ISO XXXXX-X:XXXXX XXXXX 3 分类和标记 3.1 分类 (产品的组成、结构、型式,结构、型式可用图表示、规格尺寸可列表表示) 3.2 标记 (为符合标准要求的产品(系列)建立一个分类、型号、产品代码) 4 要求 4.1外观 4.2尺寸 4.3 物理(或机械)性能 如强度、硬度、弹性、耐热性、耐磨性等。 4.4 使用性能 4.5 化学性能 如还原物质(易氧化物)、金属离子、酸碱度、蒸发残渣、紫外吸光度、环氧乙烷残留量等。 4.6 生物性能 如无菌、热原、溶血、刺激、致敏等(按GB/T16886.1) 4.7 安全性能 GB 9706医用电气设备通用安全要求系列标准; GB/T16886医疗器械生物学评价系列标准; YY/T口腔材料生物学评价系列标准; 及其他安全要求。 4.8 其他方面的要求 5 试验方法 5.1 外观 5.2 尺寸
1 医疗器械公司简介 导语:简介以全面、稳妥又要有很强的机动性、灵活性。在材料选择上以事实材料为主~如何写呢本文是品才网小编精心编辑的~希望能帮助到你! 医疗器械公司简介范文河北汉魏医疗器械有限公司成立于2016年11月1日~注册资金2000万元~公司下辖汉魏生物科技有限公司、汉魏房地产开发有限公司~是一家高起点、高标准、高品质的中高端医疗器械生产企业。公司位于国内三大医疗器械生产基地之一的衡水市滨湖新区魏家屯镇~“汉魏”即取“古汉今风、文化魏屯”之意(据考证~魏家屯镇为西汉时信都郡治所所在地~是古冀州文化的发源地~具有悠久的历史文化内涵)。 公司产品种类丰富~质量上乘~现有退热贴、颈椎牵引器、医用腰围固定带、颈椎健康枕、各种病床、按摩床、床垫、床头柜、病床餐桌、输液架、暖贴等40余个产品。公司生产的好闺女家庭护理系列产品好闺女腰护士(医用腰围固定带)、好闺女颈护士(颈椎牵引器)、好闺女健康枕、好闺女暖贴等产品一上市就赢得了消费者的认可~其中医用腰围固定带的充气加压气囊等几项技术还荣获国家专利。 汉魏医疗立足于魏家屯镇医疗器械的行业基础~扎根 ~ 1 / 4 文化沃土~整合优势资源~以传承为奠基之石~以创新为发展之源~以科技为制胜之本~力争为消费者提供更专业、更先进、更安全的医疗器械产品。 河北汉魏医疗器械有限公司将以“传承创新科技制胜”为宗旨~秉承“自强不息、大气谦和、传承创新、敢为人先”的企业文化~努力打造中国北方第一医疗器械基地~铸就家庭护理领导品牌。
医疗器械公司简介范文山东兖州华诺医疗器械有限公司是一家专业生产手术无影灯、电动手术床、医用吊塔、吊桥、空气消毒机、医用床、医用车~医用柜等护理、手术通用器械的公司。 经过多年的不懈努力~山东兖州华诺医疗器械有限公司现已成为全国一流的医疗、医护设备制造商。兖州华诺医疗器械有限公司始终坚持“精心设计、精心制作、热情服务、争创一流、以科技促发展、靠质量求生存”的质量方针~始终奉行“人诚企信、主客双赢”的经营理念~视质量为企业生命~将用户当衣食父母~用物优价廉、高品质的产品回报社会!回报用户!我公司非常希望与各企业取得真诚的合作~为合作伙伴提供优良的服务。 生产技术方面~从机械加工、注塑、冲压、钣金、焊接到总装、试验~都具有一套完事的工艺流程。拥有国内一流的数控设备、注塑设备和检测设备~具有较强的加工制造 2 / 4 能力。 % 在产品服务上~设有专门的售后服务队伍~解除客户的后顾之忧。 在今后的发展道路上~公司秉承:为顾客提供最好的护理手术设备的宗旨~完善自己的产品、服务~回报广大新老客户。 医疗器械公司简介范文深圳市科曼医疗设备有限公司成立于2002年~成立十年多以来~携手国内外研究机构和高等学府~通过产学研的紧密结合~科曼集中资源~在电生理监护、心电诊断、超声母婴监护、呼吸麻醉、婴儿保育、手术室设备等六大领域~深入研究~不断取得技术突破。拥有齐全、完整的监护产品线以及严格的质量管理控制体系.
目次 目次 (1) 前言 (4) 1.范围 (4) 2.规范性引用文件 (4) 3.分类 (4) 3.1术语与定义................................................................................................................ 错误!未定义书签。 3.2管理分类 (4) 3.3命名与型号 (4) 3.4组成 (4) 4.要求 (4) 4.1产品说明要求 (4) 4.1.1可用性 (4) 4.1.2内容 (4) 4.1.3标识和标示 (5) 4.1.4功能性陈述 (6) 4.1.4.1功能概述 (6) 4.1.4.1.1远程会诊系统 (6) 4.1.4.1.2双向转诊系统............................................................................................ 错误!未定义书签。 4.1.4.1.3计费系统.................................................................................................... 错误!未定义书签。 4.1.4.1.4医疗资源共享系统.................................................................................... 错误!未定义书签。 4.1.4.1.5管理系统.................................................................................................... 错误!未定义书签。 4.1.4.2 产品的功能........................................................................................................... 错误!未定义书签。 4.1.4.3当有软件组件的选项和版本时,应指明。 (6) 4.1.4.4功能性限制 .................................................................................................... 错误!未定义书签。 4.1.4.5对未授权访问的预防措施 (6) 4.1.5可靠性陈述 (6) 4.1.6易用性陈述 (6) 4.1.7效率陈述 (7) 4.1.8维护性陈述 (7) 4.1.9可移植性陈述 (7) 4.2用户文档集要求 (7) 4.2.1完备性 (7) 4.2.2正确性 (8) 4.2.3一致性 (8) 4.2.4易理解性 (8)
第一类医疗器械备案表 产品名称(产品分类名称): 备案人: 成都市食品药品监督管理局制
填表说明 1.本表用于进口和境内第一类医疗器械、体外诊断试剂备案。 2.要求填写的栏目内容应使用中文、打印完整、清楚、不得空白,无相关内容处应填写“∕”。 因备案表格式所限而无法填写完整时,请另附附件。 3.备案时应一并提交含有备案表内容(含附件)的电子文档(Excel形式)。 4.境内医疗器械、体外诊断试剂只填写备案人名称、注册地址和生产地址中文栏。进口医 疗器械、体外诊断试剂备案人名称、注册地址和生产地址中文栏自行选择填写。进口医疗器械产品名称(体外诊断试剂为产品分类名称,以下同)中文栏必填。 5.如系统支持,则进口医疗器械产品名称、备案人名称、注册地址和生产地址原文栏必填, 原文填写内容应与备案人注册地址或生产地址所在国家(地区)医疗器械主管部门出具的允许产品上市销售的证明文件中载明内容和文种一致。 6.境内医疗器械备案人应填写组织机构代码。 7.进口医疗器械产品名称、备案人名称、注册地址和生产地址英文栏必填。如原文非英文, 英文内容必须与原文一致。 8.所填写各项内容应与所提交备案材料内容相对应。 9.产品类别及分类编码应根据医疗器械分类规则和医疗器械分类目录、第一类医疗器械产 品目录、第一类体外诊断试剂分类子目录等相关文件填写。 10.备案人、代理人注册地址栏填写备案人和代理人企业营业执照等相关证明性文件上载明 的注册地址。 11.备案人、代理人所在地系指备案人和代理人注册地址所在国家(地区)或省(区、市)。 12.如有其他需要特别加以说明的问题,请在本表“其他需要说明的问题”栏中说明。
YZB 医疗器械注册产品标准 病床 2011-03-11发布2011-03-11实施 杭州临安庄盛工贸有限公司发布
前言 为确保“饮料”系列产品出厂成品质量,维护消费者权益,同时达到加强管理、降低成本、提高经济效益目的,本着“有标可依”原则,于2004年12月18日发布了河北公司企业标准Q/《饮料》,现决定从2005年1月28日起执行。 本标准由河北公司提出。 本标准由技术部起草并负责解释。 本标准由河北公司技术部发布。 本标准修改权属 本标准起草人:
饮料 1.范围 本标准规定了饮料的产品分类、技术要求、试验方法、检验规则和标志、包装、运输、贮存等要求。 本标准适用以为原料,添加或不添加食品添加剂与辅料,经,而制成的饮料。 2.规范性引用文件 下列文件中的条款,通过本标准的引用而成为本标准的条款。凡是注目期的引用文件,其随后所有的修改单(不包括勘误的内容)或修订版均不适用于本标准,然而,鼓励根据本标准达成协议的各方研究是否可使用这些文件的最新版本。凡是不注日期的引用文件,其最新版本适用于本标准。 GB1354-86大米 GB2760食品添加剂使用卫生标准 GB/T5009.5食品中蛋白质的测定方法 GB/T5009.7食品中还原糖的测定方法 GB/T5009.8食品中蔗糖的测定方法 GB/T5009.46乳与乳制品卫生标准的分析方法 GB7718食品标签通用标准 GB/T10790软饮料的检验规则、标志、包装、运输、贮存 GB4789.2食品卫生微生物学检验菌落总数测定 GB4789.3食品卫生微生物学检验大肠菌群测定 GB4789.4食品卫生微生物学检验沙门氏菌检验 GB4789.5食品卫生微生物学检验志贺氏菌检验 GB4789.10食品卫生微生物学检验金黄色葡萄球菌检验 GB4789.11食品卫生微生物学检验溶血性链球菌检验 GB4789.18食品卫生微生物学检验乳与乳制品检验 GB/T5009.11食品中总砷的测定方法 GB/T5009.12食品中总铅的测定方法 GB/T5009.17食品中总汞的测定方法 GB/T5009.19食品中六六六、滴滴涕残留量的测定方法 GB/T5009.24食品中黄曲霉毒素M1和B1的测定方法 GB/T4789.34食品卫生微生物学检验双歧杆菌检验
备案号: 1 第一类医疗器械备案表 产品名称(产品分类名称): 备案人: 广州市食品药品监督管理局制
填表说明 1.本表用于进口和境内第一类医疗器械、体外诊断试剂备案。 2.要求填写的栏目内容应使用中文、打印完整、清楚、不得空白,无相关内容处应填写“∕”。 因备案表格式所限而无法填写完整时,请另附附件。 3. 备案时应一并提交含有备案表内容(含附件)的电子文档(Excel形式)。 4.境内医疗器械、体外诊断试剂只填写备案人名称、注册地址和生产地址中文栏。进口医 疗器械、体外诊断试剂备案人名称、注册地址和生产地址中文栏自行选择填写。进口医疗器械产品名称(体外诊断试剂为产品分类名称,以下同)中文栏必填。 5.如系统支持,则进口医疗器械产品名称、备案人名称、注册地址和生产地址原文栏必填, 原文填写内容应与备案人注册地址或生产地址所在国家(地区)医疗器械主管部门出具 的允许产品上市销售的证明文件中载明内容和文种一致。 6.境内医疗器械备案人应填写组织机构代码。 7.进口医疗器械产品名称、备案人名称、注册地址和生产地址英文栏必填。如原文非英文, 英文内容必须与原文一致。 8.所填写各项内容应与所提交备案材料内容相对应。 9. 产品类别及分类编码应根据医疗器械分类规则和医疗器械分类目录、第一类医疗器械产 品目录、第一类体外诊断试剂分类子目录等相关文件填写。 10.备案人、代理人注册地址栏填写备案人和代理人企业营业执照等相关证明性文件 上载明的注册地址。 11.备案人、代理人所在地系指备案人和代理人注册地址所在国家(地区)或省(区、市)。 12.如有其他需要特别加以说明的问题,请在本表“其他需要说明的问题”栏中说明。
境内第一类医疗器械注册审批操作规范(试行)境内第一类医疗器械注册(重新注册)由受理、行政审批环节构成。审批总时限为自开具受理通知书之日起30个工作日内。 一、受理 主要对境内第一类医疗器械注册(重新注册)申请材料进行形式审查,保证申请材料的齐全性和规范性,并向社会公告受理情况。 医疗器械生产企业申请境内第一类医疗器械注册(重新注册),应向所在地设区市(食品)药品监督管理部门报送规定的注册申请材料。 (一)受理要求 1.《境内医疗器械注册申请表》 申请企业填交的《境内医疗器械注册申请表》应有法定代表人签字并加盖公章,所填写项目应齐全、准确,填写内容应符合以下要求: (1)“生产企业名称”、“注册地址”与《工商营业执照》相同; (2)“产品名称”、“规格型号”与所提交的产品标准、检测报告等申请材料中所用名称、规格型号一致。 2.医疗器械生产企业资格证明 资格证明包括《第一类医疗器械生产企业登记表》复印件以及《工商营业执照》副本复印件。 (1)申请注册(重新注册)的产品应在《第一类医疗器械生产企业登记表》核定的生产范围内; (2)《工商营业执照》在有效期内。 3.适用的产品标准及说明 申请企业提交的产品标准可为国家标准、行业标准或注册产品标准文本。 (1)采用国家标准、行业标准作为产品标准的,应提交所采纳的国家标准或行业标准的有效文本及采标说明; (2)采用注册产品标准作为产品标准的,应提交注册产品标准正式文本及其编制说明。4.产品全性能检测报告 产品全性能检测报告应包括以下内容: (1)产品名称、规格型号、产品编号或批号、生产日期、样品数量、抽样基数; (2)检测依据、检测项目、标准要求、检测结果、结果判定、检验人员、审核人员签字或盖章、检验日期等; (3)如属于委托检测,应提供被委托检测机构出具的检测报告和委托检验协议书。 5.企业生产产品的现有资源条件及质量管理能力(含检测手段)的说明 企业产品生产现有资源条件及质量管理能力(含检测手段)的说明应包括以下内容:(1)申请企业现有资源(人力资源、基础设施、工作环境等)条件、管理能力、生产能力、检验手段和能力的说明; (2)提供生产设备、检测仪器清单及产品检验所需计量器具的有效检定证书(复印件)。6.医疗器械说明书 医疗器械说明书至少应包括以下内容: (1)产品名称、型号、规格; (2)生产企业名称、注册地址、生产地址、联系方式; (3)《医疗器械生产企业许可证》编号、医疗器械注册证书编号(申报时内容为空白)、产品标准编号;
第二部分:对产品的销售方法的选择,例如,经销商模式,直销, 为什么会选择这种模式,或者使用混合模式第三部分:在模式选定后,可以操作的步骤,例如如何选择经销商等等 选好经销商后,如何与经销商保持信息通畅。 第四部分是销售的其他方面,例如广告和品牌的建立和促销等 ■如何写外贸销售计划书: (1)外贸业务做为一个长久不衰的行业,有着得天独厚的优势.我通常把业务分为以下 几个阶段: 阶段一:.熟悉产品好的业务员有着精湛的以下标准清单仅做参考,以最新版本为准. 标准编号标准名称 实施日 期备注 GB/T1.1-2000标准化工作导 则第一部分结 构和编写规则 2001-6- 1 国 家 标 准 GB 1.2-2002标准化工作导 则第二部分结 构和编写规则 2003-1- 1 国 家 标 准
第二部分:对产品的销售方法的选择,例如,经销商模式,直销, 为什么会选择这种模式,或者使用混合模式第三部分:在模式选定后,可以操作的步骤,例如如何选择经销商等等 选好经销商后,如何与经销商保持信息通畅。 第四部分是销售的其他方面,例如广告和品牌的建立和促销等 ■如何写外贸销售计划书: (1)外贸业务做为一个长久不衰的行业,有着得天独厚的优势.我通常把业务分为以下 几个阶段: 阶段一:.熟悉产品好的业务员有着精湛的 GB/T20001.1-2001 标准编写规则 第一部分术语国家标准 GB/T20001.2-2001 标准编写规则 第二部分符号国家标准 GB/T20001.3-2001标准编写规则 第三部分信息 分类 国 家 标
第二部分:对产品的销售方法的选择,例如,经销商模式,直销, 为什么会选择这种模式,或者使用混合模式第三部分:在模式选定后,可以操作的步骤,例如如何选择经销商等等 选好经销商后,如何与经销商保持信息通畅。 第四部分是销售的其他方面,例如广告和品牌的建立和促销等 ■如何写外贸销售计划书: (1)外贸业务做为一个长久不衰的行业,有着得天独厚的优势.我通常把业务分为以下 几个阶段: 阶段一:.熟悉产品好的业务员有着精湛的 准 GB/T20001.4-2001标准编写规则 第四部分化学 分析 国 家 标 准 GB/T1.22-1993标准化工作导 则第二部分标 准内容的确定 国 家 标 准 GB228-2002 金属材料室温 拉伸试验2002-1- 1 国 家
医疗器械CRO行业概况 一、医疗器械CRO定义 医疗器械,是指直接或者间接用于人体的仪器、设备、器具、体外诊断试剂及校准物、材料以及其他类似或者相关的物品,包括所需要的计算机软件。目的是疾病的诊断、预防、监护、治疗或者缓解;损伤的诊断、监护、治疗、缓解或者功能补偿;生理结构或者生理过程的检验、替代、调节或者支持;生命的支持或者维持;妊娠控制;通过对来自人体的样本进行检查,为医疗或者诊断目的提供信息。医疗器械行业涉及到医药、机械、电子、塑料等多个行业,是一个多学科交叉、知识密集、资金密集的高技术产业。 医疗器械CRO是接受医疗器械研发生产企业或者组织的委托,代表委托方负责实施医疗器械上市过程中全部或部分的科学或医学试验,以获取商业性的报酬的第三方组织。CRO 公司通常由熟悉药械研发过程和注册法律法规的专业化人才组成,具备规范的服务流程,在一定区域内拥有合作网络,可以帮助医疗器械生产企业降低研发投入、缩短研发周期、提高研发效率,降低研发失败的风险,加快上市的审批流程。 与创新药研发路上的卖水人(医药CRO公司)类似,从本质上看医疗器械CRO服务是服务外包的一种形式,依附于医疗器械行业,其下游是医疗器械企业,上游则是提供医疗器械临床数据的医疗机构——同时是医疗器械生产商的下游,行业的主要业务来源医疗器械公司和医疗器械研发者的委托。 医疗器械CRO公司在产业链中的位置 目前,国内医疗器械类CRO 公司数量有数百家之多,但是行业小企业居多,营业收入和盈利能力较差,行业亟需优化整合。
二、医疗器械CRO公司业务范围 一直以来,CRO行业的服务范围主要以研发、临床试验为主,药物和医疗器械从研发开始到上市销售的过程是一项高技术、高风险、高投入和长周期的复杂系统工程。近年来,医疗器械在中国飞速发展,医疗器械法律法规监管越加严格和完善,迫使医疗器械企业通过寻求专业的外包服务商来协助完成临床试验的工作以降低研究开发的成本,缩短产品的研发时间,迫使CRO行业的服务往更专业、细化的方向转变。 药物临床试验和医疗器械临床试验的异同 目前,虽然各家医疗器械CRO公司业内侧重点各有不同,但是市场上的CRO 公司基本涵盖了医疗器械设计、研发、生产、注册、上市、推广的全过程。项目主要包括医疗器械开发价值评估与分析、临床试验方案设计和实施、病例报告表的设计、临床监查工作、数据管理、医学报告的撰写、产品代理注册、临床试验方案知识产权代理、市场招商、融资创新服务和学术会议举办、员工培训等,是一种专业要求极高的外包服务。 作为被选择的委托对象,临床试验CRO企业一般均按照国家规定的相关内容开展业务,确保项目符合国家相关法律法规要求,满足客户产品在临床试验方面的各类需求。由此可见,对于CRO企业来说,对行业规则的理解和判断能力、