
肝切除术前肝脏储备功能评估的专家共识(2011版)
董家鸿郑树森陈孝平窦科峰樊嘉别平耿小平吕文平
Consensus on evaluation of hepatic functional reserve before Hepatectomy(2011 edition)Ding Jia-hong*,Zheng Shu-sun,Chen Xiao-ping, Dou Ke-feng, Fan Jia, Bie Ping,Geng Xiao-ping, LV Wen-ping.*Hospital&Institute of hepatobiliary surgery,Chines PLA General Hospital,Beijing,100853,China corresponding author: Ding Jia-hong, E-mail: dongjh301 @https://www.doczj.com/doc/9e14160599.html,
【Key words】Hepatic functional reserve;Hepatectomy;Evaluation;Consensus
【关键词】肝脏储备功能; 肝切除术; 评估; 共识
肝脏外科已走进了精准外科时代?精准肝脏外科在追求彻底清除目标病灶的同时,确保剩余肝脏解剖结构完整和功能性体积最大化,并最大限度控制手术出血和全身性创伤侵袭,最终使手术患者获得最佳康复效果[1-2]?
肝切除是肝脏外科疾患的重要治疗手段?由于肝脏外科疾患尤其是肝细胞癌多合并肝实质损害,肝脏储备功能有不同程度的降低,肝切除术后肝脏功能不全成为患者围手术期死亡的重要原因?术前精确评估肝脏储备功能,对于选择合理的治疗方法,把握安全的肝切除范围,从而降低患者术后肝脏功能衰竭的发生率具有重要意义?
1 肝脏储备功能的概念及解剖生理基础[3]
(1) 肝脏储备功能的概念:系指肝脏应对生理负荷增加时可动员的额外代偿潜能?肝脏在受到损害的病理状态下,肝脏储备功能除了需应对机体代DOI:10.3760/cma.j.issn.1673 9752.2011.01.006
(2)肝脏储备功能的解剖生理基础:肝脏储备功能主要取决于功能性肝细胞群的数量及其组织结构的完整性?
2 评估肝脏储备功能的目的
通过评估肝脏储备功能,了解患者对不同类型或范围的肝切除手术的耐受性,为设计和实施安全手术提供依据,以预防患者手术后发生肝脏功能衰竭?
3 评估肝脏储备功能的主要方法
评估肝脏储备功能的方法繁多,主要方法可分为5类:(1)肝脏血清生化学试验?(2)综合评分系统?(3)肝脏功能定量试验?(4)肝实质及脉管病变的影像学评估?(5)肝脏体积测量?
3.1 肝脏血清生化学试验
通过检测血清中肝脏合成和分泌的物质含量或酶的活性,提示肝脏损害和病变?
(1)转氨酶:主要包括丙氨酸氨基转移酶(alaninetransaminase,ALT)和门冬氨酸氨基转移酶(aspartatetransaminase,AST)?ALT主要存在于细胞质中;AST主要存在于细胞质和线粒体中?ALT和AST是肝细胞损伤的敏感指标,其水平升高提示肝实质受到了不同程度的损害,但是与肝脏储备功能并无直接的关联?
(2)碱性磷酸酶(alkalinephosphatase,ALP)和γ 谷氨酰转肽酶(gammaglutamyltranspeptidase,GGT):ALP是一组水解酶,主要存在于肝脏的毛细胆管?骨?肾和胎盘中;GGT主要存在于肝?胰?脾?肾?心?脑等细胞膜上?当存在胆汁淤滞或肝实质损害时,ALP和GGT水平增高?从毛细胆管到胆总管开口任何层面的胆道梗阻和胆汁淤滞均可导致ALP和GGT升高?
(3)胆红素:胆红素是血红蛋白代谢的主要降解产物,其血浆浓度反映了肝细胞通过肝脏网状内皮系统对胆红素进行摄取?结合和排泄的过程?肝实质严重损害和胆汁淤滞均可导致血浆总胆红素水平升高,这是与肝切除手术预后相关的独立危险因素?
(4)白蛋白:只在肝脏合成,其循环半衰期为20d,检测白蛋白可了解肝脏稳态合成功能,是Child评分的指标之一?
(5)凝血酶原时间:肝脏是合成凝血因子Ⅱ?Ⅴ?Ⅶ?Ⅹ的重要场所?凝血酶原时间反映了包括凝血因子Ⅱ?Ⅴ?Ⅶ?Ⅹ和纤维蛋白原在内的外源性凝血过程?
上述生化指标有的与肝脏功能无关,有的只从一个侧面反映了肝脏功能,对手术后肝脏功能衰竭并无预测价值?原因为[4]:(1)其中大部分指标并非特异地反映肝脏功能的损害情况,这些指标在血清中的含量或酶活性取决于其产生?分布与清除的总和效应?许多肝外因素也可引起这些指标的异常,如营养不良和肾病等导致白蛋白降低,胆道梗阻?脓血症?长期胃肠外营养?溶血等导致胆红素升高,肌病或者剧烈运动等导致ALT 或AST升高,维生素K缺乏?脂肪泻?抗生素应用等导致凝血酶原时间延长?(2)部分指标在1%~4%的正常人群中存在异常?(3)即使少量的肝细胞受损也可导致一些肝细胞结构酶指标的明显异常,并不能反映整体肝脏功能状况;而反映肝脏代谢和蛋白合成功能的指标,只有当肝脏功能严重受损而失代偿时才会出现异常改变?
建议1:肝脏血清生化学试验有助于对肝脏组织损伤及其程度作出大体的判断,可作为非肝脏手术患者术前肝脏功能代偿状态的评估方法,但不能作为肝脏手术术前精确评估肝脏储备功能和预测手术后肝脏功能衰竭的可靠指标?
3.2 综合评分系统
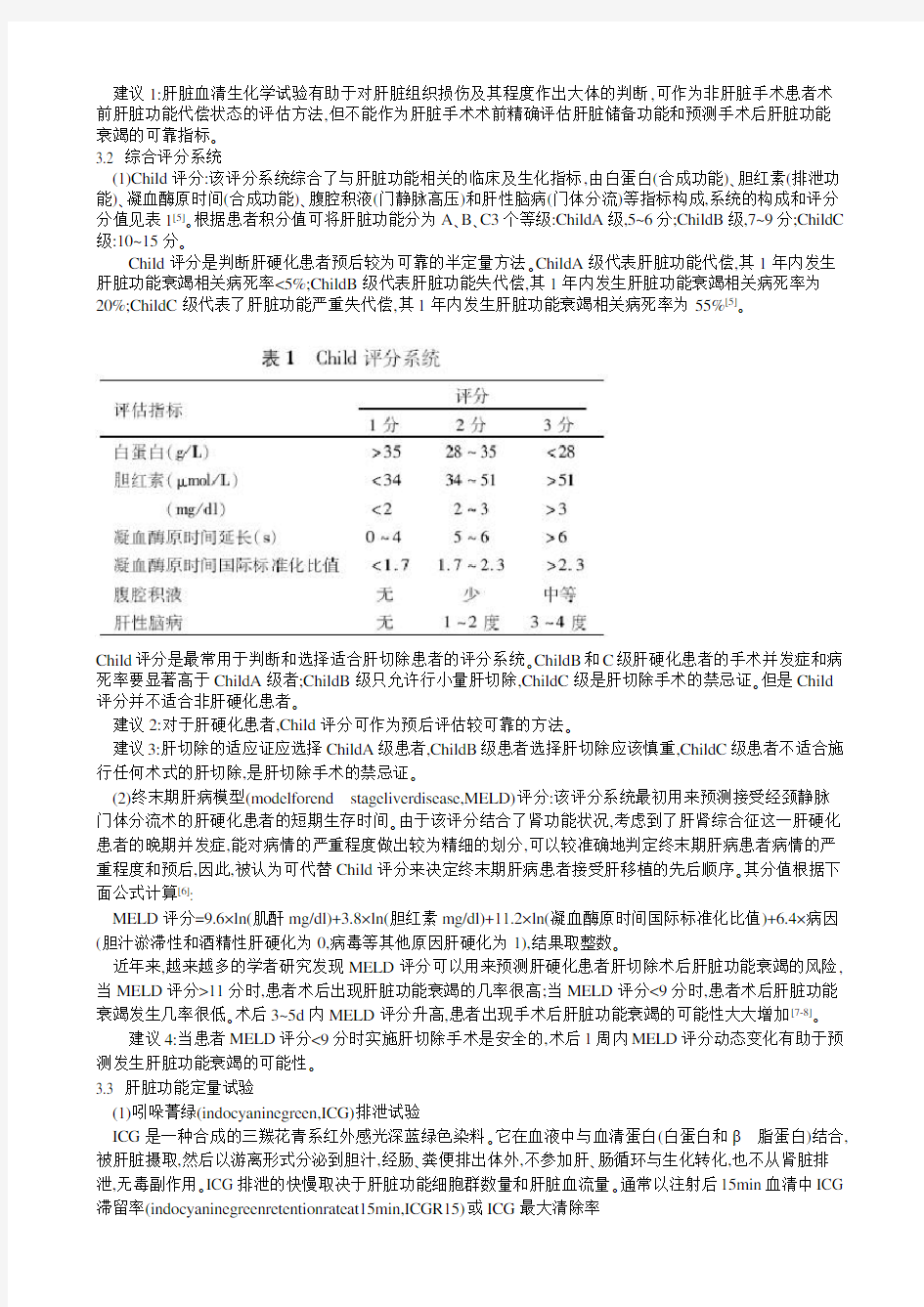
(1)Child评分:该评分系统综合了与肝脏功能相关的临床及生化指标,由白蛋白(合成功能)?胆红素(排泄功能)?凝血酶原时间(合成功能)?腹腔积液(门静脉高压)和肝性脑病(门体分流)等指标构成,系统的构成和评分分值见表1[5]?根据患者积分值可将肝脏功能分为A?B?C3个等级:ChildA级,5~6分;ChildB级,7~9分;ChildC 级:10~15分?
Child评分是判断肝硬化患者预后较为可靠的半定量方法?ChildA级代表肝脏功能代偿,其1年内发生肝脏功能衰竭相关病死率<5%;ChildB级代表肝脏功能失代偿,其1年内发生肝脏功能衰竭相关病死率为20%;ChildC级代表了肝脏功能严重失代偿,其1年内发生肝脏功能衰竭相关病死率为55%[5]?
Child评分是最常用于判断和选择适合肝切除患者的评分系统?ChildB和C级肝硬化患者的手术并发症和病死率要显著高于ChildA级者;ChildB级只允许行小量肝切除,ChildC级是肝切除手术的禁忌证?但是Child 评分并不适合非肝硬化患者?
建议2:对于肝硬化患者,Child评分可作为预后评估较可靠的方法?
建议3:肝切除的适应证应选择ChildA级患者,ChildB级患者选择肝切除应该慎重,ChildC级患者不适合施行任何术式的肝切除,是肝切除手术的禁忌证?
(2)终末期肝病模型(modelforend stageliverdisease,MELD)评分:该评分系统最初用来预测接受经颈静脉门体分流术的肝硬化患者的短期生存时间?由于该评分结合了肾功能状况,考虑到了肝肾综合征这一肝硬化患者的晚期并发症,能对病情的严重程度做出较为精细的划分,可以较准确地判定终末期肝病患者病情的严重程度和预后,因此,被认为可代替Child评分来决定终末期肝病患者接受肝移植的先后顺序?其分值根据下面公式计算[6]:
MELD评分=9.6×ln(肌酐mg/dl)+3.8×ln(胆红素mg/dl)+11.2×ln(凝血酶原时间国际标准化比值)+6.4×病因(胆汁淤滞性和酒精性肝硬化为0,病毒等其他原因肝硬化为1),结果取整数?
近年来,越来越多的学者研究发现MELD评分可以用来预测肝硬化患者肝切除术后肝脏功能衰竭的风险,当MELD评分>11分时,患者术后出现肝脏功能衰竭的几率很高;当MELD评分<9分时,患者术后肝脏功能衰竭发生几率很低?术后3~5d内MELD评分升高,患者出现手术后肝脏功能衰竭的可能性大大增加[7-8]?
建议4:当患者MELD评分<9分时实施肝切除手术是安全的,术后1周内MELD评分动态变化有助于预测发生肝脏功能衰竭的可能性?
3.3 肝脏功能定量试验
(1)吲哚菁绿(indocyaninegreen,ICG)排泄试验
ICG是一种合成的三羰花青系红外感光深蓝绿色染料?它在血液中与血清蛋白(白蛋白和β 脂蛋白)结合,被肝脏摄取,然后以游离形式分泌到胆汁,经肠?粪便排出体外,不参加肝?肠循环与生化转化,也不从肾脏排泄,无毒副作用?ICG排泄的快慢取决于肝脏功能细胞群数量和肝脏血流量?通常以注射后15min血清中ICG 滞留率(indocyaninegreenretentionrateat15min,ICGR15)或ICG最大清除率
(indocyaninegreenmaximumremovalrate,ICGRmax)作为量化评估肝脏储备功能的指标?脉动式ICG分光光度仪分析法可以替代传统的分光光度计检查方法?值得注意的是,ICG排泄速率受肝脏血流量影响较大,因而任何影响肝脏血流量的因素(如门静脉癌栓?门静脉栓塞术后以及肝脏局部血流变异等)都会对检查结果产生影响;高胆红素血症和血管扩张剂等亦有明显影响;任何原因的胆汁排泄障碍可导致ICG排泄速率延缓,此时ICG排泄试验就不能够准确反映肝脏储备功能[3]?
ICGR15对肝硬化患者肝切除的预后判断价值已经得到证实?在ChildA级患者中ICGR15>14%,则肝切除手术风险增大[9];若ICGR15>20%,则超过2个肝段的大范围肝切除的风险很大[10]?一些学者据此提出了基于ICGR15的肝切除安全限量评估系统[10]?
(2)其他一些定量检查:如动脉血酮体比?利多卡因代谢试验?氨基比林廓清实验和糖耐量试验等,由于对肝脏储备功能评估的临床价值尚未获得统一意见,且其检测方法繁琐,尚未能在临床上常规应用[3]?
建议5:ICG排泄试验是定量评估肝脏储备功能较为准确的方法,但需要注意影响ICG排泄试验准确性的因素,如肝脏血流异常(门静脉栓塞和肝内动?静脉瘘等)?胆红素水平升高?胆汁排泌障碍或者应用血管扩张剂等?
建议6:一般认为,当ChildA级患者ICGR15<_9祓_10%可以耐受4个肝段的大范围肝切除;当ICGR15为10%~19%,可耐受2~3个肝段的大范围肝切除;当ICGR15为20%~29%,只允许施行单个肝段切除;当ICGR15为30%~39%,只能施行局限性小量肝切除;当ICG R15≥40%,只能施行肿瘤
剜除术?
3.4 肝实质及脉管病变影像学评估
通过B超?CT?MRI检查显示的肝脏形态特征?肝脏脉管结构?门腔侧支循环及肝脏血流改变等影像学表现可判断肝实质病变的性质和程度,并间接推断肝脏储备功能及肝脏手术的安全性?
建议7:B超?CT?MRI等影像学检查显示重度肝硬化?脂肪肝?门腔侧支循环显著扩张?门静脉向肝血流量减低或呈逆肝血流,提示患者肝脏储备功能低下,应慎重评估其肝脏手术的安全性?
3.5 肝脏体积测量
肝脏体积的测量方法主要分为手工测算法和三维重建法两种?手工测算法是利用CT?MRI等断层影像逐层将目标肝脏区段的轮廓描出,由计算机软件自动计算得出各层面轮廓线之内的像素量,得出其横断面积,各层面肝脏面积乘以层厚再累加得出全部体积?三维重建法是利用三维重建软件,将肝脏薄层CT或MRI扫描的断层图像进行三维重建,进而基于体素的原理计算各个感兴趣肝脏区段的体积[11-13]?
通过上述两种方法均可以较准确地计算出全肝脏体积(totallivervolume,TLV)?肝脏各区段体积?肝实质体积?肿瘤体积?预计切除肝脏体积?预留肝
脏体积,进而计算出预计肝实质切除率?TLV=预留肝脏体积+预计切除肝脏体积
预计肝实质切除率=(预计切除肝脏体积-肿瘤体积)/(TLV-肿瘤体积)×100%
当肝脏实质功能均匀一致时,肝脏功能性肝细胞群的数量与肝脏体积成正比关系,因此,正确测量肝脏体积和计算肝实质切除率具有重要的临床价值?但是在肝脏不同病变状态下,肝细胞群数量减少及肝细胞功能受损可致病变肝脏功能性肝细胞群总量的降低和不同肝脏区段之间功能性肝细胞群数量的差异?因此,肝脏体积和肝实质切除率的测量尚需结合全肝及区域肝脏功能的评估才能为手术方式和肝切除范围的合理选择提供可靠的依据?
一般认为,正常肝脏可耐受肝实质切除率为75%~80%的肝切除或剩余肝脏功能性体积为肝实质体积25%~20%的肝切除[14]?
理想的方法是直接测定功能性肝脏体积,即对肝脏不同区域内功能性肝细胞群进行定量检测?功能性肝脏体积取决于具有完整解剖组织结构的功能性肝细胞群的数量?99Tc m DTPA 半乳糖人血清白蛋白(99T cm
-DTPA-galactosylhumanserum albumin,99Tc m GSA)可用于功能性肝脏体积的计算,其原理为在人与哺乳动物的肝细胞表面存在一种去唾液酸糖蛋白受体(asialoglycoproteinreceptor,ASGPR)用锝标记的去唾液酸糖蛋白类似物99Tc m GSA作为配体,通过SPECT扫描测定肝脏ASGPR量,借此可
以推断功能性肝脏体积?此项检查对于判断肝脏切除安全限量比肝脏物理体积测量更有意义,可用于全肝及分区肝脏功能性体积的测算,而且该检查不受血浆胆红素水平的影响?99Tc m GSA检查在欧美处于临床研究阶段,在日本已作为ICG排泄试验的补充方法,在临床上用于肝切除前预留肝脏功能储备状态的评估[3,11,15]?
建议8:基于CT?MRI图像的肝脏体积测量,能较为准确地反映肝脏的实际体积?
建议9:肝脏体积及肝实质切除率的精确测算结合肝脏储备功能的量化评估对于合理选择手术方式和确定肝脏切除安全限量具有重要价值?
4 肝脏储备功能的综合评定与肝脏切除安全限量的个体化评估
虽然用于评估肝脏储备功能的方法很多,但很难依据单一方法进行准确判断?目前倾向于同时应用多种方法进行综合评定以提高对肝脏储备功能评估的准确性?在综合评定中常采用的方法包括ICGR15?Child评分?肝实质及脉管病变影像学评估?肝脏体积测量?
将肝脏储备功能的评估与肝脏体积的测算相结合,可建立肝脏切除安全限量的评估系统,这是临床上针对具体患者进行肝切除量个体化手术决策和规划的前提?迄今,苏黎世大学和东京大学依据肝脏功能分级评定推断肝脏切除安全限量的决策体系具有一定的参考价值?
苏黎世大学综合肝实质病理状态?Child评分?门静脉高压症?ICGR15等参数推断患者的肝脏储备功能状况及相应的肝脏切除安全限量?肝脏切除安全限量是以预留肝脏体积所占患者自身肝脏体积比值来设定的(图1,2)[14]?在苏黎世大学的标准中认定,对于肝实质正常的患者来说,剩余肝脏占自身全部肝实质体积30%的肝切除量是安全的;对于肝脏功能代偿良好?不伴门静脉高压症?ChildA级的肝硬化患者,剩余肝脏体积不小于全部肝实质体积50%的肝切除量也是安全的?但也有研究结果表明,正常肝脏和肝脏功能代偿良好的硬化肝脏,肝脏切除安全限量可分别拓展至剩余肝脏体积为自身全部肝实质体积的20%或40%?由于在不同肝脏病变状态下,患者TLV和不同区段肝脏体积差异很大,因此,以自身病变肝脏体积的分值来设定充足安全预留肝脏体积是不准确的?对于ChildA级的肝硬化患者,其肝脏储备功能差异甚大,50%肝切除对于其中肝脏储备功能较差者显然是危险的?
图1 苏黎世大学正常肝脏切除安全限量的评估标准
图2 苏黎世大学肝硬化肝脏切除安全限量的评估标准
日本东京大学主要根据腹腔积液?胆红素水平及ICGR153个参数,确立了肝脏储备功能的分级标准,并基于不同层级肝脏储备功能状态,推测其可耐受的肝段切除数量(图3)[6,16]?但对于单纯以胆红素水平?腹腔积液替代Child评分来评定肝脏储备功能的可靠性尚存争议;且不同肝段的体积和功能在生理和病理状态下均存在显著变异,以肝切除术式和可切除肝段数量来表征肝脏切除安全限量是不准确的?例如,对于肝右叶萎缩而肝左叶增大?肝脏功能代偿良好的肝硬化患者行肝左三区甚至左半肝切除可能是危险的?
图3 东京大学肝脏切除安全限量的评估标准
个体特异性的必需功能性肝脏体积(essentialfunctional liver volume,EFLV)与标准肝脏体积(standardliver volume,SLV)的比值可能是表征个体化肝脏切除安全限量较可靠的方法?
SLV指在生理状态下每个成人相对稳定的肝脏体积,其大小取决于人体的体表面积(bodysurfacearea,BSA),是正常个体在健康状态下具有充分功能
储备和代偿潜能的理想肝脏体积?目前成人SLV多采用日本东京大学Urata等[17]建立的公式来估算?
SLV(ml)=706.2×BSA(m2)+2.4?BSA采用DuBois公式计算[18-19]?BSA(m2)=体质量(kg)0.425 ×身高
(cm)0.725×0.007184?
EFLV是指个体维持肝脏功能充分代偿所需要的最小功能性肝脏体积?由于不同患者功能性肝细胞群的数量以及肝细胞的功能状态不同,且同一个体在不同生理和病理状态下的生理负荷存在差异,不同个体所需要的功能性肝脏体积差异很大?EFLV主要取决于每一个体SLV以及肝脏储备功能状态?
EFLV=α·SLV
对于特定个体,SLV是相对恒定的,以这一因人而异的恒定量值来设定EFLV是合理的?α值是肝脏储备功能状态的函数,随着肝脏储备功能的减低,α值相应增大?目前尚无精确判定肝脏储备功能正常和不同程度减低时的对应α值?根据已有经验推断,当肝实质和肝脏储备功能正常时,α≈20%~25%;若肝实质有病变且伴肝脏储备功能降低,则
α>20%~25%,其实际分值随肝脏储备功能的减低而增大?
对于肝切除患者,决定患者肝脏功能能否代偿的是剩余肝脏的功能性体积,而非实际切除的肝脏体积的大小,因此,剩余功能性肝脏体积(remanantfunctionallivervolume,RFLV)不小于EFLV的肝切除是安全的?即安全肝切除的必要条件是RFLV≥EFLV=α·SLV?
肝脏切除安全限量(safetylimitofliverresec tion,SLLR)是指特定个体仅保留EFLV的最大允许肝脏切除量?
SLLR=TLV-EFLV=TLV-α·SLV
采用肝实质病变?Child评分?ICGR15作为肝脏储备功能量化评估标准,以α·SLV来设定肝脏切除安全限量,可构建一个较合理的肝脏切除安全限量的个体化评估决策系统(图4)?
R:剩余功能性肝脏体积;S:估算的标准肝脏体积
图4 肝脏切除安全限量的个体化评估决策系统
建议10:将ICG R15水平?Child评分?肝实质及脉管病变的影像学评估与肝脏体积测量相结合,建立肝脏切除安全限量的评估决策系统,对肝病患者肝切除方式及范围的个体化准确选择有重要意义?
建议11:EFLV与SLV的比值是设定患者肝脏切除安全限量的合理指标?对于ChildA级肝硬化患者,若ICGR15<10%,预留肝脏功能性体积须不小于SLV的40%;若ICGR15为10%~20%,预留肝脏功能性体积须不小于SLV的60%;若ICGR15为21%~30%,预留肝脏功能性体积须不小于SLV的80%?若ICGR15为
31%~40%,只能行限量肝切除;若ICGR15>40%或ChildB级,只能行肿瘤剜除术?
肝脏储备功能的评估是安全开展肝切除手术的基础与技术保证,是肝脏外科的核心问题之一?由于肝脏功能复杂,影响因素很多,肝脏储备功能的精确评估还有待不断完善?肝切除术后肝脏功能衰竭的发生除了与肝脏本身的储备功能相关,也与手术团队的技术以及围手术期管理水平有密切的关系?
参考文献
[1] 董家鸿.肝细胞癌治疗理念与策略的转变.中华消化外科杂志,2009,8(2):85-87.
[2] 董家鸿,黄志强.精准肝切除—21世纪肝脏外科新理念.中华外科杂志,2009,49(21):1601-1605.
[3] SchneiderPD.Preoperativeassessmentofliverfunction.SurgClinNorthAm,2004,84(2):355-373.
[4] 姚光弼.肝脏的生化检查//姚光弼.临床肝脏病学.上海:上海科技出版社,2004:129-151.
[5]PughRN,Murray—LyonIM,DawsonJL,etal.Transectionoftheoesophagusforbleedingoesophagealvarices.BrJSur g,1973,60(8):646-649.
[6]KamathPS,WiesnerRH,MalinchocM,etal.Amodeltopredictsurvivalinpatientswithend-stageliverdisease.Hepatolo gy,2001,33(2):464-470.
[7]CucchettiA,ErcolaniG,VivarelliM,etal.Impactofmodelforend-stageliverdisease(MELD)scoreonprognosisafterhe patectomyforhepatocellularcarcinomaoncirrhosis.LiverTranspl,2006,12(6):966-97.
[8]CesconM,CucchettiA,GraziGL,etal.Indicationoftheextentofhepatectomyforhepatocellularcarcinomaoncirrhosis byasimplealgorithmbasedonpreoperativevariables.ArchSurg,2009,144(1):57-63.
[9]PoonRT,FanST.Assessmentofhepaticreserveforindicationofhepaticresection:howIdoit.JHepatobiliaryPancreatSu rg,2005,12(1):31-37.
[10]ImamuraH,SanoK,SugawaraY,etal.Assessmentofhepaticreserveforindicationofhepaticresection:decisiontreeinc orporatingindocyaninegreentest.JHepatobiliaryPancreatSurg,2005,12(1):16-22.
[11]vandenBroekMA,OldeDaminkSW,DejongCH,etal.Liverfailureafterpartialhepaticresection:definition,pathophy siology,riskfactorsandtreatment.LiverInt,2008,28(6):767-780.
[12]GarceaG,OngSL,MaddernGJ.Predictingliverfailurefollowingmajorhepatectomy.DigLiverDis,2009,41(11):798-806.
[13]NakayamaY,LiQ,KatsuragawaS,etal.Automatedhepaticvolumetryforlivingrelatedlivertransplantationatmultise ctionCT.Radiology,2006,240(3):743-748.
[14]ClavienPA,PetrowskyH,DeOliveiraML,etal.Strategiesforsaferliversurgeryandpartiallivertransplantation.NEngl JMed,2007,356(15):1545-1559.
[15]deGraafW,BenninkRJ,V etelainenR,etal.Nuclearimagingtechniquesfortheassessmentofhepaticfunctioninliversu rgeryandtransplantation.JNuclMed,2010,51(5):742-752.
[16]MakuuchiM,KokudoN.Clinicalpracticeguidelinesforhepatocellularcarcinoma:thefirstevidencebasedguidelinesf romJapan.WorldJGastroenterol,2006,12(5):828-829.
[17]UrataK,KawasakiS,MatsunamiH,etal.Calculationofchildandadultstandardlivervolumeforlivertransplantation.H epatology,1995,21(5):1317-1321.
[18]DuBoisD,DuBoisEF.Aformulatoestimatetheapproximatesurfaceareaifheightandweightbeknown.Nutrition,198 9,5(5):303-311.
[19]VautheyJN,AbdallaEK,DohertyDA,etal.BodysurfaceareaandbodyweightpredicttotallivervolumeinWesternadul ts.LiverTransp,2002,8(3):233-240.
---------------------------------------------------------------范文最新推荐------------------------------------------------------ 肝脏储备功能护理 1临床资料1.1一般资料选择2006年7月~2007年12月我院收治的511例肝脏疾病的患者,年龄16~75岁。其中,肝癌患者387例(合并肝硬化93例),肝内外胆管结石97例,肝血管瘤27例。ICG排泄试验检测显示:493例顺利测出结果,17例二次检测才有结果,1例未出结果。1.2检测方法1.2.1检测准备正确连接DDG分析系统,打开分析仪和电脑,打开打印机,启动数据管理软件,正确安装鼻探头并予固定,正确输入患者资料(身高、体重、血红蛋白、ICG量、住院号码)。1.2.2检测嘱患者平卧,平静呼吸,身体放松,勿咳嗽,护士消毒留针后,将抽有ICG针筒妥善连接,并抽回血,在机器出现提示音后,快速(10s)推入ICG溶液,推液完毕后将准备好的10ml 生理盐水推入,以确保留置针管道内的ICG完全推入静脉,然后将留置针封管,观察DDG分析仪出现的ICG浓度趋势图,过6~7min后根据提示先后按下Stop键和Print键,取下鼻探头,数据管理软件接受信息,填写患者相关信息后将结果打印出来。2护理要点2.1心理护理向患者解释ICG排泄试验检测的重要性、检测的大致过程和需配合注意事项,以消除其紧张、不安的情绪。2.2患者准备检测血液血红蛋白;测量当日身高、体重;清理鼻腔,因检测采用的是鼻探头红外线感应装置,如鼻腔内有异物会影响表面的接触,从而导致检测失败;检测当日晨空腹、静卧;手臂预留留置针,因检测时要求推注药液的速度要快,留针部位最好选择较粗的血管,以确保药液通畅和避 1 / 3
关于三维重建技术在精准肝切除治疗原发性肝癌中的临床应用分析 目的本文主要是探讨和分析三维重建技术运用在原发性肝癌患者精准肝切除治疗过程中的方法和效果。方法选择来我院接受治疗的50例原发性肝癌患者临床资料作为研究对象,并通过肝脏三维重建系统对其CT图像数据进行相应的三维重建处理,定位并分割其病灶,对患者肝内管道、病灶相关信息加以评估,完成相应的虚拟手术设计工作,制定相应的手术治疗方案,指导医护人员更好地完成临床手术治疗。通过三维重建系统、常规性的二维法来对患者肝脏总体积、剩余肝脏面积、病灶体积、欲切除肝脏体系进行测量。把传统的二维测量和三维重建系统测量得到的数据结果进行分析和比较。结果50例患者经过三维重建模型显示效果良好,其中病灶处在患者右半肝脏的有29例、左半肝23例;其中测量患者肝脏总体积平均为1800cm3,患者病灶总体积平均为500cm3,期初的肝脏体系平均为600cm3。选择三维方法对欲切除肝脏体系进行计算时,得到的体积越大;术后切除的肝脏质量就越重。所有患者实际选择的手术切除方式和术前虚拟进行的手术结果相同。结论利用肝脏三维重建软件对原发性肝癌患者术前进行评估能够产生显著的价值,而且能够帮助医护人员更加科学有效地选择手术治疗方案。 标签:三维重建技术;精确性肝切除;原发性肝癌;临床运用 原发性肝癌表示患者肝内胆管上皮细胞、肝细胞出现恶性肿瘤现象,也是目前临床医学中较为常见的一种恶性肿瘤。肝癌患者外科治疗理念开始出现变化,并以尽可能保护患者脏器、实现最好的治疗效果为治疗目的,进一步诱发常规的经验外科模式转变成现代化的精准外科模式[1]。在进行肝脏切除时,这种精准现代化的外科治疗模式也被看成精准肝切除。为了进一步探讨和分析三维重建技术运用在原发性肝癌患者精准肝切除治疗过程中的方法和效果,本研究做了相关探讨,现报道如下。 1 资料与方法 1.1一般资料本文选择2014年11月~2015年11月来我院接受治疗的50例原发性肝癌患者临床资料作为研究对象,男性和女性分别有34例和16例,年龄为35~72岁,平均为56.5岁,所有患者在手术之前都接受了实验室检查、影像学检查、术后病理检查,并得到确诊。患者接受根治性精准肝癌切除手术治疗,其中肝部分切除患者有31例、扩大半肝切除有11例、标准半肝切除有17例。 1.2方法对50例原发性肝癌患者入院進行的最近一次CT检查数据进行收集,并获取手术之后切除标本测量相关指标。其中CT断层图像选择64排螺旋CT机进行采集,控制的层厚在1.5~5mm之间,控制扫描范围从膈顶到肝下部,分为动脉期、平扫期以及门脉期。对患者CTA数据进行收集,并将其以医学数字化图像的格式进行储存,利用PACS系统对数据进行传输、通过刻盘来对数据进行保留[2]。手术之后对所有切除的标本加以称重处理,所有称重结果和测量结果要能够建立起相应的数据库。
三维重建技术在精准肝切除中的临床应用 发表时间:2018-09-07T13:45:13.363Z 来源:《医药前沿》2018年9月第25期作者:季渝军 [导读] 原发性肝癌患者开展三维重建技术能发挥极大的应用价值,能为合理选择肝切除术提供良好的依据。 (陆军军医大学<第三军医大学> 重庆 400038) 【摘要】目的:对比CT图像二维、三维建模在原发性肝癌中应用的效果。方法:随机抽取我院2016年1月—2017年12月收治的44例原发性肝癌患者作为研究对象,分成对照组与观察组,对照组给予传统二维法,观察组对CT图像进行三维重建,对比其应用效果。结果:观察组切除部分体积明显大于对照组(P<0.05);观察组术后并发症发生率、术后复发率明显低于对照组(P<0.05)。结论:原发性肝癌患者开展三维重建技术能发挥极大的应用价值,能为合理选择肝切除术提供良好的依据。 【关键词】原发性肝癌;肝脏CT图像;三维建模;计算方法;应用价值 【中图分类号】R657.3 【文献标识码】A 【文章编号】2095-1752(2018)25-0211-01 恶性肿瘤疾病中原发性肝癌是较为常见疾病,近年来,随着我国肝癌外科治疗理念在逐渐变化,其临床治疗原则以加快康复速度、保护脏器功能、减少创伤等为主,开始往现代精准外科模式改变[3]。肝脏外科开始以精准肝切除作为基础开展肝脏外科手术,并重视普及肝切除术的内涵以及概念,确保精准肝切除概念往标准化、具体化方面发展。我远采用基于C平均模糊聚类的方法对CT图像进行三维建模取得了良好效果,现报道如下。 1.资料与方法 1.1 一般资料 本组研究对象的临床数据均来自2016年1月—2017年12月期间到我院接受治疗的原发性肝癌患者44例,所有患者均采用根治性精准肝癌切除手术进行治疗,通过病理检查、实验室检查以及相关影像学确诊为原发性肝癌疾病;男患者30例,女患者14例,年龄为30~60岁,平均年龄为(48.32±3.85)岁;其中8例扩大半肝切除术,10例标准半肝切除术,26例肝部分切除术;将手术切除肝脏无法良好代偿、病灶体积过大、肝功能受损严重的患者排除出本组研究之外。参照医学伦理学原则,获得同意且签署知情同意书后,命名为观察组与对照组,每组22例。观察组、对照组的一般资料对比差异不明显(P>0.05),有临床比较性。 1.2 方法 1.2.1资料收集分别调查本组44例研究对象近期到我院开展CT检查的相关数值以及完成手术后测量标本的数值。选择美国GE公司的64排螺旋CT机采集CT断层图像,层厚设置为1.25~5mm,从膈顶到肝下缘进行扫描,并以门脉期、动脉期、平扫期划分,对患者的CT数据进行收集后,采用医学数字化图像(DICOM)的格式存储。采用PACS系统保留数据或者传输数据,完成手术后称量切除标本的数据,将称重结果以及测量数据制作成数据库形式。 1.2.2肝脏三维重建首先将CT生成的DICOM文件导出,采用matlab软件对该图像基于C平均模糊聚类方法,使图像降噪,对图片灰度进行测定,产生CT图像边界,对图像进行分割,其次采用面、体、快速点进行绘制,通过C平均模糊聚类方法生成STL文件。其中体绘制主要是研究光纤投射算法,并实现了肝脏模型的体绘制,是3D模型能够进行旋转、上下移动等、快速点绘制主要应用于快速建模。对照组采用二维断层影像和患者的身高、体质量等基本信息计算肝脏体积和评估残肝体积。观察组主要采用三维立体影像,通过算法来计算体积。 1.3 统计学分析 采用SPSS13.0统计学软件对两组患者的数据作分析统计,以P<0.05,表示组间数据对比差异显著,有统计学意义。 2.结果 2.1 对比两组体积测量 与对照组相比,观察组切除部分体积明显较大(P<0.05);观察组、对照组剩余肝脏体积/全肝体积对比无明显差异(P>0.05),详见表1。 3.讨论 肝胆外科临床中开始全面应用精准外科理念,可加快患者康复速度[2]。近年来,随着我国影像学技术发展脚步逐渐加快,很多学者开始采用三维建模的方式,通过分析肝脏数据开展个体化量化分析,使虚拟手术得以实现。据分析本组研究结果得知,观察组、对照组切除部分体积、并发症、复发率等指标具有明显差别(P<0.05);而两组患者的剩余肝脏体积/全肝体积无明显差别(P>0.05)。由此可知,CT图像三维重建系统在个体化肝脏数据分析方面的可靠性、准确性较高,通过肝脏三维重建系统能够在较快的时间内完成肿瘤长度、管径、距离、体积等数据的测量,在较快的时间内执行虚拟手术切除计划以及解剖功能分段计划,具有易学易用、快捷性高、操作简单等基
手术室标准化护理配合在精准肝癌切除术中的应用 摘要:目的研究探讨在行精准肝癌切除术患者中采取手术标准化护理配合的价值。方法对2018年2月到2020年2月本院行精准肝癌切除术治疗的患者86例,按照入院顺序分组为观察组43例以及对照组43例。对照组接受常规护理,观察 组行手术室标准化护理配合。对比两组手术用时以及护理满意度。结果观察组手 术用时显著短于对照组(P<0.05)。观察组中患者护理满意度显著高于对照组 (P<0.05)。结论在精准肝癌切除术患者中开展手术室标准化护理配合有利于缩 短手术用,改善患者满意度。 关键词:手术室;标准化护理配合;精准肝癌切除术;手术用时 在临床上对肝癌进行治疗时,常常采用切除手术的方法,该治疗方法属于微 创范畴,在治疗的过程中需要切除最小的肝脏组织,最终切除肿瘤,在切除的过 程中需要尽可能地保留肝组织,有利于患者治疗后的恢复[1]。在对患者进行治疗 的过程中,对患者进行标准护理能够有效提高护理质量和水平,提高患者对医护 人员的满意程度。本文通过调查研究,分析手术室标准化护理在治疗过程中的应 用效果,并总结其意义,现将主要内容汇报如下。 1资料和方法 1.1一般资料 对2018年2月到2020年2月本院行精准肝癌切除术治疗的患者86例,按 照入院顺序分组为观察组43例以及对照组43例。对照组男女例数27例、16例,年龄49岁至70岁,平均年龄为(58.14±2.06)岁;观察组男女例数28例、15例,年龄48岁至70岁,平均年龄为(59.22±2.17)岁。组间患者的常规资料相近, 可以对比(P>0.05)。 1.2方法 对照组:对患者采用传统的护理方法,主要内容包括准备手术所需要的器械,更好地与手术医师进行配合。 观察组:对患者采取手术室标准化护理模式,在对患者进行治疗的过程中, 需要邀请资历较深的教授、医师、护理人员进行治疗工作,同时需要制定护理的 标准步骤,由专业人员对护理人员进行培训,提高护理人员的专业水平和职业素养。为了进一步提高护理的标准化水平,需要做好以下内容:首先,保障工作流 程的标准化。专业人员应该对参与手术治疗的工作人员进行培训,使其能够更加 熟悉不同器械的使用方法和顺序,提高自身的规范意识,要求手术医师与护理人 员应该加强沟通,对于出现的问题,应该定期集中讨论,不断优化手术工作流程 和标准[2]。为了保障流程的标准化,要求护理人员必须根据相关规定加强练习, 保障在治疗的过程中能够顺利配合医师进行手术工作,自身应该明确术前、术中、术后三个阶段的工作重点。其次,不断规范手术室。要求手术室内环境卫生,保 障处于无菌状态,严格按照相关标准对手术室进行消毒,营造良好的治疗氛围。 在对患者进行治疗的过程中,护理人员必须提前对所用器械和物品进行清点,不 得在清点之前交接器械。护理人员必须根据手术的内容不断对所用器械进行清洁,并对器械进行科学的摆放,不断规范摆放位置,节约手术治疗的时间[3]。最后, 对护理人员进行培训。负责人员需要定期对护理人员进行相关知识的培训,加强 与护理人员的沟通,了解在护理过程中存在的问题,并制定相应的解决方案,不 断规范护理人员的工作。同时可以将手术室的标准流程,制定成画册等不同方式 进行宣传教育,提高护理人员的工作主动性,使每位护理人员都能够树立标准化
肝切除术 二、肝储备功能的评估 肝切除术后一个严重的并发症是肝功能衰竭(简称肝衰)。它一旦发生往往导致病人死亡,是肝切除手术死亡的主要原因之一。肝衰的发生常常是由于对不能耐受肝切除的肝脏施行了肝切除或由于切肝量过大、超过了肝脏的代偿能力所致。正常肝脏具有强大的储备功能,可以耐受75%的切肝量。但在我国乃至亚洲,肝切除的主要适应证是肝细胞性肝癌(简称肝癌),而80%左右的肝癌伴有不同程度的肝硬化。发生硬化的肝脏还有多少储备功能、还能耐受多大范围的肝切除?这是在施行每例肝癌肝切除术前所要回答的问题。事实上,人们一直在研究精确的肝储备功能检测方法,希望籍此在术前能够确定安全的切肝量。目前临床上,在肝切除前除了作常规的肝功能试验外,越来越多采用新的更加敏感的肝功能指标来评估肝储备功能,以指导肝切除手术适应证和切肝量的掌握。 (一)常规肝功能检查 常规肝功能检查项目包括胆红素、白蛋白、球蛋白、白/球蛋白比、丙氨酸转氨酶(ALT)和门冬氨酸转氨酶(AST)、蛋白电泳、凝血酶原时间等。 1.胆红素:肝脏处理胆红素的储备能力较大,因此,一旦血清胆红素水平明显升高,则表明肝功能受损较重。一般认为胆红素>50μmol /L,不宜行任何类型肝切除;胆红素40~50μmol/L,经保肝治疗后降至30μmol/L以下,而其他肝功能指标基本正常,可行肝楔形切除、单肝段切除;胆红素20~30μmol/L,可行双肝段切除。需要指出的是,不可将肝癌伴有黄疽均判为肝功能失代偿而放弃手术治疗,部分病例是由于肿瘤压迫、胆管癌栓等阻塞胆管而引起的黄疽,临床上须注意鉴别,此时胆红素升高以结合型为主,多伴有肝内胆管扩张、碱性磷酸酶(ALP)升高,这类病人需要手术治疗,也往往能耐受手术。 2.白蛋白和球蛋白:血清白蛋白>40g/L常表明肝储备功能良好,肝切除不受限制;白蛋白在正常值的低限(35g/L),则表示肝储备功能有限,肝切除范围应限制在2个肝段以内;白蛋白在31~34g/L之间,经保肝、补充白蛋白治疗后能上升至35g/L以上,可行单肝段或肝楔形切除;白蛋白≤30g/L,则表明肝功能已失代偿,不宜作任何类型肝切除。在考察血清白蛋白水平高低时应结合球蛋白一并考虑,后者是反映肝硬化是否存在及严重程度的指标。血清球蛋白<25g/L,白/球蛋白比值>1.5,一般表示肝脏无硬化,肝切除不受限制;球蛋白>30g/L,白/球蛋白比值<1.5,表示可能有肝硬化存在,肝切除应限制在半肝以下;球蛋白>35g/L,一般表示有明显肝硬化存在,若白/球蛋白比值>1.0,则可行单肝段或肝楔形切除,若白/球蛋白比值<1.0,则应放弃肝切除。 3.ALT 和AST:ALT 和AST 不是反映肝储备功能的指标,但二者升高常表示肝硬化处
第四章常用检查和治疗护理常规 第一节肝功能储备检查 一、概述 肝功能储备系指肝脏耐受手术、创伤以及打击的额外潜能,即除了机体所需的代谢、蛋白质合成或降解、解毒功能以外的创伤修复能力和肝脏再生能力。判断肝储备功能的主要目的是在术前能够了解患者是否可耐受肝切除以及可耐受切除的范围(肿瘤局部切除或解剖性肝切除),进而降低术后肝功能衰竭的机率,保障手术的安全。 吲哚菁绿(indocyanine green,ICG)是一种色素,静脉注入后选择性地被肝细胞摄取,再逐步排入胆汁中,不经肾脏排泄,不参与肠肝循环,也不能回流到肝淋巴系统,是反映肝功能储备的理想指标。ICG清除实验是目前最能反映有功能肝细胞量的评估方法,与单纯常规生化检验比较具有明显的优势。当ICG滞留率>10%时,大多说明肝功能受损,此时常规生化检验正常亦不能排除肝功能已经受到损伤。有学者认为,ICG-R15小于14%时,行三段以上的肝脏切除是安全的;而ICG-R15于14%至20%之间,肝脏切除要依据剩余肝脏体积和肝硬化程度小心谨慎制定手术方案。 二、适应症 需做手术的肝脏病患者:肝硬化,肝纤维化,韧性肝炎,职业和药物中毒性肝病等。了解肝脏的损害程度及其储备功能。 三、禁忌症 对ICG有过敏史及有碘过敏的患者。 四、检查前准备 1.病人告知:向患者解释ICG清除试验的重要性、检测的大致过程需配合注意事项,以消除其紧张、不安的情绪,积极配合、确保检测成功。 2.病人准备:测量实时体重、身高,近1周的Hb数值,计算好所用HCG量。 3.物品准备:10ml无菌注射器2个,三通1个,头皮针1个,止血带1根,消毒碘棉签1包,无菌棉签1包,正确连接DDG分析仪系统,打开分析仪的电脑,打开打印机,启动数据管理软件。用灭菌注射用水,将ICG稀释成5mg/ml,并按0.5mg/kg的比例配置ICG溶液。
原发性肝癌通过精准肝切除术治疗的效果分析 肝癌属于临床常见恶性肿瘤,一般手术治疗是首选方式。而传统肝切除术虽然肿瘤去除率高,但创伤大,术后并发症多,恢复慢,无法准确设计手术切除术范围。由此在相关问题基础上,精准肝切除术应运而生,其可以更为精确的确定肝切除术范围,减少手术创伤,减少术后并发症,提升恢复质量,在临床逐步运用开来。 1 资料与方法 1.1 一般资料 研究我院2021年5月至2021年12月期间收治的原发性肝癌患者80例,分为对照组和观察组各40例,其中对照组男性29例,女性11例;年龄范围为32岁至65岁,平均年龄为(45.2±4.1)岁;观察组男性32例,女性8例;年龄范围为29岁至68岁,平均年龄为(46.7±3.8)岁;所有患者均属于单发性肿瘤,肝功能Child-Pugh 分级中属于A或B级,肿瘤没有侵入到第一、第二肝门与下腔静脉中,门静脉主支也不存在癌栓,没有广泛性转移;患者没有脏器病变。两组患者在基本资料上没有显著性差异,具备可比性。 1.2 方法 对照组组采用传统肝切除术,取仰卧位,采用全麻复合硬膜外麻,行气管插管,将膈肌切开后做腹腔探查,确定病灶位置与数量,将肝周韧带快速离断后游离出肝脏组织,并对切除做对应标记,运用Prinkle法进行入肝血流阻断,运用钳夹法断肝,肝端面运用对拢缝合,创面处进行腹腔引流,切口采用无损伤缝合。观察组运用精准肝切除术,术前运用CT血管造影与三维重建技术对肝切除相关静脉组织做影像重建,确定肝脏体积与肝平面,测算肿瘤之外剩余肝脏体积。术中采用仰卧位,采用气管插管全麻,在右侧肋缘下进行反L状切口,同时运用悬吊拉钩稳固。运用PMOD做第一肝门解剖,将左右肝动脉与门静脉分支有效分离出。术中采用超声技术确定术前方案,运用
精准肝切除与不规则肝切除 长治市人民医院普通外科霍凌波 外科学在其发展过程中,历经了18世纪的古代外科、19世纪的传统外科以及20世纪的现代外科,而随着新的理念、技术手段以及设备的发展,全新的21世纪外科将要向何方发展成为摆在每一位外科医生面前的首要问题。 旨在追求最小创伤侵袭、最大脏器保护、最佳治疗效果的21世纪外科向我们提出了更高的要求,基于对医疗理念和技术的更高追求“精准外科时代”应运而生。“精准外科”一词由解放军总医院(301)肝胆外科医院院长董家鸿教授提出,其产生的背景是新世纪人文医学、微创外科、循证医学和个体化医学的迅猛发展。其含义是在信息技术支持下整合应用一系列现代科技,以对个体病例的病情做出定位、定时、定量的精确评估和循证决策为基础,高精度、高效度地实施以个体化、定量化、可视化、微创化为特征的手术及围手术期处理,旨在以最小的创伤侵袭、最大脏器保护获得最佳的外科治疗效果。在这一全新的理念下催生出精准肝切除术这一手术理念。 作为肝脏肿瘤、肝内胆管结石、肝包虫病、肝脓肿、Caroli 病等肝脏疾病最有效治疗方式的肝切除术历经了不规则肝切除术、规则肝切除术以及精准肝切除术几个时期,其逐渐发展的基础是对肝脏解剖结构、生理功能和病理特征的深度认识。精准肝切除是在以肝叶、肝段为基础的规则肝切除的基础上发展而来的。肝脏疾病中肝癌呈沿载瘤肝段门静脉分支内播散而肝内胆管结石具有沿着病变胆管树区段性分布的特性,这些特性决定了解剖性肝切除才是彻底去除病灶的理想方式。涵盖以手术为核心内容的精准外科治疗全过程包括精确的术前评估、精密的手术规划、精准的手术操作、精良的术后管理,兼容科学原则和人文原则,使肝切除术告别了“浴血奋战”、盲目大块结扎和一味追求手术速度的粗矿手术时代,实现了肝切除手术的安全、有效、微创的目标,这些全新的思想也正是精准肝切除的核心。 精准肝切除采用螺旋CT、核磁共振、3D数字影像技术等现代影像学技术、ICG试验为代表的肝储备功能测试、手术预切除模拟等手段使术前评估实现准确可靠。术中超声技术、肝血流阻断技术、精确的肝段染色技术、CUSA、LigaSure、超声刀等断肝技术、胆管胰管血管重建技术、机器人辅助的腹腔镜技术等为术中精准的肝段、亚肝段切除提供了坚实的技术支持。而围手术期的临床路径管理又为患者平稳渡过手术危险期、良好康复提供有效地保驾护航,同时还兼顾了医药经济学的要求。 肝脏具有独特的再生能力,部分肝脏手术切除后剩余肝脏会在术后半年到一年的时间再生接近原肝脏的大小,并具有相应的功能。然而部分肝脏疾病患者多继发于乙型肝炎、肝硬化的基础上,严重肝硬化患者的肝脏再生能力下降的同时肝功能同样受损,因此大面积切除肝脏变为不安全,这时不规则肝切除就成为适宜的手术方式。不规则肝切除是指距离肿瘤边缘1cm的不规则的小范围肝切除,此术式适应于肝硬化基础上合并小肝癌、小的转移癌、多中心的肝癌和多发转移癌,该术式在临床上应用并不少见,它是对以肝叶、肝段、亚肝段切除的精准肝切除术的有益补充。 两种肝切除术式有着各自的特点及适用范围,但无论选用何种术式都应在充分术前评估、保证手术安全的基础上做到完整切除病灶的同时使治疗达到最佳的效果。随着人们的逐渐认识,精准肝切除及精准外科的理念必将带动整个外科的
肝胆胰外科术后加速康复专家共识(2015 版) 前言加速康复外科(enhanced recovery after surgery,ERAS)是基于循证医学依据的一系列围手术期优化处理措施,以达到快速康复为目的。ERAS 通过减轻术后应激反应、合理管理疼痛、早期恢复饮食和早期活动等措施来减少术后并发症,缩短术后住院时间,减少医疗费用。自1997 年丹麦外科医师Kehlet 提出ERAS 以来,ERAS 已在骨科、乳腺外科、心胸外科、胃肠外科、妇产科等多个外科领域开展。目前,国际上已相继发布了择期结直肠手术、直肠和(或)盆腔手术、胰十二指肠手术和胃切除手术的ERAS 指南或专家共识。肝胆胰手术较复杂、创伤大,术后并发症发生率高,近年提倡并应用的精准、微创、损伤控制的现代外科理念为ERAS 的施行奠定了基础。目前,多家医疗中心开始在肝胆胰手术患者中施行ERAS,并取得了一定成效。但如今,国内外均无一致的针对肝胆胰手术的ERAS 方案来指导临床实践。因此,《中华消化外科杂志》编辑委员会和中国研究型医院学会肝胆胰外科专业委员会组织业内专家,启动了《肝胆胰外科术后加速康复专家共识(2015 版)》(以下简称本共识)讨论会,总结国内外研究进展及专家经验,按照循征医学原则通过深入论证,最终制订本共识,旨在为实现我国肝胆胰外科手术ERAS 的规范化、标准化提供参
考意见。本共识依据的循证医学证据质量等级和推荐强度等级按照GRADE 系统(表1)。表1 为证据等级及推荐强 度术前项目1. 术前宣传教育术前通过面对面交流、书面(展板、宣传册)或多媒体方式,告知患者围术期各项相关事宜,包括:(1)告知患者麻醉和手术过程,减轻患者对麻醉和手术的恐惧和焦虑。(2)告知患者ERAS 方案的目的和主要项目,鼓励患者术后早期进食、术后早期活动、宣传疼痛控制及呼吸理疗等相关知识,增加方案施行的依从性。(3)告知患者预设的出院标准。(4)告知患者随访时间安排和再入院途径。推荐意见1:患者应接受常规的术前宣传教育和咨询解答,且宣传教育应贯穿围术期的整个过程直至患者出院(证据等级:低;推荐等级:强烈推荐)。2. 术前肠道准备传统术前肠道准备包括机械性肠道准备和口服抗菌药物清 除肠道细菌,多个领域的ERAS 方案均不建议术前行肠道 准备。有研究结果显示,机械性肠道准备可导致脱水、电解质紊乱,尤其是老年患者。同时针对胰十二指肠手术的回顾性研究结果表明,肠道准备并不能使患者获益。推荐意见2:术前不必常规行肠道准备(证据等级:低;推荐等级:强烈推荐)。3. 术前禁食传统围术期处理方案提倡术前禁食12 h、禁水6 h,认为可降低术后吸入性肺炎的发生率,但缺乏相应证据。同时有研究表明,禁食过夜可引起胰岛素抵抗和术后不适。一项纳入了22 项随机对照研究的Meta 分析结果
《肝细胞癌肝切除术后复发预防和治疗中国专家共识(2020版)》要点 肝细胞癌(HCC)是最常见的恶性肿瘤之一,全球发病率约84万/年,位居各种恶性肿瘤发病率的第7位 。我国为HCC高发地区,发病率占全世界的50%以上。最新统计资料表明,HCC在我国的肿瘤相关性死亡中位居第二位,仅次于肺癌。肝切除术仍是目前HCC治疗最常用的潜在根治性治疗手段,但文献报道的术后5年复发率>70%。有效预防与及时合理治疗复发,对降低病死率,提高总体生存率具有重大意义。 1 HCC术后复发的定义 HCC术后复发是指根治性肝切除术后HCC的再次发生。HCC复发的临床诊断主要根据既往肝切除治疗史,以及再次发生肿瘤的临床特征符合国家卫健委《原发性肝癌诊疗规范(2019年版)》(以下简称为《2019规范》)或欧洲肝脏研究协会(EASL)HCC诊疗指南的诊断标准。利用切除或穿刺获得的肿瘤组织可做出病理学诊断。 建议:(1)复发性HCC的诊断主要基于根治性肝切除术后再次发生肿瘤,如符合《2019规范》或EASL的临床诊断标准,即可做出临床诊断;组织病理学检查提供确定性诊断(证据等级:高;建议等级:强烈建议)。
(2)HCC根治性切除定义为完全切除术前影像学和术中探查可发现的所有肿瘤结节,肝切缘病理学检查阴性,无大体血管和胆管侵犯,无淋巴结或肝外远处转移,多数AFP阳性病人,术后2个月内该标记物降至正常水平,影像学检查无新发肿瘤(证据等级:中;建议等级:一般建议)。 2 HCC术后复发的类型 多数(68%~96%)病人肝切除术后HCC复发发生在肝内,即肝内复发;少数可转移至肝外组织或脏器,即肝外转移,但常同时合并有肝内复发。 建议:(1)HCC肝内复发存在单中心和多中心两种起源,分别与早期和远期复发相关(证据等级:高;建议等级:强烈建议)。(2)临床上一般可将术后2年内的复发定义为早期复发,2年之后的复发定义为远期复发(证据等级:中;建议等级:一般建议)。 3 HCC术后复发的高危因素 3.1 肿瘤分期 3.2 病人及肝脏相关特征 3.3 外科操作
肝切除术 二、肝储备功能的评估 肝切除术后一个严重的并发症是肝功能衰竭 (简称肝衰)。它一旦发生往往导致病人死 亡,是肝切除手术死亡的主要原因之一。 肝衰的发生常常是由于对不能耐受肝切除的肝脏施 行了肝切除或由于切肝量过大、超过了肝脏的代偿能力所致。正常肝脏具有强大的储备功能, 可以耐受75%勺切肝量。但在我国乃至亚洲,肝切除的主要适应证是肝细胞性肝癌 癌),而80%左右的肝癌伴有不同程度的肝硬化。发生硬化的肝脏还有多少储备功能、还能 耐受多大范围的肝切除?这是在施行每例肝癌肝切除术前所要回答的问题。事实上,人们一 直在研究精确的肝储备功能检测方法, 希望籍此在术前能够确定安全的切肝量。 目前临床上, 在肝切除前除了作常规的肝功能试验外, 越来越多采用新的更加敏感的肝功能指标来评估肝 储备功能,以指导肝切除手术适应证和切肝量的掌握。 (一) 常规肝功能检查 和门冬氨酸转氨酶(AST)、蛋白电泳、凝血酶原时间等。 1.胆红素:肝脏处理胆红素的储备能力较大,因此,一旦血清胆红素水平明显升高, 则表明肝功能受损较重。 一般认为胆红素>50卩mol /L ,不宜行任何类型肝切除; 胆红素40 50卩mol/L,经保肝治疗后降至 30卩mol/L 以下,而其他肝功能指标基本正常,可行肝楔形 切除、单肝段切除;胆红素 20?30卩mol/L ,可行双肝段切除。需要指出的是,不可将肝癌 胆管而引起的黄疽,临床上须注意鉴别, 此时胆红素升高以结合型为主, 多伴有肝内胆管扩 张、碱性磷酸酶(ALP)升高,这类病人需要手术治疗,也往往能耐受手术。 2.白蛋白和球蛋白:血清白蛋白 >40g/L 常表明肝储备功能良好,肝切除不受限制;白 蛋白在正常值的低限(35g/L),则表示肝储备功能有限, 肝切除范围应限制在 2个肝段以内; 白蛋白在31?34g/L 之间,经保肝、补充白蛋白治疗后能上升至 35g/L 以上,可行单肝段或 肝楔形切除;白蛋白W 30g/L ,则表明肝功能已失代偿,不宜作任何类型肝切除。在考察血 清白蛋白水平高低时应结合球蛋白一并考虑,后者是反映肝硬化是否存在及严重程度的指 标。血清球蛋白<25g/L ,白/球蛋白比值>1.5,一般表示肝脏无硬化,肝切除不受限制;球 蛋白>30g/L ,白/球蛋白比值<1.5,表示可能有肝硬化存在, 肝切除应限制在半肝以下; 球蛋 白>35g/L , 一般表示有明显肝硬化存在, 若白/球蛋白比值> 1.0,则可行单肝段或肝楔形切 除,若白 /球蛋白比值V 1.0,则应放弃肝切除。 3. ALT 和AST: ALT 和AST 不是反映肝储备功能的指标,但二者升高常表示肝硬化处 (简称肝 常规肝功能检查项目包括胆红素、白蛋白、球蛋白、 白/球蛋白比、丙氨酸转氨酶(ALT) 伴有黄疽均判为肝功能失代偿而放弃手术治疗, 部分病例是由于肿瘤压迫、胆管癌栓等阻塞
肝切除术患者肝储备功能的评估 肝切除术后一个严重的并发症是肝功能衰竭(简称肝衰)。它一旦发生往往导致病人死亡,是肝切除手术死亡的主要原因之一。肝衰的发生常常是由于对不能耐受肝切除的肝脏施行了肝切除或由于切肝量过大、超过了肝脏的代偿能力所致。正常肝脏具有强大的储备功能,可以耐受75%的切肝量。但在我国乃至亚洲,肝切除的主要适应证是肝细胞性肝癌(简称肝癌),而80%左右的肝癌伴有不同程度的肝硬化。发生硬化的肝脏还有多少储备功能、还能耐受多大范围的肝切除?这是在施行每例肝癌肝切除术前所要回答的问题。事实上,人们一直在研究精确的肝储备功能检测方法,希望籍此在术前能够确定安全的切肝量。目前临床上,在肝切除前除了作常规的肝功能试验外,越来越多采用新的更加敏感的肝功能指标来评估肝储备功能,以指导肝切除手术适应证和切肝量的掌握。 (一)常规肝功能检查 常规肝功能检查项目包括胆红素、白蛋白、球蛋白、白/球蛋白比、丙氨酸转氨酶(ALT)和门冬氨酸转氨酶(AST)、蛋白电泳、凝血酶原时间等。 1.胆红素:肝脏处理胆红素的储备能力较大,因此,一旦血清胆红素水平明显升高,则表明肝功能受损较重。一般认为胆红素>50μmol /L,不宜行任何类型肝切除;胆红素40~50μmol/L,经保肝治疗后降至30μmol/L以下,而其他肝功能指标基本正常,可行肝楔形切除、单肝段切除;胆红素20~30μmol/L,可行双肝段切除。需要指出的是,不可将肝癌伴有黄疽均判为肝功能失代偿而放弃手术治疗,部分病例是由于肿瘤压迫、胆管癌栓等阻塞胆管而引起的黄疽,临床上须注意鉴别,此时胆红素升高以结合型为主,多伴有肝内胆管扩张、碱性磷酸酶(ALP)升高,这类病人需要手术治疗,也往往能耐受手术。 2.白蛋白和球蛋白:血清白蛋白>40g/L常表明肝储备功能良好,肝切除不受限制;白蛋白在正常值的低限(35g/L),则表示肝储备功能有限,肝切除范围应限制在2个肝段以内;白蛋白在31~34g/L之间,经保肝、补充白蛋白治疗后能上升至35g/L以上,可行单肝段或肝楔形切除;白蛋白≤30g/L,则表明肝功能已失代偿,不宜作任何类型肝切除。在考察血清白蛋白水平高低时应结合球蛋白一并考虑,后者是反映肝硬化是否存在及严重程度的指标。血清球蛋白<25g/L,白/球蛋白比值>1.5,一般表示肝脏无硬化,肝切除不受限制;球蛋白>30g/L,白/球蛋白比值<1.5,表示可能有肝硬化存在,肝切除应限制在半肝以下;球蛋
肝切除术围手术期管理专家共识(最全版) 自1888年世界首例肝切除术成功开展以来,肝脏外科已经历了从局部肝切除到扩大半肝切除再到活体肝脏移植等漫长的发展历程。近年来随着对肝脏解剖的不断认识和血流控制技术的逐渐完善,以及新型断肝器械的相继发明,肝切除技术已日臻成熟。然而,国内外肝切除术的手术死亡率虽已下降至5%以下,但术后并发症发生率仍高达15%~50%[1]。如何进一步降低并发症发生率仍然是肝脏外科面临的重要课题。肝切除术的围手术期管理与术后并发症的发生息息相关。围手术期管理包括术前、术中及术后对病人病情的系统化评估和处理。近年来在这一领域新的理念和方法不断涌现,但目前尚无公认的针对肝切除术围手术期管理的规范。基于现有的循证医学研究证据,结合国内外多个肝脏外科中心的最新临床实践的经验,中华医学会外科学分会肝脏外科学组组织国内部分专家经过反复多次讨论和修改,制定《肝切除术围手术期管理专家共识》,供同道参考。 1术前评估和准备 1.1 全身状况评估肝切除术是一种风险较大的复杂手术,病人术前的全身机能状况对手术成败有重大影响。术前全身状况评估包括体力状况、营养状况和重要器官功能状况等方面。 1.1.1 术前体能状态评估当前,国际上多项诊疗指南均将体力状态作为手术评估的重要指标。美国东部肿瘤协作组(Eastern Cooperative
Oncology Group,ECOG)-活动状态(performance status,PS)评分简便、易行,是一个通行评估标准。有研究表明,ECOG-PS评分3~4分的肝切除病人,术后并发症发生率大大增加[3]。 推荐1:ECOG-PS评分应作为术前常规评估方法,PS 3~4分的病人应慎重考虑手术(Ⅰb、A)。 1.1.2 术前营养风险筛查营养风险筛查与肝切除术的顺利施行密切相关。当前针对腹部大手术术前营养风险筛查的工具主要有两种,即欧洲营养学会推荐的营养风险筛查(NRS)-2002评分表和美国肿瘤学会推荐的病人自评主观全面评定量表(patient-generated subjective global assessment,PG-SGA)。NRS-2002评分表具有简便、实用和容易掌握的优点。NRS-2002得分≥3分表明病人存在营养风险,需要在围手术期进行营养支持[4]。PG-SGA需要营养专业人士运用专门设备进行人体测量,目前尚难普及。但是PG-SGA准确度高,特异度强,在有条件的单位仍推荐开展。 推荐2:对拟行肝切除术的病人,特别是明显瘦弱者,建议行术前营养风险筛查(Ⅰb、A)。 1.1.3 全身重要器官功能评估肝切除手术创伤较大且手术时间较长,良好的心肺等重要器官功能是保障手术安全的关键。重要器官功能的评估应该从病史开始,首先了解病人是否存在心血管、呼吸、泌尿、消化、神经、血液、内分泌-免疫等系统的疾病病史,详细了解是否服用了治疗高血压、心脏病等方面的药物(可乐定类抗高血压药物,华法林等抗凝、抗血小板类药物应该停用或调整)。通过病史和体检可以对病
精准肝切除治疗肝胆管结石的效果分析 发表时间:2019-04-24T11:44:07.017Z 来源:《医药前沿》2019年6期作者:兰戴天 [导读] 探讨肝胆管结石病采用精准肝切除治疗的效果。方法:选择2017年3月-2018年7月收治的肝胆管结石患者80例,分为对照组与观察组各40例 兰戴天 (四川省人民医院<东院> 四川成都 610100) 【摘要】目的:探讨肝胆管结石病采用精准肝切除治疗的效果。方法:选择2017年3月-2018年7月收治的肝胆管结石患者80例,分为对照组与观察组各40例,对照组运用规则性肝切除治疗,观察组运用精准肝切除治疗,分析不同治疗后患者手术时间、住院时间、手术出血量、结石清除率、术后并发症情况。结果:在住院时间、手术出血量上,观察组少于对照组,组间对比差异有统计学意义(P<0.05);在结石清除率和术后并发症率上,观察组为90%和12.5%,对照组为72.5%和32.5%,组间对比差异有统计学意义(P<0.05)。结论:肝胆管结石病采用精准肝切除治疗可以有效的提高治疗效果,加快手术恢复,减少术后并发症。 【关键词】肝胆管结石病;精准肝切除;治疗效果 【中图分类号】R575.7 【文献标识码】A 【文章编号】2095-1752(2019)06-0148-02 肝内胆管结石属于临床常见的顽固慢性疾病之一,病情复杂,容易出现胆管狭窄、胆管炎症、肝纤维化与萎缩等不良并发症,术后容易结石残留[1]。精准肝切除方式属于相对新型的治疗理念,有效的减少手术对组织的创伤,提升康复效果。本文选择2017年3月-2018年7月收治的肝胆管结石患者80例,分析采用精准肝切除治疗后患者手术时间、住院时间、手术出血量、结石清除率、术后并发症情况,内容如下: 1.资料与方法 1.1 一般资料 选择2017年3月-2018年7月收治的肝胆管结石患者80例,随机分为对照组与观察组各40例,其中对照组男24例,女16例;年龄从34岁~69岁,平均为(45.1±4.9)岁;病灶区域中,左侧为23例,右侧为9例,双侧为8例;观察组男27例,女13例;年龄从36岁~67岁,平均为(43.7±3.2)岁;病灶区域中,左侧为21例,右侧为10例,双侧为9例;两组患者在基本的年龄、性别以及病情等状况上没有明显差异,有可比性。 1.2 方法 对照组运用规则性肝切除治疗,依据患者Child分级与影像检查结果做好检测肝脏代偿状况评估,判断切除,了解病变状况,开展规则性肝切除,做好胆道探查与取石。手术中运用Pringle法做好出血管控,不进行肝门阻断,做好创面缝合。观察组运用精准肝切除治疗,术前做好病情评估,确定结石定位,同时判断切除后的剩余肝脏功能体积状况。运用三维技术来对肝切除情况做模拟,提升切除准确定位,明确肝脏切除后的功能体积。手术中进行选择性的肝血流阻断或者不做肝门阻断。做好肝组织离断与止血等处理。 1.3 评估观察 分析不同治疗后患者手术时间、住院时间、手术出血量、结石清除率、术后并发症情况。 1.4 统计学分析 将治疗数据通过spss17.0分析,计量资料使用t检验,计数资料运用卡方检验,P<0.05为有统计学意义。 2.结果 2.1 不同治疗后患者住院时间、手术时间、手术出血量情况 如表1所示,在住院时间、手术出血量上,观察组各项显著少于对照组,组间对比有统计学意义(P<0.05)。 3.讨论 肝胆管结石治疗中,常规非规则性肝切除术治疗运用广泛,可以较快的完成手术操作,手术便捷性上更高,但是精准肝切除手术则可以更好的减少手术创伤,提升手术恢复速度,降低手术出血量,有效的降低因为盲目性切除肝脏组织而导致的术后并发症提升问题[2]。随着有关技术的升级,以及治疗观念的优化,精准肝切除治疗有效的成为当下该病治疗的首选方式。在手术治疗中,需要做好患者的综合而评估,尤其是手术时间相对较长,需要做好对应的手术耐受力评估,由此来提升手术开展的适宜平稳。术中需要做好各方面的监测,及时发现异常处理。术中需要进行肝段门静脉插管,或者采用病变肝叶引导穿刺,有效的确定染色之后有清晰的肝叶便捷,有助于手术顺利开展[3]。手术前需要做好综合情况的观察,依据个人情况做好对应治理方案调整。手术方面通过多种影像技术的辅助,可以有效的做好手术定位,明确切除范围,对清理结石有较好的辅助作用,对降低手术创伤也有较好的辅助功效。患者容易出现胆管狭窄与肝叶萎缩等情况,术中容易对手术切面、脉管受累以及破坏脉管完整性构成一定影响,提升手术难度,阴需要做好精准的评估。精准肝切除在一定程度上有
肝切除术前肝脏储备功能评估的专家共识(2011版) 董家鸿郑树森陈孝平窦科峰樊嘉别平耿小平吕文平 Consensus on evaluation of hepatic functional reserve before Hepatectomy(2011 edition)Ding Jia-hong*,Zheng Shu-sun,Chen Xiao-ping, Dou Ke-feng, Fan Jia, Bie Ping,Geng Xiao-ping, LV Wen-ping.*Hospital&Institute of hepatobiliary surgery,Chines PLA General Hospital,Beijing,100853,China corresponding author: Ding Jia-hong, E-mail: dongjh301 @https://www.doczj.com/doc/9e14160599.html, 【Key words】Hepatic functional reserve;Hepatectomy;Evaluation;Consensus 【关键词】肝脏储备功能; 肝切除术; 评估; 共识 肝脏外科已走进了精准外科时代?精准肝脏外科在追求彻底清除目标病灶的同时,确保剩余肝脏解剖结构完整和功能性体积最大化,并最大限度控制手术出血和全身性创伤侵袭,最终使手术患者获得最佳康复效果[1-2]? 肝切除是肝脏外科疾患的重要治疗手段?由于肝脏外科疾患尤其是肝细胞癌多合并肝实质损害,肝脏储备功能有不同程度的降低,肝切除术后肝脏功能不全成为患者围手术期死亡的重要原因?术前精确评估肝脏储备功能,对于选择合理的治疗方法,把握安全的肝切除范围,从而降低患者术后肝脏功能衰竭的发生率具有重要意义? 1 肝脏储备功能的概念及解剖生理基础[3] (1) 肝脏储备功能的概念:系指肝脏应对生理负荷增加时可动员的额外代偿潜能?肝脏在受到损害的病理状态下,肝脏储备功能除了需应对机体代DOI:10.3760/cma.j.issn.1673 9752.2011.01.006 (2)肝脏储备功能的解剖生理基础:肝脏储备功能主要取决于功能性肝细胞群的数量及其组织结构的完整性? 2 评估肝脏储备功能的目的 通过评估肝脏储备功能,了解患者对不同类型或范围的肝切除手术的耐受性,为设计和实施安全手术提供依据,以预防患者手术后发生肝脏功能衰竭? 3 评估肝脏储备功能的主要方法 评估肝脏储备功能的方法繁多,主要方法可分为5类:(1)肝脏血清生化学试验?(2)综合评分系统?(3)肝脏功能定量试验?(4)肝实质及脉管病变的影像学评估?(5)肝脏体积测量? 3.1 肝脏血清生化学试验 通过检测血清中肝脏合成和分泌的物质含量或酶的活性,提示肝脏损害和病变? (1)转氨酶:主要包括丙氨酸氨基转移酶(alaninetransaminase,ALT)和门冬氨酸氨基转移酶(aspartatetransaminase,AST)?ALT主要存在于细胞质中;AST主要存在于细胞质和线粒体中?ALT和AST是肝细胞损伤的敏感指标,其水平升高提示肝实质受到了不同程度的损害,但是与肝脏储备功能并无直接的关联? (2)碱性磷酸酶(alkalinephosphatase,ALP)和γ 谷氨酰转肽酶(gammaglutamyltranspeptidase,GGT):ALP是一组水解酶,主要存在于肝脏的毛细胆管?骨?肾和胎盘中;GGT主要存在于肝?胰?脾?肾?心?脑等细胞膜上?当存在胆汁淤滞或肝实质损害时,ALP和GGT水平增高?从毛细胆管到胆总管开口任何层面的胆道梗阻和胆汁淤滞均可导致ALP和GGT升高? (3)胆红素:胆红素是血红蛋白代谢的主要降解产物,其血浆浓度反映了肝细胞通过肝脏网状内皮系统对胆红素进行摄取?结合和排泄的过程?肝实质严重损害和胆汁淤滞均可导致血浆总胆红素水平升高,这是与肝切除手术预后相关的独立危险因素? (4)白蛋白:只在肝脏合成,其循环半衰期为20d,检测白蛋白可了解肝脏稳态合成功能,是Child评分的指标之一? (5)凝血酶原时间:肝脏是合成凝血因子Ⅱ?Ⅴ?Ⅶ?Ⅹ的重要场所?凝血酶原时间反映了包括凝血因子Ⅱ?Ⅴ?Ⅶ?Ⅹ和纤维蛋白原在内的外源性凝血过程? 上述生化指标有的与肝脏功能无关,有的只从一个侧面反映了肝脏功能,对手术后肝脏功能衰竭并无预测价值?原因为[4]:(1)其中大部分指标并非特异地反映肝脏功能的损害情况,这些指标在血清中的含量或酶活性取决于其产生?分布与清除的总和效应?许多肝外因素也可引起这些指标的异常,如营养不良和肾病等导致白蛋白降低,胆道梗阻?脓血症?长期胃肠外营养?溶血等导致胆红素升高,肌病或者剧烈运动等导致ALT 或AST升高,维生素K缺乏?脂肪泻?抗生素应用等导致凝血酶原时间延长?(2)部分指标在1%~4%的正常人群中存在异常?(3)即使少量的肝细胞受损也可导致一些肝细胞结构酶指标的明显异常,并不能反映整体肝脏功能状况;而反映肝脏代谢和蛋白合成功能的指标,只有当肝脏功能严重受损而失代偿时才会出现异常改变?