
还原性谷胱甘肽(GSG)主峰前依次为甘氨酸(Gly)、L-胱氨酸(Cy2,即Cys- Cys)、L-谷氨酸(Glu)、L-半胱氨酸(Cys);
还原性谷胱甘肽(GSG)主峰后依次为半胱氨酰甘氨酸(Cys- Gly)、氧化性谷胱甘肽(GSSG)。
或可能有二肽和单个氨基酸和其他杂质。L-焦谷氨酸
GSSG在碱性条件下经双氧水氧化而得。
2 GSH + ROOH → GSSG + ROH + H2O
由2个还原型谷胱甘肽以二硫键结合的产物, 氨基酸序列:
氧化型谷胱甘肽分子式为C20 H32N6 O12 S2 , 相对分子量为61263,
氧化型谷胱甘肽二钠,氧化型谷胱甘肽二钠盐
氧化还原滴定法确定谷胱甘肽的含量
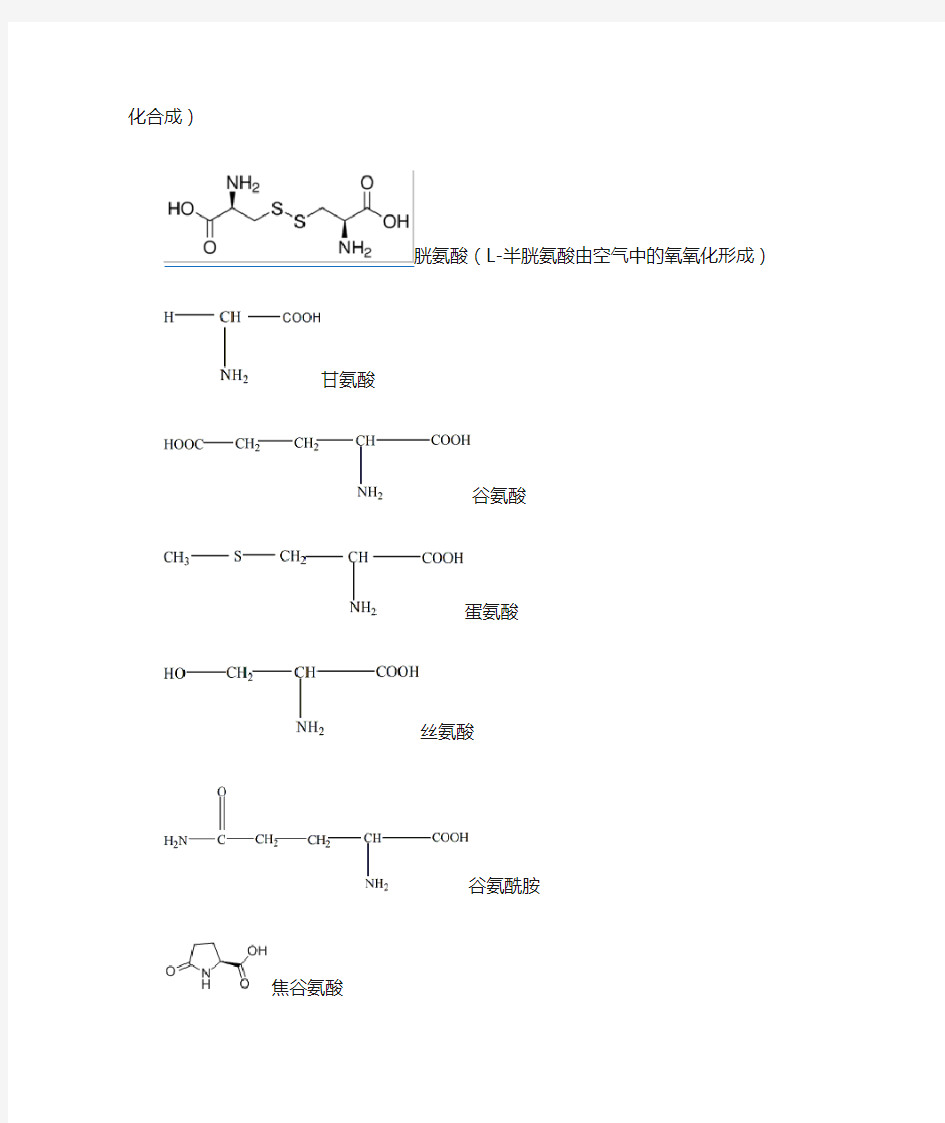
L-半胱氨酸(由体内的蛋氨酸或丝氨酸经过胱硫醚转化合成)
胱氨酸(L-半胱氨酸由空气中的氧氧化形成)
甘氨酸
谷氨酸
蛋氨酸
丝氨酸
谷氨酰胺
焦谷氨酸
天冬氨酸
丙氨酸
精氨酸
脯氨酸
L-半胱氨酸化学变化
牛磺酸丙酮酸、NH3、H2S、硫酸、亚硫酸
↖(半胱氨酸一脱巯基酶)
↖↑脱羧基氨基,在半胱氨酸一脱巯基酶作用下
高半胱氨酸←L-蛋氨酸(转移甲基)或丝氨酸→L-半胱氨酸→→谷氨酰胺→→→谷氨醇或吡
咯羧醇↑↓
↑↓合成分解或丙酯化
转化↑↓
还原电解↑↓空气中氧氧化
胱氨酸
甲基供体可以有肌酸、N-甲基烟酸、胆碱、甲基组氨酸等
L-谷氨酸化学变化
精氨酸一氧化氮合酶(NOS)、谷氨酸、谷氨酰胺→瓜氨酸(透过胞质酵素精氨基琥珀酸合成酶(ASS)及精氨基琥珀酸裂解酶(ASL)合成)
L—谷氨酸钠、聚谷氨酸↓
↖ L-脯氨酸或L-精氨酸→精氨酸盐(与酸)
↖↘转化↘↖分子内脱水145-150度(环化反应)↖↘
氨→→谷氨酸→→→→→→→焦谷氨酸
谷氨酸脱氢酶与NADPH(辅酶Ⅱ)催化作用合成↙↙↙转氨基作用谷草转氨酶或谷丙转氨酶的催化作用↙↙天冬氨酸或丙氨酸
↙↙与氨气
乙酰谷氨酸合成酶的催化与乙酰CoA↙谷氨酰胺←←缬氨酸、异亮氨酸
乙酰谷氨酸
L-甘氨酸化学变化
盐酸
L-甘氨酸→→L-甘氨酸盐
L-胱氨酸←两个半胱氨酸通过其侧链巯基氧化成二硫键后形成
↓
热酸和热碱溶液中能被分解。
谷胱甘肽 1.定义 谷胱甘肽(glutathione GSH)CAS号:70-18-8。谷胱甘肽是一种存在于自然界中的氨基酸复合物,由谷氨酸、半胱氨酸、甘氨酸等三种氨基酸组合而成的寡肽。谷胱甘肽在体内以两种形态存在,即还原型谷胱甘肽和氧化型谷胱甘肽(oxidized glutathione,简称GSSG)。通常人们所指的谷胱甘肽是还原型谷胱甘肽。还原型谷胱甘肽很容易被氧化,两分子谷胱甘肽的活泼巯基氧化脱氢后以二硫键相连得到的二聚体,即是氧化型谷胱甘肽。其中只有还原型谷胱甘肽才具有生理活性,而生物体内的氧化型谷胱甘肽需经还原后才能发挥生理功能。 2.结构和理化性质 谷胱甘肽是一种白色晶体,化学名为γ-L-谷氨酰-L-半胱氨酰-甘氨酸,其结构如图1所示。相对分子质量为307.33,熔点是192~195 °C (分解),等电点为5.93。比旋光度[α]D20为+17.60°(C=0.05,H2O),易溶于水、稀醇、液氨和二甲基甲酰氨,不溶于乙醚和丙酮。谷胱甘肽固体较为稳定,而水溶液在空气中易被氧化,谷胱甘肽在高水分活度下不易保存,只有将水分活度控制在0.3以下才能长期稳定保存。 3.生理功能
谷胱甘肽是细胞内存在最丰富的小分子硫醇类化合物,其分子中含有一个特异的γ-肽键,由谷氨酸的γ-羧基与半胱氨酸的α-氨基缩合而成,并且半胱氨酸侧链基团上连有一个活泼巯基,是谷胱甘肽许多重要生理功能的结构基础。 3.1抗氧化作用 还原型谷胱甘肽结构中含有一个活泼的巯基—SH,易被氧化脱氢。它在体内能够保护许多蛋白质和酶等分子中的巯基不被如自由基等有害物质氧化,让蛋白质和酶等分子发挥其生理功能。同时清除自由基。 机体内新陈代谢产生的许多自由基会损伤细胞膜,毁坏免疫系统,侵袭生命大分子,促进机体衰老,并诱发肿瘤或动脉粥样硬化的产生。由此,谷胱甘肽具有抗衰老和强化免疫系统等作用。 3.2整合解毒作用 谷胱甘肽半胱氨酸上的巯基为其活性基团(故谷胱甘肽常简写为G-SH),易与碘乙酸、芥子气(一种毒气)、铅、汞、砷等重金属盐或致癌物质等相结合,并促进其排出体外,起到中和解毒作用。4. 应用 4.1 谷胱甘肽在临床上的应用 谷胱甘肽在临床上有广泛的作用,对细胞有保护作用,可防止红细胞溶血,从而减少高铁血红蛋白的损失;抑制脂肪肝的形成,改善中毒性肝炎和感染性肝炎的症状;对丙烯腈、氟化物、一氧化碳、有机溶剂、重金属等中毒具有解毒作用;对缺氧血症的不适、恶心、呕
主要目的: ——测定物质还原性谷胱甘肽(GSH)的含量。 主要原理: 参照 GSH检测分析试剂盒说明书, 5,5 ’–二硫代–双–(2–硝基苯甲酸)能和 谷胱甘肽(GSH)反应产生 2–硝基– 5–巯基苯甲酸和谷胱甘肽二硫化物( GSSG), 由于 2–硝基– 5–巯基苯甲酸是一黄色产物,通过测定其在412 nm处的最大吸 收可确定样品中谷胱甘肽的含量用纯化的谷胱甘肽(GSH)抗体包被微孔板,制 成固相抗体,往包被单抗的微孔中加入谷胱甘肽(GSH),再与HRP标记的谷胱甘 肽( GSH)抗体结合,形成抗体 - 抗原 - 酶标抗体复合物,经过彻底洗涤后加底物 TMB显色。 TMB在 HRP酶的催化下转化成蓝色,并在酸的作用下转化成最终的黄色。颜色的深浅和样品中的谷胱甘肽(GSH)呈正相关。用酶标仪在412 nm波长下测定吸光度( OD值),通过标准曲线计算样品中谷胱甘肽(GSH)的含量。
实验室签章
一、试剂 ——谷还原性胱甘肽( GSH)测定试剂盒(南京建成生物研究所) 二、仪器设备 —— 96 孔酶标板 —— UV-Vis 可见多功能酶标 仪——旋涡混匀器——离心机 ——移液枪及其相应量程枪头
三、实验方法 根据试剂盒说明书具体操作步骤如下: 1.上清液的制备:取稀释后的血清或组织匀浆液 mL,加试剂一应用液 2 mL 混匀, 4000 rpm 离心 10 分钟,取上清液 1 mL 进行显色反应。 2.显色反应:空白管中加入 1 mL 试剂一,标准管加入 20μmol/LGSH标准 液 1 mL,测定管加入上步骤得到的上清液 1 mL,然后各管中分别加入mL 试剂 二、试剂三、 mL 试剂四。 3.混匀,室温静置 5 分钟后,在 412 nm处将酶标板空板进行扫描,准确吸 取 mL 各管反应液加入到新的 96 孔板中,酶标仪测定各孔吸光度( OD值)。 4.血清中 GSH含量计算公式 GSH含量( mg/L) 测定 OD值 -空白 OD 值 -3 mmol/L) ×标准品浓度( 20×10 标准 OD值-空白 OD值 ×GSH分子量( 307)×样本测试前稀释倍数 组织中 GSH含量公式 测定OD值-空白OD值 -3 GSH含量(mg/gprot )×标准品浓度(20×10 mmol/L) ×GSH分子量( 307)×样本测试前稀释倍数÷待测组织匀浆液蛋白浓度 (gprot/L ) 参考文献 Lapshina E A, Sudnikovich E J, Maksimchik J Z, et al. Antioxidative enzyme and glutathione S-transferase activities in diabetic rats exposed to long-term ASA treatment [J]. Life sciences, 2006, 79(19): 1804-1811.
小鼠谷胱甘肽S转移酶(GST)酶联免疫分析(ELISA) 试剂盒使用说明书 本试剂仅供研究使用目的:本试剂盒用于测定小鼠血清,组织及相关液体样本中谷胱甘肽S转移酶(GST)的含量。 实验原理: 本试剂盒应用双抗体夹心法测定标本中小鼠谷胱甘肽S转移酶(GST)水平。用纯化的谷胱甘肽S转移酶(GST)抗体包被微孔板,制成固相抗体,往包被单抗的微孔中依次加入谷胱甘肽S转移酶(GST),再与HRP标记的谷胱甘肽S转移酶(GST)抗体结合,形成抗体-抗原-酶标抗体复合物,经过彻底洗涤后加底物TMB显色。TMB在HRP酶的催化下转化成蓝色,并在酸的作用下转化成最终的黄色。颜色的深浅和样品中的谷胱甘肽S转移酶(GST)呈正相关。用酶标仪在450nm波长下测定吸光度(OD值),通过标准曲线计算样品中小鼠谷胱甘肽S转移酶(GST)浓度。 试剂盒组成48孔配置96孔配置保存 说明书1份1份 封板膜2片(48)2片(96) 密封袋1个1个 酶标包被板1×48 1×96 2-8℃保存 标准品:450pg/ml ×1瓶×1瓶2-8℃保存标准品稀释液×1瓶×1瓶2-8℃保存酶标试剂 3 ml×1瓶 6 ml×1瓶2-8℃保存样品稀释液 3 ml×1瓶 6 ml×1瓶2-8℃保存显色剂A液 3 ml×1瓶 6 ml×1瓶2-8℃保存显色剂B液 3 ml×1瓶 6 ml×1瓶2-8℃保存终止液3ml×1瓶6ml×1瓶2-8℃保存浓缩洗涤液(20ml×20倍)×1瓶(20ml×30倍)×1瓶2-8℃保存 样本处理及要求: 1. 血清:室温血液自然凝固10-20分钟,离心20分钟左右(2000-3000转/分)。仔细收集上 清,保存过程中如出现沉淀,应再次离心。 2. 血浆:应根据标本的要求选择EDTA或柠檬酸钠作为抗凝剂,混合10-20分钟后,离心 20分钟左右(2000-3000转/分)。仔细收集上清,保存过程中如有沉淀形成,应该再次离心。 3. 尿液:用无菌管收集,离心20分钟左右(2000-3000转/分)。仔细收集上清,保存过程 中如有沉淀形成,应再次离心。胸腹水、脑脊液参照实行。 4. 细胞培养上清:检测分泌性的成份时,用无菌管收集。离心20分钟左右(2000-3000转/
谷胱甘肽的制备 背景 谷胱甘肽(glutathione,GSH)是由L一谷氨酸、L一半胱氨酸和甘氨酸经肽键缩合而成的一种同时具有1一谷氨酰基和巯基的生物活性三肽化合物?,在生物体内具有多种重要的、独特的生理功能,因此又被称为长寿因子和抗衰老因子。作为一种重要的生理活性物质,GSH在解毒、抗辐射、肿瘤、癌症、氧化衰老和协调内分泌的治疗中效果明显且无副作用,这些同类药物所不具有的优点使得GSH在临床和医药领域有着极为广泛的用途【21。在食品加T中,GSH具有抗氧化、防止褐变、强化风味和营养等功能,已被作为生物活性添加剂应用于保健食品的生产中。但GSH在体内循环周期短、易氧化、不能穿过细胞膜,从而限制了其保健和治疗作用的发挥。据报道,脂质体包埋技术能够有效地提高GSH的保护和治疗作用。 试验步骤 1试验材料 谷胱甘肽(纯度≥98.0%) Amresco公司;乙醇、乙醚、磷酸氢二钠、磷酸二氢钠、柠檬酸(均为分析纯)、吐温一80(化学纯)、卵磷脂、胆固醇国药集团化学试剂有限公司;0.05m01·L。磷酸盐缓冲液(PBS) 自制。
2 实验方法 1.2.1脂质体的分离方法 1.2.1.1凝胶柱过滤法选用Sephadex G一25凝胶柱,取lmL脂质体混悬液进行上样分离,采用一定的洗脱剂洗脱,洗脱速度控制在0.5—1.0mL-min~,进行分部收集,测定游离的谷胱甘肽总量,计算包封率。 1.2.1.2洗脱剂的选择取1mg·mL“的谷胱甘肽溶液1mL上柱分离,分别选用去离子水、NaCI、乙醇、PBS、乙酸和PBS(NaCl)为洗脱剂进行洗脱,洗脱速度控制在0.5~1.0mL·min~,进行分部收集,。测定洗脱液中的谷胱甘肽总量,计算回收率。1.2.2脂质体包封率的测定方法 1.2.2.1 游离GSH的测定方法采用优化的Ellman?s测定法”1。 1.2.2.2包封率的计算方法将脂质体与游离谷胱甘肽分离,测定游离的谷胱甘肽量,根据下式计算脂质体包埋率:EE(%)=(1一Cf/Ct)×100%。其中:EE—GSH脂质体包封率;Cf一游离GSH含鼍;Ct一总GSH含量。 1.2.3 pH梯度法制备谷胱甘肽脂质体称取一定量的卵磷脂、胆固醇和叶温一80,溶于乙醚,得到类脂溶液;将类脂溶液置于圆底烧瓶中,在40'(2水浴中旋转蒸发除去乙醚,待类脂物在烧瓶壁上成膜后,加入一定pH的0.3tool·L。1柠檬酸10mL,继续旋转蒸发水合30min,得空白脂质体溶液;将谷胱甘肽加入空白脂质体溶液中,用0.5mol·L。1的磷酸氢二钠溶液调节pH,使pH增加3,将上述混合液在冰浴中短时超声(间歇超声,1s/1s),静置2h,即得脂质体p。 1.2.4脂质体平均粒径和粒度分布吸取少量脂质体悬液,稀释至卵磷脂的含量在0.025%(W/W),装入预处理过的透明小瓶中。用丙酮擦拭瓶外部并吹干。放人激光散射仪中进行检测旧?。激光散射测试条4r牛-:温度:25±0.1℃;角度:90。(即垂直照射);波长:632.8nm;扫描时间:300s/样 2结果与讨论 2.1 脂质体分离方法的确定 2.1.1 分离方法的选择测定包封率的前提是将未包封的游离GSH与脂质体分开,凝胶
919 还原型谷胱甘肽的稳定性研究 朱义福 (星湖生物科技股份有限公司,广东肇庆 526040) 摘要:本文研究了pH 、温度、光照以及外加抗氧化剂等因素对还原型谷胱甘肽(GSH)纯品溶液稳定性的影响。结果表明,GSH 水溶液在pH=2.0~4.0范围内最为稳定;在30 ℃以下,24 h 内自身氧化较少;应避光处理或保存;外加抗氧化剂在pH=6.0时,保护作用明显。 关键词:谷胱甘肽;稳定性;抗氧化剂 文章篇号:1673-9078(2011)8-919-923 Stability of Reduced Glutathione under Different Conditions ZHU Yi-fu (Star Lake Bioscience Co., Inc., Zhaoqing 526040, China) Abstract: The effects of pH, temperature, sunlight and antioxidant on the stability of reduced glutathione (GSH) solution were studied in this paper. Results indicated that GSH solution was relative stabile under the following conditions: pH 2.0~4.0 and temperature <30℃. And it should be kept in dark place. Besides, the GSH solution showed the highest stability in the presence of antioxidant at pH 6.0. Key words: glutathione; stability; antioxidant 谷胱甘肽(Glutathione ,GSH ),即γ-L-谷氨酰-L-半胱氨酰-甘氨酸,是由L-谷氨酸、L-半胱氨酸和甘氨酸经肽键缩合而成的生物活性三肽化合物。GSH 是许多酶反应的辅基,在生物体内具有清除体内自由基、解毒等多种重要的生理功能,特别是对于维持生物体内适宜的氧化还原环境具有重要意义[1]。国内外关于GSH 的研究主要集中在菌种选育[2]、培养条件优化[3]、分离纯化[4]和临床应用上[5],其工业化生产技术一直被国外极少数发达国家所垄断,国内尚未实现工业化生产,从而造成GSH 的市场价格居高不下,影响了GSH 的推广和应用。 GSH 易溶于水、稀醇、液氨和N,N-2甲基甲酰胺,而微溶于或不溶于醇、醚和酮。GSH 的固体较稳定,而水溶液在外界环境中受温度、pH 、光照等条件影响,易氧化,产生氧化型谷胱甘肽(即GSSG ),GSSG 是由两分子GSH 脱氢后通过二硫键相连的二聚体,其反应如下: 氧化型GSSG 不具有生理活性,只有还原型GSH 才能发挥重要的生理功能。GSH 的不稳定性是造成较难分离纯化、产品纯度不高的重要原因。因此,本文通过大量的试验对GSH 稳定性进行研究,为国内GSH 的工业化生产提供参考。 收稿日期:2011-03-26 作者简介:朱义福(1976-),男,工程师,研究方向:生物医药分离纯化技术 1 材料与方法 1.1 材料与试剂 GSH 纯品(纯度>98%):日本Kyowa 公司。四氧嘧啶(Alloxan ):美国sigma ; 二硫苏糖醇(DTT ):上海生工所;抗坏血酸(Vc ):广州化学试验厂;保险粉(Na 2S 2O 4):上海国药集团化学试剂公司;其它试剂为国产分析纯。 1.2 主要仪器 SC-15数控超级恒温槽:宁波新芝生物科技公司;CR21G 高速冷冻离心机:日本Hitachi 公司;752型紫外可见光分光光度计:南京第四分析仪器公司;S40 pH 精密测量仪,AB54-S 分析天平:瑞士METTLER TOLEDO 公司;RW20D 搅拌器:德国IKA 公司;Agilent LC1100液相色谱仪:美国HP 公司。 1.3 分析方法 GSH 含量测定采用四氧嘧啶Alloxan 试剂法 [6]:(1)标准曲线的制作:准确称取6.146 mg 的GSH 标准品,用40%乙醇溶解,定容至100 mL ,得到浓度为200 μmol/L 的标准液。取0 mL 、0.2 mL 、0.4 mL 、0.6 mL 、0.8 mL 、1.0 mL 上述标准液于试管中,补加去离子水至1.0 mL ,配成浓度为0 μmol/L 、40 μmol/L 、80 μmol/L 、120 μmol/L 、160 μmol/L 、200 μmol/L 的GSH 溶液。然后依次加入pH 7.6的磷酸缓冲液2.5 mL ,0.1 mol/L 的甘氨酸溶液0.5 mL ,以及Alloxan 试剂1.0 mL ,反应20
谷胱甘肽 谷胱甘肽全身增白胶囊美国原装进口千万不要错过这个让你变白的机会!!! 每瓶包含60 胶囊 每个胶囊包含: 谷胱甘肽500mg 维生素C 250mg 阿尔法硫辛酸50mg 天冬氨酸锌25mg 每胶囊有效含量825mg 特别优惠价格供应: 一瓶谷胱甘肽增白胶囊700元 两瓶谷胱甘肽增白胶囊推广价1280元 三瓶谷胱甘肽增白胶囊推广价1780元 什么是谷胱甘肽? 谷胱甘肽是一种小分子斯米塔等3个氨基酸组成,存在于几乎每一个细胞的身体.不过,谷胱甘肽必须产生的细胞及其前体(维生素C和阿尔法硫辛酸),才可以有效地工作人体. 在场的谷胱甘肽是要保持正常的免疫系统的功能.这已是众所周知的发挥着关键的作用,在繁殖淋巴细胞(细胞介导特异性免疫)发生在发展有效的免疫反应.此外,细胞中的免疫系统产生很多oxiradicals由于它们的正常运转,因此需要较高浓度的抗氧化剂比一般电池.谷胱甘肽发挥了重要作用,是实现这一要求. 谷胱甘肽的作用 加强人体免疫系统你体内的免疫活性,涉及乘法畅通淋巴细胞和抗体生产需要维护正常水平的谷胱甘肽内淋巴细胞.
抗氧化剂和自由基清除剂谷胱甘肽具有环保护作用的有害影响,包括细菌,病毒污染物和自由基. 调节其他抗氧化剂-谷胱甘肽其他重要的抗氧化剂如维生素C和E不能做好他们的工作,充分保护您的身体免受疾病. 解毒剂- 另一个主要功能是谷胱甘肽的解毒外国化合物等致癌物和有害代谢物. 谷胱甘肽是人体的#1防御细胞的损伤. 维他命A,C,E及贝他胡萝卜素,"抗氧化的"维生素,帮助保护细胞免受损伤. 但主要研究者发现,我们的第一道防线是一种肽(片蛋白),称为谷胱甘肽最重要的抗氧化剂和detoxifier于人体. 优秀的科学家,在史丹福大学研究的影响谷胱甘肽缺乏对人类细胞. "他们指出,如果没有适当的水平谷胱甘肽我们从字面上细胞"自杀"的"经历一个过程称为程序性细胞死亡" 殊死搏斗,在每一个细胞在你身上. 我们的细胞是在打一场仗不断地生存下去.科学家们相信,每一个细胞在体内是攻击000次,一天中的氧和氢分子(freeradicals),企图毁灭我们的身体,结束自己的生命. 这些分子撕裂孔,在我们的细胞,破坏了蛋白质,脂肪,即使是我们的基因.它们可造成的细胞发生变异,成为病害的其他方式,或者干脆停止运转和模具. 破坏氧化自由基牵连的原因是心脏病,中风,阿尔茨海默病,parkenson的疾病,癌症,白内障以及其他健康问题. 这些破坏分子所产生的身体的副产品身体的正常功能. 他们因暴露于太阳X射线和辐射,污染,压力大,体力消耗和因各种疾病. 口服谷胱甘肽(+142%谷胱甘肽)抑制酪氨酸酶活性.一旦酪氨酸酶活性的代谢一直被抑制,然后逆转的时候去合成光色素称为褐色素(phaeomelanin)而非造成皮肤黑、黯淡的合成色素称为真黑素(eumelanin). 循环不断地流,只要存在左旋谷胱甘肽并存代谢黑色素.最后,轻易将你的皮肤迅速改变为白嫩细腻. 经过美国国家食品药品管理局验证和麻萨诸州州总医院的成分及效果检测,亚当森大学的化验室分析数据材料这一切证明我们的超级全身美白胶囊,是一个最安全的,纯净,有效的口服皮肤增白剂在当今市场.
【实验目的】 了解植物组中中抗坏血酸-谷胱甘肽循环代谢过程,学习还原型谷胱甘肽含量的测定原理和方法。 【实验原理】 谷胱甘肽是有谷氨酸(Glu)、半胱氨酸(Gly)组成的天然三肽,是一种含巯基(—SH)的化合物,广泛存在于动物组织、植物组织、微生物和酵母中。谷胱甘肽能和5,5’-二硫代-双-(2-硝基苯甲酸)(5,5’-dithiobis-2-nitrobenoic acid,DTNB)反应产生2-硝基-5-巯基苯甲酸和谷胱甘肽二硫化物(GSSG)。2-硝基-5-巯基苯甲酸为一黄色产物,在波长412nm处具有最大光吸收。因此,利用分光光度计法可测定样品中谷胱甘肽的含量。 【器材与试剂】 1.实验仪器与用具 研钵、高速离心机、移液管、离心管、试管、分光光度计 2.实验试剂 还原型谷胱甘肽标准液;偏磷酸溶液;磷酸溶液缓冲液(pH7);二硫代硝基苯甲酸(5,5’-dithiobis-2-nitrobenoic acid,DTNB)溶液;蒸馏水。 3.实验材料 小麦叶片 【实验步骤】 1.标准曲线制作 取7支试管,编号,按照下表加入各种试剂,混匀,25℃保温反应10min。以1号管为参比调零,测定显色液在412nm处的吸光度。以吸光度为纵坐标,还原型谷胱甘肽物质的量(μmol)为横坐标,绘制标准曲线。 试管号 试剂(ml) 1 2 3 4 5 6 7 10μg/ml GSH标准液0 0.1 0.2 0.4 0.6 0.8 1.0
蒸馏水 2.0 1.9 1.8 1.6 1.4 1.2 1.0 pH7磷酸缓冲液 4.0 4.0 4.0 4.0 4.0 4.0 4.0 DTNB试剂0.4 0.4 0.4 0.4 0.4 0.4 0.4 GSH浓度μg/2ml 0 1 2 4 6 8 10 2.提取 取材后,称取0.2g样品置于研钵中,加入少量5%偏磷酸研磨成匀浆后,定容至6ml, 8000转离心10min。收集上清液来测定谷胱甘肽含量,测量提取液体积。 3.测定 取上清液2ml,显色,操作同标准曲线。重复3次。 显色反应后,分别记录样品管混合液的吸光度和空白对照管反应混合液的吸光度。根据吸光度差值,从标准曲线上查出相应的还原型谷胱甘肽量,计算还原型谷胱甘肽含量(μmol/g)。 4.计算 GSH含量(μmol/g)=(C x×V t)/ (FW×V S) 式中,C x为2ml样品中GSH的含量(μg);V t为样品提取液总体积(ml);V s为显色时样品液体积(ml);FW为样品质量(g)。 【实验结果】 1.标准曲线 试管编号 1 2 3 4 5 6 7 GSH浓度(μg/2ml)0 1 2 4 6 8 10 吸光度值A 0 0.067 0.134 0.314 0.452 0.579 0.723 以GSH浓度(μg/2ml)为横坐标,吸光度值为纵坐标,建立标准曲线。
实验一不同方法提取谷胱甘肽的比较 一、实验目的 1、掌握从干酵母中粗提谷胱甘肽的各种方法。 2、掌握还原型谷胱甘肽定量的方法。 二、实验原理 谷胱甘肽是种重要的三肽,以还原型(GSH)和氧化型(GSSG)广泛的存在于动、植物及微生物。在生物体内起作用的主要是GSH,是细胞内主要的还原性物质,能保护细胞免受氧化性、毒害性化合物和辐射的伤害,还是酶的辅因子。GSH在临床上是重要的解毒药物。 谷胱甘肽是小分子物质,水中溶解度较大,细胞表面出现裂缝就能分散到溶剂中,故可用一些温和的方法提取。 本实验采用热处理、冰冻处理、酸处理、有机溶剂处理等方法提取酵母细胞中的谷胱甘肽,比较最后的得率,探讨各种提取方法的优点和缺点。 三、实验器材、材料和试剂 1、器材 冰箱,离心机,水浴锅,电炉,滴定管,烧杯,玻棒,研钵。 2、实验材料 活性干酵母,2%偏磷酸,5%碘化钾,0.0001mol/l碘酸钾溶液,淀粉指示剂, 乙酸:乙醇(2:1),36%乙酸溶液。 四、实验步骤 1、热水抽提: 1g干酵母与5ml水混合,加15ml沸水,置100℃水浴保温10min,立即放入冰水速冷,取10ml离心,取5ml上清滴定,得滴定体积V1。 2、冷冻研磨后有机酸搅拌提取: 1g干酵母先在研钵中研细,与10ml水混合,-20℃冷冻成半固体状,研磨5min转入小烧杯,加10ml 36%乙酸搅拌15min,取10ml离心,取5ml上清滴定,得滴定体积V2。 3、酸热处理: 1g干酵母加20ml 2%偏磷酸,60℃水浴中搅拌抽提15min,置冰水速冷,取10ml离心,取5ml上清滴定,得滴定体积V3。 4、有机混合液处理: 1g干酵母加20ml有机混合液(甲酸:乙醇=2:1),室温搅拌抽提15min,置冰水速冷,取10ml离心,取5ml上清滴定,得滴定体积V4。 5、碘量法测定: 取5ml待测样品,置于250ml锥形瓶中,加入5ml2%偏磷酸溶液、1ml5%碘化钾溶液和2滴淀粉指示剂,用0.0001mol/L的碘酸钾滴定至溶液由无色变为蓝色为止。 KIO3+5KI+6HPO3→3I2 +6KPO3 +3H2O 五、结果及分析 1.将各种方法所消耗的碘酸钾的体积数添入下表 2.比较本实验四种提取酵母中谷胱甘肽的方法的优缺点。 六、注意事项 1、待测定的谷胱甘肽提取液置4℃冰箱保存,防止氧化。 2、酸性溶液中,淀粉会水解,使滴定终点的颜色发生变化,故滴定操作要快速完成。
含谷胱甘肽最多的食物 谷胱甘肽是一种对人的身体特别有好处的物质,因为在延缓衰老解读美白抗肿瘤形成等方面都可以发挥出谷胱甘肽的作用。同时临床医学上也发明出了含有大量谷胱甘肽的药物,这些药物可以用于治疗结膜炎肝炎等疾病。在日常生活中含有谷胱甘肽的食物也有非常多,什么食物含的谷胱甘肽是最多的呢? 在很多水果中都含有谷胱甘肽,如番茄(俗称西红柿)、樱桃、圣女果(俗称小西红柿)等。所以,在日常生活中多吃些水果,是有益于延缓衰老、延年益寿的。 应用 谷胱甘肽具有广谱解毒作用,不仅可用于药物,更可作为功能性食品的基料,在延缓衰老、增强免疫力、抗肿瘤等功能性食品广泛应用。 临床药物 已人工研制开发出了谷胱甘肽药物,广泛应用于临床,除利用其巯基以螯合重金属、氟化物、芥子气等毒素中毒外,还用在肝炎、溶血性疾病以及角膜炎、白内障和视网膜疾病等,作为治疗或辅助治疗的药物。近年来,西方科学家,尤其是日本学者发现谷胱甘肽具有抑制艾滋病毒的功能。 最新研究还表明,GSH能够纠正乙酰胆碱、胆碱酯酶的不平衡,起到抗过敏作用,还可防止皮肤老化及色素沉着,减少黑色素的形成,改善皮肤抗氧化能力并使皮肤产生光泽,另外,GSH在治疗
眼角膜病及改善性功能方面也有很好作用。 与维生素C 另外,维生素C也是体内一种重要的抗氧化剂。由于维生素C 能可逆地加氢或脱氢,故维生素C在体内许多氧化还原反应中有重要作用。例如,许多酶的活性基团是巯基(-SH),维生素C能够维持-SH处于还原状态而保持酶的活性;维生素C可以使氧化型谷胱甘肽转变为还原型谷胱甘肽(GSH),使机体代谢产生的过氧化氢(H2O2)还原;维生素C还可保护维生素A、E及某些B族维生素免受氧化。因此,运用谷胱甘肽时,与维生素C并用,能够提高其功效。 食品 添加谷胱甘肽可起到意想不到的作用 1、加入到面制品中,可起到还原作用。不仅使制造面包的时间缩短至原来的二分之一或三分之一,劳动条件大幅度改善,并起到食品营养的强化作用及其他功能。 2、将其加入到酸奶和婴幼儿食品中,相当于维生素C,可起到稳定剂的作用。 3、将其拌到鱼糕中,可防止色泽加深。 4、加到肉制品和干酪等食品中,具有强化风味的效果。
谷胱甘肽还原酶检测试剂简介 谷胱甘肽还原酶的作用: 一、谷胱甘肽还原酶(GR)在人类细胞中具有极其重要的生理功能,广泛存在于人体肝、肾、心红细胞、单核巨噬细胞等组织细胞中。它可及时地清除人体代谢过程中产生的氧自由基(OFR),是维持细胞中还原型谷胱甘肽(GSH)含量的主要黄素酶。对保护肝细胞膜完整具有非常重要的作用意义。 在《临床肝病实验诊断学》和《临床检验诊断解析》中明确标示,血清谷胱甘肽还原酶活性测定可用于协助诊断肝脏疾病,血清谷胱甘肽还原酶活性上升可以辅助诊断肝炎、肝硬化、梗阻性黄疸及相当数量引发的肝肿瘤。原发性肝细胞癌和广泛转移性肝肿瘤时,血清谷胱甘肽还原酶活性明显升高,急性病毒性肝炎或中毒性肝炎中度升高,而肝硬化是血清GR轻度升高。 二:检测谷胱甘肽还原酶的临床意义 1、急性肝炎早期阶段,血清谷胱甘肽还原酶敏感性最高,可用于肝损的早期检测; 2、急性肝炎患者GR比转氨酶更早增加达到峰值,早早期肝脏损伤判断的首选指标; 3、GR有助于判断亚临床DILI,提高临床DILI的诊断率 4、不同于ALT和AST在肝细胞膜破裂和线粒体破裂时才能检测出来,GR填补肝细胞受损早期自我修复阶段至破裂进程中诊断的空白,将更有利于早期肝炎的诊断和治疗
三、临床解读: 谷胱甘肽和谷丙、谷草在化验单上的具体解读,谷胱甘肽的血清血浆正常值是33-73U/L,共有四种情况。 1、谷胱甘肽指标升高,谷丙和谷草指标正常,提示有肝损伤的风险,建议加强对肝脏的检测频率,有利于发现早期肝损伤。 2、谷胱与谷丙,谷草同时升高,提示进入肝损伤爆发期,建议临床治疗措施干预。 3、谷胱甘肽升高,谷丙、谷草下降,提示正在进行肝损伤修复,可以结合三者评估临床治疗情况。 4、当三者都出现下降,情况有两种极端提示:(1)是修复完成,临床好转。(2)是重型肝炎出现严重情况,出现胆酶分离现象。 另外一种是红细胞的检测,正常值4.7-13.2U/gHb 红细胞主要针对“蚕豆病”和遗传性伯氨喹溶血病人,谷胱甘肽还原酶降低,红细胞的细胞膜容易被氧化和分解,导致溶血性贫血和溶血性黄疸。
总谷胱甘肽(T-GSH)检测试剂盒(DTNB 速率比色法) 简介: 谷胱甘肽(glutathione ,GSH)存在于几乎身体的每一个细胞,参与细胞许多功能活动,是一种氧自由基消除剂。还原型谷胱甘肽(GSH)是一种含γ-酰胺键和巯基的三肽,由谷氨酸、半胱氨酸及甘氨酸组成,能可逆的转变为氧化型谷胱甘肽(GSSG),其存在形式会随着细胞内代谢的情况而发生相互转变。 总谷胱甘肽(T-GSH)检测试剂盒(DTNB 速率微板法)(T otal Glutathione Assay Kit)是一种简单易行的检测总谷胱甘肽(T-GSH)的试剂盒,其检测原理是谷胱甘肽还原酶把氧化型谷胱甘肽(GSSG)还原成还原型谷胱甘肽(GSH),由GSSG 还原成的GSH 和样品本身含有的GSH 都与发色底物DTNB 反应,生成黄色的TNB 和GSSG 。该试剂盒可用于检测血浆、血清、组织、细胞等样品中总谷胱甘肽(T-GSH)含量。该试剂盒仅用于科研,不用于临床诊断或其他用途。 组成: 操作步骤(仅供参考): 1、 配制GSH 标准储存液:取10mg 还原型谷胱甘肽(GSH)标准加入3.25ml ddH 2O ,溶 解并混匀,即为还原型GSH 标准储存液(10mM)。一部分立即使用,其余适当分装后-20℃保存。 2、 配制50×GSH 还原酶:按GSH 还原酶原液:GSH assay buffer =1:49的比例混合, 即为50×GSH 还原酶。-20℃保存,3个月有效。 3、 配制T-GSH 检测工作液:按下表配制T-GSH 检测工作液。 1个样品 10个样品 50个样品 GSH assay buffer 1.6ml 16ml 80ml DTNB 储存液 5μl 50μl 250μl 编号 名称 TO1049 100T Storage 试剂(A): 还原型谷胱甘肽(GSH)标准 10mg 4℃ 避光 试剂(B): GSH assay buffer 250ml RT 试剂(D): 蛋白沉淀剂 4g RT 避光 试剂(E): NADPH 10mg -20℃ 避光 试剂(F): DMSO 1.5ml RT 避光 试剂(G): ddH 2O 50ml RT 避光 使用说明书 1份
人谷胱甘肽(GSH)酶联免疫分析 试剂盒使用说明书 厦门慧嘉生物科技有限公司 本试剂仅供研究使用目的:本试剂盒用于测定人血清,血浆及相关液体样本中谷胱甘肽(GSH)的含量。 实验原理: 本试剂盒应用双抗体夹心法测定标本中人谷胱甘肽(GSH)水平。用纯化的人谷胱甘肽(GSH)抗体包被微孔板,制成固相抗体,往包被单抗的微孔中加入谷胱甘肽(GSH),再与HRP标记的谷胱甘肽(GSH)抗体结合,形成抗体-抗原-酶标抗体复合物,经过彻底洗涤后加底物TMB显色。TMB在HRP酶的催化下转化成蓝色,并在酸的作用下转化成最终的黄色。颜色的深浅和样品中的谷胱甘肽(GSH)呈正相关。用酶标仪在450nm波长下测定吸光度(OD值),通过标准曲线计算样品中人谷胱甘肽(GSH)的含量。 样本处理及要求: 1. 血清:室温血液自然凝固10-20分钟,离心20分钟左右(2000-3000转/分)。仔细收集上 清,保存过程中如出现沉淀,应再次离心。 2. 血浆:应根据标本的要求选择EDTA或柠檬酸钠作为抗凝剂,混合10-20分钟后,离心 20分钟左右(2000-3000转/分)。仔细收集上清,保存过程中如有沉淀形成,应该再次离心。 3. 尿液:用无菌管收集,离心20分钟左右(2000-3000转/分)。仔细收集上清,保存过程
中如有沉淀形成,应再次离心。胸腹水、脑脊液参照实行。 4. 细胞培养上清:检测分泌性的成份时,用无菌管收集。离心20分钟左右(2000-3000转/ 分)。仔细收集上清。检测细胞内的成份时,用PBS(PH7.2-7.4)稀释细胞悬液,细胞浓度达到100万/ml左右。通过反复冻融,以使细胞破坏并放出细胞内成份。离心20分钟左右(2000-3000转/分)。仔细收集上清。保存过程中如有沉淀形成,应再次离心。5. 组织标本:切割标本后,称取重量。加入一定量的PBS,PH7.4。用液氮迅速冷冻保存备 用。标本融化后仍然保持2-8℃的温度。加入一定量的PBS(PH7.4),用手工或匀浆器将标本匀浆充分。离心20分钟左右(2000-3000转/分)。仔细收集上清。分装后一份待检测,其余冷冻备用。 6. 标本采集后尽早进行提取,提取按相关文献进行,提取后应尽快进行实验。若不能马上 进行试验,可将标本放于-20℃保存,但应避免反复冻融. 7. 不能检测含NaN3的样品,因NaN3抑制辣根过氧化物酶的(HRP)活性。 操作步骤: 1.标准品的稀释与加样:在酶标包被板上设标准品孔10孔,在第一、第二孔中分别加标 准品100μl,然后在第一、第二孔中加标准品稀释液50μl,混匀;然后从第一孔、第二孔中各取100μl分别加到第三孔和第四孔,再在第三、第四孔分别加标准品稀释液50μl,混匀;然后在第三孔和第四孔中先各取50μl弃掉,再各取50μl分别加到第五、第六孔中,再在第五、第六孔中分别加标准品稀释液50ul,混匀;混匀后从第五、第六孔中各取50μl分别加到第七、第八孔中,再在第七、第八孔中分别加标准品稀释液50μl,混匀后从第七、第八孔中分别取50μl加到第九、第十孔中,再在第九第十孔分别加标准品稀释液50μl,混匀后从第九第十孔中各取50μl弃掉。(稀释后各孔加样量都为50μl,浓度分别为60 ng/L,40 ng/L,20 ng/L,10 ng/L,5 ng/L)。 2.加样:分别设空白孔(空白对照孔不加样品及酶标试剂,其余各步操作相同)、待测样 品孔。在酶标包被板上待测样品孔中先加样品稀释液40μl,然后再加待测样品10μl(样品最终稀释度为5倍)。加样将样品加于酶标板孔底部,尽量不触及孔壁,轻轻晃动混匀。 3.温育:用封板膜封板后置37℃温育30分钟。 4.配液:将30(48T的20倍)倍浓缩洗涤液用蒸馏水30(48T的20倍)倍稀释后备用。 5.洗涤:小心揭掉封板膜,弃去液体,甩干,每孔加满洗涤液,静置30秒后弃去,如此 重复5次,拍干。 6.加酶:每孔加入酶标试剂50μl,空白孔除外。 7.温育:操作同3。 8.洗涤:操作同5。 9.显色:每孔先加入显色剂A50μl,再加入显色剂B50μl,轻轻震荡混匀,37℃避光显色 15分钟. 10.终止:每孔加终止液50μl,终止反应(此时蓝色立转黄色)。 11.测定:以空白空调零,450nm波长依序测量各孔的吸光度(OD值)。测定应在加终止 液后15分钟以内进行。 注意事项: 1.试剂盒从冷藏环境中取出应在室温平衡15-30分钟后方可使用,酶标包被板开封后如未用完,板条应装入密封袋中保存。 2.浓洗涤液可能会有结晶析出,稀释时可在水浴中加温助溶,洗涤时不影响结果。
植物生理学模块实验指导 玲主编 科学 还原型谷胱甘肽含量的测定方法(分光光度计法) 【实验目的】 了解植物组中中抗坏血酸-谷胱甘肽循环代过程,学习还原型谷胱甘肽含量的测定原理和方法。 【实验原理】 谷胱甘肽是有谷氨酸(Glu)、半胱氨酸(Gly)组成的天然三肽,是一种含巯基(—SH)的化合物,广泛存在于动物组织、植物组织、微生物和酵母中。谷胱甘肽能和5,5’-二硫代-双-(2-硝基苯甲酸)(5,5’-dithiobis-2-nitrobenoic acid,DTNB)反应产生2-硝基-5-巯基苯甲酸和谷胱甘肽二硫化物(GSSG)。2-硝基-5-巯基苯甲酸为一黄色产物,在波长412nm处具有最大光吸收。因此,利用分光光度计法可测定样品中谷胱甘肽的含量。 【器材与试剂】 1.实验仪器与用具 研钵、高速冷冻离心机、微量移液枪、离心管、试管、水浴锅、容量瓶(100ml、200ml、1000ml)、分光光度计 2.实验试剂 50g/L三氯乙酸(TCA)溶液(含5mmol/L Na 2 -EDTA):称取5g三氯乙酸,用蒸馏水溶 解稀释至100ml。再称取186mg Na 2-EDTA·2H 2 O,加入到100ml 50g/L三氯乙酸溶液中溶解。 0.1mol/L磷酸钠溶液缓冲液(pH7.7):配制方法见附录。 0.1mol/L(pH6.8)磷酸钠缓冲液:配制方法见附录。 4mmol/L二硫代硝基苯甲酸(5,5’-dithiobis-2-nitrobenoic acid,DTNB)溶液:称取15.8mg DTNB,用0.1mol/L、pH6.8磷酸缓冲液溶解,定容至10ml,混匀,4℃保存。现用现配。
还原型谷胱甘肽(GSH) 还原型谷胱甘肽(GSH) 还原型谷胱甘肽(GSH) 还原型谷胱甘肽(GSH) 中文别名:L-谷胱甘肽;5-L-谷氨酰-L-半胱氨酰甘氨酸;还原型谷胱甘肽;谷胱甘肽(还原型) 产品信息: 【分子式】C10H17N3O6S 【分子量】307.32 【CAS号】70-18-8 【外观】白色结晶性粉末 【产品规格】 1、含量:98%-101% 还原型谷胱甘肽原料药。 2、含量:8%,15%,50% 的谷胱甘肽酵母抽提物。 【产品的应用】 谷胱甘肽广泛应用在医药、保健品、食品添加剂、饮料、化妆品、生化试剂等领域,8%,15%,50% 的谷胱甘肽酵母抽提物,更是富含蛋白质、氨基酸、核酸、多种有机酸及丰富的B族维生素,能够提供更加全面的营养。 【产品包装与贮存】 1、1kg,5kg,10kg,20kg或25kg纸桶。 2、置于阴凉、干燥、通风处密封存放。 产品概述: 1、谷胱甘肽(GSH)是由谷氨酸(Glu)、半胱氨酸(Cys)和甘氨酸(Gly)通过肽键缩合而成的非蛋白巯基三肽化合物,是用途极广泛的活性短肽。 2、谷胱甘肽溶于水、稀醇、液氨和二甲基甲酰胺,而不溶于乙醇、醚和丙酮。谷胱甘肽的固体状态较为稳定,其水溶液在空气中易被氧化。 产品功能: 1、谷胱甘肽(GSH)是神奇的抗氧化剂 谷胱甘肽是含巯基的抗氧化剂,能够清除影响人体健康的自由基,现代医学认为,自由基是导致衰老和疾病的主要原因之一。人体细胞的抗氧化系统中含量最多和最重要的就是谷胱甘肽,谷胱甘肽是清除自由基的主力军,被科学家誉为“大师级抗氧化剂”和“谷胱甘肽防御系统”。谷胱甘肽不仅直接参于清除自由基,还对外来的抗氧化剂如维生素C和E等起到调节作用,保持它们的活性(还原)状态。 自由基是人体细胞代谢过程中产生的一类高化学活性的中间物质,它能够攻击蛋白质、DNA和细胞膜中的脂质大分子,破坏这些生物大分子的生理功能,使细胞膜变硬变脆而丧失功能,缩短细胞的寿命;能导致细胞膜形成空隙,使致病菌、病毒等侵入细胞,进一步破坏核膜,使遗传物质暴露,致使遗传物质受损,引起突变和破坏;加重免疫细胞受损,使受损的机体,免疫力低下,许多病症更容易发生。1956年,哈曼教授首先提出了自由基理论,他发现长期在强日光下作业的渔夫寿命比较短,进一步研究证明紫外线会刺激体内产生自由基,而自由基会促进生理周期老化,使死亡提前到来。 在正常状态下,人体细胞内的谷胱甘肽能够及时和人体代谢过程中产生的自由基结合,转化为低活性的物质,消除自由基对人体的伤害。但是,随着人年龄的增长,人体自身产生谷胱甘肽的能力变弱,产生的谷胱甘肽的量不足以及时清除掉人体内的自由基,多余的自由基开始破坏细胞内的生物大分子物质,细胞功能受到影响,人体开始出现衰老,疾病开始增多;另外,一些外界因素:如紫外线辐射,饮酒,吸烟,环境污染,某些药物等,也会导致人体产生过多的自由基,会加大人体内谷胱甘肽的需求,一旦谷胱甘肽供应不足,多余的自由基就会损害人的健康,影响人的寿命。
谷胱甘肽的简便测定法 药物分析杂志 2000年第1期第20卷研究简报 作者:赵旭东魏东芝万群俞俊棠单位:赵旭东魏东芝万群俞俊棠(华东理工大学生物反应器工 程国家重点实验室上海200237) 关键词:谷胱甘肽、甲醛、半胱氨酸、DTNB 摘要:目的:建立一种快速简便测定谷胱甘肽的新方法。方法:样品1式2份,pH 8.0条件下分别和甲醛反应2 min和60 min,各取1 mL加入5 mL DTNB溶液,25 ℃反应5 min后分别测定在波长412 nm的吸光度,算出2者的差值ΔA,代入标准曲线计算得出谷胱甘肽含量。结果:谷胱甘肽浓度在0.19~0.95 g·L-1之间线性关系良好,回归方程为:Y=0.715 4X-0.000 4,r=0.999 9,最大误差不超过6%。结论:方法成本低廉,简单易行,特别适合于有干扰物质存在时还原型谷胱甘肽浓度的分析。 A Simple Method for Rapid Determination of Reduced Glutathione Zhao Xudong Wei Dongzhi Wan Qun Yu Juntang (State Key Laboratory of Bioreactor Engineering, Institute of Biochemistry, East China University of Science and Technology, Shanghai 200237)
Abstract:Objective:A new simple method for rapid determination of reduced glutathione in the presence of other thiols is developed based on the reactions of formaldehyde with glutathione and interefering substances.Method:After each aliquot of two same samples reacts with formaldehyde for 2 and 60 min respectively, 1 mL of each solution is added to 5 mL DTNB and reacts for 5 min at 25 ℃. The absorbance is measured immediately at wavelength 412 nm. The difference between two absorbance(ΔA=A2 min-A60 min)is calculated, concentration of glutathione can be obtained from standard curve.Result:There is a good linearity between 0.19 to 0.95 g·L-1 glutathione. Regression equation:Y=0.715 4X-0.000 4,r=0.999 9,maximum deviation is less than 6%.Conclusion:The method is cheap, simple, practicable and is applicable to assay of reduced glutathione in the presence of other interefering substances. Key words:glutathione, formaldehyde, cysteine, DTNB▲ 谷胱甘肽(GSH)是由谷氨酸、半胱氨酸(Cys)和甘氨酸组成的天然三肽,用途广泛。利用基因工程微生物生物合成方法是生产谷胱甘肽的主要方式。作为前体之一,半胱氨酸的浓度较高,对谷胱甘肽的测定有干扰。已有几种方法用于半胱氨酸存在时谷胱甘肽的测定:酶分析方法[1,2]可测高达1 000倍半胱氨酸存在时谷胱甘肽的含量,结果较准确,但需价格昂贵的辅酶Ⅱ和谷胱甘肽还原酶,并且后者活力变