
免疫胶体金技术(Immune colloidal gold technique)
文章来源: 文章作者: 发布时间:2007-04-24 字体: [大 中 小]
(一) 原理 免疫胶体金技术是以胶体金作为示踪标志物应用于抗原抗体的一种新型的免疫标记技术。胶体金是由氯金酸(HAuCl 4)在还原剂如白磷、抗坏血酸、枸橼酸钠、鞣酸等作用下,聚合成为特定大小的金颗粒,并由
于静电作用成为一种稳定的胶体状态,称为胶体金。胶体金在弱碱环境下带负电荷,可与蛋白质分子的正电荷基团形成牢固的结合,由于这种结合是静电结合,所以不影响蛋白质的生物特性。
胶体金除了与蛋白质结合以外,还可以与许多其它生物大分子结合,如SPA 、PHA 、ConA 等。根据胶体金的一些物理性状,如高电子密度、颗粒大小、形状及颜色反应,加上结合物的免疫和生物学特性,因而使胶体金广泛地应用于免疫学、组织学、病理学和细胞生物学等领域。
(二) 胶体金的制备
根据不同的还原剂可以制备大小不同的胶体金颗粒。常用来制备胶体金颗粒的方法如下。
1.枸橼酸三钠还原法
(1)10nm 胶体金粒的制备:取0.01%HAuCl 4水溶液100ml ,加入1%枸橼酸三钠水溶液3ml ,加热煮沸30
min ,冷却至4℃,溶液呈红色。
(2)15nm 胶体金颗粒的制备:取0.01%HAuCl 4水溶液100ml ,加入1%枸橼酸三钠水溶液2ml ,加热煮沸
15min ~30min ,直至颜色变红。冷却后加入0.1Mol/L K 2CO 30.5ml ,混匀即可。
(3)15nm 、18nm ~20nm 、30nm 或50nm 胶体金颗粒的制备:取0.01%HAuCl 4水溶液100ml ,加热煮沸。根
据需要迅速加入1%枸橼酸三钠水溶液4ml 、2.5ml 、1ml 或0.75ml ,继续煮沸约5min ,出现橙红色。这样制成的胶体金颗粒则分别为15nm 、18~20nm 、30nm 和50nm 。
2.鞣酸—枸橼酸钠还原法
A 液:1%HAuCl 4水溶液1ml 加入79ml 双馏水中混匀。
B 液:1%枸橼酸三钠4ml ,1%鞣酸0.7ml ,0.1Mol/L K 2CO 3液0.2ml ,混合,加入双馏水至20ml 。
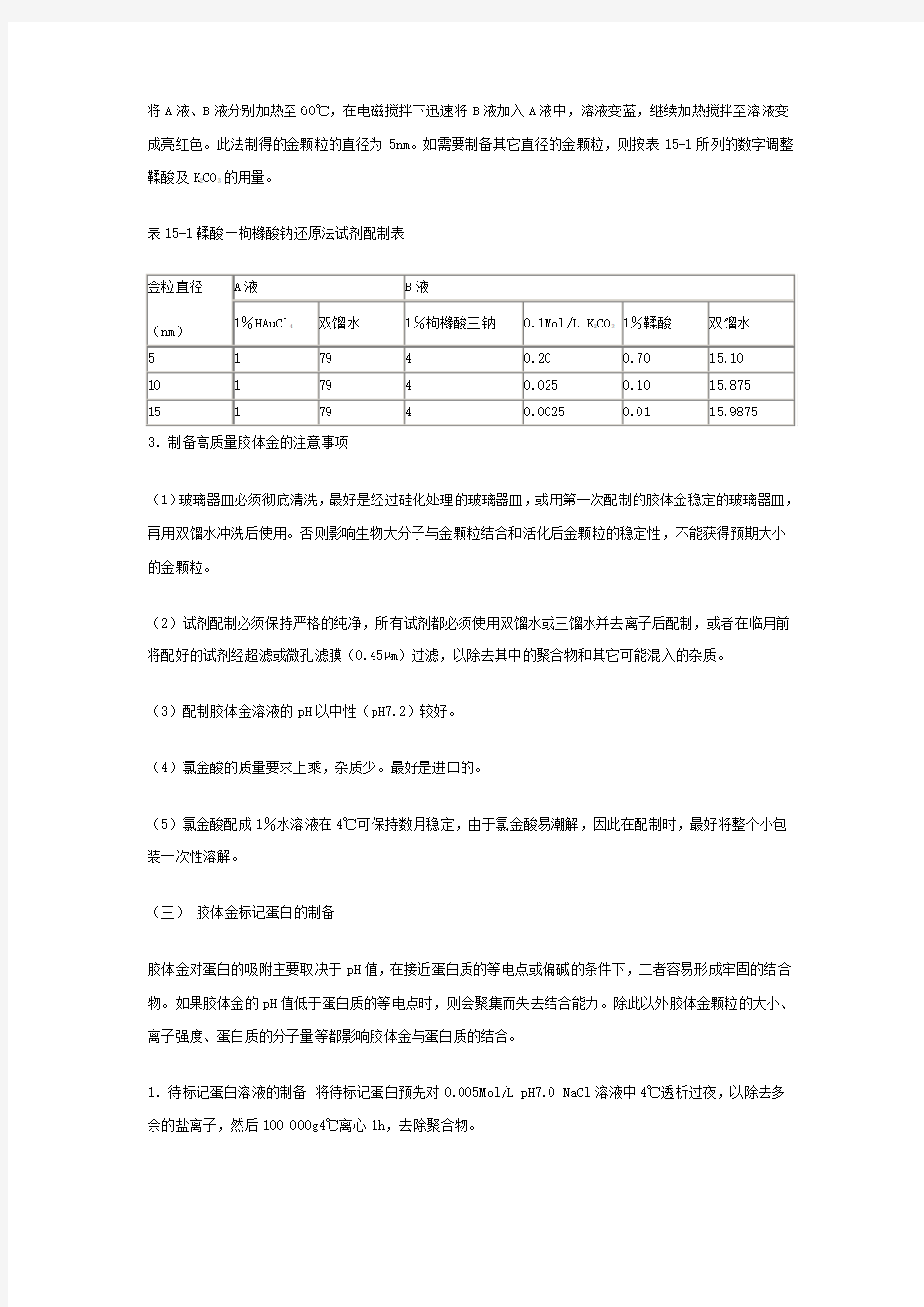
将A液、B液分别加热至60℃,在电磁搅拌下迅速将B液加入A液中,溶液变蓝,继续加热搅拌至溶液变成亮红色。此法制得的金颗粒的直径为5nm。如需要制备其它直径的金颗粒,则按表15-1所列的数字调整
鞣酸及K
2CO
3
的用量。
表15-1鞣酸—枸橼酸钠还原法试剂配制表
3.制备高质量胶体金的注意事项
(1)玻璃器皿必须彻底清洗,最好是经过硅化处理的玻璃器皿,或用第一次配制的胶体金稳定的玻璃器皿,再用双馏水冲洗后使用。否则影响生物大分子与金颗粒结合和活化后金颗粒的稳定性,不能获得预期大小的金颗粒。
(2)试剂配制必须保持严格的纯净,所有试剂都必须使用双馏水或三馏水并去离子后配制,或者在临用前将配好的试剂经超滤或微孔滤膜(0.45μm)过滤,以除去其中的聚合物和其它可能混入的杂质。
(3)配制胶体金溶液的pH以中性(pH7.2)较好。
(4)氯金酸的质量要求上乘,杂质少。最好是进口的。
(5)氯金酸配成1%水溶液在4℃可保持数月稳定,由于氯金酸易潮解,因此在配制时,最好将整个小包装一次性溶解。
(三)胶体金标记蛋白的制备
胶体金对蛋白的吸附主要取决于pH值,在接近蛋白质的等电点或偏碱的条件下,二者容易形成牢固的结合物。如果胶体金的pH值低于蛋白质的等电点时,则会聚集而失去结合能力。除此以外胶体金颗粒的大小、离子强度、蛋白质的分子量等都影响胶体金与蛋白质的结合。
1.待标记蛋白溶液的制备将待标记蛋白预先对0.005Mol/L pH7.0 NaCl溶液中4℃透析过夜,以除去多余的盐离子,然后100 000g4℃离心1h,去除聚合物。
2.待标胶体金溶液的准备以0.1Mol/L K
2CO
3
或0.1Mol/L HCl调胶体金液的pH值。标记IgG时,调至9.
0;标记McAb时,调至8.2;标记亲和层析抗体时,调至7.6;标记SPA时,调至5.9~6.2;标记ConA时,调至8.0;标记亲和素时,调至9~10。
由于胶体金溶液可能损坏pH计的电板,因此,在调节pH时,采用精密pH试纸测定为宜。
3.胶体金与标记蛋白用量之比的确定
(1)根据待标记蛋白的要求,将胶体金调好pH之后,分装10管,每管1ml。
(2)将标记蛋白(以IgG为例)以0.005Mol/L pH9.0硼酸盐缓冲液做系列稀释为5μg/ml~50μg/ml,分别取1ml,加入上列金胶溶液中,混匀。对照管只加1ml稀释液。
(3)5min后,在上述各管中加入0.1ml 10%NaCl溶液,混匀后静置2h,观察结果。
(4)结果观察,对照管(未加蛋白质)和加入蛋白质的量不足以稳定胶体金的各管,均呈现出由红变蓝的聚沉现象;而加入蛋白量达到或超过最低稳定量的各管仍保持红色不变。以稳定1ml胶体金溶液红色不变的最低蛋白质用量,即为该标记蛋白质的最低用量,在实际工作中,可适当增加10%~20%。
4.胶体金与蛋白质(IgG)的结合将胶体金和IgG溶液分别以0.1Mol/L K
2CO
3
调pH至9.0,电磁搅拌IgG
溶液,加入胶体金溶液,继续搅拌10min,加入一定量的稳定剂以防止抗体蛋白与胶体金聚合发生沉淀。常用稳定剂是5%胎牛血清(BSA)和1%聚乙二醇(分子量20KD)。加入的量:5%BSA使溶液终浓度为1%;1%聚乙二醇加至总溶液的1/10。
5.胶体金标记蛋白的纯化
(1)超速离心法:根据胶体金颗粒的大小,标记蛋白的种类及稳定剂的不同选用不同的离心速度和离心时间。
用BSA做稳定剂的胶体金—羊抗兔IgG结合物可先低速离心(20nm金胶粒用1 200r/min,5nm金胶粒用1 800r/min)20min,弃去凝聚的沉淀。然后将5nm胶体金结合物用6 000g,4℃离心1h;20nm~40nm胶体
金结合物,14 000g,4℃离心1h。仔细吸出上清,沉淀物用含1%BSA的PB液(含0.02%NaN
3
),将沉淀重悬为原体积的1/10,4℃保存。如在结合物内加50%甘油可贮存于-18℃保存一年以上。
为了得到颗粒均一的免疫金试剂,可将上述初步纯化的结合物再进一步用10%~30%蔗糖或甘油进行密度梯度离心,分带收集不同梯度的胶体金与蛋白的结合物。
(2)凝胶过滤法:此法只适用于以BSA作稳定剂的胶体金蛋白结合物的纯化。将胶体金蛋白结合物装入透
析袋,在硅胶中脱水浓缩至原体积的1/5~1/10。再经1 500r/min离心20min。取上清加至Sephacryl S-400(丙烯葡聚糖凝胶S-400)层析柱分别纯化。层析柱为0.8 cm×20cm,加样量为床体积的1/10,以
0.02Mol/L PBS液洗脱(内含0.1%BSA,0.05%NaN
3
,pH8.2者用IgG标记物),流速为8ml/h。按红色深浅分管收集洗脱液。一般先滤出的液体为微黄色,有时略混浊,内含大颗粒聚合物等杂质。继之为纯化的胶体金蛋白结合物,随浓度的增加而红色逐渐加深,清亮透明,最后洗脱出略带黄色的为标记的蛋白组分。将纯化的胶体金蛋白结合物过滤除菌、分装,4℃保存。最终可得到70%~80%的产量。
6.胶体金蛋白结合物的质量鉴定
(1)胶体金颗粒平均直径的测量:用支持膜的镍网(铜网也可)蘸取金标蛋白试剂,自然干燥后直接在透射电镜下观察。或用醋酸铀复染后观察。计算100个金颗粒的平均直径。
(2)胶体金溶液的OD
520
nm值测定:胶体金颗粒在波长510nm~550nm之间出现最大吸收值峰。用0.02Mol
/L pH8.2 PBS液(含1%BSA,0.02%NaN
3)将胶体金蛋白试剂作1︰20稀释,OD
520
=0.25左右。一般应用
液的OD
520
应为0.2~0.4。
(3)金标记蛋白的特异性与敏感性测定:采用微孔滤膜免疫金银染色法(MF-IGSSA)。将可溶性抗原(或抗体)吸附于载体上(滤纸、硝酸纤维膜、微孔滤膜),用胶体金标记的抗体(或抗原)以直接或间接染色法并经银显影来检测相应的抗原或抗体,对金标记蛋白的特异性和敏感性进行鉴定。
(四)胶体金标记技术在免疫学中的应用
胶体金标记技术由于标记物的制备简便,方法敏感、特异,不需要使用放射性同位素,或有潜在致癌物质的酶显色底物,也不要荧光显微镜,它的应用范围广,除应用于光镜或电镜的免疫组化法外,更广泛地应用于各种液相免疫测定和固相免疫分析以及流式细胞术等。
1.液相免疫测定:将胶体金与抗体结合,建立微量凝集试验检测相应的抗原,如间接血凝一样,用肉眼可直接观察到凝集颗粒。利用免疫学反应时金颗粒凝聚导致颜色减退的原理,建立均相溶胶颗粒免疫测定法(Sol particle immunoassay ,SPIA)已成功地应用于PCG的检测,直接应用分光光度计进行定量分析。2.金标记流式细胞术:胶体金可以明显改变红色激光的散射角,利用胶体金标记的羊抗鼠Ig抗体应用于流式细胞术,分析不同类型细胞的表面抗原,结果胶体金标记的细胞在波长632nm时,90度散射角可放大10倍以上,同时不影响细胞活性。而且与荧光素共同标记,彼此互不干扰。
3.胶体金固相免疫测定法
(1)斑点免疫金银染色法(Dot-IGS/IGSS)是将斑点ELISA与免疫胶体金结合起来的一种方法。将蛋白质抗原直接点样在硝酸纤维膜上,与特异性抗体反应后,再滴加胶体金标记的第二抗体,结果在抗原抗体反应处发生金颗粒聚集,形成肉眼可见的红色斑点,此称为斑点免疫金染色法(Dot-IGS)。此反应可通过银显影液增强,即斑点金银染色法(Dot-IGS/IGSS)。
(2)斑点金免疫渗滤测定法(dot immuno-gold filtration assay,DIGFA)此法原理完全同斑点免疫金染色法,只是在硝酸纤维膜下垫有吸水性强的垫料,即为渗滤装置。在加抗原(抗体)后,迅速加抗体(抗原),再加金标记第二抗体,由于有渗滤装置,反应很快,在数分钟内即可显出颜色反应。此方法已成功地应用于人的免疫缺陷病病毒(HIV)的检查和人血清中甲胎蛋白的检测。
1.免疫胶体金技术原理:胶体金用于标记的原理胶体金是一种负电荷的疏水胶,靠静电粒子相互排斥作用来维持稳定的胶体体系,其颗粒散在、红色,直径从几纳米到几十纳米不等。由于不同直径的胶体金的光散射各异,所以其溶胶颜色的深浅相应发生显著的变化,这就是胶体金用于被动凝集试验的基础。同时由于胶体金金颗粒对蛋白质有很强的吸附功能,可与SPA ,IGg,毒素、糖蛋白、酶、抗生素和激素等多种物质非共价结合,从而使其成为免疫反应的优良标记物。而且金颗粒还可催化银离子还原成金属银,因此在胶体金免疫测定时加入银染色液,能放大反应信号,大大增加测定的灵敏度。
胶体金颗粒带电情况抗体和金颗粒的耦联(图出处:IVD Technology)
胶体金免疫标记技术-蛋白-金复合体的制备
一般认为胶体金粒子表面为一层AuCl2,因此,粒子表面带有负电荷,这种负电荷粒子之间相互排斥,形成稳定悬浮的胶体金溶液。
金颗粒表面可以包被一层生物大分子(如蛋白)来稳定和保护这些粒子,以免受外来电解质的影响而相互凝聚在一起。胶体金粒子对蛋白的吸附作用取决于pH值,这是因蛋白的净电荷取决于溶液的pH值,在pH=pI时为中性。由于在pH=pI时蛋白溶解度最小,因此这时它水化程度最小,最溶液吸附到疏水的金粒子表面。但在实际的胶体金探针制备中,一般胶体金调整为pH=PI+0.5,这样蛋白带正电,有利于结合更稳定。
胶体金探针所用蛋白必须要经过前处理,其目的在于(1)去除高浓度的盐分,高浓度的盐分往往干扰蛋白与胶体金的吸附结合,或导致胶体金粒子的凝聚,这一步往往采用低浓度缓冲液中进行。(2)使蛋白分子尽量分散为单体,冻干蛋白或高浓度蛋白溶液中蛋白分子往往凝聚为多聚体大分子,可同时与多个胶体金粒子结合,影响标记的灵敏度和定量分析。(3)使蛋白具有适当的分子量。蛋白分子量过小(30 kD),形成的蛋白复合体往往是不稳定,可短时间内失活。而分子量过大时,被认为影响探针的灵敏度,特别是已知蛋白的结构与活性中心的情况下,去除对活性武影响的结构部分是提高标记灵敏度,延长探针寿命(防止凝集)的有效办法。把分子量过小的蛋白与其它蛋白(如BSA,牛血清蛋白等)结合后,能制备出稳定性更佳的探针。
当蛋白前处理完成后,接着要确定胶体金与蛋白结合的最佳pH值。对于理化性质不确定的蛋白这一步尤为重要。过量的蛋白与不同pH值得胶体金结合后,只有某一特定pH值能够形成结合最稳定的探针。在高浓度电解质(如NaCl)作用下不会凝聚。不同蛋白的适宜pH范围的宽窄大不相同。一般选择最小适宜pH 值为最佳pH值。但有些探针的实际情况并不完全如此,最稳定发探针并不完全代表活性最好。这要靠实验验证。
在确定最佳pH值后,最后要确定最小蛋白量,即能够形成稳定探针的蛋白的最小量。如果在制备探针时加入太多的蛋白,不仅造成浪费,而且更为严重的是容易造成探针凝聚,并严重影响标记活性。因为探针溶液中的游离蛋白容易抢先与标记位点结合,起到“封闭”(Blocking)作用,而胶体金探针标记不上。在标记位点希少、被标记物含量较少的情况下要特别注意。
这里需要特别指出的是,使用不同直径的胶体金与同一蛋白结合时,除了蛋白量完全不同外,往往最佳pH也有一定变化。
因此,在探针制备每一环节应随时监测探针对分布情况、负染结合及活性。
一、制备胶体金的准备 令狐文艳 (一)玻璃器皿的清洁 制备胶体金的成功与失败除试剂因素以外玻璃器皿清洁是非常关键的一步。如果玻璃器皿内不干净或者有灰尘落入就会干扰胶体金颗粒的生成,形成的颗粒大小不一,颜色微红、无色或混浊不透明。我们的经验是制备胶体金的所有玻璃器皿先用自来水把玻璃器皿上的灰尘流水冲洗干净,加入清洁液(重铬酸钾1000g,加入浓硫酸2500ml,加蒸馏水至10000ml)浸泡 24h,自来水洗净清洁液,然后每个玻璃器皿用洗洁剂洗3~4次,自来水冲洗掉洗洁剂,用蒸馏水洗3~4次,再用双蒸水把每个器皿洗3~4次,烤箱干燥后备用。通过此方法的处理玻璃器皿不需要硅化处理,而直接制备胶体金。也可用已经制备的胶体金溶液,用同等大不颗粒的金溶液去包被所用的玻璃器皿的表面,然后弃去,再用双蒸水洗净,即可使用,这样效果更好,因为减少了金颗粒的吸附作用。 (二)试剂的配制要求 按照Frens法还可以制备出其它不同颗粒大小的胶体金出来。许多研究证明用该法制备胶体金时金颗粒的大小是柠檬酸三钠
用量的函数,基本的规律是柠檬酸三钠用量多,胶体金颗粒直径小,柠檬酸三钠用量越少,腔体金颗粒直径越大。 (1)所有配制试剂的容器均按以上要求酸处理洗净,配制试剂用双蒸馏水或三蒸馏水。 (2)氯化金(HauCl4水溶液的配制:将lg的氯化金一次溶解于双蒸水中配成1%的水溶液。放在4”c冰箱内保存长达几个月至1年左右,仍保持稳定。 (3)白磷或黄磷乙醚溶液的配制:白磷在空气中易燃烧,要格外小心操作。把白磷在双蒸水中切成小块,放在滤纸上吸于水份后,迅速放入已准备好的乙醚中去,轻轻摇动,等完全溶解后即得饱和溶液。储藏于棕色密闭瓶内,放在阴凉处保存。柠檬酸三钠还原法(Frens 1973)此方法是由Frens在1973年创立的,制备程序很简单,胶体金的颗粒大小较一致,广为采用。该法一般先将0.01%的HAuCl4溶液加热至沸腾,迅速加入一定量1%柠檬酸三钠水溶液,开始有些蓝色,然后浅蓝、蓝色,再加热出现红色,煮沸7~10min出现透明的橙红色。各种颗粒的胶体金制备详见表5-2。表5-2 柠檬酸三钠用量与胶体金颗粒直径的关系
免疫层析试纸包被技术简介 试纸生产 过程中一般有三种 溶液的包被处理,即 质控溶液,检测溶 液,和结合物溶液 (胶体金)。质控和 检测溶液就是C/T 线上包被的溶液。 在免疫层 析试纸硝酸纤维素 膜表面进行 C/T线的包被,是试纸生产制作的关键环节之一。免疫诊断试剂中使用的硝酸纤维素膜有两类,一种是免疫渗滤产品用的,按孔径选择一般采用0.45um-1.2um的膜,与分子生物学中用的印迹转移膜一样。Whatman Schleicher & Schuell的膜属于纯采用100%的纯硝酸纤维素,蛋白结合能力较高。另一类即免疫层析用膜,一般按侧向流动速度来划分,常用的范围一般在120-180秒/4cm。目前市场上的硝酸 纤维素膜材以带塑料底衬 为主,也有部分的膜不带 底衬。不带底衬的膜需注 意膜面的正反面,其光滑 度有适当差别。 鉴于流动封闭技 术的普及,C/T线的包被 目前流行先将膜粘贴在塑 料支持底板上,然后直接 将塑料板放入仪器上进行 划线操作,干燥后进行其 他部分的贴板组装,这种 划膜工艺可简称为划板。 但部分产品的工艺要求先直接在膜上划好C/T线,然后用特定配方的溶液将膜进行浸泡封闭处理,干燥后再贴膜及其他部分材料,这种划膜工艺可简称为划膜。 在结合物溶液(胶体金)的包被上,较多的用户倾向于用气动喷头进行定量操作。在科研及研发项目中,往往喷一条线或几条线就够用了,因此在单维往复平台上一次喷一条线也可接受。鉴于胶体金膜切条宽度一般在 3--7mm,不方便一条条依次地在移动平台上固定和取放。因此在批量生产过程中,一般建议采用成片的胶体金垫,用三维平台往复来回地间隔喷线,一次即可喷出二三十条。此后将喷好的金干燥再裁切成条,这样的操作会效率高,适合规模生产。 在某些免疫层析试纸产品生产工艺中,层析膜材或样品垫膜材需要用特定溶液进行整平面包被,要求效果均匀,如层析膜和样品垫的特定封闭处理。
胶体金技术 问:检测cle ,金标记抗体扩大后,烘干后检测各项指标良好,但室温保存一天后,T 线下降很多是由什么原 因造成的?室内开除湿机,组装好的板子,在自封袋里加干燥剂。我烘干用了一整天,30 多个小时了,还有方法进行改进吗,这个抗体还能用来生产吗?经检测还是金子出了问题,我就是先少量做,找出各个值,然后才扩大的。我就是先3ml ,再10ml 。 T :(涛哥)那可能是生产放大过程控制的问题。重新试验,先小试,逐步放大。这就不行了啊,这还算不上生产扩大呢,怀疑误操作,重复试验试试,3ml 的、10ml 的都做一下。 0 是啊,有时标记完检测后,T 线就下降(比预实验) T :标记完检测就下降,说明你标记本身就有问题呗。你标记条件太脆弱,主要考虑你标记条件,重新优化下。 0 如果我再调整pH 值,抗体浓度,灵敏度就会达不到了 T:通过其他途径提高灵敏度。 问:请问为什么C 线包被3mg/ml 不出现条带,而2mg/ml 的就有条带出现呢? T:正常,从蛋白固定基本原理出发,好好想想。NC 结合蛋白的能力是有限的,其结合位点是会饱和的,假 设其结合能力仅仅为2mg ,你包被3mg ,那边必然有相当一部分是结合不牢固或者压根就没固定住的,样本层析之后,金标蛋白结合了这些不牢固的蛋白,就会流走,不会显色。检测线,也会有同样的情况,不过检测线包被过量的影响不止这么简单。我主要指夹心法。 0 一般调整膜上浓度时在湿法时调整还是干法时调整啊? 问:标记好的胶体金有沉淀是什么原因? T:常见的原因:标记条件不合适,封闭物质不纯,复溶液不合适都有可能,当然颗粒大了,也容易沉淀。 0 你们主要用什么方法摸索最佳PH 值? 1.用碳酸钾用量调整,搞一排,然后看变色和离心后现象,还有检测结果啊。 0 这样岂不是需要很多抗体?呵呵 2.标记又用不了多少抗体,又不是包膜。 0 离心后现象,怎么样的是理想的? 3.就是没有预期想要的略微蓬松有红色的沉淀,比如贴壁、黑点、离不干净等,离心速度时间也要选好。 0 是啊,之前就发现有点贴壁和黑点,我延长了离心时间也没用。 4.小号金子1ml 离心几分钟就够了。越大速度越低时间,这个速度和时间折中下自己调整。 问:不知道那些强假阳性有什么办法可以抑制? T:你加阻断剂试过没? 0试过几种,没有效果,能阻断C线,对T线基本没阻断。 T:照这么说的话既然是同一对抗体而且胶体金法临床假阳性率这么高,我觉得你这对抗体可能对某种因素太敏感了吧,ELISA 是共价标记胶体金是物理标记是会有差异。(涛) 0 现在就是找不到原因,那强阳漏检呢?其实也有试过好几个抗体配对,基本都是那样的结果 问:请教一下各位大虾,多抗标记的时候要注意哪些细节呢? T:尽量别标记多抗,实在是想标记多抗,把标记PH 提高点。 问:划线时的湿度条件是NC膜制备的要点之一,湿度应控制在45 %?65%,有文献支持吗? T:文献呢是有滴,不过NC 供应商也会给你建议滴,你自己也是可以探索滴,最终都是要以产业化需要为准。 1.主要膜吸收蛋白的时候要是湿度太低会比较疏水,不利于吸收,一般在40% 以上,膜在点之前在这个环境
一、制备胶体金的准备 (一)玻璃器皿的清洁 制备胶体金的成功与失败除试剂因素以外玻璃器皿清洁是非常关键的一步。如果玻璃器皿内不干净或者有灰尘落入就会干扰胶体金颗粒的生成,形成的颗粒大小不一,颜色微红、无色或混浊不透明。我们的经验是制备胶体金的所有玻璃器皿先用自来水把玻璃器皿上的灰尘流水冲洗干净,加入清洁液(重铬酸钾1000g,加入浓硫酸2500ml,加蒸馏水至10000ml)浸泡24h,自来水洗净清洁液,然后每个玻璃器皿用洗洁剂洗3~4次,自来水冲洗掉洗洁剂,用蒸馏水洗3~4次,再用双蒸水把每个器皿洗3~4次,烤箱干燥后备用。通过此方法的处理玻璃器皿不需要硅化处理,而直接制备胶体金。也可用已经制备的胶体金溶液,用同等大不颗粒的金溶液去包被所用的玻璃器皿的表面,然后弃去,再用双蒸水洗净,即可使用,这样效果更好,因为减少了金颗粒的吸附作用。 (二)试剂的配制要求 按照Frens法还可以制备出其它不同颗粒大小的胶体金出来。许多研究证明用该法制备胶体金时金颗粒的大小是柠檬酸三钠用量的函数,基本的规律是柠檬酸三钠用量多,胶体金颗粒直径小,柠檬酸三钠用量越少,腔体金颗粒直径越大。 (1)所有配制试剂的容器均按以上要求酸处理洗净,配制试剂用双蒸馏水或三蒸馏水。(2)氯化金(HauCl4水溶液的配制:将lg的氯化金一次溶解于双蒸水中配成1%的水溶液。放在4”c冰箱内保存长达几个月至1年左右,仍保持稳定。 (3)白磷或黄磷乙醚溶液的配制:白磷在空气中易燃烧,要格外小心操作。把白磷在双蒸水中切成小块,放在滤纸上吸于水份后,迅速放入已准备好的乙醚中去,轻轻摇动,等完全溶解后即得饱和溶液。储藏于棕色密闭瓶内,放在阴凉处保存。
免疫金的特性 胶体金可以和蛋白质等各种大分子物质结合,在免疫组织化学技术中,习惯上将胶体金结合蛋白质的复合物称为金探针。用于免疫测定时胶体金多与免疫活性物质(抗原或抗体)结合,这类胶体金结合物常称为免疫金复合物,或简称免疫金(immunogold)。 胶体金与蛋白质结合的机制尚有十分清楚,一般认为是物理吸附性的。胶体金颗粒带有一层表面阴性电荷,与蛋白质表面的阳性电荷通过静电感应相附。因此环境pH和离子强度是影响吸附的主要因素,其他如胶体金颗粒的大小、蛋白质的分子量及蛋白质浓度等也会影响蛋白质的吸附。 来源:Gold 2 免疫金的制备 1.用0.2mol/LK2CO3或0.1mol/LHC1调节胶体金溶液的pH至选定值。原则上可选择待标记蛋白质等电点,也可略为偏碱。但通常最适反应pH往往需经多次试验才能确定。在调节胶体金的pH值时应注意,胶体金会阻塞pH计的电极,不可直接将电极插入胶体金溶液中,宜先用终浓度为0.15的聚乙二醇(PEG,20000)稳定胶体金后,再调胶体金的pH 值。 2.将1/10体积的合适浓度的蛋白质溶液加于胶体金溶液中,放置室温反应2~5min。由于盐类成分能影响胶体金对蛋白质的吸附,并可使胶体金聚沉,因此待标记蛋白质溶液若含有较高的离子浓度,应在标记前先对低离子强度的蒸馏水透析去盐。 3.加入浓度为0.2%的PEG或BSA以饱和游离的胶体金。 4.离心分离,去除上清液中未结合的蛋白质。离心条件视胶体金颗粒的粒径而异:对5nm 金颗粒可选用40000r/min离心1h;8nm金颗粒用25000r/min离心45min;14nm金颗粒用25000r/min离心30min,40nm金颗粒用15000r/min离心30min。 5.轻吸上清液。沉淀用含PEG或BSA的缓冲液悬浮,恢复原体积后再离心。如此洗涤2~4次。以彻底除去未结合的蛋白质。 6.免疫金复合物最终用稀释液配制成工作浓度保存。稀释液通常是加入稳定剂的缓冲液。
胶体金是一种常用的标记技术,是以胶体金作为示踪标志物应用于抗原抗体的一种新型的免疫标记技术,有其独特的优点。近年已在各种生物学研究中广泛使用。在临床使用的免疫印迹技术几乎都使用其标记。同时在流式、电镜、免疫、分子生物学以至生物芯片中都可能例用到。 1971年Faulk 和Taytor将胶体金引入免疫化学,此后免疫胶体金技术作为一种新的免疫学方法,在生物医学各领域得到了日益广泛的应用。目前在医学检验中的应用主要是免疫层析法(immunochromatogra-phy)和快速免疫金渗滤法(Dot-immuogold filtration assay DIGFA),用于检测 HBsAg、HCG 和抗双链DNA抗体等,具有简单、快速、准确和无污染等优点。 免疫胶体金技术的基本原理: 胶体金是由氯金酸(HAuCl4)在还原剂如白磷、抗坏血酸、枸橼酸钠、鞣酸等作用下,可聚合成一定大小的金颗粒,并由于静电作用成为一种稳定的胶体状态,形成带负电的疏水胶溶液,由于静电作用而成为稳定的胶体状态,故称胶体金。胶体金在弱碱环境下带负电荷,可与蛋白质分子的正电荷基团形成牢固的结合,由于这种结合是静电结合,所以不影响蛋白质的生物特性。 胶体金除了与蛋白质结合以外,还可以与许多其它生物大分子结合,如SPA、PHA、ConA 等。根据胶体金的一些物理性状,如高电子密度、颗粒大小、形状及颜色反应,加上结合物的免疫和生物学特性,因而使胶体金广泛地应用于免疫学、组织学、病理学和细胞生物学等领域。 胶体金标记,实质上是蛋白质等高分子被吸附到胶体金颗粒表面的包被过程。吸附机理可能是胶体金颗粒表面负电荷,与蛋白质的正电荷基团因静电吸附而形成牢固结合。用还原法可以方便地从氯金酸制备各种不同粒径、也就是不同颜色的胶体金颗粒。这种球形的粒子对蛋白质有很强的吸附功能,可以与葡萄球菌A蛋白、免疫球蛋白、毒素、糖蛋白、酶、抗生素、激素、牛血清白蛋白多肽缀合物等非共价结合,因而在基础研究和临床实验中成为非常有用的工具。 免疫金标记技术(Immunogold labelling techique) 主要利用了金颗粒具有高电子密度的特性,在金标蛋白结合处,在显微镜下可见黑褐色颗粒,当这些标记物在相应的配体处大量聚集时,肉眼可见红色或粉红色斑点,因而用于定性或半定量的快速免疫检测方法中,这一反应也可以通过银颗粒的沉积被放大,称之为免疫金银染色。
双抗体夹心法原理 以FABP 为例(检测抗原) 阳性反应 Y1=F14A (标记了胶体金) Y2=F104B (固定在NC 膜上即T 线) Y3=羊抗鼠IgG (固定在NC 膜上即C 线) 此方法较常用,主要用于较大分子量的蛋白(抗原)的检测。要求两株抗体针对一个抗原的不同位点才可以。也有个别的检测项目是双抗原夹心检测抗体的,原理类似。 样品(血清)含FABP 蛋白 金标记F14A 抗体 金-F14A-FABP 金-F14A-FABP-F14A 金-F14A-羊抗鼠IgG 金-F14A-FABP 羊抗鼠IgG 显示红色 显示红色 金标记F14A 抗体 不显色 显示红色 金-F14A-羊抗鼠IgG 阴性反应 阳性反应
竞争法原理 以吗啡为例(检测抗原) 阳性反应 Y1=胶体金标记的吗啡单抗 Y2=吗啡-BSA 偶联物 Y3=羊抗鼠 此方法主要用于小分子抗原(毒品、农药、肽链等)的检测。由于抗原分子量小不能直接固定于NC 膜上,常常用化学方法把小分子偶联到BSA 等大分子物质上再固定于NC 膜上。此结果与双抗原夹心法相反,阴性CT 两条都是红线,阳性只有C 线一条红线。 金-吗啡抗体-吗啡 吗啡-BSA 金标记吗啡抗体 显示红色 不显色 金-吗啡抗体-吗啡 羊抗鼠 样品(尿液)含吗啡 显示红色 显示红色 金标记吗啡抗体 金-吗啡抗体-羊抗鼠 阴性尿液抗体-吗 阴性反应 阳性反应
间接法原理 以HIV 为例(检测抗体) 显示红色显示红色 显示红色 不显色 此方法主要用于血清中抗体检测,纯化或者重组的抗原固定于NC膜上,标记多为蛋 白A(ProteinA或叫SPA,抗体Fc端结合而与其它蛋白质不结合)。此方法要求胶体金 过量,一般来说样品再加入前需要稀释或者加极少量后再加缓冲液。 斑点免疫渗滤法使用就是间接法。
1、胶体金制备的基本原理 Manufacturing high-quality gold sol Understanding key engineering aspects of the production of colloidal gold can optimize the quality and stability of gold labeling components. Basab Chaudhuri and Syamal Raychaudhuri 1、Producing Gold Colloids 1.1、Before the addition of the reducing agent, 100% gold ions exist in solution. 1.2、Immediately after the reducing agent is added, gold atoms start to form in the solution, and their concentration rises rapidly until the solution reaches supersaturation. 1.3、Aggregation subsequently occurs, in a process called nucleation. Central icosahedral gold cores of 11 atoms are formed at nucleation sites. The formation of nucleation sites, in response to the supersaturation of gold atoms in solution, occurs very quickly. Once it is achieved, the remaining dissolved gold atoms continue to bind to the nucleation sites under an energy-reducing gradient until all atoms are removed from solution. 1.4、The number of nuclei formed initially determines how many particles finally grow in solution. At a fixed concentration of tetrachloroauric acid in solution, as the concentration of the reducing agent is increased the number of nuclei that form grows larger. The more nuclei, the smaller the gold particles produced. Finding the optimal concentration of the citrate in solution is therefore an important, even crucial, task. 1.5、If manufacturing conditions are optimized, all nucleation sites will be formed instantaneously and simultaneously, resulting in formation of final gold particles of exactly the same size (monodisperse gold). This is indeed difficult to achieve. Most manufacturing methods fail to accommodate this ideal and generate irreproducible gold (gold inconsistent from batch to batch) that gives unstable gold conjugates in most situations. 1.6、Gold colloids are composed of an internal core of pure gold that is surrounded by a surface layer of adsorbed AuCl–2 ions. These negatively charged ions confer a negative charge to the colloidal gold and thus, through electrostatic repulsion, prevent particle aggregation. 1.7、All colloidal gold suspensions are sensitive to electrolytes. Electrolytes compress the ionic double layer and thereby reduce electrostatic repulsion. This destabilizing effect results in particle aggregation, which is accompanied by a color change and eventual sedimentation of the gold. The detrimental effect of chloride, bromide, and iodide electrolytes on the stability of the gold colloid is greatest for chlorides and least with iodides. 1.8、All gold colloids display a single absorption peak in the visible range between 510 and 550 nm. With increasing particle size, the absorption maximum shifts to a
免疫胶体金技术常见影响因素分析 自胶体金作为特殊标记物进行研究以来,建立的各种免疫胶体金技术以其特异性强、灵敏度高、操作简捷等特点,在医学、农牧业、环境及食品检测等领域被广泛应用。免疫胶体金技术的反应过程就是一个由金颗粒、抗原与抗体动态结合的反应过程,在这个过程中每个环节的好坏都直接影响试验的成败。而试验过程中每个环节又受到很多因素的影响与制约,下面将影响免疫胶体金技术的因素作一分析,为成功制备胶体金检测产品提供参考。 1耗材的选择 1、1不同型号膜的筛选。硝酸纤维素膜的型号在试验中至关重要,作为反应载体影响到整个试验的成败。不同的生产厂家生产硝酸纤维素膜时使用的聚合物与表面活性剂的来源、类型与数量均大不相同,对生产出的膜的性能产生较大影响——膜的孔径与分布结构不同。膜孔径减小,膜的实际可用表面积递增,膜结合蛋白的量也递增;膜孔径越小,层析速度也越慢,金标复合物通过T线的时间就越长,反应也就越充分;因此膜孔径越小灵敏度越高,但就是同时也减慢了跑板速度,增加了非特异性结合的机会,也就就是假阳性越高。用于金标免疫快速试验的膜多为硝酸纤维素膜或硝酸纤维素/醋酸纤维素混合膜,不同的包被蛋白对膜有特定要求,试验者应根据蛋白质的性质选择适合孔径大小与分布结构的膜,找到合适的平衡点,使胶体金的标记物在膜上的流动速率为最佳。 1、2结合垫的选择。结合垫位于层析系统的中间,一般要求结合垫的网格均一且非特异性吸附低,能很好地负载胶体金标记物与待检测样品,而不被吸附;玻璃纤维素膜具备以上优点,同时具有一定的硬度,为试验中常用。 1、3样品垫及吸水纸的选择。样品垫与吸水纸位于胶体金免疫层析系统的两端,对于胶体金层析系统功能的实现起着举足轻重的作用。试验中应根据试纸条检测样品的性质选择合适的样品垫与吸水纸,保证样品在样品垫形成的通道中快速地流动而不被非特异性地吸附或者改变样品的性质。如检测样品为血清,则可选择网格较疏松的玻璃纤维素膜即可;如果检测样品为毒素,则可选择质量好的吸水纸与样品垫。吸水纸则要有很好的蓄水能力,保证样品中所用的液体都经过膜的反应区而被样品垫吸收与蓄积。 2关于胶体金的制备 制备颗粒均匀、分散度好的胶体金在金标免疫快速试验中非常关键,如果金颗粒直径的变异范围太大就会影响到试验的稳定性与重复性,如果金颗粒的形状不规则或粒径不均一,使得胶体金标记物容易解离与沉淀而产生金标扩散不完全、反应区底色过深与假阳性现象;而且胶体金质量不好,胶体金结合物就不能快速而完整的从玻璃纤维上解离,从而影响试验结果。
1. 适用范围 适用于乙型肝炎病毒表面抗体检测试剂盒(胶体金法)的生产和质量控制。 2. 职责 研发部:制定本规程。 生产管理部:执行本规程 质量管理部:按本规程执行,监督本规程的执行情况。 3. 内容 3.1.依据 《乙型肝炎病毒表面抗体检测试剂(胶体金法)》产品标准 3.2.产品名称、剂型、规格 3.2.1名称: (1) 商品名:乙型肝炎病毒表面抗体检测试剂(胶体金法) (2)英文名:Diagnostic Kit for Antibody to Hepatitis B Surface Antigen(Colloidal Gold Immunochromatagraphic Assay) (3)汉语拼音名:Yixing Ganyan Bingdu Biaomian Kangti Jiance Shiji(jiaotijin Fa)3.2.2.类型:三类6840体外诊断试剂。 3.2.3.规格:100T/盒(25T/筒*4筒)(无卡);25袋/盒(1支/袋)、50袋/盒(1支/袋)3.3.产品概述 乙型肝炎病毒表面抗体检测试剂(胶体金法)采用胶体金免疫层析分析原理、双抗原夹心法,在玻璃纤维纸上预包埋金标记重组乙型肝炎病毒表面抗原,在硝酸纤维素膜上检测线(T)和质控线(C)分别包被重组的乙型肝炎病毒表面抗原和羊抗兔IgG。当检测样本为阳性时,样本中的乙肝病毒表面抗体与胶体金标记的重组乙肝病毒表面抗原结合形成复合物,由于层析作用复合物沿纸条向前移动,经过检测线(T)时与预包被的重组乙肝表面抗原反应,形成免疫复合物而显现红色条带,游离金标记的兔IgG则在质控线(C)与羊抗兔IgG结合显现红色条带。阴性样本则仅在质控线(C)显色。 3.4.试剂盒组成、储存、有效期 3.4.1.试剂盒组成:
胶体金技术的发展原理及制备方法 1971年Faulk与Taylor首先将胶体金应用于免疫细胞化学研究,1974年Romano建立了间接免疫金染色法,从此胶体金作为新型的免疫标记技术得到迅速发展。 由胶体金标记技术发展起来的胶体金免疫快速诊断技术主要有两种:快速斑点免疫金渗滤法与胶体金免疫层析法。后者具有操作简便(浸入液体中就行)、快速(全程5~10分钟搞定)、无需仪器设备(结果目测就OK)、试剂稳定、成品易于保存(保质期1~2年)等优点,就是科学研究与临床诊断的有力工具。 胶体金(colloidal gold)即胶体状态的金单质,因为其单质粒径非常小可以分散于溶液中形成胶体,故名胶体金。胶体金的常规制备方法就是用还原剂还原氯金酸(HAuCl4,橘黄色晶体,易潮解,氯金酸合成见下图)里的金元素形成金胶体颗粒。这种胶体颗粒在碱性环境下带上负电荷,可与蛋白质的正电荷基团牢固结合,对蛋白进行标记,用于后续的检测,如制成胶体金试纸条(卡)进行物质的检测。 还原氯金酸的化合物很多,通常我们选择柠檬酸三钠(Na3C6H5O7·2H2O)。当用1%柠檬酸三钠还原100 mL 0、01%金氯酸时,不同体积比可以得到不同粒径与颜色的胶体金哦!
制备胶体金步骤简单(见下图),重点就是制备过程所用到的材料都必须就是彻底清洁的。例如水至少就是双蒸水,玻璃棒、玻璃容器等要酸洗后冲洗干净并且最好就是硅化的,制备好的胶体金可以加入0、02% NaN3在洁净玻璃容器内长期存放。 适合于胶体金试纸条(卡)的胶体金粒径在20~40 nm之间为宜,制备的胶体金溶液呈红色,胶体金被置于试纸条(卡)的样品垫下游。当液体样品滴加后,液体溶解胶体金并带动其与样品中的抗原(抗体),在硝酸纤维素膜的毛细作用下从一端慢慢渗移到吸收垫一端,利用抗体/抗原特异性结合及胶休金的显色(红色)反应,可以检测抗原/抗体存在与否。 胶体金试纸条(卡)主要分为双抗夹心法与竞争法两类,前者适合检测大分子物质,后者适合检测小分子物质。两种试纸条(卡)的原理见下图:
1. 适用范围适用于乙型肝炎病毒表面抗体检测试剂盒(胶体金法)的生产和质量控制。 2. 职责 研发部:制定本规程。 生产管理部:执行本规程 质量管理部:按本规程执行,监督本规程的执行情况。 3. 内容 3.1.依据 《乙型肝炎病毒表面抗体检测试剂(胶体金法)》产品标准 3.2.产品名称、剂型、规格 3.2.1名称: (1) 商品名:乙型肝炎病毒表面抗体检测试剂(胶体金法) (2)英文名:Diagnostic Kit for Antibody to Hepatitis B Surface Antigen(Colloidal Gold Immunochromatagraphic Assay) (3)汉语拼音名:Yixing Ganyan Bingdu Biaomian Kangti Jiance Shiji (jiaotijin Fa) 3.2.2.类型:三类6840体外诊断试剂。 3.2.3.规格:100T/盒(25T/筒*4筒)(无卡);25袋/盒(1支/袋)、50袋/盒(1支/袋) 3.3.产品概述 乙型肝炎病毒表面抗体检测试剂(胶体金法)采用胶体金免疫层析分析原理、双抗原夹心法,在玻璃纤维纸上预包埋金标记重组乙型肝炎病毒表面抗原,在硝酸纤维素膜上检测线(T)和质控线(C)分别包被重组的乙型肝炎病毒表面抗原和羊抗兔IgG。当检测样本为阳性时,样本中的乙肝病毒表面抗体与胶体金标记的重组乙肝病毒表面抗原结合形成复合物,由于层析作用复合物沿纸条向前移动,经过检测线(T)时与预包被的重组乙肝表面抗原反应,形成免疫复合物而显现红色条带,游离金标记的兔IgG则在质控线(C)与羊抗兔IgG结合显现红色条带。阴性样本则仅在质控线(C)显色。 3.4.试剂盒组成、储存、有效期
一、胶体金的一般性状 (一) 胶体金的颜色 溶胶的颜色取决于分散相物质的颜色、分散相物质的分散度和入射光线的种类,是散射光线还是透射光,粒子越小,分散度越高,则散射光的波长越短。对同一种物质的水溶胶来说,粒子大小不同,呈现的颜色亦不同。如胶体金颗粒在5~20nm之间,吸收波长520nm,呈红色的葡萄酒色;20~40nm之间的金溶胶主要吸收波长530nm的绿色光,溶液呈深红色;60nm的胶体金溶胶主要吸收波长600nm的橙黄色光,溶液呈蓝紫色。一般应用于免疫组织化学的胶体金颗粒为5~60nm范围内,溶液呈现红色。在相当的一段时期内保持其溶胶不变性,称为胶体金的稳定性。影响其稳定性的因素主要是电解质,其次是胶体金本身的浓度、温度及其他非电解质等。 (二) 胶体金的稳定性 溶胶的稳定性介于小分子离子溶液和粗分散相之间,其颗粒作布朗运动,不易受重力影响而下沉。然而,溶胶又是不稳定体系,它的胶粒溶剂化作用很弱,总面积较大、因在胶粒相互碰撞时,有自动合并为较大、较重的颗粒倾向。当胶体颗粒直径变大,超出胶体范围而从介质中沉淀出来的现象叫聚沉。影响其稳定性的主要原因有三点。 (1) 胶粒间的相互吸引力当胶粒相距很近时,这种吸引力可能导致胶体颗粒合并而变大。 (2) 胶粒及其溶剂化层胶粒及其溶剂化层(溶剂是水时就是水化层)的带电情况。一种溶胶的各个胶粒都带有相同的电荷。同性电荷相斥,双电子层变厚,胶粒带电量愈大,排斥力愈大,愈能阻止胶粒合并聚结,溶胶愈稳定。 (3) 胶体接口的溶剂膜当二个固体间夹有一厚层液体时,这层液体膜有一个反抗二固体接近的排斥力。两个胶粒要进一步接近,只有克服它们之间的溶剂化膜的斥力才有可能,因此溶剂膜的斥力是使溶胶稳定的原因之一。 (三) 溶胶的聚沉现象 胶粒之间存在吸引力与排斥力这对矛盾,在溶胶胶粒带电及溶剂化的情况下,排斥力成为矛盾的主要方面,溶胶稳定而不聚沉。因为某种原因使溶胶粒带电量减到很小,甚至中和其所带电荷并能去溶剂化膜,胶粒之间可在更近的距离互相接近,引力成为主要矛盾,引力超过斥力时胶粒便聚结发生聚沉。引起溶胶聚沉的原因有。 (1)少量电解质对溶胶的聚沉作用少量电解质即可使溶胶聚沉,但各种电解质的聚沉能力可用聚沉值来表示。聚沉值是在一定时间内使1L某浓度的溶胶产生聚沉所需电解质的最小物质的量(mm01)。显然,聚沉值愈小,聚沉能力愈大。聚沉值从实验中得出如下的规则:①电解质负离子对带正电的溶胶起主要聚沉作用,正离子对带负电的溶胶起主要聚沉作用;
胶体金免疫分析技术详解 随着免疫分析日益广泛应用于以临床为主以及非临床领域的诊断工业,免疫分析正在向两个方向发展:一类为全自动化的免疫分析;另一类为以硝酸纤维膜为载体的快速免疫分析。前者需要价格昂贵的全自动仪器及与仪器严格配套的各种试剂盒,目前只能在医疗及检测中心应用,虽也能较快速给出结果,但仍需一定时间,不适合远离医疗及检测中心的地区,更不能用于“患者床旁检验”和普查的需要,在酶免疫分析的基础上,主要以硝酸纤维素膜为载体的快速诊断方法迅速和广泛地发展起来。这类方法目前在文献及市场上的命名还很不统一。它实际上属于快速斑点免疫结合分析,主要有以下两种方法:斑点免疫渗滤分析DIFA和斑点免疫层析分析DICA。本篇主要介绍以金作为标志物的胶体金免疫分析技术。 金标记免疫分析技术也称免疫胶体金技术,是于1971年建立的一种信号显示技术。此技术最初用于免疫电镜检查,由胶体金颗粒标记抗原或抗体,与组织或细胞中相应的抗体或抗原相结合,在电子显微镜的检查时可起特异的示踪作用。此后,此技术与银染技术相结合建立的免疫金银染色法,使抗原抗体特异反应信号可在光学显微镜下观察。近10多年来,利用硝酸纤维素膜(NC)等为固相载体,以胶体金标记的抗原或抗体与特异配体的反应在膜上进行,建立了快速的金标记免疫渗滤技术和金标记免疫层析技术,并在传染病、心血管病、风湿病、自身免疫病的免疫学检测中广泛应用。 胶体金是指金微小粒子(0-100nm)分散在另一种物质中所形成的体系,通常指金以微小粒子分散在溶液中所形成的金溶胶,用此金溶胶标记蛋白质(抗原、抗体或SPA、SPG),胶体金颗粒具有高电子密度的特性,故在金标蛋白的抗原抗体结合处,显微镜下可见黑褐色颗粒;当这些标记物在相应的标记处大量聚集时,可在载体膜上呈现红色或粉红色斑点,从而用于抗原或抗体物质的半定量或定性。 与ELISA不同之处便是反应时间大大缩短,仅需要数分钟就完成了ELISA需数小时才能显示的结果。因为在GIFA和GICA中,高浓度的抗体集中固定在纤维素的微孔中,待测抗原在渗滤或层析时,流经微孔与固定的高浓度抗体紧密接触,很快完成免疫结合反应。这就是以膜为基础的胶体金快速免疫结合分析中的免疫浓缩作用。在ELISA中,待测抗原要在液相中经过扩散作用,逐渐与吸附在固相表面的抗体结合。同时,标记抗体也需要同样的扩散结合过程形成抗体-抗原-标记抗体复合物,故需时间较长。故此技术做到了名副其实的POCT。 原理: 将氯金酸(HAuCl4)用还原法制成一定直径的金溶胶颗粒(胶体金),标记金黄色葡萄球菌A
部门职责及设备配置需求 一.部门名称: 1.1. 前端生产:制水车间,主料库,原料库,配液/稀释/处理/黏膜/切割,标记室,喷金室,点膜室,烘房(干燥室),半成品库(光库,Buffer库,配批库,试纸条库); 1.2. 后端生产:粘膜车间,切割车间,装配车间,成品库 二.前端生产: 2.1 制水车间:制备超纯水(纯化水系统) 2.2 主料库:片材,玻纤,聚酯膜,滤纸,NC膜等(控制湿度在30%以下) 2.3 原料库:抗原,抗体等(4℃/-20℃冰箱,移液枪) 2.4 配液/稀释/处理/黏膜/切割: 1. 配制/稀释缓冲液(分析天平,量筒,PH计,磁力搅拌器,移液枪,旋涡混合仪,药品柜,生物安全柜) 2. 处理样本垫,金垫(自动化玻纤,聚酯膜处理设备) 3. 从主料库领取片材与NC膜进行黏膜(自动化黏膜机) 4. 将处理好的样本垫按要求切割成需要的宽度(切割刀,直尺) 2.5 标记室:制金,标记(灭菌器,高速离心机,温控磁力搅拌器,三角瓶量筒,移液枪,分析天平,紫外分光光度计,超声波清洗器) 2.6 喷金室:喷金(喷金仪)
2.7 点膜室:点膜(点膜仪) 2.8 烘房(干燥室):干燥喷金后的金垫,点膜后的片材(控制湿度20%以下)(干燥箱) 2.9 半成品库: 1. 光库:储存烘房干燥后的金垫与片材,以及自动化处理干燥后的样本垫和金垫(控制湿度20%以下)(封口机) 2. Buffer库:储存缓冲液(4℃冰箱,量筒,移液枪) 3. 配批库:组合好光库中喷金的金垫,点膜的片材,样本垫为一组配批(控制湿度20%以下)(封口机) 4. 试纸条库:储存切割成单条的试纸条(控制湿度20%以下)(封口机) 三.后端生产: 3.1 粘模车间:领取配批(QC检合格的半成品)根据不同产品不同要求组装成大卡(控制湿度20%以下)(封口机) 3.2 切割车间:将组装好的大卡根据不同产品不同要求切割成试纸条(切割机,封口机)(控制湿度20%以下) 3.3 装配车间:将试纸条,模板,包装袋,干燥剂装配成成品,按照相关装盒/装箱要求对产品进行操作。(经QC检合格后,入成品库)(控制湿度20%以下) 3.4 成品库:合格产品入库。
影响胶体金制备的因素 XX (单位地名邮编) 摘要:胶体金是氯金酸被还原,离子的正电荷被中和,从而稳定的悬浮在分散系中,形成均一性,均匀度良好的溶胶。本文主要以利用柠檬酸三钠作为还原剂,制备胶体金为例。从柠檬酸三钠钠添加量、反应时间、搅拌强度、沸腾时间、溶胶的PH及紫外光等六个方面,概述了影响胶体金制备因素。 关键词:柠檬酸钠;胶体金;影响 随着纳米技术的不断发展,人们发现了胶体金,并将其广泛应用在医学、生物学、分子学和免疫学等各个学科[1]。胶体金是由氯金酸制备而成的,通常主要用柠檬酸三钠还原法和抗败血酸还原法[2],因前者操作简单,成本低,后者则效果更有优势[3]。在这些试剂的作用下,氯金酸形成粒径在1 nm-100 nm之间,稳定的分散系,即就是胶体金[4]。人们经常用柠檬酸三钠还原法制备,主要机制是加入一定量的柠檬酸三钠可以将原溶液中的金离子还原为金原子,从而增加了均一性和稳定性。我们都知道,用该方法制备胶体金,受很多因素的影响,本文主要从柠檬酸三钠的添加量、搅拌强度、溶胶PH及紫外光等方面进行阐述,以期为柠檬酸三钠还原法制备胶体金提供参考。 1. 胶体金的概述 胶体金是金盐(氯金酸)在还原剂的作用下,变成金单质。悬浮在分散系中,形成的金溶胶。根据颗粒大小不同,颜色依次呈现出橙色、酒红色及紫红色[5]。 2. 影响胶体金制备的因素 胶体金的制备中,氯金酸依然是重要的材料,通过各种方法进行还原制备金溶胶,常见的制备方法有一下几种:1),紫外光引发还原;2),纳米金溶胶制备;3),磷钼酸作为光催化还原剂制备纳米金溶胶;4),超短脉冲激光诱导制备金溶胶;5),采用激光轰击固液界面连续制备纯净金溶胶。常用还原剂有柠檬酸钠、鞣酸、抗坏血酸、白磷、硼氢化钠等[6]。根据还原剂类型以及还原作用的强弱[7],可以制备0.8nm~150nm不等的胶体金。实际中多用于柠檬酸三钠制备。 有研究指出,在制作过程中,当溶胶颜色为紫红色时,达到要求,为黄色、橙色、浅紫色时,颗粒达不到要求,主要是因为在用400-700 nm可见光扫描时,仅在紫红色时出现了峰波。此外,可通过峰宽/峰高的值判断胶体金颗粒的均匀度[8]。 2.1 柠檬酸三钠添加量 在刘颖沙等[9]的试验中,使用0.75,1.00,1.50 ,2.00及4.00 mL5种不同添量的柠檬酸三钠,观察每组的扫面图谱,得出在添加2 mL1% 柠檬酸三钠时,所得胶体金的各项指标均表明,此时的均一性,均匀度,粒径大小都符合标记的要求。且随着添加量的增加,溶胶颜色和粒径也逐渐增加。宋宏新等[2]的研究也指出,添加300 、400及500 μm的实验组中,300 μm组的效果更好一些,溶液颜色透明,均一性好,最大吸收峰在523 nm处,此时得到的粒径为20 nm,综合各项指标,最终选择300 μm组作为最优组。 2.2 反应时间 孙秀兰等[10]从煮沸时间、反应时间和搅拌转速3个因素探讨了胶体金的制备。研究结果表明,其中反应时间的影响是最显著地,且不同反应时间下溶胶的均匀度的,均一性发生了很大地变化,延长反应时间,分散性降低,增加了二聚体或多聚体的含量。光谱的吸光值、峰宽均下降,最大吸收峰也发生了右移。 2.3 搅拌强度 有研究发现,随着搅拌强度增加,峰宽极显著减小,最大吸收波的变化也及其明显,说
第三节胶体金的制备方法 胶体金溶液的制备有许多种方法,其中最常用的是化学还原法,基本的原理是向一定浓度的金溶液内加入一定量的还原剂使金离子变成金原子。目前常用的还原剂有:白磷、乙醇、过氧化氢、硼氢化钠、抗坏血酸、枸橼酸钠、鞣酸等,下面分别介绍制备不同大小颗粒的胶体金溶液。 一、制备胶体金的准备 (一)玻璃器皿的清洁 制备胶体金的成功与失败除试剂因素以外玻璃器皿清洁是非常关键的一步。如果玻璃器皿内不干净或者有灰尘落入就会干扰胶体金颗粒的生成,形成的颗粒大小不一,颜色微红、无色或混浊不透明。我们的经验是制备胶体金的所有玻璃器皿先用自来水把玻璃器皿上的灰尘流水冲洗干净,加入清洁液(重铬酸钾1000g,加入浓硫酸2500ml,加蒸馏水至10000ml)浸泡24h,自来水洗净清洁液,然后每个玻璃器皿用洗洁剂洗3~4次,自来水冲洗掉洗洁剂,用蒸馏水洗3~4次,再用双蒸水把每个器皿洗3~4次,烤箱干燥后备用。通过此方法的处理玻璃器皿不需要硅化处理,而直接制备胶体金。也可用已经制备的胶体金溶液,用同等大不颗粒的金溶液去包被所用的玻璃器皿的表面,然后弃去,再用双蒸水洗净,即可使用,这样效果更好,因为减少了金颗粒的吸附作用。 (二)试剂的配制要求 (1)所有配制试剂的容器均按以上要求酸处理洗净,配制试剂用双蒸馏水或三蒸馏水。 (2)氯化金(HauCl 4 水溶液的配制:将lg的氯化金一次溶解于双蒸水中配成1%的水溶液。放在4”c冰箱内保存长达几个月至1年左右,仍保持稳定。 (3)白磷或黄磷乙醚溶液的配制:白磷在空气中易燃烧,要格外小心操作。把白磷在双蒸水中切成小块,放在滤纸上吸于水份后,迅速放入已准备好的乙醚中去,轻轻摇动,等完全溶解后即得饱和溶液。储藏于棕色密闭瓶内,放在阴凉处保存。 二、制备胶体金的方法和步骤 (一)白磷还原法 1.白磷还原法(z Sigmondy 1905年) (1)取1%的HAuCl 4水溶液1ml,加双蒸水99ml配成0.01%的HAuCl 4 水溶液。 (2)用0.2mol/l K 2CO 3 调pH至7.2。
免疫胶体金技术(Immune colloidal gold technique) 文章来源: 文章作者: 发布时间:2007-04-24 字体: [大 中 小] (一) 原理 免疫胶体金技术是以胶体金作为示踪标志物应用于抗原抗体的一种新型的免疫标记技术。胶体金是由氯金酸(HAuCl 4)在还原剂如白磷、抗坏血酸、枸橼酸钠、鞣酸等作用下,聚合成为特定大小的金颗粒,并由 于静电作用成为一种稳定的胶体状态,称为胶体金。胶体金在弱碱环境下带负电荷,可与蛋白质分子的正电荷基团形成牢固的结合,由于这种结合是静电结合,所以不影响蛋白质的生物特性。 胶体金除了与蛋白质结合以外,还可以与许多其它生物大分子结合,如SPA 、PHA 、ConA 等。根据胶体金的一些物理性状,如高电子密度、颗粒大小、形状及颜色反应,加上结合物的免疫和生物学特性,因而使胶体金广泛地应用于免疫学、组织学、病理学和细胞生物学等领域。 (二) 胶体金的制备 根据不同的还原剂可以制备大小不同的胶体金颗粒。常用来制备胶体金颗粒的方法如下。 1.枸橼酸三钠还原法 (1)10nm 胶体金粒的制备:取0.01%HAuCl 4水溶液100ml ,加入1%枸橼酸三钠水溶液3ml ,加热煮沸30 min ,冷却至4℃,溶液呈红色。 (2)15nm 胶体金颗粒的制备:取0.01%HAuCl 4水溶液100ml ,加入1%枸橼酸三钠水溶液2ml ,加热煮沸 15min ~30min ,直至颜色变红。冷却后加入0.1Mol/L K 2CO 30.5ml ,混匀即可。 (3)15nm 、18nm ~20nm 、30nm 或50nm 胶体金颗粒的制备:取0.01%HAuCl 4水溶液100ml ,加热煮沸。根 据需要迅速加入1%枸橼酸三钠水溶液4ml 、2.5ml 、1ml 或0.75ml ,继续煮沸约5min ,出现橙红色。这样制成的胶体金颗粒则分别为15nm 、18~20nm 、30nm 和50nm 。 2.鞣酸—枸橼酸钠还原法 A 液:1%HAuCl 4水溶液1ml 加入79ml 双馏水中混匀。 B 液:1%枸橼酸三钠4ml ,1%鞣酸0.7ml ,0.1Mol/L K 2CO 3液0.2ml ,混合,加入双馏水至20ml 。