化学试液配制记录
编号:REC-QC-021-00
B.ZL.JY.YL.02.009 第 1 页 制定审核批准 制定日期审核日期批准日期 颁发部门GMP办颁发数量 3 份生效日期 分发单位质管部 一目的:制定的乙醇检验标准操作规程,规范公司乙醇的检验。 二适用范围:适用于乙醇的检验。 三责任者:质管部、化验员。 四标准依据:《中华人民共和国兽药典》2010年版一部 五正文: 1 质量标准:见《乙醇质量标准》。 2 试剂:按试剂配制操作规程配制 氢氧化钠试液、碘试液、酚酞指示液、甲醇、纯化水、磷酸溶液、4-甲基-2-戊醇、糠醛液、高锰酸钾溶液、盐酸、硫酸、6%氰丙基苯基-94%二甲基聚硅氧烷、高锰酸钾滴定液、硫酸溶液、甘油。 3 仪器与用具:酒精灯、气相色谱仪、硬质高型玻璃烧杯、紫外-可见光分光光度计、密度瓶、滤纸、垂熔漏斗、蒸发皿、水浴锅、试管、量筒、小烧杯、三角瓶。 4 操作步骤 4.1性状 4.1.1本品为无色澄明液体;微有特臭,味灼烈;易挥发,易燃烧,燃烧时显淡蓝色火焰;加热至约78℃即沸腾。 4.1.2本品与水、甘油、三氯甲烷或乙醚能任意混溶。 4.1.3相对密度本品的相对密度不大于0.8129,相当于含C2H6O 不少于9 5.0%(ml/ml)。 4.2鉴别取本品1ml ,加水5ml 与氢氧化钠试液1ml 后,缓缓滴加碘试液2ml ,即发生碘仿的臭气,并生成黄色沉淀。 4.3检查 4.3.1酸碱度取本品20ml,加水20ml,摇匀,滴加酚酞指示液2 滴,溶液应为无色;再加氢氧化钠滴定液(0.01mol/L)1.0ml,溶液应显粉红色。 4.3.2溶液的澄清度与颜色本品应澄清无色。取本品适量,与同体积的水混合后,溶液应澄清;在10℃放置30分钟,溶液仍应澄清。 4.3.3吸光度取本品,以水为空白,照紫外-可见分光光度法测定吸光度,在240nm 的波长处不得过0.08;250~260nm的波长范围内不得过0.06;270~340nm的波长范围内不得过0.02. 4.3.4挥发性杂质照气相色谱法法测定 色谱条件与系统适用性试验以6%氰丙基苯基-94%二甲基聚硅氧烷为固定液;起始温度40℃,维持12分钟,以每分钟10℃的速率升温至240℃,维持10分钟;进样口温度为200℃;检测器温度为280℃。对照溶液(b)中乙醛峰与甲醇峰之间的分离
乙醇脱水制乙烯实验探究 李增祥 中学化学实验室中常用浓硫酸作为乙醇脱水制取乙烯的催化剂、脱水剂,但是实验中存在很多的弊端,如:炭化现象严重影响观察,反应所需要的时间长,制取的乙烯纯度不高等。苏教版全国高中化学新教材——《有机化学基础》(选修)P69页,关于乙醇脱水制取乙烯的实验中,没有采用传统的方法即以浓硫酸作为催化剂,而是选用石棉绒作为催化剂制取乙烯[1]。教材中采用试管作为反应仪器,将乙醇和石棉绒加入其中用酒精灯进行加热,并用水进行洗气来制取乙烯。那么石棉绒能否作为制取乙烯的催化剂,还需要从其反应机理来看。 乙醇脱水反应是按照E1机理进行的,具体过程如下: 在酸的作用下,乙醇分子上不容易离去的集团——C—O转变成易离去的集团,C—O键断裂脱水形成C+,C+的邻位碳原子上失去一个质子,一对电子转移过来中和正电荷形成双键。从反应机理上看,生成C+的一步是整个反应的速控步骤,还表明醇的脱水反应是一个可逆反应。因此可以通过控制H+的浓度即用较浓的酸来使反应向右进行,可以选用浓硫酸或五氧化二磷作为催化剂和脱水剂。另外,醇在350-400℃在氧化铝或者硅酸盐表面上脱水,不发生重排反应[2]。如: 石棉属于硅酸盐类矿物,化学成份是Mg6[Si4O10][OH]8,含有氧化镁、铝、钾、铁、硅等成分[3]。因此从理论上看石棉绒可以作为乙醇脱水制取乙烯的催化剂,那么它在实际操作中能否有良好的催化效果?与浓硫酸、五氧化二磷在实验室中的催化效果有什么不同?笔者对此进行了一系列的对比实验。 一、实验内容: 1、实验内容: (1)采用浓硫酸作催化剂; (2)采用石棉绒作为催化剂,分别采用角闪石和蛇纹石石棉; (3)采用五氧化二磷作催化剂; (4)采用浓硫酸和石棉绒作为混合催化剂; (5)采用五氧化二磷和石棉绒作为混合催化剂。 2、实验装置: 3、乙醇的具体用量及催化剂用量及见下表:
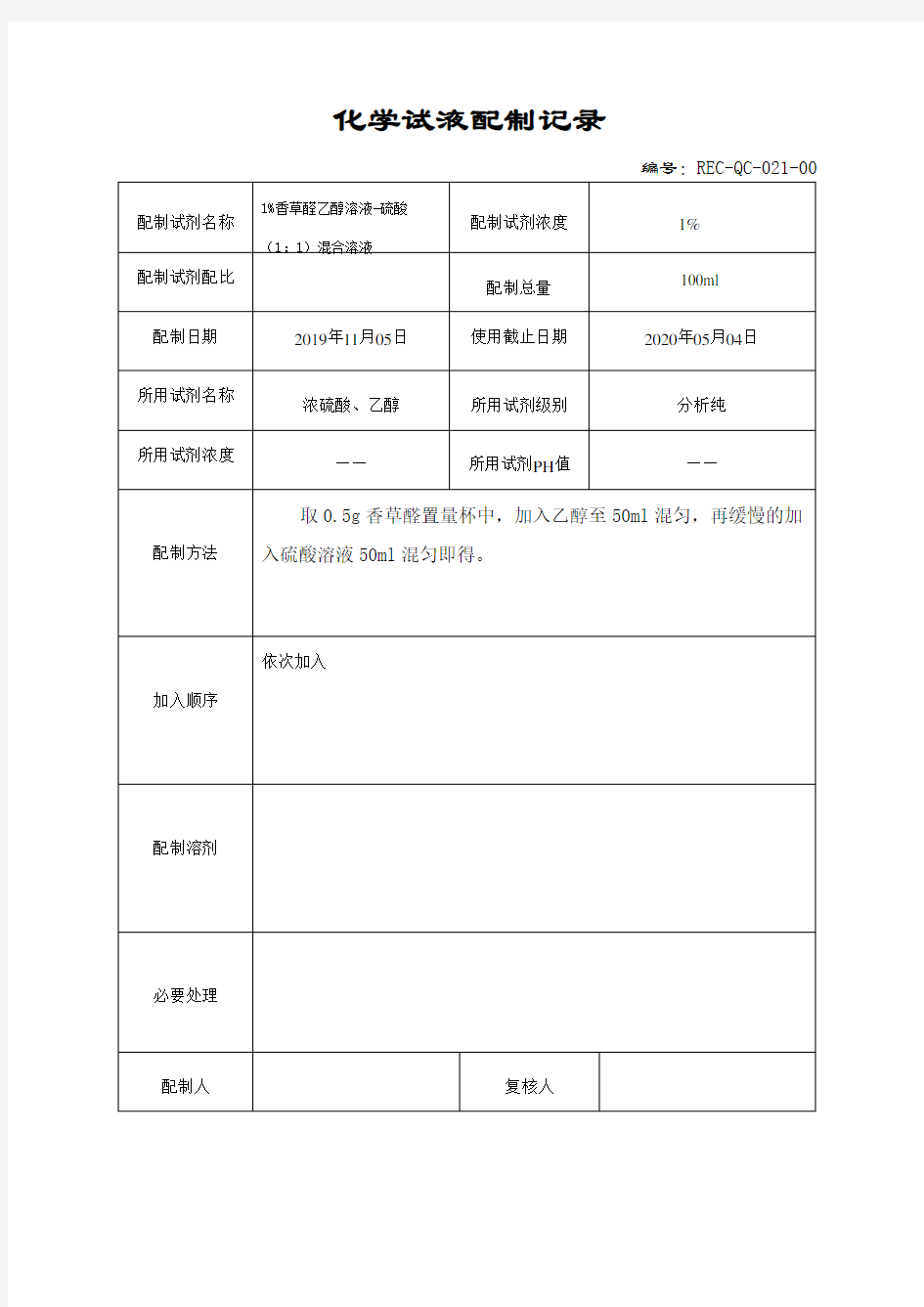
实验室最常用的显色剂及配制方法 (1)硫酸(sulphuri acid)通用显色剂。 试液: a、5%浓硫酸乙醇或乙酐溶液 b、浓硫酸与甲醇或乙醇等体积混合 c、15%浓硫酸正丁醇溶液 方法:用以上任一试液喷洒或浸湿晾干,于110摄氏度加热至呈色,或达最强荧光。 (2)碘(iodine) 通用显色剂。 试液: a:0.5%碘的氯仿溶液。 喷后处理:待薄层上过量碘挥散,喷1%淀粉溶液,斑点转为兰色,如有过量碘留在薄层上,则背景也呈兰色。 b:碘蒸气:将少许碘晶体放入一密闭的容器内,使之充满饱和碘蒸气,将薄层放入容器片刻或数分钟即显色。有时在容器内放一小杯水增加湿度,可提高显色的灵敏度,可提高显色的灵敏度。在化合物斑点处显黄-棕色。 (3)磷钼酸(molybdophosphoric acid) 用于还原性化合物、类脂、甾体化合物等。 试液:5%或10%磷钼酸乙醇溶液喷或浸后处理:于120摄氏度加热至最佳颜色形成,如将薄层放入含25%氢氧化铵溶液的容器内,可使背景颜色消退。 (4)香草醛-硫酸(vanillin-sulphuric acid)用于精油、高级醇、酚等 试液:香草醛1g溶于100ml硫酸或香草醛0.5g溶于100ml硫酸-乙醇(1:1)溶液。 喷或浸后处理:于120摄氏度加热至颜色最深。 (5)三氯化铁(ferric chloride)用于酚类、羟酰胺酸。 试液:1%~5%三氯化铁的0.5mol/L盐酸溶液。 页码,1/实验室最常用的显色剂及配制方法3 注:酚类呈兰色或绿色,羟酰胺酸呈红色。 (6)三氯化铝(aluminium chloride)用于黄酮类化合物。 试液:1%三氯化铝乙醇溶液,紫外光长波下斑点显黄色荧光。 (7)碘化铋钾试剂(dragendorff reagent)用于生物碱和某些含氮化合物。 试液:a:次硝酸铋0.85g溶于10ml冰乙酸与40 ml水中。 b:碘化钾8g溶于20ml水中。 方法:试液a和b等量混合,置棕色瓶保存试液。用前将试液1ml加2ml冰乙酸和10ml水混合。 注:显色斑点呈橙红色。 (8)茚三酮(ninhydrin)用于氨基酸、胺与氨基糖类 试液:茚三酮0.2g溶于乙醇100ml或溶于100ml正丁醇,加乙酸3ml。 喷或浸后处理:于110摄氏度加热至最佳颜色出现。 (9)邻苯二甲酸苯胺用于还原糖。 试液:苯胺0.93g和邻苯二甲酸1.66g溶于100ml以水饱和的正丁醇中。 喷或浸后处理:于105摄氏度加热10min,醛己糖及甲基戊糖呈棕色,醛戊糖呈樱桃红色。
乙醇的性质 酒精是一种无色透明、易挥发,易燃烧,不导电的液体。有酒的气味和刺激的辛辣滋味,微甘。学名是乙醇,分子式C2H5OH,因为它的化学分子式中含有羟基,所以叫做乙醇,比重0.7893(20/4°)。凝固点-117.3℃。沸点78.2℃。能与水、甲醇、乙醚和氯仿等以任何比例混溶。有吸湿性。与水能形成共沸混合物,共沸点78.15℃。乙醇蒸气与空气混合能引起爆炸,爆炸极限浓度3.5-18.0%(W)。酒精在70%(V)时,对于细菌具有强列的杀伤作用.也可以作防腐剂,溶剂等。处于临界状态(243℃、60kg/CM·CM)时的乙醇,有极强烈的溶解能力,可实现超临界淬取。由于它的溶液凝固点下降,因此,一定浓度的酒精溶液,可以作防冻剂和冷媒。酒精可以代替汽油作燃料,是一种可再生能源。 酒精 主要成分:乙醇 外观与性状:无色液体,有酒香。 燃点(℃):75
熔点(℃):-114.1 沸点(℃):78.3 相对密度(水=1):0.79 相对蒸气密度(空气=1): 1.59 饱和蒸气压(kPa): 5.33(19℃) 燃烧热(kJ/mol):1365.5 临界温度(℃):243.1 临界压力(MPa): 6.38 闪点(℃):12 引燃温度(℃):363 爆炸上限%(V/V):19.0 爆炸下限%(V/V): 3.3 乙醇:中闪点液体(闪点12℃) 危险特性:易燃、易爆、爆炸极限(3.3-19.0%),遇到明火易燃。 消防方法:用水,二氧化碳、纱布、干粉、雾状水,用水冷却容器 储存:阴凉通风,远离热源,明火,与氧化剂隔离储存。避免阳光照射 酒精储罐泄露应采取如下紧急措施:
实验五探究性实验设计 ——探究乙醇与酸性重铬酸钾溶液的反应 实验目的:学会中学化学实验中探究性实验设计的一般过程与方法。 实验要求:自行发现实验探究问题;自行设计探究性实验方案; 实验实施与实验问题发现及记录;实验报告与分析。 实验设计方案: 一、探究问题的提出 现行普通高中课程标准实验教科书,化学“有机化学基础”(选修5),第52页实验3-2,介绍了乙醇被酸性重铬酸钾溶液的氧化,说明乙醇具有一定的还原性。这是新教材增加的演示实验。同时,最开始用于检查汽车酒后驾驶也是利用了这个反应的原理。在教材里,该实验介绍比较笼统,只是粗略的说了乙醇在重铬酸钾的酸性溶液中会变成蓝绿色,对于重铬酸钾溶液浓度以及酸性溶液的浓度没有详细的介绍。因此本小组成员想通过实验探究重铬酸钾最佳浓度以及酸性溶液的最佳浓度,检验所加硫酸的量对实验现象有何影响。由此得出实验的最佳反应条件。 二、问题解决设想 查阅相关文献,探究在硫酸浓度分别为30%、50%、70%、98%和重铬酸钾浓度分别为1%、2%以及15%的条件下,乙醇溶液与重铬酸钾酸性溶液反应的现象。鉴于在演示实验中,我们希望当乙醇溶液与重铬酸钾酸性溶液反应的时候,颜色渐变过程明显,这有利于学生的观察,而在检验司机酒后驾驶的时候,我们希望反应可以在快速的时间内完成。因此本实验的两个最佳条件的判断标准是:颜色渐变过程明显;反应快速进行。通过改变溶液的浓度以及体积比来探究不同条件下的反应现象,记录实验现象,由此探究适合不同应用的最佳条件。 三、相关资料查阅综述 在硫酸介质中,乙醇可定量被重铬酸钾氧化,生成蓝绿色的二价铬。乙醇被氧化的两个过程用化学方程式表示如下: 4C 2H 5 OH +K 2 Cr 2 7 +3H 2 SO 4 →4CH 3 CHO +K 2 SO 4 +2CrSO 4 +7H 2
中药成分鉴别常用显色剂及其配制方法 一、通用显色剂 (1)硫酸 ①浓硫酸与甲醇等体积小心混合,冷却;②15%浓硫酸的正丁醇溶液;③5%浓硫酸的乙酸酐溶液;④5%浓硫酸的乙醇溶液;⑤浓硫酸与乙酸等体积混合。用以上任一试液喷薄层板后,于110℃烘烤15min,不同类的成分显不同颜色。 (2)碘 ①0.5%碘的氯仿溶液;②碘蒸气 在一密闭的玻璃缸内预先放入少许碘结晶,使缸为碘蒸气饱和。将薄层板放入缸内数分钟即可显色,碘对很多化合物显黄棕色。 (3)高锰酸钾-硫酸 高锰酸钾0.5g溶于15ml 40%硫酸中。检测易还原性物质。 (4)铬酸-硫酸 重铬酸钾5g溶于100ml 40%硫酸中。易还原性物质显色。 (5)荧光显色液 ①0.25%的罗丹明B乙醇溶液;②0.01%的荧光素乙醇溶液;③0.1%的桑色素乙醇溶液。用以上任一试液喷薄层板后,在荧光背景下可能显黑色或其他荧光斑点。 二、专属性显色剂 (一)生物碱及含氮类化合物 (1)改良碘化铋钾(Dragendorff)试剂 ①碱式硝酸铋0.85g溶于10ml冰醋酸与40ml水中;②碘化钾0.8g溶于20ml水中。试液①与试液②等量混合置棕色瓶内保存作贮备液。用前将1ml贮备液、2ml冰醋酸与10ml水混合。用于生物碱与某些含氮化合物,显橙红色。 (2)碘-碘化钾(Wagner) 碘1g与碘化钾10g溶于50ml水(微温),加2ml乙酸,加水至100ml。用于生物碱,显棕褐色。 (3)碘铂酸 5ml 15%氯化铂溶液加45ml 10%碘化钾溶液,用水稀释至100ml。用于生物碱,不同生物碱显不同颜色。 (4)碘铂酸钾 10%六氯铂酸溶液3ml与97ml水混合,加100ml 6%碘化钾溶液,混匀。新鲜配制。用于生物碱与其他有机含氮化合物,不同生物碱显不同颜色。 (5)Ehrlich ①10%对二甲氨基苯甲醛盐酸溶液与丙酮按1:4混合。②对二甲氨基苯甲醛1g,溶于100ml 96%乙醇中。用于吲哚类,有时喷后要加热。 (6)硫酸高铈铵 1%本品的85%磷酸溶液。用于吲哚类,长春花生物碱显各种颜色。 (7)对二甲氨基苯甲醛-硫酸 65ml浓硫酸与35ml水混合,放冷后加对二甲氨基苯甲醛125mg,再加入5%三氯化铁溶液0.05ml。本试液可保存一周。用于麦角生物碱。 (8)肉桂醛-盐酸 肉桂醛5ml、乙醇95ml和5ml 36%盐酸混合,新鲜配制。用于吲哚类衍生物。 (9)呫吨氢醇 0.1g本品溶于90ml乙醇中,加10ml 36%的盐酸,用前新鲜配制。用于色氨酸及其他吲哚类生物碱。 (10)氯化铁-过氯酸 0.5mol/L三氯化铁溶液1ml与35%过氯酸溶液50ml混合。用于吲哚类生物碱。 (11)三氯化铁-碘 三氯化铁5g、碘2g溶于50ml丙酮与50ml 20%酒石酸的混合液中。用于黄嘌呤生物碱类,不同生物碱显不同颜色。 (12)硫酸铈-硫酸(改良Sonnenschein试剂) 硫酸铈0.1g混悬于4ml水中,加1g三氯乙酸,加热煮沸,放冷,逐滴加入浓硫酸直至浑浊消失。用于生物碱、含碘有机化合物的显色,喷后110℃烤几分钟,不同生物碱显不同颜色。 (13)硫氰酸钴(Ⅱ)试液 硫氰酸铵3g、氯化钴1g溶于20ml水中。用于生物碱,伯、仲、叔胺类。 (14)碘化汞钾(Meyer)试剂 1.36g氯化汞和5g碘化钾各溶于20ml水中,混合后加水稀释至100ml即可。 (15)硅钨酸(Bertrand)试剂 5g硅钨酸溶于100ml水中,加盐酸少量调至pH=2左右。(16)苦味酸试剂 1g苦味酸溶于100ml水中。