
第一章
1. 列出5种使用ESA 和5种使用MSA 的分离操作。
答:属于ESA 分离操作的有精馏、萃取精馏、吸收蒸出、再沸蒸出、共沸精馏。 属于MSA 分离操作的有萃取精馏、液-液萃取、液-液萃取(双溶剂)、吸收、吸附。
5.海水的渗透压由下式近似计算:π=RTC/M ,式中C 为溶解盐的浓度,g/cm 3;M 为离子状态的各种溶剂的平均分子量。若从含盐0.035 g/cm 3的海水中制取纯水,M=,操作温度为298K 。问反渗透膜两侧的最小压差应为多少kPa? 答:渗透压π=RTC/M =×298×=。 所以反渗透膜两侧的最小压差应为。
9.假定有一绝热平衡闪蒸过程,所有变量表示在所附简图中。求: (1) 总变更量数Nv;
(2) 有关变更量的独立方程数Nc ; (3) 设计变量数Ni;
(4) 固定和可调设计变量数Nx ,
Na ;
(5) 对典型的绝热闪蒸过程,你
将推荐规定哪些变量?
思路1:
3股物流均视为单相物流, 总变量数Nv=3(C+2)=3c+6 独立方程数Nc 物料衡算式 C 个 热量衡算式1个 相平衡组成关系式C 个 1个平衡温度等式
1个平衡压力等式 共2C+3个 故设计变量Ni
=Nv-Ni=3C+6-(2C+3)=C+3
固定设计变量Nx =C+2,加上节流后的压力,共C+3个 可调设计变量Na =0 解:
V -2
F z i
T F P F
V , y i ,T v , P v
L , x i , T L , P L
习题5附图
(1) Nv = 3 ( c+2 )
(2) Nc 物 c 能 1 相 c 内在(P ,T) 2 Nc = 2c+3 (3) Ni = Nv – Nc = c+3 (4) Nxu = ( c+2 )+1 = c+3 (5) Nau = c+3 – ( c+3 ) = 0 思路2:
输出的两股物流看成是相平衡物流,所以总变量数Nv=2(C+2) 独立方程数Nc :物料衡算式 C 个 ,热量衡算式1个 ,共 C+1个 设计变量数 Ni=Nv-Ni=2C+4-(C+1)=C+3
固定设计变量Nx:有 C+2个加上节流后的压力共C+3个 可调设计变量Na :有0
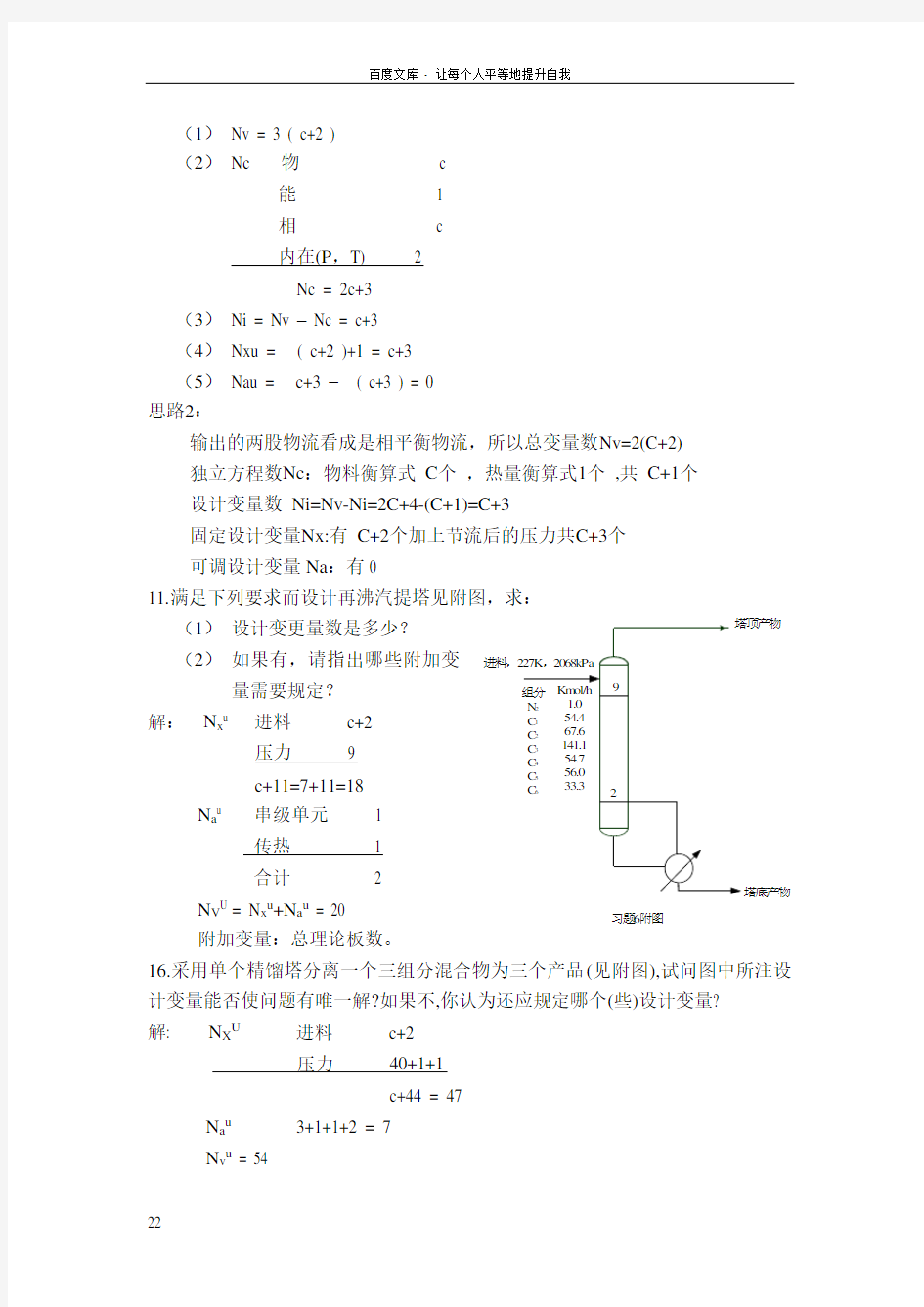
11.满足下列要求而设计再沸汽提塔见附图,求: (1) 设计变更量数是多少? (2) 如果有,请指出哪些附加变
量需要规定?
解: N x u 进料 c+2
压力 9 c+11=7+11=18
N a u 串级单元 1 传热 1 合计 2 N V U = N x u +N a u = 20 附加变量:总理论板数。
16.采用单个精馏塔分离一个三组分混合物为三个产品(见附图),试问图中所注设计变量能否使问题有唯一解?如果不,你认为还应规定哪个(些)设计变量? 解: N X U 进料 c+2 压力 40+1+1 c+44 = 47
N a u 3+1+1+2 = 7 N v u = 54
进料,227K ,2068kP a
组分N 2
C 1
C 2
C 3
C 4
C 5
C 6
K m ol/h
1.054.467.6141.154.756.033.3塔顶产物
底产物
9
2
习题6附图
设计变量:回流比,馏出液流率。
第二章
4.一液体混合物的组成为:苯;甲苯;对二甲苯(摩尔分率)。分别用平衡常数法和相对挥发度法计算该物系在100kPa 式的平衡温度和汽相组成。假设为完全理想系。
解1:
(1)平衡常数法: 设T=368K 用安托尼公式得:
kPa P s 24.1561= ;kPa P s 28.632= ;kPa P s 88.263= 由式(2-36)得:
562.11=K ;633.02=K ;269.03=K
781.01=y ;158.02=y ;067.03=y ;006.1=∑i y 由于∑i y >,表明所设温度偏高。
由题意知液相中含量最大的是苯,由式(2-62)得: 553.11
'1==
∑i
y K K 可得K T 78.367'= 重复上述步骤:
553.1'1=K ;6284.0'
2
=K ;2667.0'3=K 7765.0'1=y ;1511.0'2
=y ;066675.0'3=y ;0003.1=∑i y 在温度为时,存在与之平衡的汽相,组成为:苯、甲苯、对二甲苯。 (2)用相对挥发度法:
设温度为368K ,取对二甲苯为相对组分。计算相对挥发度的: 5.807 13=α ; 2.353 23=α ;000.133=α
组分i
苯(1) 甲苯(2) 对二甲苯(3)
∑
i x
ij α
i ij x α
∑??i
ij i
ij x x αα
解2:
(1)平衡常数法。假设为完全理想系。设t=95℃
苯: 96.11)36.5215.27395/(5.27887936.20ln 1=-+-=s P ;
∴ Pa P s 5110569.1?=
甲苯: 06.11)67.5315.27395/(52.30969065.20ln 2=-+-=s P ;
∴Pa P s 4210358.6?=
对二甲苯:204.10)84.5715.27395/(65.33469891.20ln 3=-+-=s P ;
∴Pa P s 4310702.2?=
569.11010
569.15
5
11=?==
P P K s ;6358.022==
P
P K s
2702
.033==
P
P K s
011.125.06358.025.02702.05.0596.1=?+?+?=∑i i x K
选苯为参考组分:552.1011
.1569
.112==K ;解得T 2=℃ 05.11ln 2=s P ;
Pa P s 4210281.6?= 19.10ln 3=s P ;
Pa P s 43106654.2?=
2K = 3K =
19997.025.02665.025.06281.05.0552.1≈=?+?+?=∑i i x K
故泡点温度为℃,且776.05.0552.11=?=y ;
157.025.06281.02=?=y ;067.025.02665.03=?=y
(2)相对挥发度法
设t=95℃,同上求得1K =,2K =,3K =
807.513=α,353.223=α,133=α
∑=?+?+?=74.325.0125.0353.25.0807.5i i x α
0.174.325
.0174.325.0353.274.35.0807.5=?+∑∑
?+?=∑=i
i i i i x x y αα
故泡点温度为95℃,且776.074
.35
.0807.51=?=
y ;
157.074.325.0353.22=?=
y ;067
.074.325
.013=?=y
11.组成为60%(mol)苯,25%甲苯和15%对二甲苯的100kmol 液体混合物,在和100℃下闪蒸。试计算液体和气体产物的量和组成。假设该物系为理想溶液。用安托尼方程计算蒸气压。
解:在373K 下
苯: ()36.5251.27887936.20ln 1--=T P S kPa P S 315.1791=
77.11=K
甲苯: ()67.5352.30969065.20ln 2--=T P S kPa P S 834.732=
729.02=K
对二甲苯:)84.5765.3346981.20ln 3--=T P S kPa P S 895.313=
315.03=K
计算混合组分的泡点T B T B = 计算混合组分的露点T D T D =
65
.0076.36483.377076.3643731=--=ψ
()()
()
∑
=-ψ+-=ψ040443
.011111i i i K K z f
()()
()[]
∑
-=-ψ+--=ψ414
.01112
12
1'
i i i K K z f
()()7477.01'
112=ψψ-
ψ=ψf f
()00024.02≈-=ψf
此时:x 1=,x 2=,x 3=,L=; y 1=,y 2=,y 3=,V=。
12.用图中所示系统冷却反应器出来的物料,并从较重烃中分离轻质气体。计算离开闪蒸罐的蒸汽组成和流率。从反应器出来的物料温度811K ,组成如下表。闪蒸罐操作条件下各组分的K 值:氢-80;甲烷-10;苯;甲苯
解:以氢为1,甲烷为2,苯为3,甲苯为4。 总进料量为F=460kmol/h ,
4348.01=z ,4348.02=z ,1087.03=z ,0217.04=z 又K1=80,K2=10,K3=,K4= 由式(2-72)试差可得:Ψ=, 由式(2-68)计算得:
y1=,y2=,y3=,y4=;V=h 。 14.在下,对组成为45%(摩尔)正己烷,25%正庚烷及30%正辛烷的混合物。
⑴求泡点和露点温度
⑵将此混合物在下进行闪蒸,使进料的50%汽化。求闪蒸温度,两相的组
成。
解:⑴因为各组分都是烷烃,所以汽、液相均可看成理想溶液,K I 只取决于温
度和压力,可使用烃类的P-T-K 图。 泡点温度计算得:T B =86℃。 露点温度计算得:T D =100℃。
⑵由式(2-76)组分 正己烷 正庚烷 正辛烷 z i K i
()()
111-ψ+-i i
i K z K
组分 流率,mol/h 氢 200 甲烷 200 苯 50 甲苯
10
()()∑≈=-ψ+-00006
.0111i
i
i K z K
所以闪蒸温度为93℃。 由式(2-77)、(2-68)计算得:
x C6=,x C7=,x C8= y C6=,y C7=,y C8=
所以液相中含正己烷%,正庚烷%,正辛烷%; 汽相中含正己烷%,正庚烷%,正辛烷%。
第三章
12.在压力下氯仿(1)-甲醇(2)系统的NRTL 参数为: 12τ=mol ,12τ=mol ,12α=。试确定共沸温度和共沸组成。 安托尼方程(S P :Pa ;T :K)
氯仿:)(16.4679.26968660.20ln 1--=T P S
甲醇:)(29.3455.36264803.23ln 2--=T P S 解:设T 为℃ 则)(16.4665.32679.26968660.20ln 1--=S P )
(29.3465.32655.36264803.23ln 2--=S P S P 1= S P 2=
由)(ij ij ij G τα-=exp ,ij α=ji α
)(121212exp τα-=G =)(9665.83.0exp ?-= )(212121exp τα-=G =)
(8365.03.0exp ?=
??????+++=212
1212
12221212
21212
2
1ln )()(G x x G G x x G x ττγ =???
???+-?+?-+?--21122122
1]06788.01[06788.09665.8]2852.11[2852.18365.01x x x x x )()(
)()(
=??????-+---21
212
193212.016086
.02852.02852.13817.11)()()(x x x
??
????+++=2212121
21212122
12122
1
2
ln )()(G x x G G x x G x ττγ =??????-+?-++-?21
121122
1
]12852.1[2852.18365.006788.0106788.09665.8)()(x x x x x =??????--+-2121212852.02852.107507.193212.0104131.0)()(x x x 1ln γ-2ln γ=S S P P 2
1ln =6.645951
.76990ln
= 求得1x = 1γ= 2γ=
222111γγγ
S
S i S
i i P x P x P x +=∑
=8971.06.6459568.02092.11.7699032.0??+??
= 设T 为60℃
则)
(16.4615.33379.26968660.20ln 1--=S P )(29.3415.33355.36264803.23ln 2--=S P
S P 1= S P 2=
1ln γ-2ln γ=S S P P 21ln =9.845999
.95721ln
= 设T 为56℃
则)(16.4615.32979.26968660.20ln 1--=S P
)(29.3415.32955.36264803.23ln 2--=S P
S P 1= S P 2=
1ln γ-2ln γ=S S P P 21ln =3.717592
.83815ln
= 当1ln γ-2ln γ=时求得1x = 1γ= 2γ=
222111γγγ
S
S i S
i i P x P x P x +=∑
=9500.03.7175970.01099.12.8381530.0??+??
= 某1、2两组分构成二元系,活度系数方程为221ln Ax =γ,2
12ln Ax =γ,端
值常数与温度的关系:A=? (T ,K) 蒸汽压方程为
T P S
4050
0826.16ln 1-
=
T P S 4050
3526.16ln 2-
= (P :kPa :T :K)
假设汽相是理想气体,试问时①系统是否形成共沸物?②共沸温度是多少? 解:设T 为350K
则A=??
3504050
0826.16ln 1-
=S P ;∴S
P 1= kPa
3504050
3526.16ln 2-
=S P ;S
P 2= kPa
因为在恒沸点
由1221112==S S
P P γγα得S
S P
P 1221
=γγ ∴)
()(12122212
1
2121ln ln ln ln x A x x A P P S S -=-=-==γγγγ
)
(1213009.02439.1190284
.91ln
x -=
解得:1x =
2x =
∴2
10513.03009.0ln ?=γ;1γ=
229487.03009.0ln ?=γ;2γ=
P=∑S
i i i P
x γ=????75.99≠ kPa
设T 为340K
则A=??
3404050
0826.16ln 1-
=S P ;S
P 1= kPa
3404050
3526.16ln 2-
=S P ;S
P 2= kPa
由)(121
21ln x A P P S S -=;)(1213434.08458.847695.64ln x -=
解得:1x = 2x ==
∴2
11069.03434.0ln ?=γ;1γ=
228931.03434.0ln ?=γ;2γ=
P=∑S
i i i P
x γ=????75.99≠ kPa
设T 为352K
则A=??
3524050
0826.16ln 1-
=S P ;S
P 1= kPa
3524050
3526.16ln 2-
=S P ;S
P 2= kPa
由)(121
21ln x A P P S S -=;)(1212924.03473.1272143.97ln x -=
∴1x =
2x ==
∴2
10383.02924.0ln ?=γ;1γ=
229617.02924.0ln ?=γ;2γ=
P=∑S
i i i P
x γ=????75.99≈ kPa
说明系统形成共沸物,其共沸温度为352K 。
判断
31
.16738
.7513
.991
2==S S
P
P ,而1γ=,2γ=
? 2
121γγ>>
S
S P P ,且S
S P P P 21,>,
? 故形成最低沸点恒沸物,恒沸物温度为。
? ?
?
第四章 ?
1.某原料气组成如下:
组分 CH 4 C 2H 6 C 3H 8 i-C 4H 10 n-C 4H 10 i-C 5H 12 n-C 5H 12 n-C 6H 14
y 0(摩尔分率)
先拟用不挥发的烃类液体为吸收剂在板式塔吸收塔中进行吸收,平均吸收温度为38℃,压力为,如果要求将i-C 4H 10回收90%。试求: (1) 为完成此吸收任务所需的最小液气比。
(2) 操作液气比为组小液气比的倍时,为完成此吸收任务所需理论板数。 (3) 各组分的吸收分率和离塔尾气的组成。 (4)
求塔底的吸收液量
解:(1)最小液气比的计算:
在最小液气比下 N=∞,A 关=?关=关关)(A K V L ?=min ?=
(2)理论板数的计算: 操
作
液
气
比
min
2.1)
(V L V L
==
?
02
.156
.05712
.0===
关关关V K L A 32.5102
.1log 85.0185.002.1log 1log 1log =---=---=
)
()(A A N ??尾气的数量和组成计算: 非关键组分的i
i VK L
A =
吸收率
11
1--=++N i N i i
A A A ?
被吸收的量为
i N v ??+1,塔顶尾气数量
i
i N v v =-?+)1(1?
塔顶组成
V v y i
i =
1 组分 1+N v
Kmol/h K i
i A
i φ i N v φ1+
i v i y
CH 4 C 2H 6 C 3H 8
i-C 4H 10 n-C 4H 10
i-C 5H 12 n-C 5H 12 n-C 6H 14 合计
-
-
-
(4)塔底的吸收量N L
塔内气体平均流率:
185.90237
.80100=+=
v Kmol/h
塔内液体平均流率:514.51185.905712.020=?=?=+=
均均)(V V L
L L L N
而
N
N L V L V +=++101,即100+0
L =+
N
L
联立求解得N L =h. 0L =h 解2:由题意知,i-C 4H 10为关键组分
由P=,t 平=38℃ 查得K 关= (P-T-K 图) (1)在最小液气比下 N=∞,A 关=中关=
关关)(A K V L ?=min = ?=
(2)min 1.1)(V L V L ==?99.056
.05544
.0===关关关V K L A 所以 理论板数
为
48.9199
.0log 9
.019.099.0log 1log 1log =---=---=
)
()(A A N ??
(3)它组分吸收率公式 i i
VK L
A =,1
1
1
--=++N i N i i A A A ? 组分 进料量 相平衡常数K i i A
i φ 被吸收
量
塔顶尾气 数量
组成 CH 4 C 2H 6 C 3H 8
i-C 4H 10 n-C 4H 10 i-C 5H 12 n-C 5H 12 n-C 6H 14 合计
-
-
-
以CH4为例:
i A =
032.04
.175544
.0==i VK L
i
φ=32.01032.099
.0032.0148.9148.9=--++
V1(CH4)=(1-
i
φ)VN+1=?=
923
.05.7605
.741
1144==
=
V V y CH CH )()(
(3) 塔内气体平均流率:10.902
190
.80100=+=
v Kmol/h
塔内液体平均流率:L=905.92
81.19000+=++L L L )
(
由v l =
0L =h
1.例题2-2 以枯草杆菌为菌种发酵生产蛋白酶,拟用过滤法分离菌体,加助滤剂硅藻土后料液含固体悬浮物的质量体积比为%6.3,黏度 s Pa ??=-3106.6μ。在实验室用直径为的布氏漏斗进行真空抽滤试验,真空 度维持在Pa 4100.9?,经24min 获得滤液34101m -?;且测得滤饼的的压缩系数3 2 =s ,现使用每板面积2352.0m ,框数15的板框压滤机过滤,处理33m 上述发酵液,若操作过程不排渣,且过滤介质阻力m R 可忽略不计。求过滤压降Pa p 510448.3?=?时所需的过滤时间。 2.例题2-3 欲使用转鼓真空过滤机处理一抗生素发酵液,处理量为每小时315m ,过滤面积240m A =,回转速度为min /1r ,操作真空度为Pa 4107?。由于加入了硅藻土助滤剂,滤饼可视作不可压缩的。若滤饼过滤阻力参数 250 /109.22m s p ?=?μαρ,洗涤后滞留于滤饼的可溶性物质为洗涤前的1% (01.0=r ),洗涤效率%70=ε,滤液滞留量为%0.1=f ,求:?转鼓回转一周的过滤时间f t ,?洗涤时间w t 325.00 .160 360015m V f =?= , s t f 3.11)40 25.0(109.22 5=??=, 根据滤饼洗涤效率方程,n r )1(ε-=,代入题给数据得n %)701(01.0-=,n=; 由式子(2-23)可得 01.08.323 .11??=w t ,解得滤饼洗涤时间为s t w 86.0= 3.例题3-1 许多动物细胞都能在葡聚糖颗粒的载体上培养,这些细胞沉降颗粒或微团密度为3/02.1m g ,直径m μ150,一个50升的反应器用来培养细胞,使其生长出一种疫苗,当搅拌停止时,游离的微团下沉而与抗体分
土木工程材料课后习题 第一章 2、当某种材料得孔隙率增大时,表17内其她性质如何变化?(用符号表示:↑增大、↓下降、不变、?不定) 材料长期在水得作用下不被破坏,强度也不显著降低得性质称耐水性 用软化系数来表示K R=f b/f g 工程中将K R>0、85得材料瞧做就是耐水材料,可以用在水中或潮湿环境中得重要结构;用于受潮较轻或次要结构时,材料得K R值也不得低于0、75 4、材料发生渗水与冻融破坏得主要原因就是什么?如何提高材料得抗渗性与抗冻性?材料得孔隙率大,孔径大、开口并连通得空隙多、强度低就是发生渗水与冻融破坏得主要原因。 工程上常采用降低孔隙率、提高密实度、提高闭口孔隙比例、减少裂缝或进行憎水处理等方法提高材料得抗渗性。 工程上常采用降低孔隙率、提高密实度、提高闭口孔隙比例、提高材料得强度等方法提高材料得抗冻性。 5、什么就是材料得导热性?用什么表示?一般如何利用孔隙提高材料得保温性能?导热性就是指材料传导热量得能力。用导热系数来表示。 减少开口孔隙率,提高闭口孔隙率比例。 7、什么就是材料得耐久性?通常用哪些性质来反映? 材料得耐久性就是指其在长期得使用过程中,能抵抗环境得破坏作用,并保持原有性质不变、不破坏得一项综合性质。 通常用抗渗性、抗冻性、抗老化与抗碳化等性质。 8、某工地有砂50t,密度为2、65g/cm3,堆积密度为1450kg/m3;石子100t,密度为2、70g/cm3,堆积密度为1500kg/m3、试计算砂石得空隙率,若堆积高度为1、2m,各需要多大面积存放? 砂:绝对密实体积V1=50*1000/2650=18、87m3 自然状态下得体积V2=50*1000/1450=34、48m3 砂得空隙率为P1=(34、4818、87)/34、48=45、28% 存放面积为S1=3*34、48/1、2=86、2m2 石:绝对密实体积V3=100*1000/2700=37、04m3 自然状态下得体积V4=100*1000/1500=66、67m3 砂得空隙率为P2=(66、6737、04)/66、67=44、44% 存放面积为S2=3*66、67/1、2=166、675m2 第二章 3、花岗石与大理石各有何特性及用途? 花岗石特性:(1)、密度大。(2)、结构致密,抗压强度高。(3)、孔隙率小,吸水率低。(4)、材质坚硬。(5)、装饰性好。(6)、耐久性好。 用途:用于高级建筑结构材料与装饰材料
化工分离过程试题库(复习重点) 第一部分填空题 1、分离作用是由于加入(分离剂)而引起的,因为分离过程是(混合过程)的逆过程。 2、分离因子是根据(气液相平衡)来计算的。它与实际分离因子的差别用(板效率)来表示。 3、汽液相平衡是处理(汽液传质分离)过程的基础。相平衡的条件是(所有相中温度压力相等,每一组分的化学位相等)。 4、精馏塔计算中每块板由于(组成)改变而引起的温度变化,可用(泡露点方程)确定。 5、多组分精馏根据指定设计变量不同可分为(设计)型计算和(操作)型计算。 6、在塔顶和塔釜同时出现的组分为(分配组分)。 7、吸收有(轻)关键组分,这是因为(单向传质)的缘故。 8、对多组分吸收,当吸收气体中关键组分为重组分时,可采用(吸收蒸出塔)的流程。 9、对宽沸程的精馏过程,其各板的温度变化由(进料热焓)决定,故可由(热量衡算)计算各板的温度。 10、对窄沸程的精馏过程,其各板的温度变化由(组成的改变)决定,故可由(相平衡方程)计算各板的温度。 11、为表示塔传质效率的大小,可用(级效率)表示。 12、对多组分物系的分离,应将(分离要求高)或(最困难)的组分最后分离。 13、泡沫分离技术是根据(表面吸附)原理来实现的,而膜分离是根据(膜的选择渗透作用)原理来实现的。 14、新型的节能分离过程有(膜分离)、(吸附分离)。 15、传质分离过程分为(平衡分离过程)和(速率分离过程)两大类。 16、分离剂可以是(能量)和(物质)。 17、Lewis 提出了等价于化学位的物理量(逸度)。 18、设计变量与独立量之间的关系可用下式来表示( Ni=Nv-Nc即设计变量数=独立变量数-约束关系 ) 19、设计变量分为(固定设计变量)与(可调设计变量)。 20、温度越高对吸收越(不利) 21、萃取精馏塔在萃取剂加入口以上需设(萃取剂回收段)。 22、用于吸收过程的相平衡关系可表示为(V = SL)。 23、精馏有(两个)个关键组分,这是由于(双向传质)的缘故。 24、精馏过程的不可逆性表现在三个方面,即(通过一定压力梯度的动量传递),(通过一定温度梯度的热量传递或不同温度物流的直接混合)和(通过一定浓度梯度的质量传递或者不同化学位物流的直接混合)。 25、通过精馏多级平衡过程的计算,可以决定完成一定分离任务所需的(理论板数),为表示塔实际传质效率的大小,则用(级效率)加以考虑。 27、常用吸附剂有(硅胶),(活性氧化铝),(活性炭)。 28、恒沸剂与组分形成最低温度的恒沸物时,恒沸剂从塔(顶)出来。
[例2-3] 求含正丁烷(1)0.15、正戊烷(2)0.4、和正已烷(3)0.45(摩尔分数)之烃类混合物在0.2MPa 压力下的泡点温度。B. 露点温度 a. 解:因各组分都是烷烃,所以汽、液相均可看成理想溶液, K i 只取决于温度和压力。如计算要求不高,可使用烃类的 p -T -K 图(见图 2-1)。 假设 T = 50℃, p =0.2MPa ,查图求 K i , 组分 xi Ki yi=Kixi 正丁烷 0.15 2.5 0.375 正戊烷 0.40 0.76 0.304 正已烷 0.45 0.28 0.126 说明所设温度偏低,选正丁烷为K G ,95.0805 .076 .03==∑=i G y K K 。查p-t-k 图t 为58.7, 再设 T = 58.7℃,重复上述计算得 故泡点温度为 58.7℃。 解:B. 露点温度, 假设 T = 80℃, p =0.2MPa ,查图求 K i , 组分 xi Ki yi/Ki=xi 正丁烷 0.15 4.2 0.036 正戊烷 0.40 1.6 0.25 正已烷 0.45 0.65 0.692 1978.0≠=∑=∑∴i i i K y x 选正戊烷为参考组分,则 56.1978.06.14=?=∑?=i G x K K 由56.14=K ,查图2-1a 得t=78℃ K 1=4,K 2=1.56, K 3=0.6, 1053.175.0267.00375.0≈=++=∑ =∑∴i i i K y x
故混合物在78℃。 [例2-7] 进料流率为 1000kmol/ h的轻烃混合物,其组成为:丙烷 (1)30% ;正丁烷 (2)10% ;正戊烷 (3)15% ;正已烷 (4)45%( 摩尔 ) 。求在50 ℃和 200kPa 条件下闪蒸的汽、液相组成及流率。 解:该物系为轻烃混合物,可按理想溶液处理。由给定的T 和p ,从p - T - K 图查K i ,再采用上述顺序解法求解。 (1)核实闪蒸温度 假设50℃为进料泡点温度,则 假设50℃为进料的露点温度,则 说明进料的实际泡点和露点温度分别低于和高于规定的闪蒸温度,闪蒸问题成立。 (2)求Ψ ,令Ψ 1 =0.1(最不利的初值) =0.8785 因f (0.1)>0,应增大Ψ 值。因为每一项的分母中仅有一项变化,所以可以写出仅含未知数Ψ 的一个方程: 计算R - R 方程导数公式为:
第一章 金属的性能 一、填空(将正确答案填在横线上。下同) 1、金属材料的性能一般分为两类。一类是使用性能,它包括物理性能、化学性能和力学性能等。另一类是工艺性能,它包括铸造性能、锻造性能、焊接性能和切削加工性能等。 2、大小不变或变化很慢的载荷称为静载荷,在短时间内以较高速度作用于零件上的载荷称为冲击载荷,大小和方向随时间发生周期变化的载荷称为交变载荷。 3、变形一般分为弹性变形和塑性变形两种。不能随载荷的去除而消失的变形称为塑性变形。 4、强度是指金属材料在静载荷作用下,抵抗塑性变形或断裂的能力。 5、强度的常用衡量指标有抗拉强度和屈服强度,分别用符号σb 和σs 表示。 6、如果零件工作时所受的应力低于材料的σb 或σ0.2,则不会产生过量的塑性变形。 7、有一钢试样其截面积为100mm 2,已知钢试样的MPa S 314=σ MPa b 530=σ 。拉伸试验时,当受到拉力为—————— 试样出现屈服现象,当受到拉力为—————— 时,试样出现缩颈。 8、断裂前金属材料产生永久变形的能力称为塑性。金属材料的延伸率和断面收缩率的数值越大,表示材料的塑性越好。 9、一拉伸试样的原标距长度为50mm,直径为10mm 拉断后试样的标距长度为79mm ,缩颈处的最小直径为4.9 mm ,此材料的伸长率为—————,断面收缩率为——————。 10.金属材料抵抗冲击载荷作用而不破坏能力。称为冲击韧性。 11.填出下列力学性能指标的符号:屈服点σs ,抗拉强度σb ,洛氏硬度C 标尺HRC , 伸长率δ,断面收缩率ψ,冲击韧度αk ,疲劳极限σ-1。 二、判断(正确打√,错误打×。下同) 1、弹性变形能随载荷的去除而消失。(√ ) 2、所有金属材料在拉伸试验时都会出现显着的屈服现象。(× ) 3、材料的屈服点越低,则允许的工作应力越高。(× ) 4、洛氏硬度值无单位。(√ ) 5、做布氏硬度试验时,当试验条件相同时,其压痕直径越小,材料的硬度越低。(× ) 6、材料对小能量多次冲击抗力的大小主要取决于材料的强度和塑性。( ×) 7、布氏硬度测量法不宜于测量成品及较薄零件。( √) 8、洛氏硬度值是根据压头压入被测定材料的压痕深度得出的。(√ ) 9、铸铁的铸造性能比钢好,故常用来铸造形状复杂的工件。(√ ) 三.选择(把正确答案填入括号内。下同) 1、拉伸试验时,试样拉断前所能承受的最大应力称为材料的(B )。 A.屈服点 B.抗拉强度 C.弹性极限 2、做疲劳试验时,试样承受的载荷为(C ) A.静载荷 B.冲击载荷 C 交变载荷 3、洛氏硬度C 标尺所用的压头是( B ) A..淬硬钢球 B.金刚石圆锥体 C.硬质合金球 4.金属材料抵抗塑性变形或断裂的能力称为(C ) A..塑性 B.硬度 C.强度 5.用拉伸试验可测定材料的(A )性能指标。 A..强度 B.硬度 C.韧性
生物分离工程练习题1 https://www.doczj.com/doc/152706968.html,work Information Technology Company.2020YEAR
《生物分离工程》练习题 绪论 1.生物分离过程包括目标产物的提取、浓缩、纯化。 2.生物分离过程的显著特点是什么? 1、条件温和 2、安全性、卫生性要求高 3、方法需要具有高选择性 4、对原料高度浓 缩 3.评价一个分离过程的效率主要有三个标准,目标产物的浓缩程度、分离纯化程 度、回收率。 4.图中F表示流速,c表示浓度;下标T和X分别表示目标产物和杂质。C、P和W分别 表示原料、产品和废料。写出产品浓缩率m、分离因子α、回收率REC的计算公式。 书本第九页 第一章细胞分离与破碎 1.在细胞分离中,细胞的密度ρS越大,细胞培养液的密度ρL越小,则细胞沉降 速率越大。 2.过滤中推动力要克服的阻力有过滤介质阻力和滤饼阻力,其中滤饼占 主导作用。 3.B可以提高总回收率。 A.增加操作步骤 B.减少操作步骤 C.缩短操作时间 D.降低每一步的收率 4.重力沉降过程中,固体颗粒不受C的作用。 A.重力 B.摩擦力 C.静电力 D.浮力 5.过滤的透过推动力是D 。 A.渗透压 B.电位差 C.自由扩散 D.压力差 6.在错流过滤中,流动的剪切作用可以B。 A.减轻浓度极化,但增加凝胶层的厚度 B.减轻浓度极化,但降低凝胶层的 厚度 C.加重浓度极化,但增加凝胶层的厚度 D.加重浓度极化,但降低凝胶层的 厚度 7.重力沉降过程中,固体颗粒受到重力,浮力,流体摩擦阻力的作用,当 固体匀速下降时,三个力的关系平衡 8.撞击破碎适用于D的回收。 A.蛋白质 B.核酸 C.细胞壁 D.细胞器
工程材料 第一章金属的晶体结构与结晶 1.解释下列名词 点缺陷:原子排列不规则的区域在空间三个方向尺寸都很小,主要指空位间隙原子、置换原子等。 线缺陷:原子排列的不规则区域在空间一个方向上的尺寸很大,而在其余两个方向上的尺寸很小。 如位错。 面缺陷:原子排列不规则的区域在空间两个方向上的尺寸很大,而另一方向上的尺寸很小。如晶界和亚晶界。 亚晶粒:在多晶体的每一个晶粒内,晶格位向也并非完全一致,而是存在着许多尺寸很小、位向差很小的小晶块,它们相互镶嵌而成晶粒,称亚晶粒。 亚晶界:两相邻亚晶粒间的边界称为亚晶界。 刃型位错:位错可认为是晶格中一部分晶体相对于另一部分晶体的局部滑移而造成。滑移部分与未滑移部分的交界线即为位错线。如果相对滑移的结果上半部分多出一半原子面,多余半 原子面的边缘好像插入晶体中的一把刀的刃口,故称“刃型位错”。 单晶体:如果一块晶体,其内部的晶格位向完全一致,则称这块晶体为单晶体。 多晶体:由多种晶粒组成的晶体结构称为“多晶体”。 过冷度:实际结晶温度与理论结晶温度之差称为过冷度。 自发形核:在一定条件下,从液态金属中直接产生,原子呈规则排列的结晶核心。 非自发形核:是液态金属依附在一些未溶颗粒表面所形成的晶核。 变质处理:在液态金属结晶前,特意加入某些难熔固态颗粒,造成大量可以成为非自发晶核的固态质点,使结晶时的晶核数目大大增加,从而提高了形核率,细化晶粒,这种处理方法即 为变质处理。 变质剂:在浇注前所加入的难熔杂质称为变质剂。 2.常见的金属晶体结构有哪几种?α-Fe 、γ- Fe 、Al 、Cu 、Ni 、Pb 、Cr 、V 、Mg、Zn 各属何种晶体结构?
2007 —2008 学年第1、2学期分离工程课程期末考试试卷(A 卷)答案及评分标准 二、选择题(本大题20分,每小题2分) 1、由1-2两组分组成的混合物,在一定T 、P 下达到汽液平衡,液相和汽相组成分别为 11,y x ,若体系加入10 mol 的组分(1),在相同T 、P 下使体系重新达到汽液平衡,此时汽、液相的组成分别为 ' 1'1,y x ,则 ( C ) (A )1'1x x >和 1'1y y > (B )1'1x x <和1'1y y < (C )1'1x x =和1'1y y = (D )不确定 2、对于绝热闪蒸过程,当进料的流量组成及热状态给定之后,经自由度分析,只剩下一个自由度由闪蒸罐确定,则还应该确定的一个条件是 ( D ) (A )闪蒸罐的温度 (B )闪蒸罐的压力 (C )气化率 (D )任意选定其中之一 3、某二元混合物,其中A 为易挥发组分,液相组成5.0=A x 时泡点为1t ,与之相平衡的气相组成75.0=A y 时,相应的露点为2t ,则 ( A ) (A )21t t = (B )21t t > (C )21t t < (D )不能确定 4、用郭氏法分析可知理论板和部分冷凝可调设计变量数分别为 ( A ) (A )1,1 (B )1,0 (C )0,1 (D )0,0 5、如果二元物系有最高压力恒沸物存在,则此二元物系所形成的溶液一定是 ( A ) (A )正偏差溶液 (B )理想溶液 (C )负偏差溶液 (D )不一定 6、用纯溶剂吸收混合气中的溶质,逆流操作,平衡关系满足亨利定律。当入塔气体浓度y 1上升,而其它入塔条件不变,则气体出塔浓度y 2和吸收率的变化为 ( C ) (A )y 2上升,下降 (B )y 2下降,上升 (C )y 2上升,不变 (D )y 2上升,变化不确定 7、逆流填料吸收塔,当吸收因数A 1且填料为无穷高时,气液两相将在哪个部位达到平衡 ( B ) (A) 塔顶 (B)塔底 (C)塔中部 (D)塔外部 8、平衡常数较小的组分是 ( D ) (A )难吸收的组分 (B )较轻组份 (C )挥发能力大的组分 (D )吸收剂中的溶解度大 9、吸附等温线是指不同温度下哪一个参数与吸附质分压或浓度的关系曲线。 ( A ) (A) 平衡吸附量 (B) 吸附量 (C) 满吸附量 (D)最大吸附量 10、液相双分子吸附中,U 型吸附是指在吸附过程中吸附剂 ( A ) (A) 始终优先吸附一个组分的曲线 (B) 溶质和溶剂吸附量相当的情况 (C) 溶质先吸附,溶剂后吸附 (D) 溶剂先吸附,溶质后吸附
【最新资料,WORD文档,可编辑修改】
工程材料 思考题参考答案 第一章金属的晶体结构与结晶 1.解释下列名词 点缺陷,线缺陷,面缺陷,亚晶粒,亚晶界,刃型位错,单晶体,多晶体,过冷度,自发形核,非自发形核,变质处理,变质剂。 答:点缺陷:原子排列不规则的区域在空间三个方向尺寸都很小,主要指空位 间隙原子、 置换原子等。 线缺陷:原子排列的不规则区域在空间一个方向上的尺寸很大,而在其余两个 方向 上的尺寸很小。如位错。 面缺陷:原子排列不规则的区域在空间两个方向上的尺寸很大,而另一方向上 的尺 寸很小。如晶界和亚晶界。 亚晶粒:在多晶体的每一个晶粒内,晶格位向也并非完全一致,而是存在着许 多尺寸 很小、位向差很小的小晶块,它们相互镶嵌而成晶粒,称亚晶粒。 亚晶界:两相邻亚晶粒间的边界称为亚晶界。 刃型位错:位错可认为是晶格中一部分晶体相对于另一部分晶体的局部滑移而 造成。 滑移部分与未滑移部分的交界线即为位错线。如果相对滑移的结果上半部
口,故称“刃型位错”。 单晶体:如果一块晶体,其内部的晶格位向完全一致,则称这块晶体为单晶体。 多晶体:由多种晶粒组成的晶体结构称为“多晶体”。 2 过冷度:实际结晶温度与理论结晶温度之差称为过冷度。 自发形核:在一定条件下,从液态金属中直接产生,原子呈规则排列的结晶核 心。 非自发形核:是液态金属依附在一些未溶颗粒表面所形成的晶核。 变质处理:在液态金属结晶前,特意加入某些难熔固态颗粒,造成大量可以成 为非自 发晶核的固态质点,使结晶时的晶核数目大大增加,从而提高了形核率, 细化晶粒,这种处理方法即为变质处理。 变质剂:在浇注前所加入的难熔杂质称为变质剂。 2. 常见的金属晶体结构有哪几种?α-Fe 、γ- Fe 、Al 、Cu 、Ni 、Pb 、 Cr 、V 、 Mg 、Zn 各属何种晶体结构? 答:常见金属晶体结构:体心立方晶格、面心立方晶格、密排六方晶格; α-Fe、Cr、V 属于体心立方晶格; γ-Fe 、Al、Cu、Ni、Pb 属于面心立方晶格; Mg、Zn 属于密排六方晶格; 3. 配位数和致密度可以用来说明哪些问题? 答:用来说明晶体中原子排列的紧密程度。晶体中配位数和致密度越大,则晶
MESH方程。 一、填空(每空2分,共20分) 1. 如果设计中给定数值的物理量的数目等于 设计变量,设计才有结果。 2. 在最小回流比条件下,若只有重组分是非分 配组分,轻组分为分配组分,存在着两个 恒浓区,出现在精镏段和进料板 位置。 3. 在萃取精镏中,当原溶液非理想性不大时, 加入溶剂后,溶剂与组分1形成具有较强正 偏差的非理想溶液,与组分2形成 负偏差或理想溶液,可提高组分1对2的 相对挥发度。 4. 化学吸收中用增强因子表示化学反应对传质 速率的增强程度,增强因子E的定义是化学吸 收的液相分传质系数(k L)/无化学吸收的液相 分传质系数(k0L)。 5. 对普通的N级逆流装置进行变量分析,若组 分数为C个,建立的MESH方程在全塔有 NC+NC+2N+N=N(2C+3) 个。 η; 6. 热力学效率定义为= 实际的分离过程是不可逆的,所以热力学效 率必定于1。 7. 反渗透是利用反渗透膜选择性的只透过 溶剂的性质,对溶液施加压力,克服溶 剂的渗透压,是一种用来浓缩溶液的膜 分离过程。 二、推导(20分) 1. 由物料衡算,相平衡关系式推导图1单 级分离基本关系式。 ——相平衡常数; 式中: K i ψ——气相分 率(气体量/进料量)。 2. 精馏塔第j级进出物料如图1,建立
三、简答(每题5分,共25分) 1.什么叫相平衡相平衡常数的定义是什么 由混合物或溶液形成若干相,这些相保持物理平衡而共存状态。热力学上看物系的自由焓最小;动力学上看相间表观传递速率为零。 K i =y i /x i 。 2.关键组分的定义是什么;在精馏操作中, 一般关键组分与非关键组分在顶、釜的 分配情况如何 由设计者指定浓度或提出回收率的组分。 LK绝大多数在塔顶出现,在釜中量严格控制; HK绝大多数在塔釜出现,在顶中量严格控制; LNK全部或接近全部在塔顶出现; HNK全部或接近全部在塔釜出现。 3.在吸收过程中,塔中每级汽、液流量为 什么不能视为恒摩尔流 吸收为单相传质过程,吸收剂吸收了气体中的溶质而流量在下降过程中不断增加,气体的流量相应的减少,因此气液相流量在塔内都不能视为恒定。 4.在精馏塔中设中间换热器为什么会提高 热力学效率 在中间再沸器所加入的热量其温度低于塔 底加入热量的温度,在中间冷凝器所引出的 热量其温度高于塔顶引出热量的温度,相对 于无中间换热器的精馏塔传热温差小,热力 学效率高。 5.反应精馏的主要优点有那些 (1)产物一旦生成立即移出反应区;(2)反应区反应物浓度高,生产能力大;(3)反应热可由精馏过程利用;(4)节省设备投资费用;(5)对于难分离物系通过反应分离成较纯产品。 四、计算(1、2题10分,3题15分,共35分) 1. 将含苯(mol分数)的苯(1)—甲苯(2)混合物在下绝热闪蒸,若闪蒸温度为94℃,用计算结果说明该温度能否满足闪蒸要求 已知:94℃时P 1 0= P 2 0= 2. 已知甲醇(1)和醋酸甲酯(2)在常压、54℃ 下形成共沸物,共沸组成X 2 =(mol分率), 在此条件下:kPa P kPa p98 . 65 , 24 . 9002 1 = =求 该系统的活度系数。 3. 气体混合物含乙烷、丙烷、丁烷(均为摩尔分数),用不挥发的烃类进行吸收,已知吸收后丙烷的吸收率为81%,取丙烷在全塔的平均吸收因子A=,求所需理论板数;若其它条件不变,提高平均液汽比到原来的2倍,此时丙烷的吸 收率可达到多少。
1- 5在下面几种情况下,该用什么方法来测试硬度?写出硬度符号。 (1 )检查锉刀、钻头成品硬度;(2)检查材料库中钢材硬度;(3)检查薄壁工件的硬度或工件表面很薄的硬化层;(4)黄铜轴套;(5)硬质合金刀片; (1 )检查锉刀、钻头成品硬度采用洛氏硬度试验来测定,硬度值符号HRC。 (2)检查材料库中钢材硬度采用布氏硬度试验来测定,硬度值符号 HBW。 (3 )检查薄壁工件的硬度或工件表面很薄的硬化层硬度采用洛氏硬度试验来测定,硬度值符号HRC。 (4)黄铜轴套硬度采用布氏硬度试验来测定,硬度值符号HBW。(5)硬质合金刀片采用洛氏硬度试验来测定,硬度值符号HRC。 2- 4单晶体和多晶体有何差别?为什么单晶体具有各向异性,多晶体具有各项同性? 单晶体是由原子排列位向或方式完全一致的晶格组成的;多晶体是由很多个小的单晶体所组成的,每个晶粒的原子位向是不同的。因为单晶体内各个方向上原子排列密度不同,造成原子间结合力不同,因而表现出 各向异性;而多晶体是由很多个单晶体所组成,它在各个方向上的力相互抵消平衡,因而表现各向同性。 2-5简述实际金属晶体和理想晶体在结构与性能上的主要差异。理想晶体中原子完全为规则排列,实际金属晶体由于许多因素的影响,使这些原子排列受到干扰和破坏,内部总是存在大量缺陷。如果金属中 无晶体缺陷时,通过理论计算具有极高的强度,随着晶体中缺陷的增加,金属的强度迅速下降,当缺陷增加到一定值后,金属的强度又随晶体缺陷的增加而增加。因此,无论点缺陷,线缺陷和面缺陷都会造成晶格崎变,从而使晶体强度增加。同时晶体缺陷的存在还会增加金属的电阻,
降低金属的抗腐蚀性能。 2- 6简述间隙固溶体和间隙化合物的异同点。 间隙固溶体和间隙化合物都是溶质原子嵌入晶格间隙形成的。间隙固溶体的晶体结构与溶剂的结构相同,而间隙化合物的晶体结构不同于组成它的任一组元,它是以分子式来表示其组成。 3- 3常用的管路焊锡为成分w(Pb=50%)、w(Sn=50%)的Pb-Sn合金。 若该合金以及慢速度冷却至室温,求合金显微组织中相组成物和组织组成物的相对量。 吨r-i ⑷ I叽 Sn
资料内容仅供您学习参考,如有不当或者侵权,请联系改正或者删除。 《分离工程》练习题 第一章绪论 ( 一) 填空题 1、分离作用是由于加入_______而引起的, 因为分离过程是熵________过程。 2、分离过程是________的逆过程, 因此需加入__________来达到分离目的。 3、衡量分离的程度用____________表示, 处于相平衡状态的分离程度是_________________.。 4、分离因子表示任一分离过程所达到的____________, 其定义为_____________________。 5、分离因子____________, 则表示组分i及j之间不能被分离。 6、分离剂能够是___________或____________, 有时也可两种同时应用。 7、平衡分离的分离基础是利用两相平衡_____________的原理, 常采用____________作为处理手段, 并把其它影响归纳于___________。 8、速率分离的机理是利用溶液中不同组分在某种___________作用下经过某种介质时的__________差异而实现分离。 9、分离过程是将一混合物转变为组成__________的两种或几种产品的哪些操作。 10、分离工程研究分离过程中分离设备的___________。 11、传质分离过程分为____________和____________两类。 12、速率分离可分为__________和__________两大类。 13、分离过程中按有无物质传递现象发生来划分, 分离过程可分为__________和__________。 ( 二) 简答题 1、列出5种使用ESA和5种使用MSA的分离操作。 2、比较使用ESA与MSA分离方法的优缺点。 3、平衡分离过程和速率分离过程各有何特点? 4、怎样用分离因子判断分离过程进行的难易程度? 5、根据两相状态不同 , 平衡分离过程可分成几类 6、为什么要进行分离过程的的耦合及集成, 有何好处?
二、选择题(本大题20分,每小题2分) 1、由1-2两组分组成的混合物,在一定T 、P 下达到汽液平衡,液相和汽相组成分别为 11,y x ,若体系加入10 mol 的组分(1),在相同T 、P 下使体系重新达到汽液平衡,此时汽、液相的组成分别为 '1'1,y x ,则 ( C ) (A )1'1x x >和 1'1y y > (B )1'1x x <和1'1y y < (C )1'1x x =和1'1y y = (D )不确定 2、对于绝热闪蒸过程,当进料的流量组成及热状态给定之后,经自由度分析,只剩下一个自由度由闪蒸罐确定,则还应该确定的一个条件是 ( D ) (A )闪蒸罐的温度 (B )闪蒸罐的压力 (C )气化率 (D )任意选定其中之一 3、某二元混合物,其中A 为易挥发组分,液相组成5.0=A x 时泡点为1t ,与之相平衡的气相组成75.0=A y 时,相 应的露点为2t ,则 ( A ) (A )21t t = (B )21t t > (C )21t t < (D )不能确定 4、用郭氏法分析可知理论板和部分冷凝可调设计变量数分别为 ( A ) (A )1,1 (B )1,0 (C )0,1 (D )0,0 5、如果二元物系有最高压力恒沸物存在,则此二元物系所形成的溶液一定是 ( A ) (A )正偏差溶液 (B )理想溶液 (C )负偏差溶液 (D )不一定 6、用纯溶剂吸收混合气中的溶质,逆流操作,平衡关系满足亨利定律。当入塔气体浓度y 1上升,而其它入塔条件不变,则气体出塔浓度y 2和吸收率的变化为 ( C ) (A )y 2上升,下降 (B )y 2下降,上升 (C )y 2上升,不变 (D )y 2上升,变化不确定 7、逆流填料吸收塔,当吸收因数A 1且填料为无穷高时,气液两相将在哪个部位达到平衡 ( B ) (A) 塔顶 (B)塔底 (C)塔中部 (D)塔外部 8、平衡常数较小的组分是 ( D ) (A )难吸收的组分 (B )较轻组份 (C )挥发能力大的组分 (D )吸收剂中的溶解度大 9、吸附等温线是指不同温度下哪一个参数与吸附质分压或浓度的关系曲线。 ( A ) (A) 平衡吸附量 (B) 吸附量 (C) 满吸附量 (D)最大吸附量
分离工程习题 四、计算题: 1、已知某混合物含0.05乙烷,0.30丙烷和0.65正丁烷(摩尔分率),操作压力下各组分的平衡常数可按下式进行计算,试求其泡点温度。 乙烷: K=0.13333t+5.46667 丙烷: K=0.06667t+1.13333 正丁烷: K=0.02857t+0.08571 (t 的单位为℃) 解:设温度为10℃, 用泡点方程∑=1x K i i 进行试差,不满足泡点方程, 设温度为7.2℃,重新试差,满足泡点方程,泡点温度为7.2℃,结果见表。 2、已知某混合物含0.05乙烷,0.30丙烷和0.65正丁烷(摩尔分率),操作压力下各组分的平衡常数可按下式进行计算,试求其露点温度。 乙烷: K=0.13333t+5.46667 丙烷: K=0.06667t+1.13333 正丁烷: K=0.02857t+0.08571 (t 的单位为℃) 解:设温度为24℃, 用泡点方程∑=1K /y i i 进行试差,不满足露点方程, 设温度为23℃,重新试差,满足露点方程,露点温度为23℃,结果见表。 3、一轻烃混合物进行精馏塔的计算,求得最小回流 比Rm=1.45,最小理论板数Nm=8.6,现取操作回流比 为R=1.25Rm ,全塔平均板效率为n=0.60,求所 需的实际塔板数。 解:R=1.25Rm=1.25×1.45=1.8125 R R R m -+=-+=118125145181251013.. .. 由图查得, N Nm -=053.
实际板数为=19.43/0.6 =32.4=33块 4、某多组分精馏塔的原料组成、产品组成(组分1为轻关键组分)及各组分的相对挥发度如表所示,已知提馏段第n 板上升的气相组成,提馏段操作线方程为x n+1,i =0.8y n,i +0.2x w,i ,精馏段操作线方程为 x y x n i n i D i ,,,..=--12021。试求离开第n+2板的液相组成。(要求各板组成列表)(塔序从下往上,第n+1 解:(1)用提馏段操作线方程x n+1,i =0.8y n,i +0.2x w,i ,计算'i ,1n x +,即 381.0013.02.0473.08.0x 2.0y 8.0x 1,W 1,n 1,1n =?+?=+=+ 其他组分的计算结果列于表。 (2)用相平衡方程 ∑ +++αα= 'i ,1n 'i ,1n 'i ,1n x x y ,计算'i ,1n y +,计算结果列于表。 (3)由于第n+1板为进料板为进料板,所以,用精馏段操作线方程x y x n i n i D i ,,,..=--12021,计算'i ,2n x +,即 5508.0980.02.06223.02.1x 2.0y 2.1x 1,D 1,1n 1,2n =?-?=-=++其他组分的计算结果列于表。 (4)计算结果汇总 'i ,1n x + 'i ,1n x +α y 'i ,1n + i ,2n x + 1 0.3810 0.9335 0.6223 0.5508 2 0.5234 0.5234 0.3489 0.4147 3 0.0502 0.0246 0.016 4 0.0197 4 0.0454 0.0186 0.0124 0.0149 Σ 1.0000 1.5000 1.0001 5、已知组分1和组分2所构成的二元系统, 当处于汽-液-液平衡时, 两个平衡的液相组成如 下:x x 21005005αβ==.,., 两个纯组分的饱和蒸汽压此时分别为P amt P atm 1020065075==.,.,此对称系统的范拉尔常数(用Ln 表示)为A=3.272 求:(1)γγαβ21, (2)平衡压力 (3)平衡的气相 组成。 解:(1)由范拉尔方程计算活度系数 00818 .00.053.272)A(x ln γ953.20.05)(13.272)x 1A(ln γ2 2β1 β 2 2221=?== =-?=-=ββ 008 .1γ 16 .19γβ2 1==β 16 .19γ 008.1γ2 α1==α (2)3411.17185.06226.0x γP x γP P α 2α202β1β101=+=+=
第一章 2.图1-79为五种材料的应力-应变曲线:①45钢,②铝青铜,③35钢,④硬铝,⑤纯铜。试问: (1)当外加应力为300MPa时,各材料处于什么状态? (2)有一用35钢制作的杆,使用中发现弹性弯曲较大,如改用45钢制作该杆,能否减少弹性变形? (3)有一用35钢制作的杆,使用中发现塑性变形较大,如改用45钢制作该杆,能否减少塑性变形? 答:(1)①45钢:弹性变形②铝青铜:塑性变形③35钢:屈服状态④硬铝:塑性变形⑤纯铜:断裂。 (2)不能,弹性变形与弹性模量E有关,由E=σ/ε可以看出在同样的条件下45钢的弹性模量要大,所以不能减少弹性变形。 (3)能,当35钢处于塑性变形阶段时,45钢可能处在弹性或塑性变形之间,且无论处于何种阶段,45钢变形长度明显低于35钢,所以能减少塑性变形。 4.下列符号表示的力学性能指标的名称和含义是什么? σb 、σs、σ0.2、σ-1、δ、αk、HRC、HBS、HBW 答:σb抗拉强度,是试样保持最大均匀塑性的极限应力。 σs屈服强度,表示材料在外力作用下开始产生塑性变形时的最低应力。 σ0.2条件屈服强度,作为屈服强度的指标。 σ-1疲劳强度,材料循环次数N次后达到无穷大时仍不发生疲劳断裂的交变应力值。 δ伸长率,材料拉断后增加的变形长度与原长的比率。 HRC洛氏硬度,表示用金刚石圆锥为压头测定的硬度值。 HBS布氏硬度,表示用淬硬钢球为压头测定的硬度值。 HBW布氏硬度,表示用硬质合金为压头测定的硬度值。 7.常见的金属晶体结构有哪几种?α-Fe 、γ- Fe 、Al 、Cu 、Ni 、Pb 、Cr 、V 、Mg、Zn 各属何种晶体结构? 答:常见金属晶体结构:体心立方晶格、面心立方晶格、密排六方晶格; α-Fe、Cr、V属于体心立方晶格; γ-Fe 、Al、Cu、Ni、Pb属于面心立方晶格; Mg、Zn属于密排六方晶格; 8.什么是固溶强化?造成固溶强化的原因是什么? 答:形成固溶体使金属强度和硬度提高,塑性和韧性略有下降的现象称为固溶强化。
2013化工分离过程期中考试试题答案 一、填空题(每空1分,共20分) 1. 传质分离过程分为(平衡分离过程)和(速率分离过程)两大类。 2. 分离作用是由于加入(分离剂)而引起的,因为分离过程是(混合过程)的逆过程。 3. 汽液相平衡是处理(传质分离)过程的基础,相平衡的条件是(各相温度压力相等,各组分在每一相中的化学位相等)。 4. 当混合物在一定的温度、压力下,进料组成z i 和相平衡常数K i 满足 ( 1,1>>∑∑i i i i K z z K )条件即处于两相区,可通过(物料平衡和相平衡)计算求出其平衡汽液相组成。 5. 精馏塔计算中每块板由于(组成)改变而引起的温度变化,可用(泡露点方程)确定。 6. 多组分精馏根据指定设计变量不同可分为(设计)型计算和(操作)型计算。 7. 最低恒沸物,压力降低使恒沸组成中汽化潜热(小)的组分增加。 8. 萃取精馏中塔顶产品不合格时,经常采取(增加萃取剂用量)或(减小进料量)的措施使产品达到分离要求。 9. 吸收有(1个)关键组分,这是因为(单向传质)的缘故。 10.吸收剂的再生常采用的是(用蒸汽或惰性气体的蒸出塔)、(用再沸器的蒸出塔)和(用蒸馏塔)。 二、单项选择题(每小题1分,共10分) 1. 吸收属于(A ) A.平衡分离;B.速率分离;C.机械分离;D.膜分离。 2. 计算溶液泡点时,若∑=>-C i i i X K 101,则说明(C ) A. 温度偏低; B. 正好泡点; C. 温度偏高。 3. 如果体系的汽相为理想气体,液相为非理想溶液;则相平衡常数可以简化表示为 ( D ) A. L i i V i K φφ= B. s i i P K P = C. $$L i i V i K φ φ= D. s i i i P K P γ= 4. 汽液相平衡K 值越大,说明该组分越( A ) A.易挥发; B.难挥发; C.沸点高; D.蒸汽压小。 5. 如果塔顶采用全凝器,计算塔顶第一级的温度可以利用方程( B ) A.泡点方程; B.露点方程; C. 闪蒸方程; D.相平衡方程。 6. 计算在一定温度下与已知液相组成成平衡的汽相组成和压力的问题是计算( B ) A.泡点温度; B.泡点压力; C.等温闪蒸; D.露点压力。 7. 精馏中用HNK 表示( C ) A. 轻关键组分; B. 重关键组分; C. 重非关键组分; D. 轻非关键组分。 8. 以下描述中,不属于萃取精馏中溶剂的作用的是( D )
分离工程习题 一、填空: 1、分离过程分为(机械分离方法)和(传质分离)两大类。 2、传质分离过程分为(平衡分离过程)和(速率分离过程)两大类。 3、分离剂可以是(能量)和(物质)。 4、机械分离过程是(过滤、离心分离)、旋风分离、静电除尘 5、速率分离过程是超滤、渗析(膜分离、渗透)。 6、平衡分离过程是(吸收、萃取)、精馏、蒸发。 7、气液平相衡常数定义为(气相组成与液相组成的比值)。 8、理想气体的平衡常数与(组成)无关。 9、活度是(修正的)浓度。 10、低压下二元非理想溶液的相对挥发度α12等于(02 201 1p p γγ)。 11、气液两相处于平衡时,(化学位)相等。 12、Lewis 提出了等价于化学位的物理量(逸度)。 13、逸度是(修正的)压力。 14、在多组分精馏中塔顶温度是由(露点方程)方程求定的。 15、露点方程的表达式为(∑=1K /y i i ) 16、泡点方程的表达式为(∑=1x K i i )。 17、泡点温度计算时若1x K i i >∑,温度应调(小)。 18、泡点压力计算时若1x K i i >∑,压力应调(大)。 19、在多组分精馏中塔底温度是由(泡点)方程求定的。 20、绝热闪蒸过程,节流后的温度(降低)。 21、若组成为Z i 的物系,1K /Z 1Z K i i i i >∑>∑且时,其相态为(气液两相)。 22、若组成为Z i 的物系,1Z K i i <∑时,其相态为(过冷液相)。 23、若组成为Z i 的物系,1K /Z i i <∑时,其相态为(过热气相)。 24、绝热闪蒸过程,饱和液相经节流后会有(气相)产生。 25、设计变量与独立变量之间的关系可用下式来表示(Ni =Nv -Nc )。 26、设计变量分为(固定设计变量)与(可调设计变量)。 27、回流比是(可调)(固定、可调)设计变量。 28、关键组分的相挥发度越大,精馏过程所需的最少理论板数(越少)。 29、分离要求越大,精馏过程所需的最少理论板数(越多)。 30、进料中易挥发含量越大,精馏过程所需的最少理论板数(不变)。 31、在萃取精馏中所选的萃取剂希望与塔顶馏出组份形成具有(正)偏差的非理想溶液。 32、在萃取精馏中所选的萃取剂使A P 1'值越(大)越 好。 33、在萃取精馏中所选的萃取剂希望与塔底组分形成具有(负)偏差的非理想溶液。 34、在萃取精馏中所选的萃取剂使A P 1'值越大,溶剂的选择性(增大)。 35、萃取精馏塔中,萃取剂是从塔(底)出来。 36、恒沸剂与组分形成最低温度的恒沸物时,恒沸剂从塔(顶)出来。 37、均相恒沸物在低压下其活度系数之比γγ12/应等于(02P )与(o 1P )之比。 38、在板式塔的吸收中,原料中的平衡常数小的组分主要在塔内(底)板被吸收。 39、吸收中平衡常数大的组分主要在塔内(顶)板被吸收。 40、吸收中平衡常数大的组分是(难)吸收组分。 41、吸收中平衡常数小的组分是(易)吸收组分。 42、吸收因子越大对吸收越(有利)。 43、温度越高对吸收越(不利)。 44、压力越高对吸收越(有利)。 45、吸收因子A (反比)于平衡常数。 46、吸收因子A (正比)于吸收剂用量L 。 47、吸收因子A (反比)于液气比。 48、完成一个给定的分离要求所需功最小的过程是(可逆)。
分离工程习题 第一章 1.列出5种使用ESA和5种使用MSA的分离操作。 答:属于ESA分离操作的有精馏、萃取精馏、吸收蒸出、再沸蒸出、共沸精馏。 属于MSA分离操作的有萃取精馏、液-液萃取、液-液萃取(双溶剂)、吸收、吸附。 5.海水的渗透压由下式近似计算:π=RTC/M,式中C为溶解盐的浓度,g/cm3;M为离子状态的各种溶剂的平均分子量。若从含盐0.035 g/cm3的海水中制取纯水,M=31.5,操作温度为298K。问反渗透膜两侧的最小压差应为多少kPa? 答:渗透压π=RTC/M=8.314×298×0.035/31.5=2.753kPa。 所以反渗透膜两侧的最小压差应为2.753kPa。 9.假定有一绝热平衡闪蒸过程,所有变量表示在所附简图中。求: (1)总变更量数Nv; (2)有关变更量的独立方程数Nc; (3)设计变量数Ni; (4)固定和可调设计变量数Nx , Na; (5)对典型的绝热闪蒸过程,你将推荐规定哪些变量? 思路1: 3股物流均视为单相物流, 总变量数Nv=3(C+2)=3c+6 独立方程数Nc 物料衡算式C个 热量衡算式1个 相平衡组成关系式C个 1个平衡温度等式 1个平衡压力等式共2C+3个 故设计变量Ni =Nv-Ni=3C+6-(2C+3)=C+3 固定设计变量Nx=C+2,加上节流后的压力,共C+3个 可调设计变量Na=0 解: (1)Nv = 3 ( c+2 ) (2)Nc 物 c
能 1 相 c 内在(P,T) 2 Nc = 2c+3 (3)Ni = Nv – Nc = c+3 (4)Nxu = ( c+2 )+1 = c+3 (5)Nau = c+3 –( c+3 ) = 0 思路2: 输出的两股物流看成是相平衡物流,所以总变量数Nv=2(C+2) 独立方程数Nc:物料衡算式C个,热量衡算式1个,共C+1个 设计变量数Ni=Nv-Ni=2C+4-(C+1)=C+3 固定设计变量Nx:有C+2个加上节流后的压力共C+3个 可调设计变量Na:有0 11.满足下列要求而设计再沸汽提塔见附图,求: (1)设计变更量数是多少? (2)如果有,请指出哪些附加变量需要规定? 解:N x u 进料c+2 压力9 c+11=7+11=18 N a u 串级单元 1 传热 1 合计 2 N V U = N x u+N a u = 20 附加变量:总理论板数。 16.采用单个精馏塔分离一个三组分混合物为三个产品(见附图),试问图中所注设计变量能否使问题有唯一解?如果不,你认为还应规定哪个(些)设计变量? 解: N X U进料c+2 压力40+1+1 c+44 = 47 N a u3+1+1+2 = 7 N v u = 54 设计变量:回流比,馏出液流率。 第二章 4.一液体混合物的组成为:苯0.50;甲苯0.25;对二甲苯0.25(摩尔分率)。分别