钒渣生产原理(钒渣-五氧化二钒-三氧化二钒-金属钒-钒铁-钒铝合金-碳氮化钒-钒电池)
- 格式:doc
- 大小:94.00 KB
- 文档页数:4

钒及钒生产工艺钒及钒生产工艺第一章钒的性质及应用一、钒的性质:钒是一种十分重要的战略物资,在钢铁、电子、化工、宇航、原子能、航海、建筑、体育、医疗、电源、陶瓷等在国民经济和国防中占有十分重要的位置。
常温下钒的化学性质较稳定,但在高温下能与碳、硅、氮、氧、硫、氯、溴等大部分非金属元素生成化合物。
例如:钒在空气中加热至不同温度时可生成不同的钒氧化物。
在180C下,钒与氯作用生成四氯化钒(VC14);当温度超过800C时,钒与氮反应生成氮化钒(VN;在800〜1000 C时,钒与碳生成碳化钒(VQ。
钒具有较好的耐腐蚀性能,能耐淡水和海水的侵蚀,亦能耐氢氟酸以外的非氧化性酸(如盐酸、稀硫酸)和碱溶液的侵蚀,但能被氧化性酸(浓硫酸、浓氯酸、硝酸和王水)溶解。
在空气中,熔融的碱、碱金属碳酸盐可将金属钒溶解而生成相应的钒酸盐。
此外,钒亦具有一定的耐液态金属和合金(钠、铅、铋等)的腐蚀能力。
钒有多种氧化物。
和MC4之间,存在着可用通式VO n-i(3 <n W9)表示的同族氧化物,在V2O到V2O之间,已知有VO、VO、VO、VO、V5O、V6O i、V6O3等氧化物。
工业上钒氧化物主要是以V2O、V2C4和V2Q形式存在,特别是V2Q和生产尤为重要。
它们的主要性质列于下表:二、钒的应用三、五氧化二钒的性质V2Q是一种无味、无嗅、有毒的橙黄色或红棕色的粉末,微溶于水(质量浓度约为0.07g/L ),溶液呈黄色。
它在约670C熔融,冷却时结晶成黑紫色正交晶系的针状晶体,它的结晶热很大,当迅速结晶时会因灼热而发光。
V2O是两性氧化物,但主要呈酸性。
当溶解在极浓的NaOF中时,得到一种含有八面体钒酸根离子VQ3-的无色溶液。
它与NaCQ—起共熔得到不同的可溶性钒酸钠。
第二章五氧化二钒生产工艺方法概述五氧化二钒生产工艺大致历经了70年,通过几代人的不断总结、探讨,已初步形成了不同的生产工艺模式。
一、五氧化二钒生产工艺方法:五氧化二钒生产按冶炼方法不同可分为火法与湿法冶金:1、火法冶金:将含钒钛磁铁矿经过火法冶金处理后得到含钒铁水,再从铁水氧化出钒渣,使钒得到富集后再使用。

五氧化二钒生产工艺五氧化二钒(V2O5)是一种重要的过渡金属氧化物,广泛应用于钒电池、染料、催化剂以及合金的生产中。
下面我们将介绍五氧化二钒的生产工艺。
五氧化二钒的生产工艺可以分为两个主要步骤:钒矿选矿和氧化步骤。
首先是钒矿选矿。
钒矿一般包含钒矿石和非钒矿石,含有较高钒含量的矿石主要有钒磁铁矿和钒钛磁铁矿。
选矿的目的是通过物理和化学方法将钒矿石从非钒矿石中分离出来。
选矿主要包括矿石的研磨、浮选、磁选和重选等步骤。
其中浮选是最常用的方法,通过对矿石进行研磨,然后将其与若干种药剂混合,使得钒矿石沉入泡沫中,而非钒矿石沉入底层,从而实现分离。
经过选矿,得到的钒矿石可以含有较高的钒含量,以便进行后续的氧化步骤。
接下来是氧化步骤。
将得到的钒矿石进行氧化,主要有两种方法:湿法氧化和干法氧化。
湿法氧化是通过将钒矿石与硫酸等溶液反应,使得钒矿石中的钒转化成溶液中的可溶性钒酸盐。
这种方法需要酸洗设备,操作相对较复杂。
经过氧化,得到的钒酸盐溶液可以用于制备其他钒化合物。
干法氧化是通过将钒矿石与空气或氧气进行氧化反应,使得矿石中的钒转化成五氧化二钒。
这种方法需要高温反应炉或回转窑,操作相对简单。
干法氧化还可以分为两个步骤:初级氧化和终末氧化。
初级氧化是将矿石在较低温度下进行氧化,从而得到较低钒含量的氧化物;而终末氧化是将初级氧化产物在较高温度下继续氧化,从而得到较高钒含量的五氧化二钒。
在进行干法氧化的过程中,需要控制氧化反应的温度、气氛以及反应时间等参数,以确保反应得到理想的产物。
反应完成后,得到的五氧化二钒可以进行粉碎、磁选和过滤等步骤,以得到纯度较高的产品。
总的来说,五氧化二钒的生产工艺主要包括钒矿选矿和氧化两个步骤。
通过选矿将含有较高钒含量的矿石从钒矿石中提取出来,然后通过氧化将钒矿石中的钒转化为五氧化二钒。
这些步骤需要适当控制操作条件,以确保产品的质量和产量。
同时,为了提高产品的纯度,还可以进行粉碎、磁选和过滤等后续步骤。
第五章钒材料制备原理及主要工艺5.1 钒渣5.1.1 钒渣的生产原理世界上钒铁磁铁矿冶炼,主要是用回转窑-电炉或用高炉,冶炼出含钒铁水。
含钒铁水提钒的主要任务有三:一是把含钒铁水吹炼成高含碳量的满足下一步炼钢的要求的半钢;二是最大限度地把铁水中的钒氧化进入钒渣;三是通过提钒得到适合于下一步提取V 2O 5要求的钒渣。
5.1.1.1铁水提钒过程的主要反应 铁水中元素氧化的T G -∆ϑ图吹钒过程是氧气流与金属熔体表面相互作用的过程,铁水中铁、钒、碳、硅、锰、钛、磷、硫等元素的氧化反应过程,这些元素的氧化反应进行的速度取决于铁水本身的化学成分、吹钒时的热力学和动力学条件。
气-液相间的氧化反应可用通式表示为:m/n[Me]+1/2{O 2}=1/n(Me m O n )式中 [Me]─为铁水中的组元; {O 2}─为气相中的氧气;(Me m O n )─为炉渣中的氧化物或气体氧化物; m 、n ─为化学反应的平衡系数。
反应能力的大小取决于铁水组分与氧的化学亲合力,通常称之为标准生成自由能ϑG ∆。
ϑG ∆值越负,氧化反应越容易进行。
许多资料提供了氧化物的标准生成自由能ϑG ∆与温度的方程式。
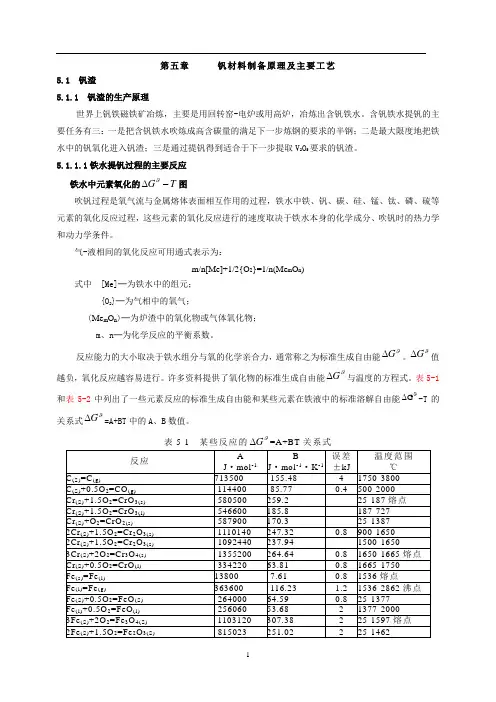
表5-1和表5-2中列出了一些元素反应的标准生成自由能和某些元素在铁液中的标准溶解自由能ϑ∆G -T 的关系式ϑG ∆=A+BT 中的A 、B 数值。
表5-1 某些反应的ϑG ∆=A+BT 关系式表5-2 某些元素在铁液中的标准溶解自由能(ϑG ∆=A+BT)注:以1%溶液为标准态,γ°I 为活度系数。
图5-1示出了铁水中各元素与氧生成氧化物的标准生成自由能ϑG ∆与温度T 的关系曲线。
图5-1 铁水中元素氧化的ϑG ∆-T 图由图5-1可见,在铁水中各元素原始活度相等和不存在动力学困难的情况下,各元素氧化的情况。
钛的氧化优先,硅和钒的氧化较慢。
同时,从图中还可以求出标准状态下铁水中某元素与碳的氧化顺序交换的温度──选择性氧化的转化温度T 转 (P CO =0.1MPa 下被固体碳还原的初始温度)。


钒及钒生产工艺第一章钒的性质及应用一、钒的性质:钒是一种十分重要的战略物资,在钢铁、电子、化工、宇航、原子能、航海、建筑、体育、医疗、电源、陶瓷等在国民经济和国防中占有十分重要的位置。
常温下钒的化学性质较稳定,但在高温下能与碳、硅、氮、氧、硫、氯、溴等大部分非金属元素生成化合物。
例如:钒在空气中加热至不同温度时可生成不同的钒氧化物。
在180℃下,钒与氯作用生成四氯化钒(VCl4);当温度超过800℃时,钒与氮反应生成氮化钒(VN);在800~1000℃时,钒与碳生成碳化钒(VC)。
钒具有较好的耐腐蚀性能,能耐淡水和海水的侵蚀,亦能耐氢氟酸以外的非氧化性酸(如盐酸、稀硫酸)和碱溶液的侵蚀,但能被氧化性酸(浓硫酸、浓氯酸、硝酸和王水)溶解。
在空气中,熔融的碱、碱金属碳酸盐可将金属钒溶解而生成相应的钒酸盐。
此外,钒亦具有一定的耐液态金属和合金(钠、铅、铋等)的腐蚀能力。
钒有多种氧化物。
V2O3和V2O4之间,存在着可用通式V n O2n-1(3≤n≤9)表示的同族氧化物,在V2O4到V2O5之间,已知有V3O5、V3O7、V4O7、V4O9、V5O9、V6O11、V6O13等氧化物。
工业上钒氧化物主要是以V2O5、V2O4和V2O3形式存在,特别是V2O5和生产尤为重要。
它们的主要性质列于下表:二、钒的应用三、五氧化二钒的性质V2O5是一种无味、无嗅、有毒的橙黄色或红棕色的粉末,微溶于水(质量浓度约为L),溶液呈黄色。
它在约670℃熔融,冷却时结晶成黑紫色正交晶系的针状晶体,它的结晶热很大,当迅速结晶时会因灼热而发光。
V2O5是两性氧化物,但主要呈酸性。
当溶解在极浓的NaOH 中时,得到一种含有八面体钒酸根离子VO43-的无色溶液。
它与Na2CO3一起共熔得到不同的可溶性钒酸钠。
第二章五氧化二钒生产工艺方法概述五氧化二钒生产工艺大致历经了70年,通过几代人的不断总结、探讨,已初步形成了不同的生产工艺模式。

钒材料的分类与用途
邹建新
由钒矿物通过各种生产工艺流程可以获得如下钒材料:
※含钒铁水
※钒渣
※V2O5
※V2O3
※钒铁(FeV)
※钒氮合金(VN)
※金属钒
※VO2
※碳化钒
等。
几种钒材料的工艺流程关系:
钒渣(除杂提纯)→V2O5 (还原)→V2O3(还原)→金属钒
钒渣:作为生产V2O5的原料。
V2O5:生产V2O3;生产FeV;作为化工行业催化剂。
V2O3 :生产FeV;作为化工行业催化剂。
FeV :作为合金元素大量应用于钢铁中,提高金属件的强度等性能,如重轨,飞机。
此外,钒还可作为薄膜材料,电池材料领域。
总之,钒材料的两大主要用途是:在钢中作为合金强化剂;催化剂。
——《钒钛产品生产工艺与设备》,北京:化工出版社,2014.01。

五氧化二钒三步法五氧化二钒是一种无机化合物,其化学式为V2O5。
它是一种重要的过渡金属氧化物,具有广泛的应用。
本文将从三个方面介绍五氧化二钒的制备方法。
一、溶剂法制备五氧化二钒溶剂法制备五氧化二钒是一种常见的方法。
首先,将适量的五氯化钒溶解于适当的溶剂中,如甲醇或乙醇。
然后,在搅拌下缓慢加入适量的氧化剂,如过氧化氢或氧气。
随着氧化反应的进行,溶液逐渐变成黄色或橙色。
最后,将溶液过滤,得到五氧化二钒的沉淀。
通过干燥和煅烧处理,可以得到纯净的五氧化二钒产品。
二、热分解法制备五氧化二钒热分解法是另一种制备五氧化二钒的常用方法。
首先,将适量的钒酸铵或钒酸钠溶解于适当的溶剂中,如水或醇类。
然后,将溶液加热至一定温度,通常在300-500摄氏度之间。
在这个温度范围内,钒酸根离子开始发生分解,生成五氧化二钒。
最后,将反应产物经过过滤、洗涤和干燥处理,得到纯净的五氧化二钒。
三、氧化法制备五氧化二钒氧化法是一种简单而高效的制备五氧化二钒的方法。
首先,将适量的钒粉置于反应器中。
然后,通过加热或添加氧化剂,如氧气或过氧化氢,使钒粉发生氧化反应。
在适当的温度和氧气流量下,钒粉逐渐转化为五氧化二钒。
最后,将反应产物经过冷却、过滤和干燥处理,得到纯净的五氧化二钒。
总结:本文介绍了三种常用的制备五氧化二钒的方法:溶剂法、热分解法和氧化法。
溶剂法利用溶剂中的氧化剂氧化五氯化钒或钒酸盐,得到五氧化二钒的沉淀。
热分解法通过加热钒酸盐使其分解,生成五氧化二钒。
氧化法则是直接将钒粉与氧气或过氧化氢反应,得到五氧化二钒。
这些方法制备的五氧化二钒可以通过适当的后处理,如过滤、洗涤和干燥,得到纯净的产物。
五氧化二钒在化学工业中具有重要的应用,如催化剂、电池材料和玻璃着色剂等。

五氧化二钒三步法五氧化二钒是一种无机化合物,化学式为V2O5。
它是一种重要的钒化合物,具有广泛的应用领域。
本文将从三个步骤来介绍五氧化二钒的制备方法。
第一步是从钒矿石中提取钒。
钒矿石主要有钒磁铁矿和钒镍矿两种,其中钒磁铁矿是最常见的钒矿石。
提取钒的方法有多种,常用的方法是氧化焙烧法。
首先将钒矿石破碎成粉末状,然后进行焙烧。
焙烧过程中,钒矿石中的钒会与氧气发生反应,生成氧化钒。
焙烧后的产物中含有氧化钒和其他杂质,需要经过酸浸提取来得到纯净的氧化钒。
第二步是将氧化钒还原为金属钒。
这一步通常采用煅烧还原法。
将氧化钒与还原剂(如碳粉)混合后,放入高温炉中进行煅烧。
在高温下,还原剂会与氧化钒发生反应,将氧化钒还原为金属钒。
煅烧后得到的产物是金属钒的粉末。
第三步是将金属钒与氧气反应生成五氧化二钒。
将金属钒粉末与氧气充分接触,放入反应器中进行反应。
反应过程中,金属钒与氧气发生氧化反应,生成五氧化二钒。
反应后的产物是五氧化二钒的粉末。
通过以上三个步骤,我们可以得到纯净的五氧化二钒。
五氧化二钒是一种重要的化工原料,广泛应用于电池、催化剂、颜料等领域。
除此之外,五氧化二钒还具有一定的毒性,需要注意安全使用。
在制备过程中,应采取必要的防护措施,避免对人体和环境造成伤害。
五氧化二钒的制备包括从钒矿石中提取钒、将氧化钒还原为金属钒,以及金属钒与氧气反应生成五氧化二钒三个步骤。
这些步骤需要严格控制反应条件和操作方法,以确保得到纯净的五氧化二钒。
五氧化二钒的制备方法对于相关产业的发展和应用具有重要意义,也为我们深入了解钒化合物的性质和应用提供了基础。


欢迎阅读钒及钒生产工艺第一章 钒的性质及应用一、钒的性质:钒是一种十分重要的战略物资,在钢铁、电子、化工、宇航、原子能、航海、建筑、体育、医疗、电源、陶瓷等在国民经济和国防中占有十分重要的位置。
力。
V 6O 135和生产尤为重要。
它们的主要性质列于下表:二、钒的应用三、五氧化二钒的性质V2O5是一种无味、无嗅、有毒的橙黄色或红棕色的粉末,微溶于水(质量浓度约为0.07g/L),溶液呈黄色。
它在约670℃熔融,冷却时结晶成黑紫色正交晶系的针状晶体,它的结晶热很大,当迅速结晶时会因灼热而发光。
V2O5是两性氧化物,但主要呈酸性。
当溶解在极浓的NaOH中时,得到一种含有八面体钒酸根离子VO43-的无色1(1)(2)使用这种方法的国家有南非、新西兰。
从含钒铁水中吹炼钒渣将含钒铁水在转炉(中国、俄罗斯)、摇包(南非)或铁水包(新西兰)内、通入氧化性气体(氧气、空气),使铁水中的钒氧化出来,得到钒渣。
钒渣作为提取五氧化二钒的原料。
火法提钒的工艺流程见图1所示。
此方法的优点:钒渣作为提取五氧化二钒原料含钒高,处理量少;可回收铁;焙烧温度低(800℃)左右,提取V2O5时动力、辅助原材料消耗少。
(火法主要是指钒渣以前,从钒渣以后至五氧化二钒生产所用仍然是湿法冶金)图1火法提钒工艺流程图2、湿法冶金:传统湿法提钒典型的工艺流程(以南非德兰士瓦合金公司为例)如图2所示。
首先把钒钛磁铁矿磨细(湿磨),磨细后的矿粉与钠盐(硫酸钠)混合造球,球团直接送到链篦回转窑的链篦上,利用回转窑的余热烘干并加热至900℃,随后在回转窑内于1270℃左右停留60—110min,钒转化率可达到92%以上。
此方法的优点:原料处理简单;钒回收率高,从精矿→V2O5收率达80%以上。
二、湿法冶金生产五氧化二钒生产工艺简介:湿法冶金工艺生产五氧化二钒主要经历以下生产阶段:1、原料预处理;2、固见图31或酸溶性的钒盐或钒酸盐。
典型的方法有: (1)钠化焙烧提钒:钒渣(或钒矿)磨细和选去所夹带的金属铁后,配入适当的钠盐附加剂,经过高温焙烧氧化、钠化反应,钒铁尖晶石等不溶性三价钒化合物氧化成五氧化二钒并与钠盐反应,生成可熔性钒酸钠。

钒及钒生产工艺第一章钒的性质及应用一、钒的性质:钒是一种十分重要的战略物资,在钢铁、电子、化工、宇航、原子能、航海、建筑、体育、医疗、电源、陶瓷等在国民经济和国防中占有十分重要的位置。
常温下钒的化学性质较稳定,但在高温下能与碳、硅、氮、氧、硫、氯、溴等大部分非金属元素生成化合物。
例如:钒在空气中加热至不同温度时可生成不同的钒氧化物。
在180℃下,钒与氯作用生成四氯化钒(VCl4);当温度超过800℃时,钒与氮反应生成氮化钒(VN);在800~1000℃时,钒与碳生成碳化钒(VC)。
钒具有较好的耐腐蚀性能,能耐淡水和海水的侵蚀,亦能耐氢氟酸以外的非氧化性酸(如盐酸、稀硫酸)和碱溶液的侵蚀,但能被氧化性酸(浓硫酸、浓氯酸、硝酸和王水)溶解。
在空气中,熔融的碱、碱金属碳酸盐可将金属钒溶解而生成相应的钒酸盐。
此外,钒亦具有一定的耐液态金属和合金(钠、铅、铋等)的腐蚀能力。
钒有多种氧化物。
V2O3和V2O4之间,存在着可用通式V n O2n-1(3≤n≤9)表示的同族氧化物,在V2O4到V2O5之间,已知有V3O5、V3O7、V4O7、V4O9、V5O9、V6O11、V6O13等氧化物。
工业上钒氧化物主要是以V2O5、V2O4和V2O3形式存在,特别是V2O5和生产尤为重要。
它们的主要性质列于下表:二、钒的应用三、五氧化二钒的性质V2O5是一种无味、无嗅、有毒的橙黄色或红棕色的粉末,微溶于水(质量浓度约为0.07g/L),溶液呈黄色。
它在约670℃熔融,冷却时结晶成黑紫色正交晶系的针状晶体,它的结晶热很大,当迅速结晶时会因灼热而发光。
V2O5是两性氧化物,但主要呈酸性。
当溶解在极浓的NaOH中时,得到一种含有八面体钒酸根离子VO43-的无色溶液。
它与Na2CO3一起共熔得到不同的可溶性钒酸钠。
第二章五氧化二钒生产工艺方法概述五氧化二钒生产工艺大致历经了70年,通过几代人的不断总结、探讨,已初步形成了不同的生产工艺模式。
钒及钒生产工艺第一章钒的性质及应用一、钒的性质:钒是一种十分重要的战略物资,在钢铁、电子、化工、宇航、原子能、航海、建筑、体育、医疗、电源、陶瓷等在国民经济和国防中占有十分重要的位置。
常温下钒的化学性质较稳定,但在高温下能与碳、硅、氮、氧、硫、氯、溴等大部分非金属元素生成化合物。
例如:钒在空气中加热至不同温度时可生成不同的钒氧化物。
在180℃下,钒与氯作用生成四氯化钒(VCl4);当温度超过800℃时,钒与氮反应生成氮化钒(VN);在800~1000℃时,钒与碳生成碳化钒(VC)。
钒具有较好的耐腐蚀性能,能耐淡水和海水的侵蚀,亦能耐氢氟酸以外的非氧化性酸(如盐酸、稀硫酸)和碱溶液的侵蚀,但能被氧化性酸(浓硫酸、浓氯酸、硝酸和王水)溶解。
在空气中,熔融的碱、碱金属碳酸盐可将金属钒溶解而生成相应的钒酸盐。
此外,钒亦具有一定的耐液态金属和合金(钠、铅、铋等)的腐蚀能力。
钒有多种氧化物。
V2O3和V2O4之间,存在着可用通式V n O2n-1(3≤n≤9)表示的同族氧化物,在V2O4到V2O5之间,已知有V3O5、V3O7、V4O7、V4O9、V5O9、V6O11、V6O13等氧化物。
工业上钒氧化物主要是以V2O5、V2O4和V2O3形式存在,特别是V2O5和生产尤为重要。
它们的主要性质列于下表:二、钒的应用三、五氧化二钒的性质V2O5是一种无味、无嗅、有毒的橙黄色或红棕色的粉末,微溶于水(质量浓度约为L),溶液呈黄色。
它在约670℃熔融,冷却时结晶成黑紫色正交晶系的针状晶体,它的结晶热很大,当迅速结晶时会因灼热而发光。
V2O5是两性氧化物,但主要呈酸性。
当溶解在极浓的NaOH 中时,得到一种含有八面体钒酸根离子VO43-的无色溶液。
它与Na2CO3一起共熔得到不同的可溶性钒酸钠。
第二章五氧化二钒生产工艺方法概述五氧化二钒生产工艺大致历经了70年,通过几代人的不断总结、探讨,已初步形成了不同的生产工艺模式。
五氧化二钒的生产工艺
五氧化二钒的生产工艺一般分为两步:钒氧化和二次氧化。
第一步:钒氧化
1. 精选原料:选用含有足够钒含量的钒矿石或工业废渣作为原料。
2. 粉碎矿石:将原料矿石通过破碎设备进行粉碎,得到细碎的粉末。
3. 钒酸化:将粉碎后的矿石与硅石、石灰等添加剂混合,将混合物在高温条件下进行煅烧,使钒转变为钒酸化合物。
4. 酸浸:将经过煅烧得到的钒酸盐进行酸浸,通常使用硫酸进行浸出。
5. 沉淀:通过添加适当的试剂,将钒与其他元素分离沉淀,得到含有钒的沉淀物。
6. 返溶:将钒沉淀物进行返溶,使用硫酸进行回溶,得到含有钒的硫酸溶液。
7. 氧化:将得到的钒盐溶液进行氧化反应,得到五氧化二钒。
第二步:二次氧化
1. 浸湿:将五氧化二钒沉淀物浸湿加水悬浮液。
2. 过滤:将悬浮液进行过滤,得到含有五氧化二钒的滤饼。
3. 清洗:用适量水洗涤滤饼,去除杂质。
4. 干燥:将洗净的滤饼进行干燥,得到五氧化二钒颗粒。
5. 煅烧:将五氧化二钒颗粒进行煅烧,使其更加纯净。
6. 粉碎:将煅烧后的五氧化二钒颗粒进行粉碎,得到符合要求的五氧化二钒粉末。
7. 包装:将粉碎后的五氧化二钒粉末进行包装,储存和运输。
以上是一种常用的五氧化二钒生产工艺流程,具体实施方案可能因厂家和原料的不同而有所差异。
钒渣生产原理(钒渣-五氧化二钒-三氧化二钒-金属钒-钒铁-钒铝合金-碳氮化钒-钒电池)
原创邹建新崔旭梅教授等
1 钒渣生产方法简介
提钒原料有钒钛磁铁矿、石煤等。
要从钒钛磁铁矿中回收钒,首先需将钒钛磁铁矿在高炉或电炉中冶炼出含钒铁水。
含钒铁水提钒的主要任务有以下几方面:
⑴把含钒铁水吹炼成满足下一步炼钢要求的高碳含量的半钢;
⑵最大限度的把铁水中钒选择性氧化进入到钒渣中;
⑶得到的钒渣能作为下一步提取五氧化二钒的原料。
提钒的方法很多,但有些方法已经被淘汰(如雾化提钒)。
目前世界上铁水提钒的方法主要有四种:
⑴摇包提钒(南非海威尔德用);
⑵铁水包提钒(新西兰);
⑶空气底吹转炉提钒(俄罗斯丘索夫);
⑷氧气顶吹(复合吹炼)转炉提钒(俄罗斯下塔吉尔和中国攀钢、马钢、承钢)。
钒钛磁铁矿的火法提钒工艺流程图如图5.1.1所示。
图5.1.1 火法提钒工艺
2 转炉提钒的主要化学反应
转炉提钒过程:转炉提钒是氧射流与金属熔体表面相互作用,与铁水中铁、钒、碳、硅、锰、钛、磷、硫等元素的氧化反应过程。
这些元素氧化反应进行的速度取决于铁水本身化学成分、吹钒时的动力学条件和热力学条件。
转炉提钒中的化学反应:转炉提钒就是利用选择性氧化的原理,采用高速氧射流在转炉中对含钒铁水进行搅拌,将铁水中钒氧化成稳定的钒氧化物,以制取钒渣的一种物理化学反应过程。
在反应过程中,通过加入冷却剂控制熔池温度在碳钒转化温度以下,达到“去钒保碳”的目的。
元素的氧化反应可用以下通式表示:
m/n[Me]+1/2{O 2}=1/n(Me m O n )
式中 [Me]─为铁水中的组元;{O 2}─为气相中的氧气;(Me m O n )─为炉渣中的氧化物或气体氧化物,m 、n ─为化学反应的平衡系数。
V 的氧化主反应为:
2/3 [V] + 1/2 {O 2} =1/3 (V 2O 3) 2/5 [V] + 1/2 {O 2} =1/5 (V 2O 5) 1/3 (V 2O 3) + 1/2 {O 2} = 1/5 (V 2O 5)
其他杂质的氧化副反应为:
1/2 [Si] +1/2 {O 2}=1/2 (SiO 2) [Ca] +1/2 {O 2} = (CaO) [Mn] + 1/2 {O 2} = (MnO) [Fe] + 1/2 {O 2} = (FeO) 2(FeO) + 1/2 {O 2} = (Fe 2O 3)
(C) +{O 2} ={CO 2}
反应能力的大小取决于铁水组分与氧的化学亲合力,即标准生成自由能θG ∆。
θ
G ∆值越负,表明氧化反应越容易进行。
铁水中元素氧化的θ
G ∆-T 图如图5.1.2所示。
反应完成后,液态的Fe 留在转炉里,称为半钢;固态(熔融态)的渣敝出后放入渣罐,称为钒渣。
钒渣是由 FeO 、SiO 2、V 2O 3、TiO 2、CaO 、Al 2O 3、MgO 、Cr 2O 3等组分构成的。
一般情况下,钒渣中 CaO 、P 、SiO 2的含量越低则钒渣评级越高。
高炉铁水、钒渣和半钢典型化学成分如表5.1.1~5.1.3所示。
3 转炉提钒脱钒、脱碳规律
脱钒规律:吹钒前期熔池处于“纯脱钒”状态,脱钒量占总提钒量的70%,进入中后期,碳氧化逐渐处于优先,随钒含量的降低,脱钒速度也随之降低。
图5.1.2 铁水中元素氧化的θG ∆-T 图
脱碳规律:在吹炼前期,脱碳较少,反应进行速度较低,中后期脱碳速度明显加快,在此期间碳氧化率达70%。
另外,在倒炉及出半钢期间,也有少量碳氧化。
在熔池区域,碳的氧化反应按下列反应进行: [C] + [O] = CO
在射流区域碳的氧化反应按下列反应进行: 2[C] + O 2 = 2CO
表 5.1.1高炉铁水典型化学成分 (%)
表 5.1.2 钒渣典型化学成分 (%)
参考文献:《钒钛产品生产工艺与设备》,北京:化学工业出版社,作者:邹建新等,
2014.01
《钒钛物理化学》,北京:化工出版社,作者:邹建新,2016
(钒钛资源综合利用四川省重点实验室【攀枝花学院】,cnzoujx@)
四川省钒钛工程技术中心。